侵袭性肺毛霉菌病诊治及预后分析
姜华 李春梅 南岩东 李王平 金发光
侵袭性肺毛霉菌病(invasive pulmonary mucormycosis)是一种罕见肺部真菌感染性疾病,近年发病率有所升高[1-3]。根据累及的器官不同,分为鼻脑型、肺型、中枢神经系统型、胃肠型、肾型、播散型和皮肤型,其临床表现多样,缺乏特异性,诊断难度较大,极易被误诊,预后较差[4-6]。本文回顾性分析空军军医大学(第四军医大学)唐都医院呼吸内科确诊的8例侵袭性肺毛霉菌病患者的病例资料,总结其临床表现、影像学特征、气管镜下表现、治疗过程及预后,报道如下。
资料和方法
一、临床资料
在空军军医大学唐都医院病案室计算机病历数据库中,检索2015年1月至2018年7月呼吸与危重症医学科住院患者中诊断含“毛霉菌病”的病例,并逐个筛选含“肺毛霉菌病”或符合侵袭性肺毛霉菌病诊断标准的病例。诊断标准参照中华医学会呼吸病学分会2007年《肺真菌病诊断和治疗专家共识》规定的诊断标准[7],共纳入符合侵袭性肺毛霉菌病诊断的8例患者,无拟诊病例。入选的8例患者,男性6例,女性2例;中位年龄52岁。8例患者从症状出现到确诊平均时间为48.34(10~145)d,从首次就诊到确诊平均时间为21.25(5~57)d,发病初期被误诊为细菌性肺炎5例(62.5%)、肺曲霉菌病3例(37.5%),肺结核1例(12.5%),肺癌1例(12.5%),仅1例首诊考虑侵袭性肺毛霉菌病。
二、观察方法
对8例侵袭性肺毛霉菌病患者的性别、年龄、基础病、临床表现、实验室检查、影像学特点、气管镜下表现、治疗方法及预后等临床资料进行分析。以查阅门诊、住院病历以及电话随访的方式进行随访,内容包括治疗过程、生存情况,以及死亡时间和原因。将临床疗效评定为痊愈、好转、恶化、死亡和无法判断[8]:①痊愈:症状和体征完全消失,影像学检查肺部病变明显吸收或完全吸收;②好转:症状和体征好转,肺部病变吸收或无明显恶化;③恶化:出现新的肺部感染症状或体征,影像学检查肺部病变进展或无改善;④死亡;⑤无法判断。
结 果
一、临床特征
8例患者基础疾病患糖尿病者7例(87.5%),其中4例合并其他基础疾病,包括高血压2例,多囊肾1例,白癜风1例;有长期粉尘吸入史并肺气肿1例。常见的症状有咳嗽7例(87.5%),气短及呼吸困难6例(75.0%),发热5例(62.5%),痰中带血或咯血4例(50.0%);少见的症状包括胸痛1例(12.5%)、乏力2例(25.0%)。查体闻及喘鸣音4例(50.0%),湿啰音3例(37.5%),其他阳性体征少见。
二、辅助检查
1. 实验室检查: 2例白细胞升高者,均为中性粒细胞增高,其余白细胞计数及分类均正常;血小板计数(415.13±183.10)×109/L,血沉(67.63±33.21)mm/hr,C-反应蛋白(C-reactive protein, CRP)明显增高者3例,G试验阳性1例,GM试验阳性1例,血降钙素原(procalcitonin, PCT)均正常。
2. 影像学检查: 8例患者均行胸部CT检查,7例(87.5%)病变主要位于右肺,1例(12.5%)位于左肺;单个病变2例,多发病6例变,影像学特征,见表1。
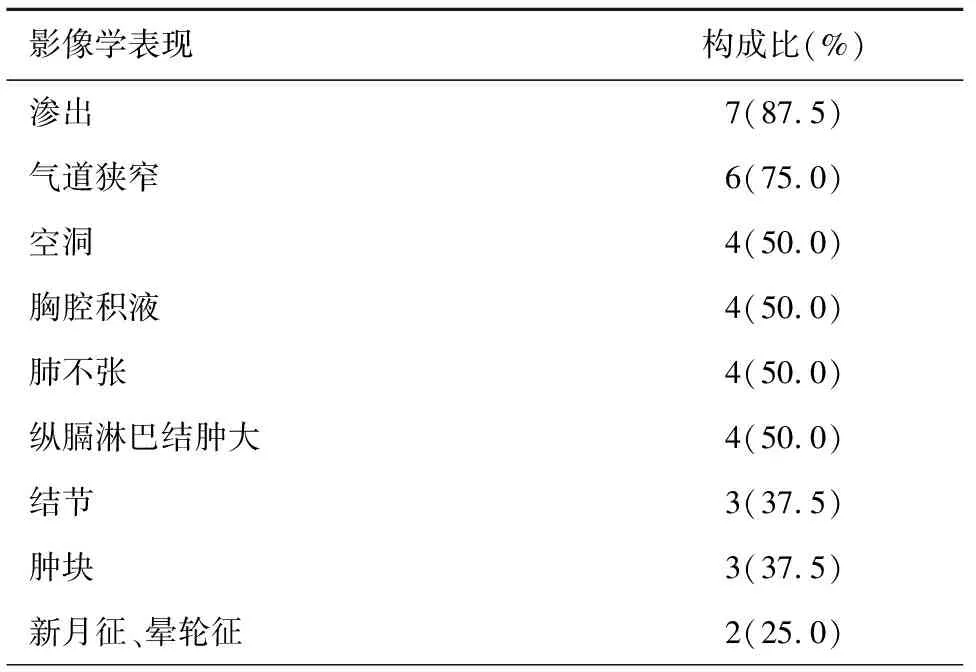
表1 8例肺毛霉菌病患者胸CT影像学特征[n(%)]
3. 气管镜下表现: 8例患者均行气管镜检查,其中1例镜下未见明显异常,7例患者有一种或多种异常表现,包括气道狭窄6例,坏死或伪膜5例,肉芽组织增生4例,黏膜水肿3例,溃疡、出血各2例,1例患者可见瘘口、窦道形成,见图1。
4. 微生物学及病理检查: 6例患者经支气管活检,组织病理学诊断为侵袭性肺毛霉菌病,1例术后病理为肺毛霉菌与曲霉菌混合感染,该7例患者反复痰培养及痰涂片均未查到毛霉菌;1例患者4次痰培养均为毛霉菌。
三、治疗预后
1例静滴两性霉素B脂质体治疗2个月,复查胸CT病变局限,行手术治疗后未再抗真菌治疗,随访评估为治愈;1例两性霉素B脂质体静滴治疗21 d,因肾功能明显异常,改为两性霉素B脂质体雾化吸入,3个月后复查胸部CT,病变明显缩小,随访评估为好转;1例两性霉素B脂质体静滴联合雾化吸入治疗3个月,随访评估为好转;2例两性霉素B脂质体治疗(1例为1个月,1例为12 d)后出现肾功能损害、低钾血症,更换成泊沙康唑治疗1个月,疗效评估为好转;1例确诊后静滴两性霉素B脂质体单药治疗7 d,疗效评估为好转,但拒绝进一步治疗;1例确诊后拒绝治疗,疗效无法评价;1例患者确诊第2天,因气道内大出血死亡。
讨 论
侵袭性肺毛霉菌病是由毛霉菌目毛霉科真菌引起的机会性真菌感染[1],发病率约占侵袭性真菌病的1.6%,男、女均可发病,以中青年男性为主,主要的危险因素有糖尿病酮症酸中毒、长期糖皮质激素治疗、器官移植、自身免疫性疾病、持续性中性粒细胞减少等[9-10]。本组8例患者均有基础疾病史,7例有糖尿病史,其中4例同时合并其他疾病。有研究认为,糖尿病患者免疫力低下,加之高糖和酸性环境有利于毛霉菌的生长繁殖[11]。糖尿病患者血清pH值下降,运铁蛋白转运铁的能力受到抑制,使血清中的游离铁增多,而铁离子正是毛霉菌生长所必需的,因此糖尿病合并酮症酸中毒患者吸入毛霉菌孢子后很容易发展为侵袭性肺毛霉病[12-13]。
毛霉菌可侵犯多种组织器官,包括鼻眶、脑、肺、胃肠道、皮肤[14]。侵袭性肺毛霉菌病临床表现无特异性,常见症状有咳嗽、气短、发热、痰中带血,合并气道狭窄可闻及喘鸣音[15-16]。值得注意的是由于毛霉菌容易侵犯气道软骨及血管,可引起痰中带血,甚至大咯血。实验室检查亦无特异性,炎性指标白细胞、中性粒细胞、血降钙素原、C反应蛋白大都正常,血沉可轻度增快。侵袭性肺毛霉菌病一般G试验和GM试验均为阴性,而阳性虽具有一定的排除意义,但需警惕同时有两种真菌感染可能,本组中1例G试验和GM试验阳性,病理结果显示为曲霉菌和毛霉菌混合感染。此外,本组中6例患者血小板明显高于正常,分析可能与毛霉菌感染破坏血管完整性,导致血小板粘附、血栓形成有关,但尚需进一步大样本研究证实。
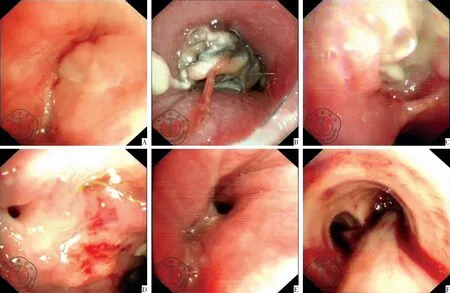
图1 (A-F) 侵袭性肺毛霉菌病气管镜下表现;注:A: 肉芽组织增生(右主支气管闭塞) ;B: 肉芽组织增生,局部坏死(右主支气管);C、D: 窦道形成,可见瘘口(右主支气管左侧壁靠隆突处);E: 气道扭曲变形、狭窄(右上叶);F: 出血(右主支气管出血倒灌入左主支气管)
胸部CT是侵袭性肺毛霉菌病的一项重要检查,影像学表现有渗出、气道狭窄、空洞、胸腔积液,纵膈淋巴结肿大、晕轮征、反晕征等[17]。研究证实肺毛霉菌病胸部CT变化规律如下:发病初期病变中心实变周围磨玻璃影,表现为晕轮征,随后毛霉菌血管侵袭引起出血,出现反晕征,病变进一步发展表现为中央坏死、周围实变,到病程后期,脓肿形成,伴液平面[18]。此外有研究证实胸腔积液是毛霉菌性肺炎的独立危险因素,毛霉菌侵蚀肺实质可在局部形成空洞,空洞多呈光滑厚壁;病灶内部易出现坏死液化,增强扫描呈不均匀强化或不规则环形强化,实质部分强化明显,但以延迟强化为主,侵犯血管可能发生危及生命的大咯血[19-20]。本组资料显示病变部位右肺较左肺多见,可能系肺毛霉菌多经吸入途径感染有关[21]。气管镜下检查及活检是确诊肺毛霉菌病的重要手段,包括支气管镜下超声引导细针抽吸,镜下常见表现有肉芽组织增生、坏死伪膜、管腔狭窄等,难以与支气管结核鉴别[22]。侵袭性肺毛霉菌病诊断金标准是病理组织活检中可见宽大、少分隔的无嗜酸鞘的特征性菌丝,或组织、无菌体液毛霉菌培养阳性[14]。本病临床相对少见,重视程度不够,极易误诊。本组患者从出现症状到确诊经历48 d,从首次就诊到确诊经历21 d,其中1例患者经多个医院病理会诊才修正诊断为毛霉菌,历时145 d。因此,对于高度怀疑毛霉菌感染者,应该尽早行组织活检、病理学检查。
目前针对侵袭性肺毛霉菌的治疗措施包括积极控制基础病,适当时机选择手术、恰当的抗真菌药物。手术切除患肺并且使用抗真菌治疗防止再次感染,患者的生存率可大大提高,尤其是对于年轻患者。研究表明在肺毛霉菌病患者中70%的幸存者采用外科手术和抗真菌治疗,单用抗真菌治疗仅有61%的存活率,单纯外科手术存活率为57%,不做任何治疗仅有3% 的存活率[23-24]。侵袭性肺毛霉菌病常用的治疗药物有两性霉素B、两性霉素B脂质体、泊沙康唑、氟康唑等[25-29]。本组患者中6例应用两性霉素B脂质体治疗,2例出现低血钾,3例出现肾毒性反应,2例换用泊沙康唑治疗。对于气道内病变较重的2例患者,本研究采用两性霉素B脂质体雾化吸入治疗,虽属超说明书使用,但是取得了良好的疗效,与以往病例报道一致[30]。此外,Mihara等[31]对小鼠进行雾化吸入两性霉素B脂质体的研究表明,该途径对侵袭性肺毛霉菌病的小鼠可起到提高生存率及降低真菌负荷的效果,但是对于两性霉素B雾化吸入的方法治疗肺毛霉菌病的应用剂量、疗程、不良反应、是否联合静脉应用等问题尚需进一步研究。另外,研究证实,糖尿病患者毛霉菌性肺炎更倾向于支气管的管腔内病变,对于肺部合并气管腔内病变的侵袭性肺毛霉菌病,可考虑镜下治疗清除肉芽及坏死[32]。本组8例患者中有4例合并气道内病变,曾采用电圈套扎、冷冻、氩气刀、球囊扩张等介入技术进行多次镜下治疗,有效清除了坏死及肉芽,起到了解除气道阻塞,缓解呼吸困难的作用,但需考虑到毛霉菌侵袭性强,容易侵犯血管导致大咯血,也存在较大风险,需严格把握适应症,因本研究病例较少,气管镜下局部治疗尚需更大样本研究来证实其安全性及有效性。
综上所述,侵袭性肺毛霉菌病相对少见,多合并基础疾病,早期易被误诊,预后较其他类型侵袭性肺真菌病差,需要引起临床高度重视[33]。

