柠檬酸改性USY催化纤维素合成乙酰丙酸乙酯
常 春,肖 泽,何玉远,邓 琳,戚小各,徐艳丽
(郑州大学 化工与能源学院,河南 郑州 450001)
乙酰丙酸乙酯(ethyl levulinate,EL)是一种含有羰基和酯基的生物质基化学品,具有良好的反应特性,不仅被广泛应用于香料、溶剂和增塑剂等工业,而且被认为是一种新型的生物液体燃料[1](图1)。目前,由生物质原料合成EL的工艺主要包括:乙酰丙酸酯化法、5-氯甲基糠醛醇解法、糠醇醇解法和生物质一锅法等[2]。上述这些方法中,生物质一锅法因工艺简单、过程无废水、原料转化率高等优点,已成为生物质基EL合成研究的热点之一[3]。

图1 生物质基乙酰丙酸的合成与应用Fig.1 Synthesis and application of biomass-based levulinicacid
固体酸催化剂因环境友好、选择性高和可回收重复利用的优点,在乙酰丙酸酯绿色合成的研究中得到广泛应用。不同类型的固体酸催化剂,如:超强酸类、离子交换树脂类、金属盐类、杂多酸类和分子筛类等被研究报道[4-5],其中,分子筛不仅具有良好的水热稳定性、独特的孔结构和酸性可调的特点,而且商品化程度较高,在生物质一锅法催化合成EL的研究中极具工业应用潜力[6]。

在本研究中,笔者首先筛选出柠檬酸改性的USY分子筛,并对其催化纤维素一锅法合成EL的工艺条件进行优化。同时,采用X线衍射(XRD)、傅里叶变换红外光谱(FT-IR)、比表面积测试(BET)、氨气程序升温脱附(NH3-TPD)和吡啶吸附红外光谱(Py-IR)等对改性USY分子筛进行表征,以期为深入理解改性USY的催化机制提供参考依据。
1 材料与方法
1.1 材料和仪器
葡萄糖、蔗糖、草酸(分析纯),天津科密欧试剂有限公司;果糖、菊糖、纤维素、乙酰丙酸乙酯(EL)(分析纯),上海阿拉丁有限公司;无水乙醇、正辛醇(分析纯),天津风船试剂有限公司;USY 分子筛(工业级),天津南化催化剂公司;柠檬酸、酒石酸(分析纯),天津市瑞金特化学试剂有限公司;盐酸、硝酸(分析纯),洛阳昊华化学试剂有限公司。
GC1690型气相色谱仪,杭州科晓化工仪器设备有限公司;FT-IR200型傅里叶红外光谱仪,美国Nicolet公司;D8 Advance型X线衍射仪,德国Bruker AXS公司;ASAP2420-4M型全自动比表面及孔隙度分析仪,美国Micromeritics公司;FT-IR Frontier 型吡啶-红外光谱仪,美国PE公司;AutoChem1Ⅱ型全自动化学吸附仪,美国麦克仪器公司;DTG-60 型热重分析仪,日本岛津公司;高温高压反应釜,河南予华仪器有限公司;集热式恒温加热磁力搅拌器,郑州国瑞仪器有限公司。
1.2 催化剂的改性
称取一定质量的USY分子筛置入三口烧瓶,加入0.001 mol/L的稀硝酸作为修饰催化剂及其溶剂,升温至90 ℃回流。然后逐滴加入0.2 mol/L的酸溶液,继续回流2 h后停止反应。将处理后的分子筛离心分离,去离子水反复洗涤至中性,之后120 ℃干燥,400 ℃焙烧。
1.3 实验步骤
将40 mL无水乙醇、一定质量的原料及催化剂加入到高压釜(容积100 mL)中,密闭升温至设定的温度,并在设定温度下反应一定的时间(将达到设定温度时刻记为零时刻),反应结束后迅速水冷,中止反应。将反应后的混合物经真空抽滤分离,得到的液体经0.22 μm有机膜过滤后,用气相色谱进行分析。
1.4 催化剂回收与表征
反应后的固相残渣经无水乙醇多次洗涤后,经120 ℃干燥,400 ℃焙烧4 h 进行活化,多次重复使用该催化剂以考察其使用效果,并通过XRD、FT-IR、BET、Py-IR和NH3-TPD等对反应前后的USY催化剂进行表征。
1.5 产物分析及计算
反应液中目的产物EL的含量采用气相色谱内标法测定,EL的产率计算见式(1)。

(1)
式中:m0和m1分别为原料和EL的质量,g;M1为EL的摩尔质量,144 g/mol;当原料为果糖和葡萄糖时,其摩尔质量M0为180 g/mol,当原料为纤维素和菊糖时,其摩尔质量M0为162 g/mol(以单糖计);当原料为蔗糖时,其摩尔质量M0为171 g/mol(以单糖计)。
2 结果与讨论
2.1 柠檬酸改性USY的筛选
选取几种常见的酸,包括:盐酸、草酸、酒石酸和柠檬酸对USY分子筛进行脱铝改性,并对改性USY催化纤维素一锅法生成EL的产率进行比较,结果见图2。由图2(a)可以看到:经盐酸、草酸和酒石酸改性的USY显示出相似的催化能力,催化纤维素得到EL的产率基本相同(~32%)。而经柠檬酸改性的USY具有较好的催化效果,EL的产率达到了36.1%。在此基础上,进一步考察了0.1~0.5 mol/L范围内的柠檬酸溶液对USY改性效果。由图2(b)可以看到:柠檬酸浓度对USY分子筛的改性程度影响较大,存在适宜的范围。当柠檬酸浓度为0.2 mol/L时,改性USY催化纤维素醇解生成EL的产率最高。所以,后续的实验采用0.2 mol/L柠檬酸改性的USY分子筛(DUSY)进行研究。
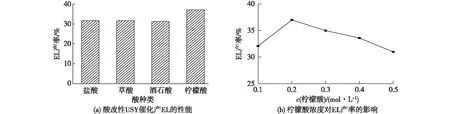
图2 不同酸改性USY(a)和不同柠檬酸浓度改性USY(b)对EL产率的影响Fig.2 Effects of different acid modified USY(a)and different citric acidconcentration modified USY(b)on EL yield
2.2 催化剂的表征
图3分别是未改性的USY和柠檬酸改性的DUSY的XRD和FT-IR图谱。从图3(a)中可以看出:酸处理后各样品仍保持原有晶型,各衍射峰位置不变,但峰强度有所差别。尤其是当柠檬酸的浓度超过0.2 mol/L时,分子筛的特征峰强度明显减弱,这是由于部分铝骨架脱离造成的。图3(b)是USY及DUSY分子筛的红外光谱图。经过柠檬酸处理后的分子筛在1 050和810 cm-1两处的特征峰较未处理的USY向高波段偏移,这是因为经过柠檬酸溶液处理后,USY分子筛中的部分骨架铝脱离了分子筛骨架,并造成USY的硅铝比变大[13]。
USY分子筛改性前后的N2物理吸附结果见表1。由表1可知:经过柠檬酸改性之后的DUSY比表面积较初始USY比表面积增大,介孔孔容也明显增加,但微孔孔容几乎没变。这表明利用柠檬酸对USY分子筛进行脱铝改性,能够达到增加介孔的效果。这是因为在USY分子筛制备过程中,会产生许多非骨架铝,这些非骨架铝的存在堵塞了分子筛孔道或覆盖其酸中心,不利于物质的扩散及物质与活性位的接触。而利用柠檬酸能够脱除大部分非骨架铝,在疏通其孔道的同时提高了酸性位的利用效率[14]。

图3 USY和DUSY的XRD(a)和FT-IR(b)谱图Fig.3 XRD patterns (a) and FT-IR spectra (b) of USY and DUSY

表1 改性前后分子筛的表面积及孔隙
表2为改性前后USY的Py-IR数据。由表2可以看出:USY经柠檬酸改性后,DUSY的B酸中心有所减少,L酸中心增加,L/B比例明显提高。L酸的增加能够提高USY的异构化能力,有利于EL的合成[11]。

表2 催化剂的Py-IR分析结果
利用NH3-TPD对其改性前后USY的总酸量及酸强度分布进行表征,结果见图4。从图4可以看出,USY和DUSY催化剂均出现2个脱附峰:150~250 ℃间的脱附峰对应弱酸中心,350~450 ℃间的脱附峰对应强酸中心。DUSY分子筛各处酸量与USY相比,弱酸量由0.573 mmol/g降到0.354 mmol/g,强酸量由0.618 mmol/g降到0.416 mmol/g,而总酸量则由1.191 mmol/g降到0.770 mmol/g。这可能是由于柠檬酸在脱除非骨架铝的时候,也脱除了少量的骨架铝。而分子筛的酸量是由其骨架铝和非骨架铝提供的,因而造成DUSY分子筛酸量的减少。另外,由于B酸中心的减少和L酸中心的增加,导致弱酸中心的酸强度减弱而强酸中心的酸强度增强,从而DUSY酸性中心的脱附峰也发生了稍微变化,低温峰和高温峰分别向低温和高温轻微的偏移。

图4 催化剂USY和DUSY的NH3-TPD图谱Fig.4 Characterization of catalyst USY and DUSY by NH3-TPD
2.3 反应条件对EL产率的影响
在确定了柠檬酸改性DUSY的基础上,对纤维素用量、反应温度、催化剂用量和反应时间对EL产率的影响进行了考察。在反应温度220 ℃、反应时间2 h、催化剂用量0.3 g时,考察了纤维素加入量对EL产率的影响,结果见图5。
由图5(a)可知:当纤维素加入量由0.2 g增加到0.6 g时,EL的产率逐渐增加,但增加幅度逐渐趋于水平;而当纤维素量超过0.6 g,EL的产率反而下降。这可能是由于较大的固液比不利于反应体系中的传质,而且催化剂的活性中心相比于纤维素的量也会下降,两者导致了纤维素转化合成EL产率的降低。
由图5(b)可知:在纤维素用量0.6 g、反应时间2 h、柠檬酸改性的DUSY用量0.3 g的条件下,随着反应温度的不断升高,EL的产率也逐渐增加。当温度在220 ℃时,EL的最大产率为34.2%;然而,随着温度的继续升高,EL产率呈下降趋势。这表明DUSY催化纤维素生成EL存在着适宜的反应温度,过高的温度会引起副反应的发生,从而导致EL产率的降低。这一现象与前期的研究结果相一致[10]。
由图5(c)可知:在纤维素量为0.6 g、反应温度220 ℃、时间2 h的条件下,当催化剂量为0.3 g时,EL的产率最大;随着DUSY量的继续增加,EL产率反而稍微下降。这说明当催化剂用量达到一定值时,活性中心数量足以满足反应的需要,而当催化剂量超过一定值后,反而促进了副反应的进行,不利于EL产率的提高[15]。
由图5(d)可知:在纤维素量0.6 g、催化剂量0.3 g、反应温度220 ℃时,EL产率随着反应时间的延长而增加。当反应时间为3 h时,EL产率达到最大,最大产率为35.7%,但继续延长反应时间则会导致EL产率的下降。因此,在纤维素催化合成EL的工艺过程中,需要选定适宜的反应时间。
2.4 柠檬酸改性的DUSY催化工艺的优化
从上述反应条件对EL产率的影响可以看出,各反应条件都存在着较适宜的范围。因此,为了得到适宜的催化工艺条件,利用响应面试验设计优化了DUSY催化纤维素合成EL的工艺条件。优化实验采用Box-Behnken中心组合进行设计,对纤维素加入量、催化剂量、反应温度及反应时间4个因素进行三水平选取(表3)。

表3 响应面分析实验因素水平表
利用Design Expert 8.0软件对实验数据进行拟合,可以得到EL产率与各因素之间的二次回归方程,见式(2)。

(2)
该模型的复相关系数R2为0.930 7,表明模型的相关性较好;其校正相关系数为0.861 4,说明86.43%的实验数据都是可以用模型进行解释;其中变异系数为6.61,说明该模型可以用于预测。根据式(2)可求出最佳工艺条件,对各个变量求偏导,然后用求解方程组,得到回归模型的稳定点(X1,X2,X3,X4)为(0.6,0.3,220,3),即纤维素醇解制备EL的最佳工艺条件:纤维素量0.6 g,催化剂用量0.3 g,反应温度220 ℃,反应时间3 h,模型理论EL的产率为35.99%。在优化出的最佳实验条件下重复试验,得到EL的产率为36.1%,与模型结果接近。
2.5 催化剂的重复使用
将反应后的DUSY经干燥焙烧活化后重复利用。在纤维素加入量为0.6 g、DUSY用量为0.3 g、反应温度为220 ℃以及反应时间为3 h的条件下,考察DUSY回收次数对EL产率的影响,结果见图6。由图6可以看出:EL的产率随着回收次数的增加而有所下降,同时,实验中也发现催化剂颜色逐渐加深,可能是DUSY附着的黑色腐殖质引起的。DUSY经过4次重复利用后,其催化纤维素合成EL的产率均在30%以上,与未改性USY的EL产率(14.9%)相比有了显著提高,这进一步表明柠檬酸脱铝改性USY是促进纤维素合成EL的一种有效方式。

图6 催化剂回收次数对EL产率的影响Fig.6 Effects of catalyst recovery times on EL yield
2.6 不同碳水化合物的考察
以DUSY为催化剂,催化不同的碳水化合物(果糖、葡萄糖、蔗糖和菊糖)合成EL,结果如图7所示。从图7可以看出:DUSY对不同的碳水化合物都具有良好的催化效果,其中果糖转化生成EL的产率最高,EL产率为50.7%;而葡萄糖的EL产率为41.0%,表明果糖更易被醇解转化生成EL,这也与前人的研究结论相一致[16-17]。此外,蔗糖和菊糖的分子中都含有果糖,因此有利于EL的生成,二者的EL产率均高于葡萄糖,分别为47.9%和42.9%。纤维素是由葡萄糖构成的大分子碳水化合物,在催化合成EL的过程中,需要解聚为葡萄糖后才能进行催化转化,因此,相比于其他碳水化合物合成EL会更加困难,这也是纤维素类生物质催化合成EL存在的共性问题,这需要针对纤维素生物质结构特点,开发出催化能力更强、选择性更好的固体酸催化剂。

图7 DUSY催化不同碳水化合物合成ELFig.7 DUSY catalyzes different carbohydrates to EL synthesis
3 结论
以0.2 mol/L的柠檬酸对USY进行脱铝改性,得到的DUSY能够有效催化纤维素合成EL。通过对改性前后USY的表征发现,柠檬酸改性能够丰富USY的多孔结构,增强L酸位,提高其催化纤维素合成EL的活性。在纤维素加入量0.6 g、DUSY量0.3 g、反应温度220 ℃和反应时间3 h的条件下,EL的产率达到36.1%。经过4次重复利用,DUSY仍具有较高的催化活性。当以果糖、葡萄糖、蔗糖和菊糖为原料时,EL的产率分别为50.7%、41.0%、47.9%和42.9%。为了进一步促进纤维素生物质催化合成EL,开发出催化能力更强、选择性更高的固体酸催化剂将是后续研究的主要方向。
[1] AHMAD E,ALAM M I,PANT K K,et al.Catalytic and mechanistic insights into the production of ethyl levulinate from biorenewablefeedstocks[J].Green Chem,2016,18:4804-4823.
[2] 孔鹏飞,徐桂转,常春,等.生物质直接醇解制备液体燃料的研究进展[J].现代化工,2015,35(9):43-47.
[3] TAN J,LIU Q,CHEN L,et al.Efficient production of ethyl levulinate from cassava over Al2(SO4)3catalyst in ethanol-water system[J].J Energy Chem,2017,26(1):115-120.
[4] 孙培勤,李博,常春.固体酸催化生物质制备乙酰丙酸酯的研究进展[J].化工新型材料,2012,40(6):14-16.
[5] 常春,邓琳,戚小各,等.固体催化剂在生物质转化乙酰丙酸和乙酰丙酸酯应用的研究进展[J].林产化学与工业,2017,37(2):1-13.
[6] KUBICKA D,KIKHTYANIN O.Opportunities for zeolites in biomass upgrading-lessons from the refining and petrochemical industry[J].Catal Today,2015,243:10-22.
[7] SARAVANANURUGAN S,PANIAGUA M,MELERO JA,et al.Efficient isomerization of glucose to fructose over zeolites in consecutive reactions in alcohol and aqueous media[J].J Am Soc,2013,135:5246-5249.
[8] SARAVANAMURUGAN S,RIISAGER A.Zeolite catalyzed transformation of carbohydrates to alkyl levulinates[J].ChemCatChem,2013,5:1754-1757.
[9] 孙培勤,赵世强,常春,等.固体酸USY催化纤维素生成乙酰丙酸乙酯的实验研究[J].郑州大学学报(工学版),2015,35(3):22-26.
[10] 李博,常春,朱伟娜,等.固体酸催化纤维素生成乙酰丙酸乙酯的试验研究[J].太阳能学报,2015,36(7):1768-1772.
[11] 安冉,孔鹏飞,徐桂转,等.脱铝超稳Y沸石负载Cu催化纤维素醇解合成乙酰丙酸乙酯[J].化工学报,2016,67(11):4643-4651.
[12] ZHOU L,ZHAO H,CUI L,et al.Promotion effect of mesopore on the conversion of carbohydrates to methyl levulinate over H-USY zeolite[J].Catal Commun,2015,71:74-78.
[13] 黄朝晖,刘乃旺,姚佳佳,等.USY分子筛表面酸性的调变及其在催化脱除芳烃中烯烃的应用[J].化工进展,2016,35(1):138-144.
[14] 汪颖军,孙羽佳,所艳华,等.超稳Y分子筛改性的研究进展[J].硅酸盐通报,2015,34(11):3243-3246.
[15] MORALES G,OSATIASHTIANI A,HERNANDEZ B,et al.Conformal sulfated zirconia monolayer catalysts for the one-pot synthesis of ethyl levulinate from glucose[J].Chem Commun,2014,50:11742-11745.
[16] CHEN J,ZHAO G,CHEN L.Efficient production of 5-hydroxymethylfurfural and alkyl levulinate from biomass carbohydrate using ionic liquid-based polyoxometalate salts[J].RSC Adv,2014,4(8):4194-4202.
[17] LIU B,ZHANG Z,HUANG K,et al.Efficient conversion of carbohydrates into 5-ethoxymethylfurfural in ethanol catalyzed by AlCl3[J].Fuel,2013,113:625-631.

