冠心病合并2型糖尿病与单纯冠心病发病机制及危险因素分析
,,,
·心血管病临床观察/研究·
冠心病合并2型糖尿病与单纯冠心病发病机制及危险因素分析
王婧文,孔维颖,白云浩,王显
目的探讨冠心病合并2型糖尿病与单纯冠心病发病机制及危险因素。方法选择2015年10月—2016年10月在北京中医药大学附属东直门医院心内科病房住院的冠心病合并2型糖尿病病人100例(糖尿病组);不合并糖尿病的单纯冠心病病人100例(非糖尿病组)。分析2型糖尿病合并冠心病的危险因素。结果与非糖尿病组比较,糖尿病组冠心病症状总积分、是否有高血压、血糖和三酰甘油差异有统计学意义(P<0.05)。结论血糖可增加140%的冠心病合并糖尿病发病风险;三酰甘油升高可增加170%的冠心病合并糖尿病发病风险。合并高血压是冠心病合并2型糖尿病的危险因素,但不增加冠心病合并2型糖尿病的发病风险;中医主症总积分与冠心病合并糖尿病的发病呈正相关。
冠心病;2型糖尿病;发病机制;危险因素
冠状动脉粥样硬化性心脏病是指冠状动脉发生粥样硬化导致管腔狭窄或闭塞,引起心肌缺血缺氧或坏死而导致的心脏病,简称冠心病,也称缺血性心脏病[1]。2型糖尿病又称为非胰岛素依赖性糖尿病,是临床主要表现为胰岛素抵抗伴胰岛素相对不足的异质性较大的一类疾病。心血管事件是2型糖尿病的主要死亡原因,其中高血糖是2型糖尿病发生心血管事件独立危险因素[2]。除高血糖危害外,2型糖尿病病人常存在其他多种心血管疾病的高危因素,如高血压、高脂血症、肥胖等,极大增加心血管事件危险性。
1 资料与方法
1.1 病例来源 选择2015年10月—2016年10月在北京中医药大学附属东直门医院心内科病房住院的冠心病合并2型糖尿病病人100例(糖尿病组);不合并糖尿病的单纯冠心病病人100例(非糖尿病组)。
1.2 诊断标准 冠心病诊断参照年国际心脏病学会和协会及世界卫生组织临床命名标准化联合专题组报告《缺血性心脏病的命名及诊断标准》。经冠状动脉造影检查证实至少有一支血管狭窄≥50%诊断冠心病。糖尿病诊断标准采用WHO(1999年)糖尿病诊断标准。糖代谢状态分类标准具备以下条件之一的即可诊断为糖尿病:①高血糖导致的多饮、多食、多尿、体重下降、皮肤瘙痒、视力模糊等急性代谢紊乱临床表现加上随机血糖检测≥11.1mmol/L;②空腹血糖(至少8h未进食热量)≥7.0mmol/L;葡萄糖负荷后2h血糖≥11.1mmol/L无糖尿病症状者,需改日重复检查。
1.3 方法 全部研究对象均进行详细病史采集和相应血生化指标测定。病史采集包括:病案号、姓名、性别、年龄、过敏史、有无经皮冠状动脉介入术(PCI)、既往史、高血压病史(高血压入选标准:既往有明确高血压病;本次入院确诊者)、高脂血症病史(高脂血症入选标准:既往有明确高脂血症;本次入院确诊者)、冠心病病程(本次确诊的冠心病,病程为0年;②冠心病病程不满1年者均记为1年)、糖尿病病程、吸烟史(每日吸烟5支以上,超过1年确定为吸烟者)、饮酒史(每日饮酒50g以上,超过1年确定为饮酒者)。辅助检查:血清总胆固醇(TC)、三酰甘油(triglycerides,TG)、低密度脂蛋白胆固醇(lowdensitylipoproteincholesterol,LDL-C)、高密度脂蛋白胆固醇(highdensitylipoproteincholesterol,HDL-C)、空腹血糖(GLU)、尿素氮(bloodureanitrogen,BUN)、肌酐(creatinine,Cr)、尿酸(uricacid,UA)。
1.4 冠心病的发病机制 动脉粥样硬化(AS)是冠心病的主要病理基础。解释AS发病机制的学说有脂质浸润学说、血管平滑肌细胞克隆学说、氧化应激学说、血小板功能亢进学说、血栓形成学说、免疫功能异常学说、内皮损伤反应学说、炎症学说等。
1.4.1 脂质浸润学说 脂质浸润学说是1856年由Virohow首先提出,此学说自提出后经过不断验证得到证实。该学说认为冠状动脉粥样硬化的形成原因是血液增高的脂质以LDL-C、极低密度脂蛋白胆固醇(VLDL-C)或其残粒方式侵入动脉壁,堆积在平滑肌细胞、弹性纤维及胶原纤维之间,使平滑肌细胞增生并吞噬大量的脂质形成泡珠细胞。LDL-C与动脉壁多糖结合产生沉淀,刺激纤维组织增生。上述物质相合形成粥样斑块。
1.4.2 平滑肌细胞克隆学说 平滑肌细胞克隆学说认为每一个斑块都由一个突变的平滑肌细胞衍化而来,一个斑块相当于被病毒或化学因素转化的平滑肌细胞增生而成的良性平滑肌瘤。同时强调平滑肌细胞的单克隆繁殖,使之不断增生并吞嗟脂质,形成动脉粥样硬化。
1.4.3 氧化应激学说 氧化应激是指机体收到各种有害刺激时,体内或细胞内活性氧(ROS)生成速率大于清除速率,在体内蓄积,ROS对构成生物体的脂类、蛋白质、核酸产生氧化作用。氧化应激导致氧化低密度脂蛋白(ox-LDL)水平升高,导致构成生物膜的脂质过氧化,促进AS形成及发展[3]。
1.4.4 血小板功能亢进学说 血小板参与动脉粥样硬化斑块形成的全部过程,即血小板本身具有致斑块性,血小板参与体内血脂调节、促炎症及致氧化应激作用,上述过程均可在一定程度上诱发动脉硬化和粥样斑块形成[4]。
1.4.5 内皮损伤反应学说 “内皮损伤反应学说”是近年来备受关注的理论。内皮细胞是一种半透膜,能促进水和小分子物质在组织与血液中交换,是血管腔和血管壁之间的重要屏障,为血流提供光滑的表面,且在凝血和纤溶系统发挥巨大作用。血管内皮细胞可分泌多种生物活性物质,这些因子可预防血小板聚集、防止中性粒细胞等炎症细胞在血管内壁的黏附、调节血管平滑肌细胞的增殖和迁移。内皮损伤可表现为多种内皮功能紊乱,引起动脉硬化粥样斑块的形成。
1.4.6 炎症学说Ross[5]于1999年提出“AS是一种炎症性疾病”,指出AS是具有慢性炎症反应特征的病理过程,其发展伴随炎症反应。由于血管内皮细胞和平滑肌细胞受到各种危险因子如病毒、免疫复合物、机械损伤、ox-LDL的损伤,使血管局部产生慢性炎性增生性反应,形成动脉粥样硬化斑块。
1.5 冠心病合并2型糖尿病的发病机制
1.5.1 氧化应激学说 2004年Ceriello教授提出共同土壤学说,即氧化应激是胰岛素抵抗、2型糖尿病和心血管疾病的共同发病基础。氧化应激增强是冠心病伴2型糖尿病的主要发病机制之一。高血糖导致体内糖基化蛋白质的氧化、脂肪的氧化等氧化还原反应增多,体内产生大量氧自由基,细胞内自由基生成、清除失衡,引起氧化应激;氧化应激可直接影响心肌细胞功能,使成纤维细胞和内皮细胞功能受损,其中内皮源性血管舒张因子即一氧化氮(NO)介导的内皮依赖性血管舒张功能障碍显著[6]。内皮型一氧化氮合酶(eNOS)是调控NO产生的关键酶,其激活与PI3K/PKB通路有关;同时,血管内皮细胞表达胰岛素受体,eNOS的活性可被胰岛素激活,促使内皮细胞释放NO。高血糖时,糖基化产物增多,抑制PI3K活性及eNOS表达,同时体内存在的胰岛素抵抗抑制eNOS的活化,最终导致NO释放减少,血管舒张功能异常,导致血管功能障碍和动脉粥样硬化形成。内皮细胞凋亡是冠心病伴2型糖尿病的始发事件[7],动脉粥样硬化是受累动脉的病变从内膜开始,首先局部有脂质和复合糖类积聚或纤维组织增生和钙质沉着,且动脉中层的逐渐退变,进一步病变是斑块内出血、斑块破裂及局部血栓形成。内皮细胞凋亡损害血管内皮结构,影响内皮细胞的正常功能,促进血管病变的发生。
1.5.2 糖基化终产物(AGEs)学说 关于冠心病合并糖尿病的发病机制,除氧化应激学说之外,研究较多的是糖基化终产物学说。糖基化产物包括早期糖基化产物和糖基化终产物,早期糖基化产物是高糖环境下葡萄糖与活性氨基酸基团发生化学反应产物,包括糖化血红蛋白(HbA1c)和糖化白蛋白(GA);早期糖基化产物刺激单核巨噬细胞和血管内皮细胞表达黏附分子、分泌促炎症细胞因子及基质金属蛋白酶,加速脂质斑块的形成和破裂[8]。在高血糖状态下,体内葡萄糖、葡萄糖核酸、果糖等物质与体内如胶原蛋白、基质蛋白等蛋白质发生非酶促糖基化反应,最终生成糖基化终末产物[9]。
AGEs主要通过两个途径发挥生物学效应:一方面通过对蛋白质、脂质、核酸等的直接修饰改变其结构功能;二是通过与特异受体结合导致机体的病理改变[10]。AGEs可促进单核细胞释放细胞因子,如白介素-1(IL-1),肿瘤坏死因子-α(TNF-α)等,这些因子可引起血管壁增厚,管腔变窄,血管弹性下降;IL-1与TNF-α可上调内皮细胞黏附分子的表达,增加单核细胞浸润、放大炎症反应,加速动脉粥样硬化形成。
1.5.3 脂质代谢紊乱TG增高,HDL-C降低,LDL-C正常或轻度增高是2型糖尿病病人脂质代谢紊乱的特征。胰岛素抵抗可通过升高血清游离饱和脂肪酸引起斑块易损,糖尿病病人在胰岛素抵抗状态下血清游离饱和脂肪酸密度较高,游离脂肪酸和TG等脂肪颗粒在心肌细胞内聚积增加,LDL-C活性增强,高脂血症又引起胰岛β细胞损伤加重胰岛素抵抗,这种恶性循环引起斑块内积累的脂肪酸增多,促进动脉粥样硬化进展。这类病人脂质斑块通常更不稳定,易发生斑块破裂[11]。
1.6 统计学处理 相关危险因素采用Logistic回归分析。
2 结 果
2.1 相关危险因素单因素Logistic回归分析 采用单因素非条件Logistic回归,纳入10个分析变量:年龄、冠心病病程、性别(女=1,男=2)、冠心病症状总积分、吸烟(否=0,是=1)、高血压(否=0,是=1)、GLU、TG、LDL-C、HDL-C。有冠心病症状总积分、高血压、GLU和TG(P<0.05)。糖尿病组与非糖尿病组比较:高血压可增加233%的冠心病合并糖尿病发病风险(OR=3.33,95%CI=1.51~7.32);血糖可增加62%的冠心病合并糖尿病发病风险(OR=1.62,95%CI1.33~1.98);三酰甘油异常可增加138%的冠心病合并糖尿病发病风险(OR=2.38,95%CI1.38~4.10)。详见表1。
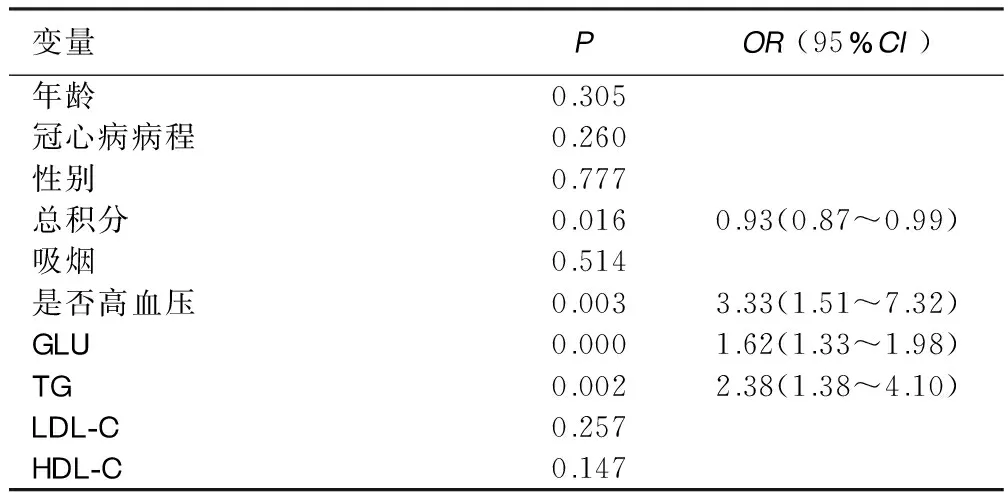
表1 单因素Logistic回归分析
2.2 相关危险因素二元Logistic回归分析 选择单因素Logistic回归分析中P<0.05变量进行二元Logistic回归,纳入4个变量:总积分、高血压(否=0,是=1)、GLU、TG。糖尿病组与非糖尿病组比较:GLU可增加140%的冠心病合并糖尿病发病风险(OR=1.62,95%CI1.33~1.98);TG异常可增加170%的冠心病合并糖尿病发病风险(OR=2.38,95%CI1.38~4.10)。详见表2。
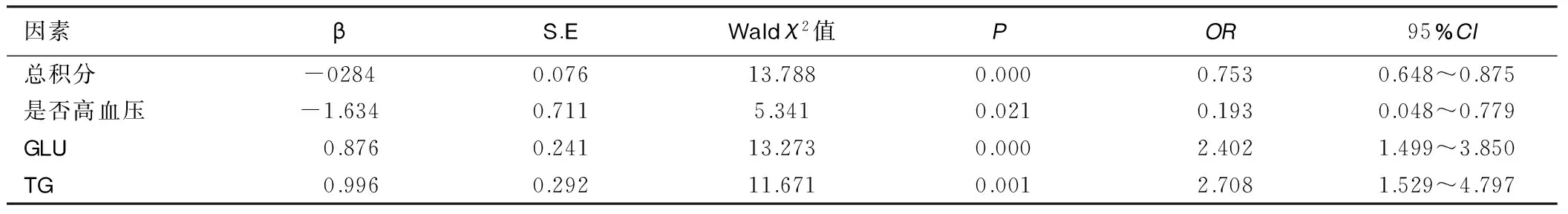
表2 相关危险因素二元Logistic回归分析
3 讨 论
本研究结果可知,两组病人冠心病症状总积分、是否有高血压、GLU和TG是冠心病合并2型糖尿病的危险因素,GLU可增加140%的冠心病合并糖尿病发病风险,TG异常可增加170%的冠心病合并糖尿病发病风险。
有研究表明,血脂异常是心血管疾病发生发展的独立危险因素[12],而血脂异常亦与糖尿病高风险密切相关[13]。因而冠心病合并糖尿病病人均合并继发性血脂紊乱,血糖代谢与血脂代谢密切相关。高血糖症可使血脂尤其是LDL-C及TG水平升高,这由于2型糖尿病通常与肥胖、胰岛素抵抗相关,引起脂肪组织释放大量游离脂肪酸及脂蛋白脂酶活性下降。通常导致TG、TC、LDL-C升高,HDL-C降低等,使血管壁和内皮细胞脂质沉积增多清除减少,增加AS发生风险[14]。
高血压在冠心病合并糖尿病病人中占40%~60%,高血压尤其是舒张压增高被认为是本病的独立危险因素[15]。张磊等[16]研究表明:血压与2型糖尿病合并冠心病之间存在关联性,随着病人血压升高,其合并冠心病危险性增大。经糖尿病病程调整后关联仍存在,但经高血压史调整后关联消失,既往有高血压病史的2型糖尿病病人合并冠心病危险性是无高血压病史者3倍,随着高血压病程延长,2型糖尿病病人合并冠心病的危险性逐渐增加。胰岛素抵抗认为是高血压的发病机制之一,持续性血压升高,可使动脉后壁及分支开口处由于血流冲击力较大造成机械性损伤,或使动脉壁反复痉挛,管壁缺氧,内皮细胞变性,进一步导致AS发生[17]。
高血糖病人冠心病发生率高于正常人群:Hu等[18]进行多中心大型临床试验对入院的冠心病病人进行糖耐量试验筛查,发现冠心病病人有87.4%同时合并糖代谢异常。高血糖很大程度促进冠心病发生,高血糖可引起动脉血管壁的胶原蛋白及脂蛋白中的载脂蛋白非酶糖化和氧化,改变血管壁的物理性质,防碍脂质的正常代谢。高血糖可抑制内皮细胞受损后的修复,致凝血系统异常及纤溶系统障碍,这些都加速动脉粥样硬化进程。餐后高血糖与大血管并发症关系密切,且与心血管事件及其伴随的病死率之间有独立的相关性。
综上所述,根据冠心病合并糖尿病的发病机制及危险因素研究,高血糖可加速冠状动脉病变进展,若合并高血压、高脂血症等,将增加心血管事件危险性。因此治疗冠心病合并糖尿病时,可控制其发病机制,如积极保护内皮功能、抑制炎症细胞因子活性、抗血管内皮生长因子等。深入研究高血糖加速冠状动脉病变进展机制,关注冠心病合并糖尿病病人的治疗策略,可能有效减少糖尿病病人发生冠心病的风险。
[1] 葛均波,徐永健.内科学[M].北京:人民卫生出版社,2013:227.
[2] 郭颖,张思宁.冠心病合并2型糖尿病患者临床及冠状动脉造影对比分析[J].心肺血管病杂志,2010,29(3):218-219.
[3] 李震霄,邹洪梅,孟晓萍.氧化应激促进动脉粥样硬化机制研究进展[J].中国动脉硬化杂志,2009,17(8):702-705.
[4] 陈熤,李剑,施海明.血小板致动脉粥样硬化斑块形成的相关研究[J].国际心血管病杂志,2010,39(6):357-360.
[5]RossR.Atherosclerosisaninflammatorydisease[J].NewEnglJMed,1999,340(2):115.
[6] 魏聪,申锷,胡兵.糖尿病大血管病变的研究进展[J].上海交通大学学报(医学版),2010,30(10):1292-1296.
[7]TedguiA,MallatZ.Apoptosisasadeterminantofatherothrombosis[J].ThrombHaemost,2001,86(1):420-426.
[8]BartnikM,MalmbergK,NorhammarA,etal.Newlydetectedabnormalglucosetolerance:animportantpredictoroflong-termoutcomeaftermyocardialinfarction[J].EurHeartJ,2004,25(22):1990-1997.
[9] 刘杰,韦金儒.糖基化代谢终产物与动脉粥样硬化关系的研究进展[J].医学综述,2006,12(20):1275-1277.
[10] 牛丽丽,许玉韵.糖基化终末产物与急性冠状动脉综合征[J].中华老年心脑血管病杂志,2009,11(2):150-152.
[11]WinhoferY,KrssákM,JankovicD,etal.Short-termhyperinsulinemiaandhyperglycemiaincreasemyocardiallipidcontentinnormalsubjects[J].Diabetes,2012,61(5):1210-1216.
[12] 崔芳.糖尿病的年龄分布特点及患病年轻化相关因素分析[J].糖尿病新世界,2015(24):195-198.
[13] 金晔,王炜.血脂异常对糖尿病发病及相关危险因素的影响[J].中国实验诊断学,2011,15(5):860-862.
[14]NassarPO,WalkerCS,SalvadorCS,etal.Lipidprofileofpeoplewithdiabetesmellitustype2andperiodontaldisease[J].DiabetesResClinPract,2012,96(1):35-39.
[15] 唐晓君,张素华,李革,等.老年人群糖尿病和IGT患病率及其影响因素[J].现代预防医学,2005,32(12):1614-1616.
[16] 张磊,王岩,齐秀英.高血压与2型糖尿病合并冠心病[J].实用糖尿病杂志,2007,3(2):27-29.
[17] 黄通,刘志慧,周华,等.2型糖尿病合并冠心病患者血管病变危险因素分析[J].中国热带医学,2011,11(3):372-373.
[18]HuDY,PanCY,YuJM,etal.TherelationshipbetweencoronaryarterydiseaseandabnormalglucoseregulationinChina:theChinaHeartSurvey[J].EurHeartJ,2006,27(21):2573-2579.
R541.4 R256.2
B
10.3969/j.issn.1672-1349.2017.23.017
1672-1349(2017)23-2999-04
国家中医药管理局国家中医临床研究基地业务建设科研专项课题(No.JDZX2015208);国家自然科学基金(No.81273913)
北京中医药大学东直门医院(北京 100700)
王显,E-mailwx0515@hotmail.com
信息:王婧文,孔维颖,白云浩,等.冠心病合并2型糖尿病与单纯冠心病发病机制及危险因素分析J.中西医结合心脑血管病杂志,2017,15(23):2999-3002.
2017-04-28)
(本文编辑 薛妮)

