胃动脉介入联合替吉奥治疗16例晚期胃癌的疗效观察
马骖, 单宏杰, 梅天明, 贾兴胜, 包召玉, 芦亚楠
临床与基础研究
胃动脉介入联合替吉奥治疗16例晚期胃癌的疗效观察
马骖, 单宏杰, 梅天明, 贾兴胜, 包召玉, 芦亚楠
目的分析胃动脉介入联合替吉奥口服治疗晚期胃癌的近期疗效。方法2014年1月至2016年12月,安徽省宿州市立医院收治16例晚期胃癌患者,行胃动脉介入灌注治疗,每月1次,共2次。药物及剂量:氟尿嘧啶 750 mg/m2、表柔比星50 mg/m2、奥沙利铂130 mg/m2。介入后给予替吉奥口服,每次40 mg, 每天2次;持续口服20 d,休息10 d。3个月后评估疗效。临床疗效以症状改善评估,如腹痛,食欲缺乏,黑便症状缓解。病灶以腹部CT检查结果进行评估。结果转化手术9例,7例改变治疗方案。病理性完全缓解1例,完全缓解1例,部分缓解9例,病情稳定3例,病情进展2例。16例患者中,腹痛14例缓解11例,15例食欲缺乏患者缓解10例,隐血阳性10例患者全部缓解。症状得到有效控制,化疗不良反应较轻。结论晚期胃癌行动脉区域灌注联合替吉奥治疗,可提高晚期胃癌的缓解率,使部分患者获得转化手术治疗机会。该治疗方法不良反应轻,患者可耐受。
胃肿瘤; 药物疗法,联合; 投药,口服; 替吉奥; 晚期胃癌; 区域灌注化疗; 转化手术
胃癌发病率与死亡率在常见恶性肿瘤中居第2位,我国每年新发病例大约占全球的42%[1]。我国胃癌病例众多,但早期胃癌仅占10%左右,少数胃癌临床中心达到20%~25%,因此对大量进展期或晚期胃癌患者采取积极合理的治疗策略并进一步改善其生存率是我们面临的长期挑战[2]。对仅侵及胰腺或累及血管,没有腹膜播散或远处脏器转移的局部晚期胃癌,全身静脉化疗是其主要治疗方式之一。但这种治疗在病灶局部的药物有效浓度较低,使病灶缩小不理想,且患者不良反应大,不能达到预期结果[3]。胃动脉区域灌注介入化疗由于灌注药物直接作用于肿瘤的血管内皮细胞,局部药物浓度高,可使肿瘤明显缩小,使无法手术的病灶转化为可手术切除,明显改善患者的预后[4-5]。我们观察16例局部晚期胃癌患者行胃动脉区域灌注化疗联合低剂量替吉奥口服后转化手术的疗效,现报道如下。
1 资料与方法
1.1 一般资料 收集2014年1月至2016年12月安徽省宿州市立医院肿瘤外科经胃镜检查,并行活检病理诊断的进展期胃癌患者16例,均行增强螺旋CT薄层扫描检查进行分期。入选标准:① 临床分期Ⅲ期,部分Ⅳ期。无肿瘤腹腔内广泛播散;② 无梗阻及上消化道大出血等严重并发症;③ 肝、肾、心、肺等脏器功能无明显异常,KPS(Karnofsky,卡氏)评分>70分,可以耐受手术及化疗;④ 患者及家属同意进行动脉灌注化疗。其中男13例,女3例;年龄45~82岁,平均年龄60岁。病灶位于胃窦部4例,胃体小弯侧10例,胃食管结合部2例。病理类型:高分化腺癌4例,中低分化腺癌7例,未分化腺癌3例,印戒细胞癌2例。腹痛14例,食欲缺乏15例,大便隐血阳性10例。
1.2 治疗方法 采用Seldinger技术经股动脉穿刺插管,行腹腔动脉数字化血管造影,确定肿瘤的供血动脉后,实施超选择性动脉插管。如肿瘤位于胃底贲门部或胃体小弯侧,选择插管至胃左动脉;肿瘤位于胃窦大弯侧,选择胃十二指肠动脉。氟尿嘧啶 750 mg/m2、表柔比星50 mg/m2、奥沙利铂130 mg/m2经动脉灌注给药,然后用明胶海绵颗粒或弹簧圈作为栓塞剂进行动脉栓塞。治疗前后注射止吐药物昂丹司琼8 mg,术后严密观察生命体征的变化,并常规给予胃黏膜保护剂、止痛和支持治疗。全部介入手术均由同一治疗组完成。1周后开始口服替吉奥,每次40 mg,每日2次,连用20 d,停药10 d为1个周期。每例患者介入治疗2次,替吉奥口服3个周期。观察肿瘤缩小情况,是否可转化手术。
1.3 不良反应评判 观察治疗后患者恶心、呕吐、腹泻及血液毒性等情况,按照世界卫生组织抗癌药物急性及亚急性毒性反应分度标准分为0~Ⅳ度。
1.4 疗效判定 疗效评价包括原发肿瘤、淋巴结和转移灶。疗效根据2000年公布执行的RECIST标准评估[6]:分为完全缓解(CR)、部分缓解(PR)、病情稳定(SD)、病情进展(PD)。有效率(RR)为PR加CR。疗效判定依据螺旋CT检查,部分患者加做MRI评估。手术标本中无肿瘤病灶残留或仅有原位癌残留,则判定为病理性完全缓解(PCR)。
2 结果
2.1 疗效 治疗3个周期后评估,如病灶缩小明显则转化手术,不明显则继续口服至6个周期评估。治疗后临床症状均有明显改善,腹痛、腹胀症状缓解或消失,体重增加,患者贫血症状明显改善。14例腹痛患者缓解11例,15例食欲缺乏患者缓解10例,10例大便隐血阳性患者全部转阴。治疗结束后复查CT等以评价疗效。转化手术9例;7例改变治疗方式,更换化疗方案,再行局部放疗。依据评价标准,本组病例病理性完全缓解1例、完全缓解1例、部分缓解9例、病情稳定3例、病情进展2例。见表1。
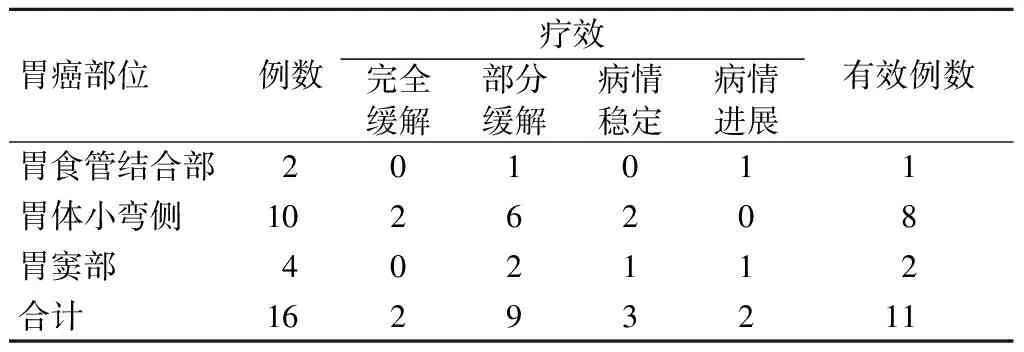
表1 16例胃癌患者部位及疗效(例)
2.2 不良反应 本组16例患者无因化疗不良反应而终止治疗,亦未出现化疗相关死亡者。化疗不良反应在血液系统中的白细胞减少均在Ⅱ度以内。贫血Ⅰ度6例、Ⅱ度2例;白细胞减少Ⅰ度8例、Ⅱ度3例;血小板减少Ⅰ度3例;消化道反应恶心、呕吐、腹泻Ⅰ度8例、Ⅱ度2例;肝功能异常Ⅰ度4例;神经毒性Ⅰ度3例。
2.3 典型病例 如图1至图3所示,患者男,81岁,病灶位于胃底小弯侧,胃镜活检病理为中分化腺癌。
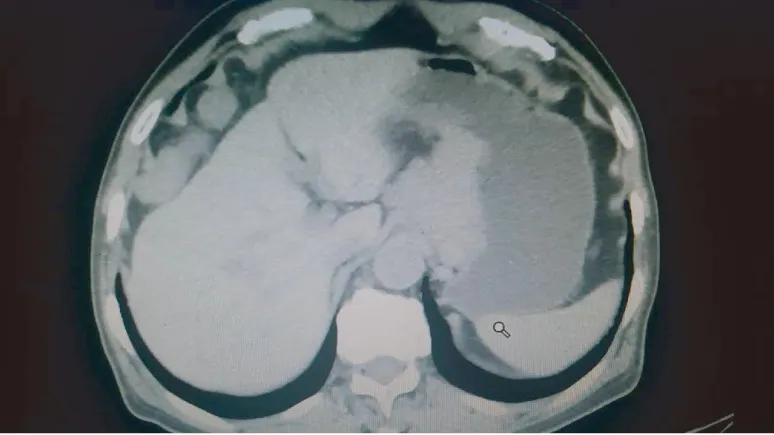
图1 治疗前,CT显示病灶位于胃小弯侧,累及胃左血管,术前评估无法切除,给予新辅助转化治疗
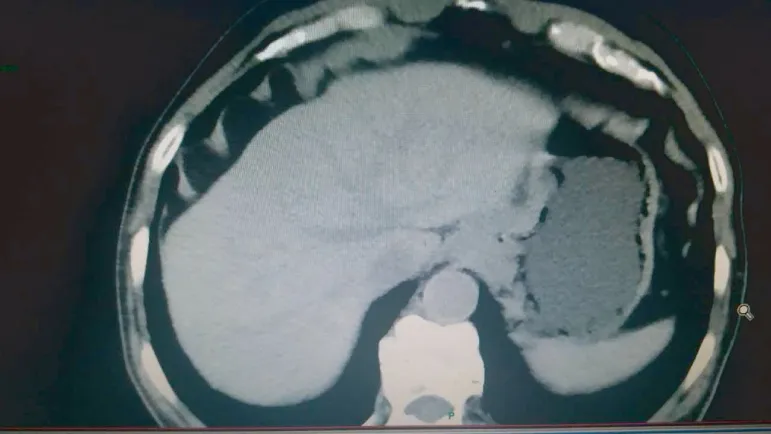
图2 治疗3个月后,经胃左血管两次介入治疗,口服替吉奥1个月后CT复查,病灶缩小50%
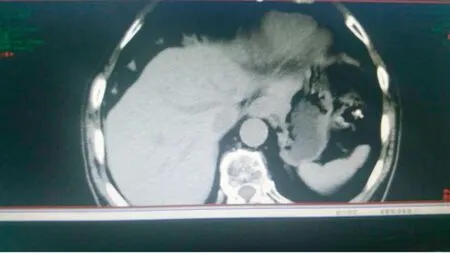
图3 治疗6个月后,继续口服替吉奥3个月CT复查,病灶缩小90%
3 讨论
近年来,区域动脉灌注化疗逐渐受到重视,尤其是对局部晚期胃癌的术前转化治疗[7]。其优点在于:①有效杀灭肿瘤细胞,明显降低肿瘤负荷,减轻了组织水肿,使肿瘤缩小,提高手术切除率,使不可手术转化为可手术。②较早的全身治疗,可控制术前存在的微小病灶及亚临床灶,抑制由于手术创伤引起的肿瘤增大,减少术后复发转移的可能。③术前疗效的判定有助于术后化疗方案的选择和预后评估。④在原发病灶的血管供应未被切断之前,经区域动脉进入肿瘤组织的化疗药物浓度比周围静脉或口服给药更高。有研究显示,在临床切除的组织标本中,胃左动脉灌注化疗组的肿瘤组织和周围淋巴结组织中的氟尿嘧啶浓度为静脉化疗组的19倍[8]。⑤经肿瘤供血动脉灌注的化疗药物经伴行静脉流向门静脉,在门静脉内的药物浓度也较高,有助于预防和早期治疗肝转移。⑥相当于体内药敏试验,可得到肿瘤的药物敏感资料,为术后化疗选择敏感的抗肿瘤药物提供依据。
区域动脉灌注化疗的机制是诱导癌细胞凋亡[9],抑制癌细胞的增殖。但其抑制癌细胞增殖是短暂的,7~10 d后会出现反跳现象,又进入下一增殖期。故而我们选择区域动脉灌注联合口服替吉奥,介入后低剂量连续口服20 d,休息10 d的治疗方法,作为有效补充。替吉奥与奥沙利铂同时还有互补性抑制的协同作用。临床正常替吉奥剂量80 mg/次,每天2次,连续口服14 d,休息1周,但患者大多不能耐受,使治疗终止。而每次40 mg低剂量的持续应用,患者不良反应轻,疗程多能完成。有效缓解多在3个月后,完全缓解有时在半年后。本组研究中不良反应主要表现为白细胞降低和消化道反应,对症处理后均缓解。无1例患者因化疗不良反应而终止治疗。日本JACCRO GC.01试验对49例肿瘤侵及浆膜的胃癌患者采用S-1加顺铂的术前辅助化疗方案,结果显示病理缓解率39%,无1例完全缓解[10]。国外研究表明,对于不能施行手术的局部进展期或晚期的胃癌患者可以通过综合治疗的方式获得接受根治性手术切除的机会。转化手术后获得较长的术后生存。其3年总生存率可达40%[11-12]。徐幼龙等[13]报道区域动脉灌注化疗后,肿瘤与邻近器官间疏松,与血管间浸润程度减轻,肿瘤界限清晰,解剖分离较易,使转化手术率得以提高。本文结果显示,16例中完全缓解2例,其中1例病理缓解;镜下见广泛组织坏死,周边炎症改变,部分纤维组织增生,未见明显的癌组织。本文病例转化手术9例,7例改变治疗方案。
综上所述,局部晚期胃癌行区域动脉灌注加替吉奥低剂量口服转化治疗安全有效,无严重不良反应发生,组织学疗效确切,可降低分期,提高手术切除率,部分转化手术成功。近期疗效较好。由于研究入组病例较少,对于转化治疗的疗效评价标准,手术时机的选择,灌注方法的选择、次数,替吉奥口服的疗程,是否联合局部放疗以及远期治疗效果还需进一步观察。
[1] Ferlay J,Soerjomataram I,Dikshit R.Cancer incidence and mortality worldwide: sources,methods and major patherns in GLOBOCAN 2012[J].Int J Cancer.2015 Mar 1;136(5):E359-E386.
[2] 朱正纲.胃癌腹膜转移转化性治疗的临床意义[J].中国肿瘤外科杂志,2016,8(4):213-216.
[3] Schuhmacher C, Gretschel S, Lordick F, et al. Neoadjuvant chemotherapy compared with surgery alone for locally advanced cancer of the stomach and cardia: European Organisation for Research and Treatment of Cancer randomized trial 40954[J]. J Clin Oncol, 2010,28(35):5210-5218.
[4] Zhang J, Chen RX, Zhang J, et al. Efficacy and safety of neoadjuvant chemotherapy with modified FOLFOX7 regimen on the treatment of advanced gastric cancer[J]. Chin Med J (Engl), 2012,125(12):2144-2150.
[5] 高峰,黄祥忠,任冬青,等.经动脉灌注化疗联合不同化疗方法治疗进展期胃癌的60例对照研究[J].介入放射学杂志,2013,22(10):857-859.
[6] Therasse P, Arbuck SG, Eisenhauer EA, et al. New guidelines to evaluate the response to treatment in solid tumors. European Organization for Research and Treatment of Cancer, National Cancer Institute of the United States, National Cancer Institute of Canada[J]. J Natl Cancer Inst, 2000,92(3):205-216.
[7] 吴震峰, 朱文强, 曹勤洪, 等. 区域动脉灌注化疗在进展期胃癌短程新辅助化疗中的应用[J].中华胃肠外科杂志,2014,17(11):1092-1095.
[8] 弥海宁, 何科基, 杨言苹, 等. 进展期胃癌术前动脉灌注化疗临床疗效观察[J].中国肿瘤临床,2009,36(11):613-616.
[9] 胡阳.术前区域动脉灌注化疗对进展期胃癌患者血清学指标及肿瘤组织中凋亡基因表达的影响[J].海南医学院学报,2015,21(6):808-810,814.
[10] Yoshikawa T, Sasako M, Yamamoto S, et al. Phase II study of neoadjuvant chemotherapy and extended surgery for locally advanced gastric cancer[J]. Br J Surg, 2009,96(9):1015-1022.
[11] Kinoshita J,Fushida S,Tsukada T,et al.Efficacy of conversion gastrectomy following docetaxel, cisplatin, nds-1therapyin potentially resectable stage IV gastric cancer[J].Eur J Surg Oncol. 2015,41(10):1354-1360.
[12] Ratosa I, Oblak I, Anderluh F, et al. Preoperative treatment with radiochemotherapy for locally advanced gastroesophageal junction cancer and unresectable locally advanced gastric cancer[J]. Radiol Oncol, 2015,49(2):163-172.
[13] 徐幼龙, 周金良, 金雪熙, 等. 晚期胃癌术前选择性动脉内介入治疗[J].中国癌症杂志,2003,13(1):57-58,66.
234000 安徽 宿州,宿州市立医院 肿瘤外科(马骖, 单宏杰, 梅天明, 贾兴胜, 包召玉); 介入科(芦亚楠)
马骖,Email:symc924@126.com
10.3969/j.issn.1674-4136.2017.05.011
1674-4136(2017)05-0314-03
2017-02-24][本文编辑:钦嫣]

