单发直径≤3 cm肝肿瘤No-touch射频消融治疗的安全性及近期疗效分析(附50例报告)
柴跃龙 李昆 俞仁涛 邹孟达 马宽生
·论 著·(临床实践)
单发直径≤3 cm肝肿瘤No-touch射频消融治疗的安全性及近期疗效分析(附50例报告)
柴跃龙 李昆 俞仁涛 邹孟达 马宽生
目的探讨No-touch射频消融术(radiofrequency ablation,RFA)治疗直径≤3 cm单发肝肿瘤的安全性和疗效。方法2015年9月至2017年6月采用cooltip电极对直径小于3 cm单发肝肿瘤50例病人进行No-touch RFA治疗。其中,治疗原发性肝癌49例(初发31例、复发18例),转移性肝癌1例。肿瘤平均直径1.8 cm,治疗前、后检查肝功能、增强CT扫描、磁共振检查、超声造影以及细针肝穿刺活检。观察RFA治疗时间、次数和术后住院时间,RFA治疗后的并发症以及肿瘤完全毁损率,并随访病人的生存情况。结果50例病人共行No-touch RFA治疗51次,其中1例病人1个月内连续治疗2次。每例平均为1.02次;每次治疗时间平均为8.2 min;术后平均住院时间为3.2 d。No-touch RFA治疗后1个月内复查CT或磁共振,单次治疗后的肿瘤完全毁损率为98.0%,甲胎蛋白(AFP)阳性的22例病人在No-touch RFA治疗后6~12个月内有14例转阴,5例明显下降。50例病人随访时间从2015年9月开始至2017年6月止,其总体生存率为100%,术后总体无瘤生存率为90.0%(45/50)。结论No-touch RFA对直径小于3 cm的单发肝肿瘤的治疗是一种微创、安全有效的方法。
肝癌; 经典射频消融; No-touch射频消融
随着影像学诊断水平不断发展以及肝病病人的肝癌筛查意识逐年提高,小肝癌诊断率及小病灶的转移性肝癌发现率逐年提高[1]。经典射频消融(classic-radiofrequency ablation, C-RFA)作为治愈性手段的潜质正在日益凸显,它可以治疗直径小于3 cm的肝癌,其安全性已获得国内外证实,且疗效与手术切除相近[2-3]。然而RFA术后高复发率是C-RFA治疗肝癌所面临的最主要难题,原因可能是C-RFA直接穿刺肿瘤并在治疗过程中促使肿瘤内产生高压环境,不符合肿瘤外科的无瘤原则,可能会加速肿瘤细胞的微小转移[4]或肿瘤干细胞的播散[5],且可能毁损范围较小而无法保证足够的安全消融边缘[6]。从而可能增强了肝癌的残留及复发转移。
No-touch RFA是近年提出的治疗小肝癌的最新的术式,凭借术后低复发率的优势,已成为国际上RFA研究的热点领域[7]。它是将多根射频电极穿刺到肿瘤周边,通过射频发生器同时或几乎同时输出射频波,将多根电极之间的肿瘤组织消融的新技术。它严格遵循无瘤原则,在手术过程中射频针的操作均不会直接接触肿瘤本身,是很有前景的一种新型实体肿瘤消融治疗技术。我院率先在国内应用No-touch RFA治疗肝肿瘤病人50例,同时通过回顾性研究评估No-touch RFA治疗直径小于3 cm的肝肿瘤的安全性和有效性。
资料与方法
一、一般资料
从2015年9月至2017年6月,我院采用No-touch RFA的方法治疗了50例肝肿瘤病人。包括原发性肝癌病人49例(其中初发小肝癌31 例,复发性肝癌18例)和1例结直肠癌术后肝转移的病人。入组标准:①经B超引导下肝活检,或经2个及以上的增强影像学临床诊断;②影像学显示肿瘤直径≤3 cm;③肿瘤未侵犯门静脉及肝静脉主干和二级分支;④病人肝功能分级为Child-Pugh A级或B级;⑤肝储备功能检测,吲哚菁绿15 min滞留率(indocyanine green retention at 15 min,ICG-R15)≤30%,且重要脏器功能可耐受RFA或者肝部分切除术;⑥无明显出血倾向:血小板计数>50×109/L,凝血酶原时间延长<5 s;⑦年龄18~70岁;⑧术前未接受其他抗肿瘤治疗。
50例病人中,女性4例,占8.0%;平均年龄为(51.5±10.1)岁;绝大多数病人(44例,占88.0%)为乙肝相关性肝癌;超过一半(28例,占56.0%)的病人有肝硬化基础,94.0%(47/50)的病人Child-Pugh评分为A级,3例为B级;肝硬化基础病人中,失代偿期有2 例(4.0%)。50例肝肿瘤的术前检查均为单发病灶,31例为初发病人。肿瘤直径范围为0.9~3 cm,平均直径1.9 cm。
二、主要设备
美敦力公司的进口设备,LDRF-120S型多极射频消融仪及灌注电极针均购自四川绵阳立德电子股份有限公司;EUB-405型超声扫描仪为日本日立公司生产。
三、治疗方法
No-touch RFA治疗前给予镇静剂及预防性应用止痛剂。病人取平卧位或左侧卧位,超声检查明确肿瘤位置,左肝肿瘤取剑突下、右肝肿瘤取右侧肋间或肋缘下作穿刺点,局部皮肤消毒,2%利多卡因麻醉,切开皮肤约0.5 cm长,在超声引导下将灌注电极针插入肿瘤内部(图1);主要步骤如下:①术前行影像定位,选择最佳治疗体位及进针路径,进针路径须经过部分肝组织,避开大血管、胆管及重要脏器,标记好穿刺点;②根据超声探查病灶的结果决定使用的射频穿刺电极数量;③超声引导下将射频电极针穿刺进入病灶旁无瘤区(沿肿瘤边缘5 mm);④根据肿瘤大小及术中超声扫描实时监控情况决定治疗次数,为确保肿瘤消融治疗效果,消融范围应包括肿瘤及瘤周0.5~1 cm肝组织,以获取安全的消融边缘;⑤射频治疗完成后根据肿瘤消融时超声显示的一过性高回声区、CT显示的低密度区来评估肿瘤损毁大概范围。当确认消融区达到预消融范围后撤出射频电极针,同时行针道消融,并行影像检查确认有无出血、气胸等并发症。与经典射频消融术一样,大多病人在术后24 h内密切观察生命体征变化,必要时给予保肝及消炎止痛等对症处理,如无异常即可出院,或进入门诊接受治疗。No-touch RFA治疗后于1~3 d内行超声造影扫描,发现或疑有肿瘤残余时,在1周内行第二次治疗。出院病人在术后每2~3个月复查一次,如发现肿瘤复发,但无多发转移灶且病人尚能承受RFA者,继续给予治疗。采用No-touch RFA治疗后除部分病人需一般的保肝对症处理外,均未再接受其他特殊治疗。
四、观察指标
对No-touch RFA治疗前(入院日)和治疗后(术后3 d内)的肝功能、甲胎蛋白(AFP)水平及血小板计数进行检测。术后3~5 d内行上腹部增强CT及超声造影,比较治疗前后肿瘤的影像学变化,此后每2~3个月复查1 次,记录肿瘤的大小、位置、单发与多发情况、手术消融面积。对复发监测中可疑肿瘤病灶行磁共振肝肿瘤特异性成像检查或细针肝穿刺活检以明确诊断。整个No-touch RFA治疗的过程中,记录手术的次数和手术时间、住院总时间、并发症情况以及治疗后肿瘤残余率和坏死率,并对病人进行随访,观察病人的生存情况。
五、统计方法
所有的数据分析在SPSS(22.0版,美国IBM公司)上完成。Kolmogorov-Smirnov检验用于评估数据是否均一或符合正态分布,t检验或Mann-Whitney检验用于比较两组的差异水平。生存分析用Kaplan-Meier生存曲线来表示,不同组别的差异用Log-rank检验来计算。P<0.05被认为是差异有统计学意义。
结 果
一、手术情况及并发症
病人随访时间为3~21个月,平均7.8个月。50例病人的50个病灶共行No-touch RFA治疗51次,每例病人治疗平均1.02次,其中49例病人的49个病灶均仅治疗1次;每次治疗时间为6~10 min,平均8.2 min;术后平均住院时间为3.2 d (2~6 d)。手术中最大的平均消融面积为46.7 mm×35.8 mm。所有的病人在手术后24 h内均有轻度的肝区疼痛,1 例病人出现低热(38℃);50例病人均在治疗后24 h内出现丙氨酸转氨酶(ALT)及天冬氨酸转氨酶(AST)的升高(1~3 倍);27例病人总胆红素在治疗后24 h内升高1~3倍,最高升至69.6 μmol/L;此外,本组No-touch RFA治疗后发生的特殊并发症是少量反应性胸腔积液1例(2.0%),术后少量出血1例(2.0%)。总的并发症发生率为4.0%,无一例住院期间死亡。
二、治疗前后各项指标及影像学对比
表1显示了No-touch RFA前后,病人生化指标的变化。AFP阳性的22例病人在No-touch RFA治疗后1个月有14例转阴,5例明显下降,总体的AFP平均水平由(132.7±362.7) μg/L下降到(45.7±111.7) μg/L (P=0.019 5)。其余各项指标均有不同程度的下降(表1),而碱性磷酸酶水平略有上升,但差异无统计学意义(P=0.112 1)。其中有20例病人在第1次No-touch RFA治疗时进行了细针穿刺活检,活检均在超声引导下于肿瘤中心及周边共取2~3处,结果有18例发现癌细胞,2例为结节型肝硬化。
No-touch RFA治疗前病灶的彩超成像多为低回声或不均匀高回声,边界欠清,点线状血流信号。治疗后原病灶变为无增强回声区,彩色多普勒未见血流信号,超声造影亦可见造影剂充盈的无强化区(图1A、D);治疗后完全坏死的病灶在CT增强扫描下显示原低密度病灶扩大,动脉期病灶内无明显强化(图1E、F)。No-touch RFA治疗后1个月需再次复查CT或磁共振以确定病灶是否完全毁损。本研究的单次治疗后的肿瘤完全毁损率为98.0%。1例病人1个月内做2次治疗后复查后肿瘤完全毁损。
三、No-touch RFA治疗肝肿瘤的效果及病人的生存情况
50例病人从2015年9月至2017年6月随访,其总体生存率为100%,术后总体无瘤生存率90.0%(45/50)。根据病人的基线情况对病人进行分组分析,AFP阴性病人的无瘤生存率要好于AFP阳性病人,但差异无统计学意义(Log-rankP=0.294);对于有肝硬化基础的病人,其总体无瘤生存率要明显差于无肝硬化基础的病人,但差异仍无统计学意义(Log-rankP=0.157)。这样的结果我们考虑是由于每个亚组只有20多名病人,考察的基数太小造成的。(图2)
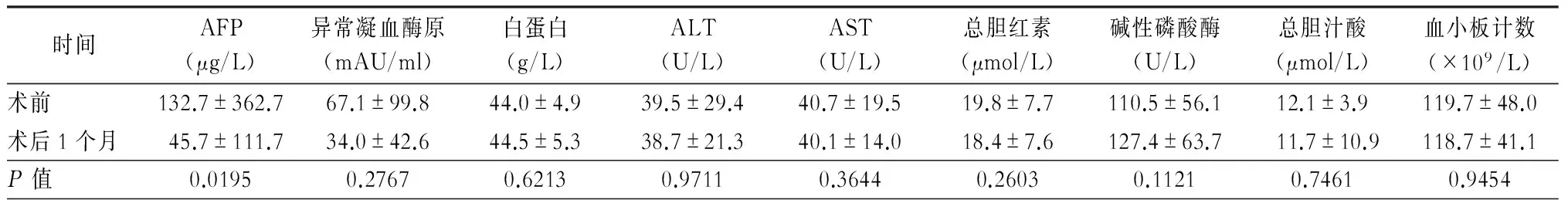
表1 No-touch射频消融前后病人生化指标的变化
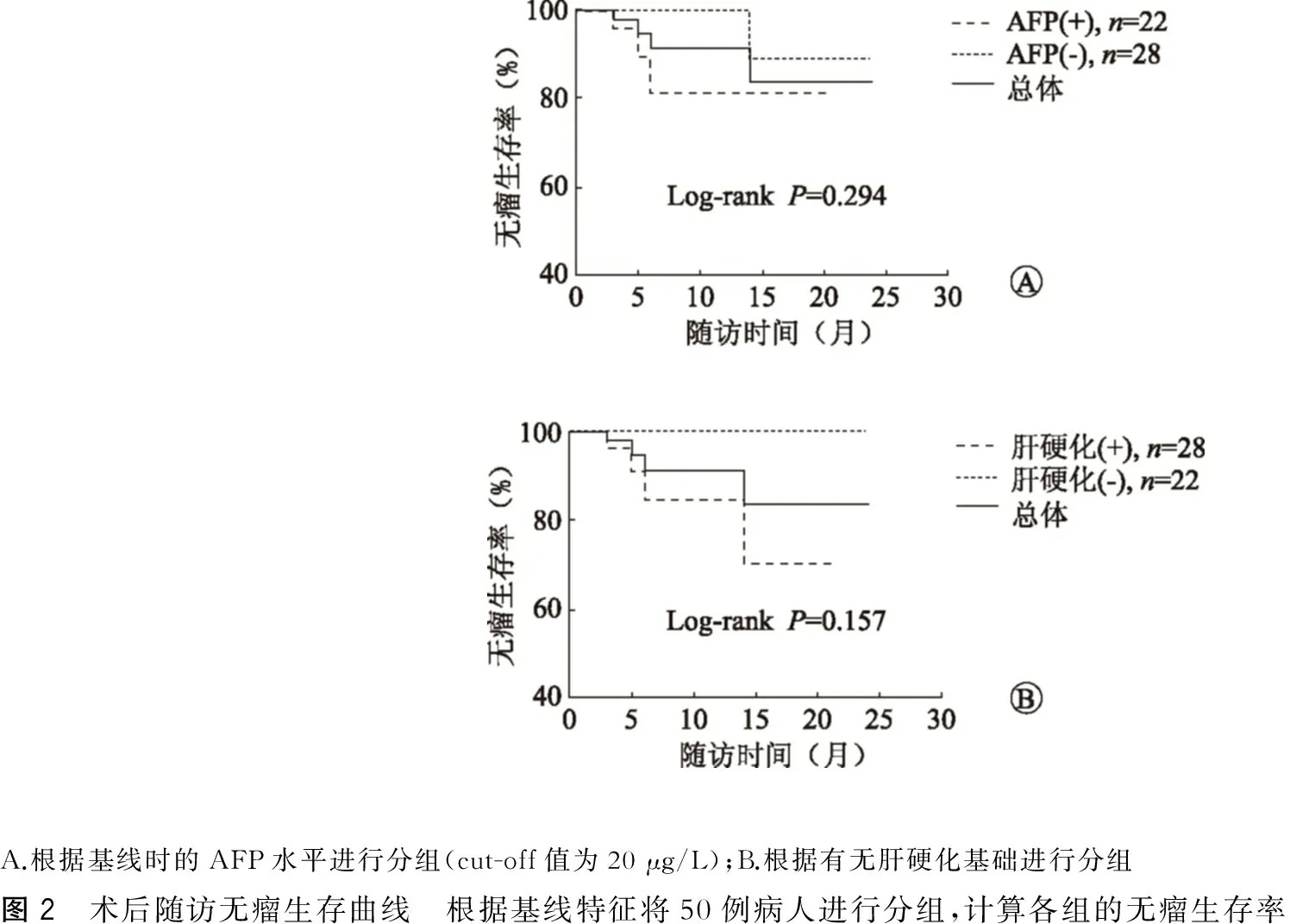
A.根据基线时的AFP水平进行分组(cut-off值为20μg/L);B.根据有无肝硬化基础进行分组图2 术后随访无瘤生存曲线 根据基线特征将50例病人进行分组,计算各组的无瘤生存率
讨 论
一、RFA对小肝癌的治疗效果
20世纪90年代中期,C-RFA正式被应用于肝癌的临床治疗,而临床上的实践也充分证明C-RFA不仅能够较彻底地损毁肿瘤组织,还可在有效杀死肿瘤细胞的同时保护好健康的肝脏组织[8]。但在临床的实际应用中,C-RFA术后5年复发率高达83%[9]。其原因可能是C-RFA直接穿刺肿瘤,治疗过程中高温高压,促进肿瘤沿微小血管转移或直接导致肿瘤干细胞入血播散[5,10],最终都因无法保证足够的消融安全边缘而导致复发[11]。2014年,Kawamura等[12]首次报道No-touch钳式消融技术治疗小肝癌的动物实验研究,摸索并探讨射频针布针规律,认为射频针摆放的针距在20 mm范围以内,No-touch钳式消融技术对肝表面肿瘤有明确的治疗效果。同年Morimoto等[13]率先报道1例腔镜辅助下的No-touch RFA。他认为No-touch RFA适用治疗小肝癌,尤其突出肝脏表面的小肝癌,建议把No-touch RFA技术推广于肝癌的临床治疗实践中。国内对于直径≤3 cm的肝肿瘤的No-touch RFA的安全性及近期疗效分析研究尚未见报道。
本次临床研究资料显示,50例病人的50个病灶经过51次的No-touch RFA治疗后,术后3 d左右行CT扫描及超声造影显示病灶完全坏死率为100%。Seror等[14]对2组符合米兰标准的小肝癌在肝移植术前分别进行No-touch RFA(n=29)和单针C-RFA(n=30),进行较为详细的临床病理研究,其中,No-touch RFA组完全消融率为26/29,远远高于单针C-RFA(14/30),他认为C-RFA是从肿瘤中心向周边离心消融,无法保证足够的消融安全边缘,而No-touch RFA通过从肿瘤周边到肿瘤中心的向心消融方式,不仅确保充足的消融安全边缘,而且明显提高病理性的完全消融率。我们的研究也认为No-touch RFA对病灶消融彻底,不容易产生残留。
2010年以后双极射频系统开始广泛应用于肝癌治疗[15],而建立其基础上的No-touch RFA治疗效果的研究仍在起步阶段[16]。本组50例病人随访从2015年9月开始至2017年6月,总体生存率为100%,总体无瘤生存率为90.0%(45/50)。我们发现No-touch RFA通过2根cooltip电极单次治疗的毁损范围可达到直径3~5 cm的椭圆形病灶,对于直径≤2 cm病灶的治疗相对容易,但对2 cm<直径≤3 cm的病灶则需要一定技术性。为了最大限度地毁损肿瘤病灶,我们在进行消融之前,首先通过超声造影从不同角度观察病灶位置,治疗时要设计好进针的线路、角度、方向,保证治疗结束时所有病灶均在治疗范围内,并包括病灶周围0.5 cm的癌旁组织2根电极针,每根电极针均插入所在方向的最深处,在其针道上反复消融使所形成的圆柱体毁损范围尽可能涵盖肿瘤的全部,两根电极可能毁损的范围重叠50%左右,电极针布好位置后进行实时连续消融,直至整个病灶及其周围0.5~1.0 cm的组织均被消融完毕,这样既可最大限度地避免癌灶残留,又节约了时间。术后3 d内复查CT和(或)超声造影,早期发现残余病灶并及时进行补充治疗;此后,每2~3个月复查彩超或CT一次,发现复发或再发者及时进行更多次的治疗。单次No-touch RFA治疗后残余肿瘤发生率为2.0%,仅1例病人在第1次治疗后复查超声造影发现残瘤。此例考虑消融不完全,1个月内行第2次No-touch RFA消融,治疗后复查CT及消融未见肝癌病灶。由于转移性肝癌多为多发,本组仅有1例单发的结直肠癌肝转移的病人,无瘤生存已5个月。No-touch RFA为治疗直径≤3 cm的肝肿瘤提供了一种新的治疗思路,其远期疗效也需进一步观察。
二、RFA治疗小肝癌的安全性
已报道的不良反应或微小并发症有肝内血肿、膈肌灼伤、肝区疼痛、腹腔少量积血、胸腔积液、发热、转氨酶升高、偶发的肿瘤针道转移以及治疗过程中电极针尖端可扩张部分回缩故障等[17]。尚未见到有致命的并发症或No-touch RFA治疗直接引起病人死亡的报道。
经过本次临床研究,我们认为No-touch RFA治疗和C-RFA一样,是一种微创、安全的有效方法,本组资料中50 例中有少量反应性胸腔积液1例(2.0%),术后少量出血1例(2.0%)。总的并发症发生率为4.0%,无一例住院期间死亡。这可能是因为本组为小肝癌病例,No-touch RFA治疗耗时短,平均为8.2 min,引起全身反应较轻。本组病例的治疗时间最短为6 min,最长为12 min。其他的不良反应如转氨酶升高,胆红素升高,肝区疼痛以及一过性的发热等与文献报道的一致。本组无一例发生危及生命的并发症或因RFA本身的操作而死亡,2个月后的死亡均是由于肝癌本身的并发症所致。与文献报道的有关C-RFA治疗小肝癌的安全情况类似。可见,No-touch RFA治疗小肝癌同样具有微创、安全的特性。
近年来,国际上对No-touch RFA逐渐重视,笔者认为No-touch RFA的适应证和禁忌证目前还在摸索阶段,主要是基于以下考虑:①国际上对肝癌No-touch RFA治疗的研究仍缺少多中心的前瞻性随机对照研究;②国内目前除我院外尚无任何一家医院启动或开展此项医疗技术,安全性仍需要进一步验证;③No-touch RFA减少射频术后复发率的机制仍未完全明了。
(本文图1~4见封二)
1 钱林学, 刘玉江, 丁惠国.小肝癌的影像学诊断进展. 世界华人消化杂志,2010,18: 479-486.DOI:10.3969/j.issn.1009-3079.2010.05.010.
2 陈敏山. 肝癌射频消融治疗的现状与展望.中华普通外科学文献:电子版,2011,5: 453-456,558.DOI:10.3877/cma.j.issn.1674-0793.2011.06. 001.
3 Kim Ys, Lim HK, Rhim H, et al.Ten-year outcomes of percutaneous radiofrequency ablation as first-line therapy of early hepatocellular carcinoma: analysis of prognostic factors. J Hepatol,2013,58: 89-97. DOI:10.1016/j.jhep.2012.09.020.
4 Suh SW, Lee KW, Lee JM, et al. Prediction of aggressiveness in early-stage hepatocellular carcinoma for selection of surgical resection. J Hepatol,2014,60:1219-1224. DOI: 10.1016/j.jhep.2014.01.027.
5 Ikemoto T, Shimada M, Yamada S. Pathophysiology of recurrent hepatocellular carcinoma after radiofrequency ablation. Hepatol Res,2017,47: 23-30. DOI: 10.1111/hepr.12705.
6 Li Y, Xu KS, Li JS, et al. The research of No-touch isolation technique on the prevention of postoperative recurrence and metastasis of hepato cellular carcinoma after hepatectomy. Hepatogastroenterology,2014,61: 784-791.
7 Hocquelet A, Papadopoulos P, Trillaud H. No-touch multibipolar radiofrequency ablation: the new standard ablative technique for hepatocellular carcinoma 5 cm or smaller. Radiology,2016,281:975-976. DOI: 10.1148/radiol.2016160774.
8 马宽生,陈敏,蔡景修.多电极射频治疗肝肿瘤的安全性和可靠性分析.中华肝胆外科杂志,2001,7: 198-201. DOI:10.3760/cma.j.issn.1007-8118.2001.04.002.
9 Machi J, Oishi AJ, Sumida K, et al.Long-term outcome of radiofrequency ablation for unresectable liver metastases from colorectal cancer: evaluation of prognostic factors and effectiveness in first- and second-line management. Cancer J,2006,12: 318-326.
10Patel PA, Ingram L, Wilson ID,et al.No-touch wedge ablation technique of microwave ablation for the treatment of subcapsular tumors in the liver.J Vasc Interv Radiol,2013,24:1257-262.DOI: 10.1016/j.jvir.2013.04.014.
11Zytoon AA, Ishii H, Murakami K, et al. Recurrence-free survival after radiofrequency ablation of hepatocellular carcinoma. A registry report of the impact of risk factors on outcome. Jpn J Clin Oncol,2007,37: 658-672. DOI: 10.1093/jjco/hym086.
12Kawamura Y,Ikeda K,Fukushima T, et al.Potential of a no-touch pincer ablation procedure for small hepatocellular carcinoma that uses a multipolar radiofrequency ablation system: An experimental animal study. Hepatol Res,2014,44:1234-1240. DOI: 10.1111/hepr.12240.
13Morimoto N, Isoda N, Watanabe S, et al. A case of small hepatocellular carcinoma treated with laparoscopic multipolar radiofrequency ablation with a no-touch ablation procedure. Clin J Gastroenterol,2014,7:510-515. DOI: 10.1007/s12328-014-0531-1.
14Seror O, N'Kontchou G, Van Nhieu JT, et al.Histopathologic comparison of monopolar versus no-touch multipolar radiofrequency ablation to treat hepatocellular carcinoma within Milan criteria. J Vasc Interv Radiol,2014,25: 599-607. DOI: 10.1016/j.jvir.2013.11.025.
15Ikeda K, Osaki Y, Nakanishi H, et al. Recent progress in radiofrequency ablation therapy for hepatocellular carcinoma. Oncology,2014,87 Suppl 1: 73-77. DOI: 10.1159/000368148.
16Hocquelet A,Aub C,Rode A,et al.Comparison of no-touch multi-bipolar vs. monopolar radiofrequency ablation for small HCC. J Hepatol,2017,66: 67-74. DOI: 10.1016/j.jhep.2016.07.010.
17Seror O, N'Kontchou G, Nault JC, et al. Hepatocellular carcinoma within Milan criteria: No-touch multibipolar radiofrequency ablation for treatment-long-term results. Radiology,2016,280:611-621.DOI: 10.1148/radiol.2016150743.
SafetyandefficacyofNo-touchradiofrequencyablationintreatingsinglelivertumor≤3cm(areportof50cases)
ChaiYuelong*,LiKun,YuRentao,ZouMengda,MaKuansheng.
*InstituteofHepatobiliarySurgery,SouthwestHospital,ArmyMedicalUniversity,Chongqing400038,China
MaKuansheng,Email:makuansheng@vip.sina.com
ObjectiveTo investigate the efficacy and safety of No-touch radiofrequency ablation (RFA) in the treatment of liver tumors with diameters of less than 3 cm.MethodsA total of 50 patients with liver tumor ≤3 cm were enrolled in this study and the Cooltip electrode was used in No-touch RFA. Among them, there were 49 cases of primary liver cancer (31 cases of primary hepatocellular carcinoma and 18 cases of recurrent hepatocellular carcinoma) and 1 case of metastatic liver cancer, with an average tumor size of 1.9 cm in diameter. Pre- and post-operative examinations of hepatic function, enhanced computed tomography (CT) scan, magnetic resonance imaging (MRI), ultrasonography, and fine-needle liver biopsy were performed and the results were compared. In addition, therapy time and frequency, postoperative length of hospital stay, the complications after RFA treatment and the total necrosis rate of the tumor were recorded, and continuously observed. The survival rate was also followed.ResultsFifty patients were treated with No-touch RFA up to 51 times, of which one patient was treated twice within one month. The average time of therapy was 8.2 min and the postoperative length of hospital stay was 3.2 days. CT or MRI examinations within one month after No-touch RFA showed that the total tumor necrosis rate was 98.0%. Among 22 patients positive for AFP, 14 cases were transferred into negative AFP and serum AFP level in 5 cases decreased significantly during the period of 6-12 months after RFA treatment. By following up 50 patients from September of 2015 to June of 2017, the total survival rate was 100% and the tumor-free survival rate was 90.0% (45/50).ConclusionsNo-touch RFA is a minimally invasive, safe and effective method for the treatment of liver tumors with a diameter of less than 3 cm.
Small hepatocellular carcinoma; Classic-radiofrequency ablation; No-touch radiofrequency ablation
重庆市社会事业与民生保障科技创新专项(cstc2016shms-ztzx130001)
400038 重庆,陆军军医大学第一附属医院肝胆外科(柴跃龙、李昆、邹孟达、马宽生),感染科(俞仁涛)
马宽生,Email: makuansheng@vip.sina.com
R657.3
A
10.3969/j.issn.1003-5591.2017.05.011
2017-07-23)

