EGFR基因突变对靶向治疗非小细胞肺癌患者的疗效影响及生存分析
赵振波
EGFR基因突变对靶向治疗非小细胞肺癌患者的疗效影响及生存分析
赵振波
目的探讨表皮生长因子受体(EGFR)基因不同染色体上外显子突变对靶向治疗非小细胞肺癌患者的疗效影响及生存分析。方法选取76例EGFR基因敏感突变非小细胞肺癌患者,根据EGFR基因检测结果分为四组:A组,EGFR基因18号染色体上外显子突变型组(18例);B组,EGFR基因19号染色体上外显子突变型组(20例);C组,EGFR基因20号染色体上外显子突变型组(19例);D组,EGFR基因21号染色体上外显子突变型组(19例)。同时选取同期住院治疗的20例EGFR基因野生型(EGFR基因未突变)非小细胞肺癌患者作为E组(对照组)。各组患者均给予吉非替尼(250 mg/d)治疗。结果与E组比较,A、B、D组的总有效率和疾病控制率均升高,差异均有统计学意义(P均<0.05);与E组比较,C组的总有效率和疾病控制率均降低,差异均有统计学意义(P均<0.05)。与E组比较,A、B、D组PFS、OS和QOL均升高,差异均有统计学意义(P均<0.05);与E组比较,C组的PFS、OS和QOL均降低,差异均有统计学意义(P均<0.05)。与E组比较,A、B、D组总不良反应发生率均降低,差异均有统计学意义(P均<0.05);与E组比较,C组的总不良反应发生率升高,差异有统计学意义(P<0.05)。结论采用靶向药物吉非替尼治疗EGFR基因18、19和21号染色体上外显子突变的非小细胞肺癌患者效果较好,同时延长患者生存时间,降低不良反应;相反,采用靶向药物吉非替尼治疗EGFR基因20号染色体上外显子突变的非小细胞肺癌患者因出现耐药而效果不佳。
靶向治疗;EGFR基因突变;非小细胞肺癌
(ThePracticalJournalofCancer,2017,32:1641~1644)
非小细胞肺癌是临床上较为常见的癌症疾病,其具有较高的发病率和死亡率。目前研究证实[1],以表皮生长因子受体络氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor,EGFR-TK1)为代表的分子靶向药物吉非替尼能使EGFR基因突变阳性的非小细胞肺癌患者生存时间得到明显延长。研究报道[2],EGFR-TKI类分子靶向药物治疗肿瘤的机制可能是该类药物抑制了外周血循环肿瘤细胞(CTC)、围术期的微转移病灶和术中的微残存病灶,但确切的机制有待进一步的研究。鉴于此,本文将探讨靶向药物吉非替尼治疗EGFR基因不同染色体上外显子突变的非小细胞肺癌患者的疗效,旨在为临床EGFR突变阳性的非小细胞肺癌患者的治疗提高参考依据。
1 资料与方法
1.1 一般资料
选取2010年1月至2012年1月间我院收治的EGFR基因敏感突变的非小细胞肺癌患者76例,纳入标准[3]:①肺部病理诊断结果均为非小细胞肺癌患者,且均存在EGFR基因敏感突变;②依从性好,可以定期进行随访的患者;③体力状况(performance status,PS)评分0~2分,预计生存期>3个月。排除标准[4]:①妊娠女性;②曾使用EGFR-TAI类药物治疗的患者;③合并精神障碍的患者。同时选取同期住院治疗的20例EGFR基因野生型(EGFR基因未突变)非小细胞肺癌患者作为对照研究。采用蝎形探针扩增阻滞突变系统(scorpions amplification refractory mutation system,Scorpions,ARMS法,目前肺癌分子生物学研究领域比较认可的检测方法)测定癌组织EGFR基因突变情况[5],检查结果显示:EGFR基因18号染色体上外显子点突变18例、19号染色体上外显子点突变20例、20号染色体上外显子点突变19例,21号染色体上外显子点突变19例。其中男性38例,女性38例,年龄40~86岁,平均(58.3±2.9)岁,体力状况评分:0~1分40例,2分36例。肿瘤直径1.8~16.0 cm,平均直径(6.65±1.91)cm;肿瘤分级:Ⅰ级19例,Ⅱ级19例,Ⅲ级20例,Ⅳ级18例。本研究通过我院伦理委员会审核,所有患者在治疗前均知情同意并签署同意书。
1.2 治疗方法[6]
根据EGFR基因检测结果分为四组:A组,EGFR基因18号染色体上外显子突变型组(18例);B组,EGFR基因19号染色体上外显子突变型组(20例);C组,EGFR基因20号染色体上外显子突变型组(19例);D组,EGFR基因21号染色体上外显子突变型组(19例)。同时选取同期住院治疗的20例EGFR基因野生型(EGFR基因未突变)非小细胞肺癌患者作为E组(对照组)。各组患者均给予吉非替尼(250 mg/d)治疗,各组患者均治疗至出现疾病进展或患者无法耐受药物不良反应为止。
1.3 观察指标
比较各组患者疗效[7],疗效评价分为完全缓解(complete response,CR),部分缓解(panial response,PR),疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)。疗效评价标准:①CR,肺癌病灶完全消失,且维持时问>1个月;②PR,肺癌病灶体积缩小>50%,且维持时间>1个月;③SD,肺癌病灶缩小25%~50%;④PD,肺癌病灶增大>25%或出现新的病灶。以(CR+PR)计算总体有效率,以(CR+PR+SD)计算疾病控制率(DCR)。
比较各组患者的肿瘤无进展生存期(progression free survival,PFS)、总生存期(overall survival,OS)和患者生活质量评分(quality of life,QOL)[8]。比较各组患者不良反应发生情况,包括腹泻、皮疹、肝功能异常、消化道反应和凝血异常等[9]。
1.4 统计学方法
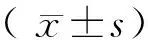
2 结果
2.1 各组实体肿瘤疗效比较
与E组比较,A、B、D组的总有效率和疾病控制率均升高,差异均有统计学意义(P均<0.05);与E组比较,C组的总有效率和疾病控制率均降低,差异均有统计学意义(P均<0.05),见表1。
2.2 各组患者PFS、OS和QOL分析
与E组比较,A,B,D组的PFS、OS和QOL均升高,差异均有统计学意义(P均<0.05);与E组比较,C组的PFS、OS和QOL均降低,差异均有统计学意义(P均<0.05),见表2。
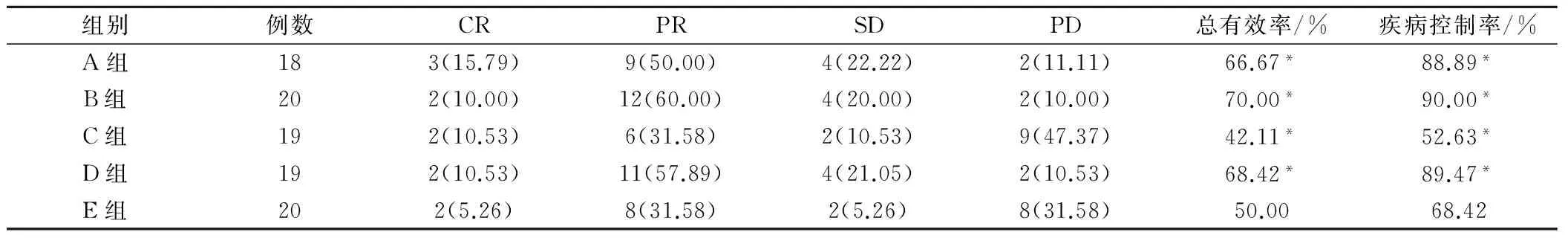
表1 各组疗效比较(例,%)
注:与E组比较,*为P<0.05。
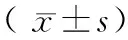
表2 各组患者PFS、OS和QOL分析
注:与E组比较,* 为P<0.05。
2.3 各组患者治疗后不良反应情况比较
主要不良反应包括腹泻、皮疹、肝功能异常、消化道反应和凝血异常。与E组比较,A,B,D组的总不良反应发生率均降低,差异均有统计学意义(P均<0.05);与E组比较,C组的总不良反应发生率升高,差异有统计学意义(P<0.05)。见表3。
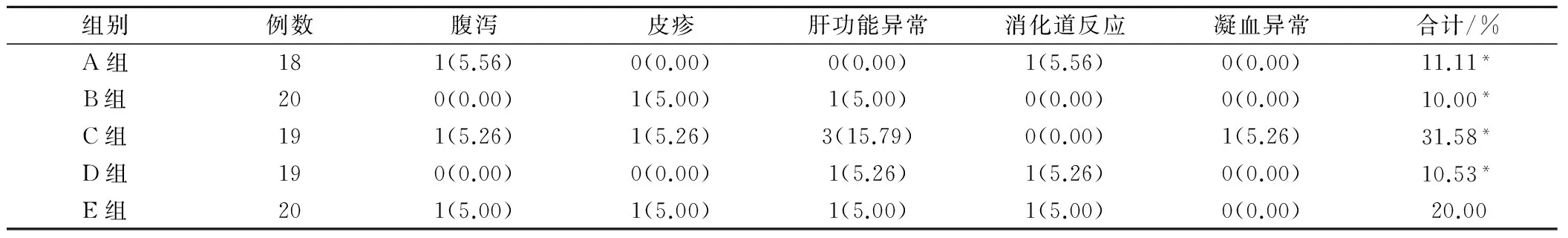
表3 各组患者治疗后不良反应情况比较(例,%)
注:与E组比较,*为P<0.05。
3 讨论
近些年来,非小细胞肺癌的发病率和死亡率在全球范围内均不断升高,大部分患者在就诊时已处于晚期,失去了手术根治的最佳机会。但是近些年来发现,越来越多的非小细胞肺癌患者存在EGFR基因突变现象[10-11]。EGFR基因突变情况包括19号染色体上外显子的缺失突变;21号染色体上外显子L858R突变,即858位亮氨酸被精氨酸替代的突变;21号染色体上外显子L861Q突变,即861位丝氨酸被异亮氨酸替代的突变; 20号染色体上外显子T790M突变,即790位苏氨酸被甲硫氨酸替代的突变;18号染色体上外显子G719X突变,包括G719A、G719C、G719S的3种突变,即719位甘氨酸被丙氨酸、半胱氨酸或者丝氨酸替代的突变[12-13]。对于EGFR基因突变阳性的非小细胞肺癌患者,传统的化疗模式远期治疗效果并不理想,并且该类患者的生存时间较短。目前随着分子靶向药物特别是EGFR-TKI的出现,为EGFR突变阳性的非小细胞肺癌的治疗开辟了一条新的路径,多项研究[14-16]证实了分子靶向药物可延长EGFR突变阳性的非小细胞肺癌患者的生存时间。
国外对于非小细胞肺癌的分子靶向治疗药物做了大量研究,Johnson等[17]研究结果表明,分子靶向药物吉非替尼治疗EGFR基因18,19,21号染色体上外显子突变阳性的非小细胞肺癌患者,能够显著提高患者客观缓解率,并且延长患者的生存时间。而Lynch,TJ等[18]研究结果表明,分子靶向药物吉非替尼治疗EGFR基因20号染色体上外显子突变阳性的非小细胞肺癌患者,反而降低患者治疗效果,缩短生存时间。由此看来,分子靶向药物吉非替尼治疗EGFR基因突变阳性非小细胞肺癌患者因EGFR基因的不同染色体上外显子突变而疗效不同。但在国内,关于非小细胞肺癌患者EGFR基因的不同染色体上外显子突变类型与分子靶向药物治疗效果的研究不多。本文将探讨靶向药物吉非替尼治疗EGFR基因的不同染色体上外显子突变的非小细胞肺癌患者的疗效,旨在为临床EGFR突变阳性的非小细胞肺癌患者的治疗提高参考依据。
本文研究表明,与EGFR基因野生型(EGFR基因未突变)非小细胞肺癌患者比较,采用靶向药物吉非替尼治疗EGFR基因18,19,21号染色体上外显子突变阳性患者的总有效率、疾病控制率、PFS、OS和QOL均升高,不良反应发生率均降低,差异均有统计学意义(P均<0.05);而与EGFR基因野生型非小细胞肺癌患者比较,采用靶向药物吉非替尼治疗EGFR基因20号染色体上外显子突变阳性患者的总有效率、疾病控制率、PFS、OS和QOL均降低,不良反应发生率升高,差异均有统计学意义(P均<0.05),此结果与Paez等[19]研究报道一致,Paez等[19]的研究结果表明,采用靶向药物吉非替尼治疗EGFR基因20号染色体上外显子突变的非小细胞肺癌患者,由于出现耐药性问题,其治疗效果反而降低。综上所述,采用靶向药物吉非替尼治疗EGFR基因18、19和21号染色体上外显子突变的非小细胞肺癌患者效果较好,同时延长患者生存时间,降低不良反应;相反,采用靶向药物吉非替尼治疗EGFR基因20号染色体上外显子突变的非小细胞肺癌患者因出现耐药而效果不佳。
[1] 董立新,李文军,董淑芬,等.晚期非小细胞肺癌放射治疗联合靶向治疗效果分析〔J〕.中国综合临床,2011,27(7):744-746.
[2] Cheng L,ZhaIlg S,AlexaIlder,et al.The laIldscape of EGFR pathways and perSonaIized maⅡagement of nonsmali-cell lung cancer〔J〕.Future Oncol,2016,7(4):519-541.
[3] Qiwx,TangLN,HeAN,et al.The role of vandetanib in the Second line treament for advanced non.small-cell-lung cancer:a meta-a11alysis of four randomized controlled trials〔J〕.Lung,2015,189(6):437-443.
[4] Miller,Mnler vA,Politi KA,et al.Acquired resistance of lung adenocarinomas to gentinib or erlotinib is associated with a second mutation in the EGFR kinase domain〔J〕.PLoS Med,2015,2(3):73-80.
[5] 周 荻,徐 欣,谢华英,等.全脑放疗联合靶向治疗与同步放、化疗治疗非小细胞肺癌脑转移疗效分析〔J〕.上海交通大学学报(医学版),2013,33(4):480-484.
[6] 黄晓慧.非小细胞肺癌的多靶点联合靶向治疗进展〔J〕.现代中西医结合杂志,2013,22(12):1363-1365.
[7] 孙 燕,吴一龙,李龙芸,等.吉非替尼或多西他赛治疗一线化疗失败的非小细胞肺癌的临床分析〔J〕.中华肿瘤杂志,2011,33(5):377-380.
[8] 陈 红,张瑞虹,杜改萍,等.三维适形放疗联合吉非替尼治疗老年非小细胞肺癌的疗效〔J〕.中国老年学杂志,2011,31(21):4131-4132.
[9] Krishnasamy MJ,Corner JJ,Bredin MJ,et al.Cancer nursing practice development:understanding breathlessness〔J〕.J Clin NursJ,2016,10(1):103-108.
[10] Kunik ME,Azzam PN,SouchekJ,et al.A practical screening tool for anxiety and depression in patients with chronic breathing disorder〔J〕.Psychosomatics,2016,48(1):16-21.
[11] Costa DB.Pooled analysis of the prospective trials of gefitinib monotherapy for EGFR-mutant non-small cell lung cancers〔J〕.Lung Cancer,2016,58(1):95-103.
[12] Kris MG. Efficacy of gefitinib,an inhibitor of the epidermal growth factor receptor tyrosine kinase,in symptomatic patients with non-small cell lung cancer:a randomized trial 〔J〕.JAMA,2013,290(16):2149-2158.
[13] Engelman JA,Janne PA.Factors predicting response to EGFR tyrosine kinase inhibitors〔J〕.Semin Respir Crit Care Med,2015,26(3):314-322.
[14] Rosell R,Taron M,Reguart N,et al.Epidermal growth factor receptor activation:how exon 19 and 21 mutations changed our understanding of the pathway〔J〕.Clin Cancer Res,2016,12(24):7222-7231.
[15] Hidalgo M,Siu LL,Nemunaitis J,et al.Phase I and pharmacologic study of OSI-774,an epidermal growth factor receptor tyrosine kinase inhibitor,in patients with advanced solid malignancies〔J〕.J Clin Oncol,2011,19(13):3267-3279.
[16] Siegel-Lakhai WS,Beijnen JH,Schellens JH.Current kno-
wledge and future directions of the selective epidermal growth factor receptor inhibitors erlotinib (Tarceva) and gefitinib (Iressa)〔J〕.Oncologist,2015,10(8):579-589.
[17] Johnson JR,Cohen M,Sridhara R,et al.Approval summary for erlotinib for treatment of patients with locally advanced or metastatic non-small cell lung cancer after failure of at least one prior chemotherapy regimen〔J〕.Clin Cancer Res,2015,11(18):6414-6421.
[18] Lynch TJ,Bell DW,Sordella R,et al.Activating mutations in the epidermal growth factor receptor underlying responsiveness of non-small-cell lung cancer to gefitinib〔J〕.N Engl J Med,2014,350(21):2129-2139.
[19] Paez JG,Jänne PA,Lee JC,et al.EGFR mutations in lung cancer:correlation with clinical response to gefitinib therapy〔J〕.Science,2014,304(5676):1497-1500.
EffectofEGFRMutationsonTargetedTherapyintheTreatmentofPatientswithNon-smallCellLungCancerandPrognosisAnalysis
ZHAOZhenbo.
XinxiangCentralHospital,Xinxiang,453000
ObjectiveTo investigate the effect of EGFR mutations on targeted therapy in the treatment of patients with non-small cell lung cancer and prognosis analysis.Methods76 cases patients with non-small cell lung cancer and EGFR mutation were analyzed,and divided into four groups.A group (18 cases):patients with non-small cell lung cancer and EGFR mutation in exon 18.B group (20 cases):patients with non-small cell lung cancer and EGFR mutation in exon 19.C group (19 cases):patients with non-small cell lung cancer and EGFR mutation in exon 20.D group (19 cases):patients with non-small cell lung cancer and EGFR mutation in exon 21.All patients were treated with gefitinib (250 mg/d).After treatment,clinical efficacy,survival and toxicity were compared in all groups.ResultsCompared with E group,the total effective rate and the disease control rate in A,B and D groups were all higher (Pall<0.05).Compared with E group,the total effective rate and the disease control rate in C group were all lower (Pall<0.05).Compared with E group,the levels of PFS,OS and QOL in A,B and D groups were all higher (Pall<0.05).Compared with E group,the levels of PFS,OS and QOL in C group were all lower (Pall<0.05).Compared with E group,the levels of adverse reactions in A,B and D groups were all lower (Pall<0.05).Compared with E group,the level of adverse reactions in C group was higher (Pall<0.05).ConclusionTargeted therapy in the treatment of patients with non-small cell lung cancer with EGFR mutation in exon 18,19,21 can effectively improve the clinical symptoms and prognosis,reduce the rate of adverse reactions.On the contrary,targeted therapy in the treatment of patients with non-small cell lung cancer with EGFR mutation in exon 20 can effectively reduce the clinical symptoms and prognosis,reduce the rate of adverse reactions.
Targeted therapy;EGFR mutations;Non-small cell lung cancer
4530000 河南省新乡市中心医院
10.3969/j.issn.1001-5930.2017.10.022
R734.2
A
1001-5930(2017)10-1641-04
2017-03-24
2017-05-23)
(编辑吴小红)

