不同CYP2C9及GGCX基因型在人工瓣膜置换术后的抗凝效果比较
陈洪晔,于波,谭启明,李勇,秦良光,杨研
(1.江苏省连云港市第一人民医院 心血管外科,江苏 连云港 222000;2.中国医学科学院阜外心血管病医院 外科,北京 100037)
不同CYP2C9及GGCX基因型在人工瓣膜置换术后的抗凝效果比较
陈洪晔1,于波1,谭启明1,李勇1,秦良光1,杨研2
(1.江苏省连云港市第一人民医院 心血管外科,江苏 连云港 222000;2.中国医学科学院阜外心血管病医院 外科,北京 100037)
目的了解不同CYP2C9及GGCX基因型对人工瓣膜置换术后抗凝效果的影响。方法选取2013年1月-2016年12月在该院心脏外科接受心脏瓣膜置换术的患者,采集服药后空腹12 h的外周静脉血3ml进行CYP2C9和GGCX基因型检测,收集患者相关临床资料,采用SPSS 21.0软件进行数据分析。结果选取80例患者,CYP2C9基因型有2种,包括73例CYP2C9*1*1和7例CYP2C9*1*3患者;42例GGCX*A*G型和38例GGCX*G*G型患者。两种基因型患者在性别、年龄、体质指数(BMI)、凝血酶原时间(PT)、国家标准化比值(INR)值及达到稳定抗凝效果后的华法林血药浓度差异无统计学意义(P<0.05),但CYP2C9*1*1型患者INR首次达标时间>CYP2C9*1*3型患者(P=0.013),CYP2C9*1*1型患者华法林日均稳定维持剂量>CYP2C9*1*3型患者(P=0.011),GGCX*A*G型患者华法林日均稳定维持剂量>GGCX*G*G型患者(P=0.000),同时为CYP2C9*1*1型和GGCX*A*G型的患者华法林日均稳定维持剂量>其他3组(P=0.024)。CYP2C9基因型(P=0.001)和GGCX基因型是影响患者术后第6天是否能达到治疗窗的影响因素(P=0.032)。结论根据CYP2C9基因型和GGCX基因型确定个人使用剂量,可提高患者抗凝治疗效果。
CYP2C9基因型;GGCX基因型;瓣膜置换;抗凝
人工瓣膜置换术可以改善病变瓣膜所致的血流动力障碍,改善患者的心脏功能,但同时也会导致血栓等并发症。为预防发生血栓,接受人工瓣膜置换术的患者需长期服用抗凝药物。相关研究表明[1-3],华法林是人工瓣膜置换术患者的重要抗凝药物选择之一,在临床应用中,华法林的有效用药剂量个体差异较大,且较难控制其有效抗凝维持剂量,剂量不足时难以发挥预防血栓形成的作用,剂量过多时会引起出血,造成生命危险。目前,临床用药以经验为主,首剂常给予标准剂量,然后根据监测的凝血酶原时间(prothrombin time,PT)和国家标准化比值(international normalized ratio,INR)来调整剂量,使INR值处于一个合理的范围内,我国建议人工瓣膜置换术患者的INR处于1.8~2.5。华法林是由S-型和R-型异构体组成的消旋化合物,其中S-型对映体是发挥抗凝作用的主要成分。人体细胞色素P450酶2C9基因(cytochrome P450 2C9,CYP2C9)所编码的细胞色素P450酶是华法林的重要代谢酶,S-型对映体即通过CYP2C9代谢。CYP2C9的不同基因型可影响酶的活性,从而影响华法林的药物代谢动力学,最终影响其抗凝效果[4-6]。GGCX基因则是编码药物作用的靶点、血浆转运蛋白等,影响药物效应动力学。为了解不同CYP2C9基因型和GGCX基因型对抗凝效果的影响。
1 资料与方法
1.1 研究对象
选取2013-2016年在本院心脏外科接受心脏瓣膜置换术的患者,所有入选对象均为汉族,相互间无血缘关系。入选标准:①心脏瓣膜置换术后接受华法林长期抗凝治疗;②年龄>18岁;③接受稳定抗凝治疗>3个月;④2次复查PT及INR均达到抗凝标准(INR:1.7~3.0);⑤无出血及血栓等并发症;⑥术后超声复查未见人工瓣膜异常、肝肾功能正常。排除标准:①无血样本;②肝肾功能异常;③华法林过敏、服用可能与华法林相互作用的药物(如胺碘酮、利福平或阿司匹林等);④有凝血功能障碍;⑤心肌梗死<1个月。
1.2 仪器与试剂
采用CA530型血凝仪(日本东亚医用电子仪器有限公司),聚合酶链反应(polymerase chain reaction,PCR)扩增仪(日本TaKaRa有限公司),培清JS-680D全自动凝胶成像分析仪(上海培清科技有限公司),外周全血基因组DNA提取试剂盒(上海百傲科技有限公司),Bio Base生物安全柜(上海巴艾贝斯科技有限公司),ABBOTT的D-37520台式高速离心机(美国雅培公司),进行本研究的基因型测定。在研究对象知情同意后采集服药后空腹12 h的外周静脉血3ml,全血标本置入-20℃冰箱冷冻保存备用。
1.3 资料收集
收集患者的基本资料,包括年龄、性别、身高、身体重指数(body mass index,BMI)、用药时间、各次随访时的PT值和INR值、术后抗凝治疗药物剂量、同时服用其他药物及达标时的药物日均服用剂量。
1.4 统计学方法
数据分析采用SPSS 21.0统计软件,计量资料以均数±标准差(±s)表示,比较用t检验或方差分析,两两比较SNK-q检验法,计数资料用频数表示,比较用χ2检验,P<0.05为差异有统计学意义;影响因素的分析采用多元Logistic回归分析。
2 结果
2.1 患者基本特征及华法林治疗情况
本研究纳入符合标准的患者共80例。其中,男性37例,女性43例;年龄42~73岁;体重48~83 kg。研究对象中CYP2C9基因型有2种,分别为CYP2C9* 1*1(73例)和CYP2C9*1*3(7例);GGCX基因型也有2种,分别为GGCX*A*G型(42例)和GGCX*G* G型(38例)患者。2种基因型患者在性别、年龄、BMI、PT、INR值及达到稳定抗凝效果后的华法林血药浓度差异无统计学意义(P<0.05),但CYP2C9*1* 1型患者INR首次达标时间>CYP2C9*1*3型患者(P=0.013),CYP2C9*1*1型患者华法林日均稳定维持剂量 >CYP2C9*1*3型患者(P=0.011),GGCX*A*G型患者华法林日均稳定维持剂量>GGC X*G*G型患者(P=0.000),两者差异有统计学意义。见表1、2。
2.2 华法林治疗有效性情况
在80例研究对象中,有59例(73.8%)在术后第6日进入治疗窗,有10例(12.5%)超出治疗窗,有11例(13.7%)仍未达到治疗窗。在2种基因型患者中,CYP2C9*1*1型患者前5天累计服用华法林(19.3±3.9)mg,CYP2C9*1*3型患者前5天累计服用华法林(17.2±4.1)mg,两者差异无统计学意义(P=0.179 );GGCX*A*G型患者前5天累计服用华法林(19.2±3.7)mg,GGCX*G*G型患者前5天累计服用华法林(17.4±4.0)mg,两者差异无统计学意义(P=0.108)。见表2。

表1 一般资料的华法林治疗情况 例
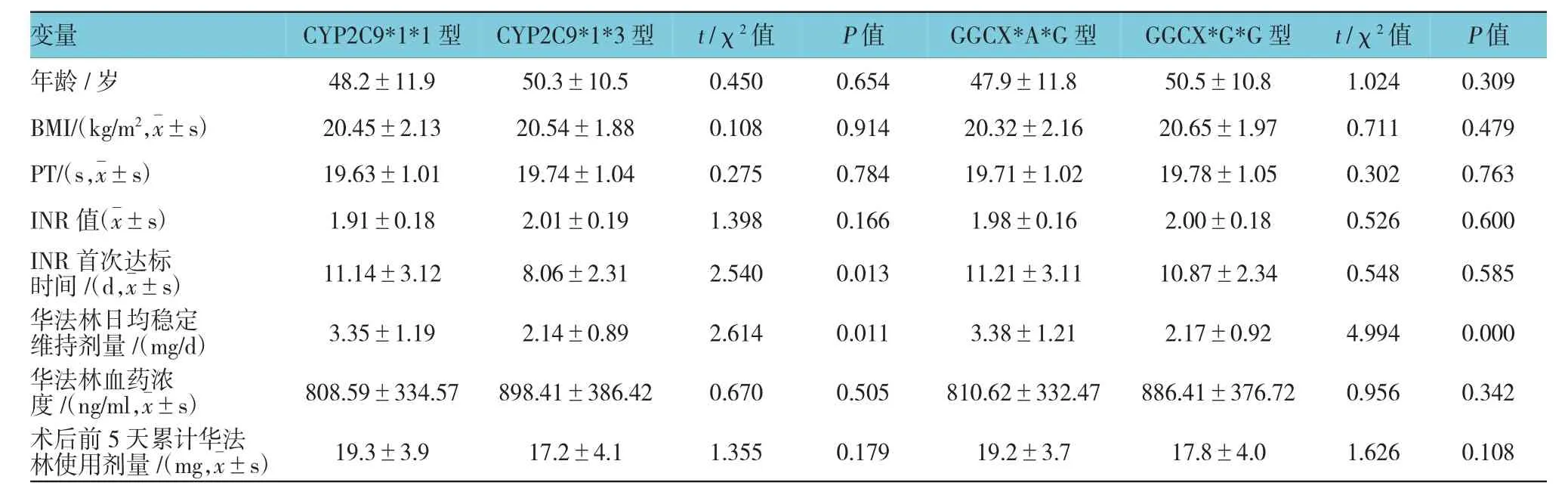
表2 患者一般情况和华法林治疗情况
在2种基因型的4种组合中,所需的华法林日均稳定维持剂量差异有统计学意义(F=4.121,P=0.024);其中,同时为CYP2C9*1*1型和GGCX*A*G型的患者华法林日均稳定维持剂量>其他3组(P<0.05)。见表3。
2.3 影响华法林治疗有效性的因素
以华法林治疗是否有效为因变量,将可能影响华法林治疗有效性的因素纳入非条件多元Logistic回归方程,以0.05为引入水准采用逐步法进行回归分析。包括CYP2C9基因型、GGCX基因型、性别、年龄、BMI、INR、术前Cr、术后Cr、术前PLT及术后PLT等。结果表明,CYP2C9基因型、GGCX基因型及术前血清Cr水平是影响患者术后第6天是否能达到治疗窗的影响因素。见表4。
表3 患者接受华法林治疗的日均稳定维持剂量 (±s)
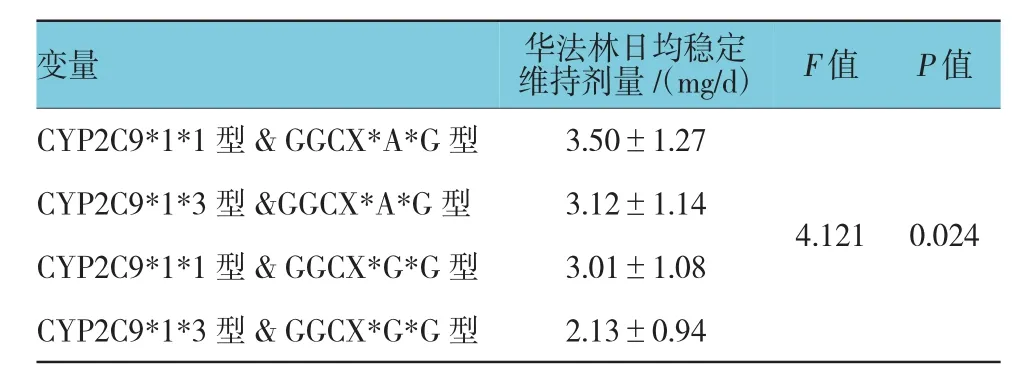
表3 患者接受华法林治疗的日均稳定维持剂量 (±s)
变量P值CYP2C9*1*1型&GGCX*A*G型 3.50±1.27华法林日均稳定维持剂量/(mg/d)F值CYP2C9*1*3型&GGCX*A*G型 3.12±1.14 CYP2C9*1*1型&GGCX*G*G型 3.01±1.08 CYP2C9*1*3型&GGCX*G*G型 2.13±0.94 4.121 0.024
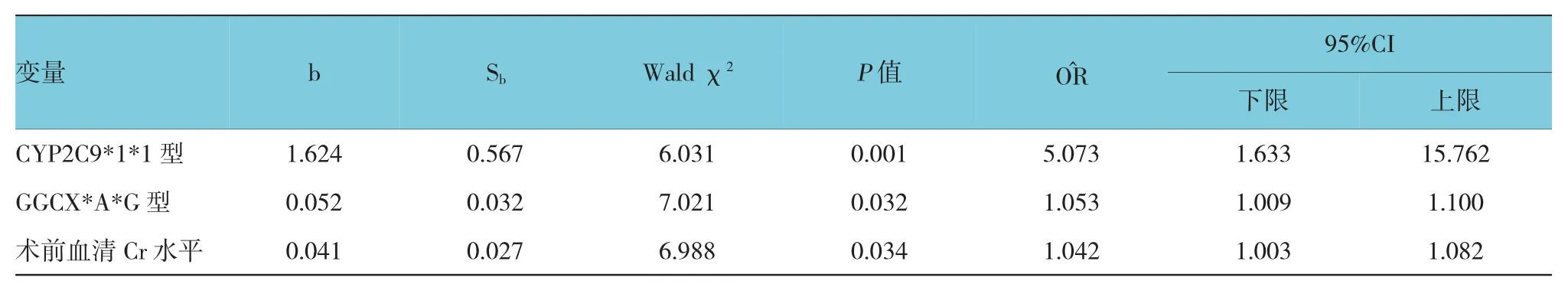
表4 影响华法林治疗有效性影响因素的多因素Logistic回归分析相关参数
3 讨论
人工瓣膜置换术是治疗严重心脏瓣膜疾病的有效方法,但人工瓣膜表面材料易与血液相互作用导致血液动力学发生改变而形成血栓。华法林是香豆素类口服抗凝药,在人工瓣膜置换术后预防血栓时常用[7]。由于治疗窗口较窄,不同个体间的稳定治疗剂量差异大,合理选择个性化的用药方案是心脏瓣膜置换术后远期疗效的重要影响因素之一。CYP2C9是代谢华法林S-型对映体的重要酶,不同基因型会影响肝脏中华法林的代谢,从而影响华法林的抗凝效果,使到达治疗窗的时间及日均稳定维持剂量不同。本研究发现,CYP2C9*1*1型患者INR首次达标时间>CYP2C9*1*3型患者,CYP2C9*1*1型患者华法林日均稳定维持剂量>CYP2C9*1*3型患者,但两者间的华法林血药浓度无差异,表明不同基因型的治疗效果差异可能与其编码的酶活性有关。CYP2C9*1*3型患者所编码的代谢酶受到损伤,其活性<CYP2C9* 1*1型患者的酶活性,使该型患者的肝脏对华法林代谢变慢,延长华法林在体内的分布和代谢时间,使得S-型对映体的药理活性延长,从而促使INR达标时间变短,并只需相对较低的剂量即可维持稳定的抗凝效果[8-9]。相关研究也表明,GGCX G3261A多态位点与华法林稳定剂量相关[10]。
本研究80例患者中,华法林的日均稳定维持剂量在1.8~8.7mg/d,个体差异性很大,提示采用个性化治疗方案的重要性。本研究选择的目标INR值为1.8~2.5,属于低度抗凝标准,研究对象未发生严重出血,仅有3例发生血栓,表明该抗凝标准较为合理有效[11]。
本研究发现,CYP2C9*1*1型患者和CYP2C9* 1*3型患者术后前5天累计华法林使用剂量两者比较无差异,表明CYP2C9不同基因型对初始抗凝阶段的华法林剂量并无影响。在CYP2C9*1*1型患者中有76.7%进入治疗窗,而在CYP2C9*1*3型患者中有42.9%进入治疗窗,同时还有42.9%超过治疗窗,Logistics多元回归分析也发现,不同CYP2C9基因型是影响患者术后第6天是否能达到治疗窗的影响因素,提示对于CYP2C9*1*3型患者使用华法林治疗时会更容易出现INR超出治疗窗的风险,从而使得发生出血等并发症的风险增加,因此要减少该类患者的法华林起始剂量,并注意使用较低的日均稳定维持剂量[12-15]。
综上所述,对于人工瓣膜置换术后使用华法林进行抗凝治疗的患者,先行进行CYP2C9基因型检测,然后再确定华法林的使用剂量可以减少出血等并发症的发生,尽快进入治疗窗,提高患者生存质量。
[1]吴颖猛,黄伟钊,姜海明,等.人工瓣膜置换治疗重症心脏瓣膜病的临床研究[J].实用医学杂志,2013,29(13):2162-2164.
[2]沈凯,王晓臣.生物瓣膜置换术治疗老年心脏瓣膜病的安全性及疗效[J].西部医学,2016,28(3):403-405.
[3]范永峰,张大国,向道康,等.人工瓣膜置换治疗重症心脏瓣膜病的临床分析[J].中外医疗,2015(22):93-94.
[4]JORGENSEN A L,FITZGERALD R J,OYEE J,et al.Influence of CYP2C9 and VKORC1 on patient response to warfarin:a systematic review and meta-analysis[J].PloS One,2012,7(8):e44064.
[5]潘耀东,李胜军.CYP2C9*3(1061A/C)基因多态性与瓣膜置换术后患者华法林用量关系的临床研[J].外科学杂志,2011,17(6):1-2.
[6]郭刚.云南汉族GGCX基因多态性与华法林治疗剂量的相关性研究[D].昆明:昆明医学院,2011.
[7]谢爽.CYP4F2基因多态性与华法林维持剂量关系的研究进展[J].中国新药杂志,2011,20(13):1183-1187.
[8]TATARUNAS V,LESAUSKAITE V,VEIKUTIENE A,et al.The effect of CYP2C9,VKORC1 and CYP4F2 polymorphism and of clinical factors on warfarin dosage during initiation and long-term treatment after heart valve surgery[J].Journal of Thrombosis and Thrombolysis,2013,5(6):24-28.
[9]张亚同.基于连接酶反应检测华法林相关基因VKORC1、CYP2C9多态性[J].中国临床药理学与治疗学,2010,15(12):1395-1401.
[10]李文慧,许冰莹,邓建强,等.云南汉族人群GGCX(rs699664)基因多态性与华法林抗凝治疗剂量的相关性研究[J].现代诊断与治疗,2014(14):3121-3123.
[11]张海霞,葛卫红.临床医师参与抗凝治疗管理的实践与体会[J].医药导报,2012,29(6):813-815.
[12]刘娟.人工心脏瓣膜置换术患者术后护理体会[J].临床医药文献杂志,2016,3(4):694-695.
[13]卢珊,张清媛.心脏瓣膜置换术后服用华法林抗凝指导及健康教育[J].临床医学工程,2012,19(2):263-264.
[14]谭胜蓝,周新民,李智,等.华法林与苯妥英钠合用导致出血1例报道[J].中国现代医学杂志,2012,22(25):111-112.
[15]李俊,梁法禹,曹森垚,等.人工瓣膜置换治疗后华法林抗凝的安全性分析[J].中西医结合心脑血管病杂志,2016,14(12):1432-1433.
Anticoagulation effect among patients with differentCYP2C9and GGCXgentypes who
mechanical heart valve prostheses replacement
Hong-ye Chen1,Bo Yu1,Qi-ming Tan1,Yong Li1,Liang-guang Qin1,Yan Yang2
(1.Department of Cardiovascular Surgery,Lianyungang First People's Hospital,Lianyungang, Jiangsu 222000,China;2.Fuwai Hospital,Chinese Academy of Medical Sciences, Beijing 100037,China)
ObjectiveToinvestigatetheimpactofdifferentgenotypesofCYP2C9 and GGCX on anticoagulative effect after prosthetic valve replacement.MethodsPatients who received prosthetic valve replacement in our hospital between 2013 and 2016 were enrolled in the research,CYP2C9andGGCX genotypes were tested with 3ml peripheral venous blood sample which was collected after taking medicire and fasting for 12 h and clinical data were collected for all the patients enrolled.SPSS 21.0 software was used for statistical analysis.ResultsEighty patients were enrolled in this research,and two types ofCYP2C9gene were found,including CYP2C9*1*1 in 73 patients and CYP2C9*1*3 in 7 patients.ForGGCXgene,there were 42GGCX*A*G patients and 38 GGCX*G*G patients.There was no significant difference between the two groups in the gender,age,BMI,PT,INR value,or the maintenance blood concentration of Warfarin. Honever it was longer for CYP2C9*1*1 patients to reach the first effective INR value than that of theCYP2C9*1*3 patients (P=0.013).The daily maintenance dosage of Warfarin for CYP2C9*1*1 patients was higher than that of CYP2C9*1*3 patients (P=0.011),and GGCX*A*G patients'daily maintenance dosage of Warfarin was higher than GGCX*G*G patients' (P=0.000).Those patients with both CYP2C9*1*1 and GGCX*A*G needed higher daily maintenance dosage of Warfarin than others(P=0.024).CYP2C9gene was a significant influencing factor associated with INR within the therapeutic window on the 6th day after operation.ConclusionsPrediction of individual Warfarin dosage based on patient'sCYP2C9gene andGGCXgene can improve the anticoagulative effect.
CYP2C9gene;GGCXgene;prosthetic valve replacement;anticoagulation
R542.5
A
10.3969/j.issn.1005-8982.2017.18.012
1005-8982(2017)18-0062-04
2017-01-25
杨研,E-mail:docyy@tom.com;Tel:13683210212

