GnRH-a联合妈富隆治疗子宫内膜异位症效果观察
徐凌燕
(青海省人民医院,西宁 810001)
GnRH-a联合妈富隆治疗子宫内膜异位症效果观察
徐凌燕
(青海省人民医院,西宁 810001)
目的 探讨促性腺激素释放激素(GnRH-a)与妈富隆联合应用治疗子宫内膜异位症(EM)的疗效。方法 选择EM患者100例,分为对照组48例、观察组52例。对照组予GnRH-a类药物醋酸曲普瑞林3.6 mg经腹部皮下注射,每隔 28 d注射 1次,共 6次。观察组采用醋酸曲普瑞林皮下注射联合妈富隆口服治疗。治疗3个月时评价临床疗效,采用女性性功能指数FSFI问卷调查表评价治疗前后腹部疼痛症状评分,采用阴道B超检测子宫内膜厚度,采用电化学发光全自动免疫分析仪检测血清炎症因子IL-18、TNF-α及性激素卵泡刺激素(FSH)、雌二醇(E2)水平。结果 观察组、对照组有效率分别为96.15%(50/52)、83.33%(40/48),观察组有效率高于对照组(P<0.05)。观察组治疗后盆腔痛、痛经、性交痛和疼痛总分均低于对照组(P均<0.05)。观察组治疗后子宫内膜厚度低于对照组(P<0.05)。观察组治疗后血清IL-18、TNF-α、FSH、E2水平均低于对照组(P均<0.05)。结论 GnRH-a联合妈富隆对EM患者有较好的治疗效果,可明显改善患者的临床症状、炎症程度及激素水平。
促性腺激素释放激素;妈富隆;子宫内膜异位症;腹部疼痛;性激素;炎症因子
子宫内膜异位症(EM)是临床较常见的妇科良性增生性疾病,发病率可达0.006%以上,且近年来呈明显上升趋势[1]。EM往往呈侵袭性生长趋势,病情发生发展可导致患者痛经、下腹痛不适甚至不孕等临床结局[2]。促性腺激素释放激素(GnRH-a)是治疗EM的常用药物,可以通过抑制下丘脑-垂体-卵巢轴激素的异常分泌,进而抑制局部子宫内膜或者卵巢等EM病灶组织中的雌激素水平,避免长期雌激素导致的病灶侵袭性增殖。但GnRH-a治疗后的临床总体有效率仍然不足45%,且治疗后的病情缓解率不高,复发率仍可达25%以上,提示GnRH-a治疗具有一定局限性[3]。妈富隆是新型的孕激素拮抗剂,在拮抗孕激素导致的病灶增殖的同时,可以通过拮抗雌激素导致的异位症病灶组织细胞的侵袭,进而改善症状[4~6]。2015年3月~2016年8月,我们应用GnRH-a类药物注射用醋酸曲普瑞林与妈富隆联合应用治疗EM,探讨GnRH-a联合妈富隆治疗EM的临床效果。现报告如下。
1 资料与方法
1.1 临床资料 选取同期在我院治疗的EM患者100例,年龄23~45(35.68±3.15)岁,EM病程1~8(5.03±0.98)年。随机分为对照组48例、观察组52例。纳入标准:年龄≥18岁;无其他系统严重疾病。排除标准:临床资料不全;合并内分泌系统疾病。两组年龄、病程等资料差异无统计学意义,具有可比性。本研究经医院伦理委员会批准。
1.2 治疗方法 对照组予注射用醋酸曲普瑞林3.6 mg经腹部皮下注射,每隔 28 d注射 1次,共 6次。
观察组于注射第4支时同时口服避孕药妈富隆1片/d,共 21 d,待停药后月经会自行来潮,于月经第5天继续服用下一周期妈富隆。
1.3 临床疗效评价 治疗3个月时评价临床疗效,显效为激素水平和子宫内膜厚度完全恢复正常;有效为激素水平和子宫内膜厚度基本恢复正常;无效为激素水平和子宫内膜厚度均未恢复正常。总有效率=(显效+有效)/总例数×100%。
1.4 腹部疼痛症状评分评价 治疗3个月时,采用女性性功能指数FSFI问卷调查表评价治疗前后腹部疼痛症状评分。
1.5 子宫内膜厚度检测 治疗3个月时,采用阴道B超检测子宫内膜厚度。
1.6 血清炎症因子及性激素水平检测 治疗3个月时,清晨采集空腹静脉血,分离血清后,采用电化学发光全自动免疫分析仪检测血清炎症因子IL-18、TNF-α及性激素卵泡刺激素(FSH)、雌二醇(E2)水平。
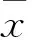
2 结果
2.1 两组临床疗效比较 观察组显效28例、有效22例、无效2例、总有效率为96.15%,对照组分别为22、18、8例及83.33%,观察组总有效率高于对照组(P<0.05)。
2.2 两组治疗前后腹部疼痛症状评分比较 两组治疗前疼痛评分差异无统计学意义。两组治疗后盆腔痛、痛经、性交痛和疼痛总分均低于治疗前(P均<0.05),观察组治疗后盆腔痛、痛经、性交痛和疼痛总分均低于对照组(P均<0.05)。见表1。
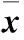
表1 两组治疗前后腹部疼痛症状评分比较(分,±s)
注:与同组治疗前比较,*P<0.05;与对照组治疗后比较,﹟P<0.05。
2.3 两组治疗前后子宫内膜厚度比较 两组治疗前子宫内膜厚度差异无统计学意义。两组治疗后子宫内膜厚度均低于治疗前(P均<0.05),观察组治疗后子宫内膜厚度低于对照组(P<0.05)。见表2。
2.4 两组炎症因子及性激素水平比较 两组治疗前血清IL-18、TNF-α、FSH、E2水平差异无统计学意义。两组治疗后血清IL-18、TNF-α、FSH、E2水平均低于治疗前(P均<0.05),观察组治疗后血清IL-18、TNF-α、FSH、E2水平均低于对照组(P均<0.05)。见表2。
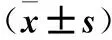
表2 两组治疗前后子宫内膜厚度及血清IL-18、TNF-α、FSH、E2水平比较
注:与同组治疗前比较,*P<0.05;与对照组治疗后比较,#P<0.05。
3 讨论
多次人工流产、长期的盆腔慢性炎症性疾病及遗传易感因素等,均可以促进EM的发生发展,特别是在具有异常流产病史的人群中,EM的发病率更高。临床上EM的发生可以导致患者盆腔内输卵管或卵巢组织的破坏,进而导致卵巢内分泌功能、输卵管输送卵子等的功能障碍,导致不良临床结局的发生。GnRH-a可以通过拮抗中枢神经系统的性激素释放激素受体,进而长期、稳定地抑制卵巢雌激素的分泌,促进异位症病灶组织的凋亡。但相关研究显示,单纯GnRH-a治疗后的患者异位症病灶组织的凋亡程度不足35%[7,8],仍然存在部分异位症病灶内膜腺体细胞的持续性增生,且长期GnRH-a治疗容易导致患者内分泌激素的紊乱,并可反射性刺激患者雄激素的分泌[9~11]。
妈富隆为口服避孕药,其可通过减少内膜内甾体受体,抑制FSH、LH和内源性雌激素水平,使内膜蜕膜化,抑制排卵,减轻排卵后的雌激素波动导致的异位症病灶组织细胞的增生。药理学研究也显示,妈富隆的抗孕激素作用可以在拮抗孕激素受体的同时,拮抗雌激素受体,并通过抑制细胞膜表面的糖蛋白受体,进而抑制卵巢组织中卵泡的增生导致的雌激素的释放,进而促进异位症病灶新生血管或者新生组织的萎缩[12~14]。已有研究表明,妈富隆治疗EM具有一定的临床效果,但尚缺乏妈富隆联合GnRH-a治疗的相关研究。妈富隆的应用,可以在促进病灶组织新生血管的萎缩、抑制病灶对于卵巢皮层的侵袭,并改善局部盆腔内微环境等方面发挥作用,从而减轻异位症病灶持续性增殖导致的盆腔痛或性交痛等的发生。朱英宏等[15]研究发现,GnRH-a联合妈富隆治疗可以降低25%的EM患者的性交痛。本研究发现,观察组治疗后盆腔痛、痛经、性交痛和疼痛总分均低于对照组,提示在GnRH-a治疗的基础上联合妈富隆治疗,可以进一步改善EM患者的自主症状,有利于改善患者的治疗依从性。本研究发现,观察组治疗后子宫内膜厚度低于对照组,提示妈富隆能够拮抗子宫内膜的过度雌激素刺激,稳定子宫内膜的增生期改变,并拮抗过度增生导致的内膜腺体对子宫内膜基底膜的浸润。
IL-18和TNF-α等炎症因子可以通过加剧盆腔局部氧化应激反应,促进局部单核细胞、巨噬细胞等富集导致的异位症病灶组织的侵袭或正常组织的持续性破坏。研究发现,妈富隆可抑制局部异位症病灶的对临近组织的侵袭能力,可以减轻自身免疫性因素导致的反应性炎症反应的发生,且对于孕激素及雌激素受体具有协同性抑制作用,可以抑制炎症信号通路如Rock的激活导致的IL-18和TNF-α等的释放。本研究发现,观察组治疗后血清IL-18、TNF-α水平均低于对照组,提示在GnRH-a治疗的基础上联合妈富隆治疗可明显降低血清炎症程度。
FSH、E2是促进蜕膜增殖、维持病灶组织活性的重要因素。妈富隆可稳定性激素水平,可通过抑制下游促进卵巢性激素分泌的作用,降低过度激素分泌紊乱导致的雌激素分泌,也可通过调控下丘脑-垂体-卵巢轴,稳定负反馈调节机制,抑制FSH、E2的分泌。本研究发现,观察组治疗后血清FSH、E2水平均低于对照组,提示妈富隆能够进一步稳定性激素水平,GnRH-a联合妈富隆可通过改善FSH及E2的分泌提高EM的治疗效果。
综上所述,GnRH-a联合妈富隆对EM患者有较好的治疗效果,可明显改善患者的临床症状、炎症程度及激素水平,具有良好的应用价值。
[1] Gao H, Wang Q, Li Q, et al. Efficacy and safety investigation of Kuntai capsule for the add-back therapy of gonadotropin releasing hormone agonist administration to endometriosis patients: a randomized, double-blind, blank- and tibolone-controlled study[J]. Chin Med J (Engl), 2015,128(4):427-431.
[2] Divasta AD, Feldman HA, Sadler GJ, et al. Hormonal add-back therapy for females treated with gonadotropin-releasing hormone agonist for endometriosis[J]. Obstet Gynecol, 2015,126(3):617-627.
[3] Lee D, Park HG, Yoon B, et al. Effects of different add-back regimens on hypoestrogenic problems by postoperative gonadotropin-releasing hormone agonist treatment in endometriosis[J]. Obstet Gynecol Sci, 2016,59(1):32-34.
[4] 芦延峰. 腹腔镜配合妈富隆、孕三烯酮以及亮丙瑞林治疗子宫内膜异位症的比较研究[J]. 中国妇幼保健,2013,42(30):5075-5076.
[5] 付丽. 腹腔镜术后联合GnRH-a及去氧孕烯炔雌醇片治疗子宫内膜异位症疗效观察[J]. 中国现代医生,2015,25(32):58-60.
[6] 卞美璐,黄书慧,邓文红,等. 醋酸亮丙瑞林微球治疗子宫内膜异位症随机盲法Ⅱ期临床试验[J]. 中华妇产科杂志,2015,24(3):188-193.
[7] Takaesu Y, Nishi H, Kojima J, et al. Dienogest compared with gonadotropin-releasing hormone agonist after conservative surgery for endometriosis[J]. J Obstet Gynaecol Res, 2016,42(9):1152-1158.
[8] Sadler GJ, Feldman HA, Stokes NA, et al. The effects of gonadotropin-releasing hormone agonist combined with add-back therapy on quality of life for adolescents with endometriosis: a randomized controlled trial[J]. J Pediatr Adolesc Gynecol, 2016,25(5):90-92.
[9] 隋敏,张秀枝,邹珺. 中重度子宫内膜异位症腹腔镜术后辅助妈富隆或孕三烯酮的疗效比较[J]. 湖北医药学院学报,2014,32(3):273-275.
[10] 施秀,徐炜,孙莹,等. 甾体激素受体辅激活子对子宫内膜异位症患者异位子宫内膜基质细胞中基质细胞衍生因子1表达的影响[J]. 中华妇产科杂志,2014,25(2):114-119.
[11] 吕淑霞,许秀芹. 诺雷德联合妈富隆口服对子宫内膜异位症术后复发的预防效果观察[J]. 山东医药,2012,52(6):38-39.
[12] 徐乐乐,叶箐华. 妈富隆联合红金消结片治疗子宫内膜异位症临床观察[J]. 浙江中西医结合杂志,2012,25(7):545-547.
[13] 王丽钗,陈剑红,史华平. 戈舍瑞林联合妈富隆对腹腔镜治疗子宫内膜异位症疗效观察[J]. 中华内分泌外科杂志,2015,24(5):415-418.
[14] 汪具荣. 诺雷德联合妈富隆预防子宫内膜异位症术后复发的效果观察[J]. 牡丹江医学院学报,2012,22(5):53-54.
[15] 朱英宏. 促性腺激素释放激素激动剂联合妈富隆治疗重度子宫内膜异位症的临床评价[J]. 中国妇幼保健,2015,34(29):4969-4970.
10.3969/j.issn.1002-266X.2017.30.022
R711.71
B
1002-266X(2017)30-0070-03
2017-01-12)

