高效液相色谱法测定茶叶中的氟含量
陈小聪,刘珈伶,段玉林,刘 星,杨 黎
(广西—东盟食品药品安全检验检测中心,南宁 530001)
高效液相色谱法测定茶叶中的氟含量
陈小聪,刘珈伶,段玉林,刘 星,杨 黎
(广西—东盟食品药品安全检验检测中心,南宁 530001)
建立了一种高效液相色谱法快速、准确测定茶叶中氟。样品经浸泡提取后,以邻苯二甲酸为背景吸收,以Agilent ZORBAX-ODS柱(4.6mm×250mm,5μm),流动相为乙腈-0.1mol/L邻苯二甲酸溶液(15∶85,V∶V),柱温35℃,检测波长294nm,流速1.0mL/min的条件进行实验。结果表明:氟在0.5~10.0μg/mL范围内线性关系良好,平均回收率为101.0%。建立的方法准确、可靠,可以用于茶叶中氟的含量检测。
茶叶;氟;高效液相色谱;邻苯二甲酸
氟是人体必需的微量元素,世界卫生组织规定其适宜量是人均每天摄入量2.5~4.0mg[1-2],摄入过量时可引起氟牙病、氟骨症、氟尿和钙代谢紊乱等疾病[3-4],快速准确检测茶叶中氟含量具有重要的意义。当前常见测定氟的方法有分光光度法[5-6]、离子选择性电极[7-8]和离子色谱法[9]。离子色谱测定时受到样品基体效应影响大、预处理要求高,对于氟离子、弱酸根离子和活泼阴离子的测定难度较大;离子选择电极和分光光度法在其灵敏度和选择性方面有待继续提升。本文利用邻苯二甲酸吸收为背景建立起F-的高效液相色谱法,具有较广泛的应用普及性和较高的灵敏度,可用于茶叶中氟的测定。
1 材料与方法
1.1 主要仪器与试剂
仪器:带二极管阵列检测器的高效液相色谱仪(PDA-HPLC,Waters e2695- 2998)。主要试剂:氟离子标准溶液(NaF,1 000mg/L溶于 H2O)、乙腈(色谱纯)、邻苯二甲酸(优级纯)、水(超级纯,电阻率为18.2MΩ·cm)、氢氧化钠(优级纯)、绿茶(市售,生产日期2016/11/06)。
1.2 液相色谱条件
Agilent ZORBAX-ODS柱子(4.6mm×250mm,5μm),流动相为0.1mol/L的邻苯二甲酸水溶液和乙腈,其体积比为85:15。检测波长294nm,柱温35℃,流速1.0mL/min,进样量10μL。
1.3 标准溶液的配制
移取1mL浓度为100mg/mL的标准溶液到100mL容量瓶中,用纯水定容至刻度摇匀,得浓度为1mg/mL的标准储备液;取标准储备液10~100mL容量瓶中,用纯水定容至刻度摇匀,得浓度为100μg/mL的标准使用液;分别移取0.5、1.0、2.5、5.0、10.0mL于100mL容量瓶中,用纯水定容至刻度,摇匀,得标准系列工作液质量浓度分别为0.5、1.0、2.5、5.0、10.0μg/mL。
1.4 样品处理
称取3.0g绿茶于高52mm、上口内径80mm、底径45mm的杯子中,注满沸水,加盖浸泡5min后过滤得茶水[10]。滤液转移至100mL容量瓶后定容后待测。
1.5 离子色谱法
1.5.1 样品处理 按1.5法处理样品,滤液经C18柱、Ag柱和Na柱过柱净化后,过0.45μm滤膜,待离子色谱仪检测。
1.5.2 离子色谱条件 检测器:电导检测器;色谱柱为Metrosep A Supp 7-250(250mm×4.0 mm);淋洗液为3.6mmol/L碳酸钠溶液;流速为0.7mL/min;柱温为45℃;进样量250μL。
2 结果与分析
2.1 样品前处理方法
样品前处理采用茶叶感官评审国家标准中规定的方法[10],以定量的样品、浸泡水和固定的浸泡时间来评判茶叶中含氟物质的浸出,具有可重复性和科学性。
2.2 检测波长与流动相的选择
选用具有较强紫外吸收的邻苯二甲酸作为背景吸收[11],当无吸收的F-试样通过检测器流通池时,紫外吸收将会降低,在谱图中将会出现一个负吸收的峰,其峰面积同F-的含量成正比。以二极管阵列检测器(PDA)扫描5μg/mL氟离子标准溶液(扫描波长200~400nm),最大负吸收位置为294nm处,提取294nm处的液相色谱图,确定F-离子最大负吸收位置为294nm处(图1)。
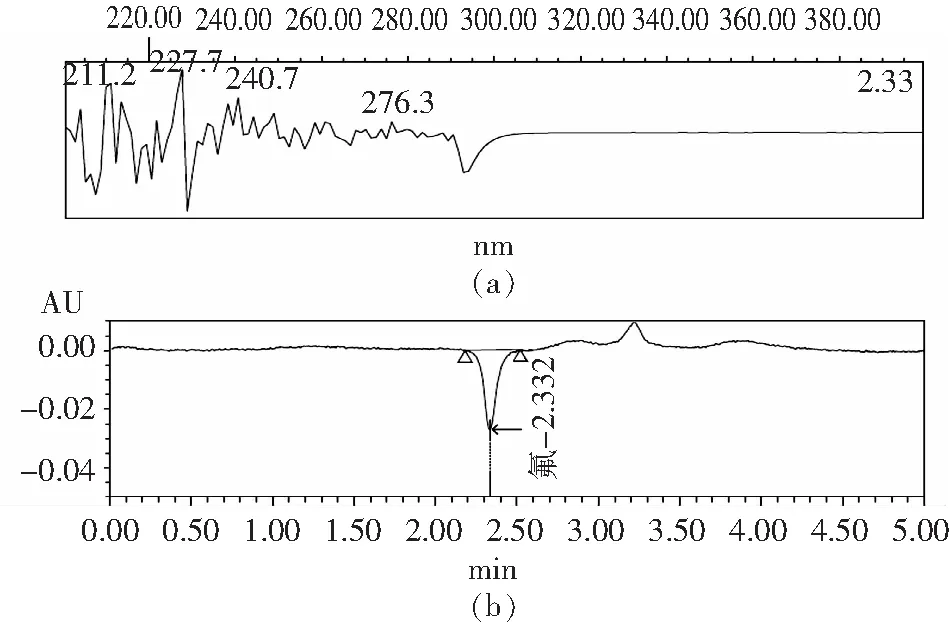
(a)PDA光谱图;(b)294nm处的液相色谱图图1 氟的电子吸收光谱
参照标准GB/T 5009.167-2003需将邻苯二甲酸同乙腈按86:14比例混合后再以0.1mol/L的氢氧化钠溶液调节pH至8.6作为流动相,但氟离子并未出峰(图2)。
因此不再调节流动相pH值,但流动相比例也影响着色谱图效果,实验以5μg/mL氟离子标准溶液进样10μL,考察邻苯二甲酸溶液-乙腈比例分别为92∶8、80∶20、85∶15时的液相色谱结果。通过优化其比例,本方法最终采用邻苯二甲酸溶液:乙腈=85∶15为流动相,并在该流动相条件下,测得样品中被测组分的保留时间为2.376min(图3)。
2.3 线性关系及仪器检出限
取质量浓度为0.5、1.0、2.5、5.0、10.0μg/mL的系列标准溶液分别进样10μL,记录色谱峰峰面积,以峰面积与浓度作线性回归,得氟离子的线性回归方程为Y=14 116X+10 516,相关系数r=0.999 8(图4)。
图4结果表明,氟离子在0.5~10μg/mL质量浓度范围内色谱峰面积与质量浓度之间具有较好的线性关系。信噪比为3时,仪器响应值N=3×10-5,由线性方程Y=14 116X+10 516,可知斜率为b=14 116,理论检出限计算式如式(1)所示:
LOD=3N/b
(1)

图2 氟离子标准溶液液相色谱(流动相pH=8.6)

(a)氟离子标准溶液;(b)样品 图3 氟离子标准溶液和样品的液相色谱图
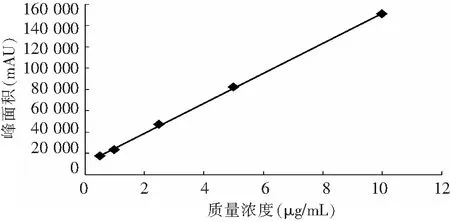
图4 氟离子的回归线性方程曲线
由此计算出理论最低检出限为9.0×10-11μg。由于样品检出,不断地稀释样品,当质量浓度稀释到0.02μg/ mL时还有检测信号,再向下稀释时信号不明显,得出该方法的最低检出限为0.02μg/ mL。
2.4 重复性试验
以2.5μg/mL的氟离子标准溶液连续重复进样6次,每次进样量为10μL。表1结果表明,溶液氟离子的平均浓度为2.598 3μg/mL,相对标准偏差(RSD)为0.13%,该方法精密度较好。

表1 重复性试验(n=6)
2.5 加标回收率试验
取10μg/mL标准溶液3.00mL,加入到3.0g样品中(该样品经3次测定后氟离子的平均含量为17.1μg/g),按样品同法处理,最终定容至100mL。平行测定5次,表2结果表明,样品平均回收率为101.0%,RSD=1.67%,该方法回收率良好。
2.6 液相色谱法与离子色谱法的测定结果对比
离子色谱(IC)是目前阴离子分析的首选方法[12]。由表3可以看出,2种检测方法对同一茶叶的检测相对偏差都在3%以内,可证明采用反相色谱法测定茶叶中的氟的方法的稳定有效。采用离子色谱法测定的整体偏低,这是由于离子色谱法对茶叶的浸泡液需要经过C18柱、Ag柱和Na柱的净化,然后才能过膜上机测试,在样品的处理过程存在着损失。

表2 回收率试验(n=5)
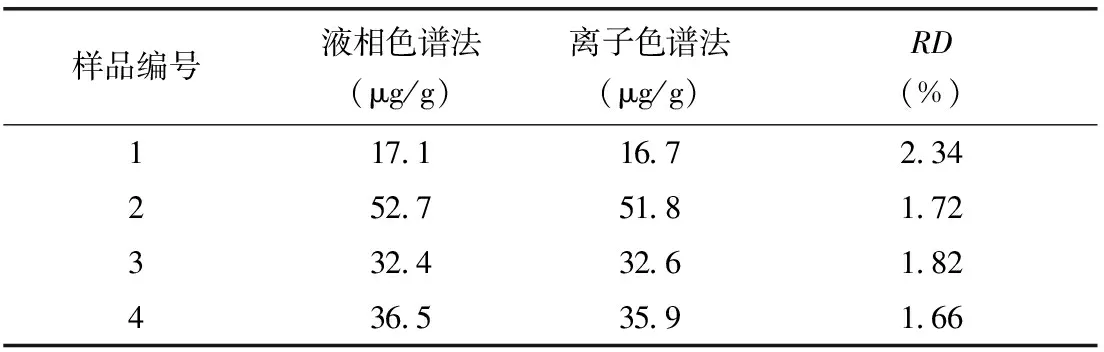
表3 液相色谱法和离子色谱法结果
3 结论
本实验采用高效液相色谱法对茶叶中溶出的氟含量进行检测,并与离子色谱法对比。在样品前处理方面省去了过柱净化的步骤,节约了实验时间,降低了实验成本,提高检测结果准确度。同时达到了一机多用的目的,对最大发挥大型仪器设备的利用率具有积极的意义。◇
[1]BORAH K K,BHUYAN B,SARMA H P.Lead,arsenic,fluoride,and iron contamination of drinking water in the tea garden belt of Darrang district,Assam,India[J]. Environmental Monitoring & Assessment,2010,169(1-4):347-352.
[2]张云桂,张昊,朱雯.砖茶氟的防龋功效及其应用[J]. 茶叶通讯,2010,37(4):7-8.
[3]SUYAMA E,TAMURA T,OZAWA T,et al.Remineralization and acid resistance of enamel lesions after chewing gum containing fluoride extracted from green tea[J]. Australian Dental Journal,2011,56(4):394-400.
[4]刘庆斌,李海蓉,王玉华,等.人体对砖茶中氟和铝的吸收与排泄作用观察[J]. 中华地方病学杂志,2011,30(2):134-136.
[5]IZUORA K,TWOMBLY J G,WHITFORD G M,et al.Skeletal fluorosis from brewed tea[J]. Journal of Clinical Endocrinology & Metabolism,2011,96(8):2318.
[6]赵成祥,李振林,张慧敏,等.饮茶型氟中毒病区居民健康教育干预的研究[J]. 医学动物防制,2013(2):153-155.
[7]周才碧,张敏星,穆瑞禄,等.茶叶中氟的研究进展[J]. 饮料工业,2014(7):10-14.
[8]YAMAMURA S S,WADE M A,SIKES J H.Direct Spectrophotometric Fluoride Determination.[J]. Analytical Chemistry,1962,34(10):1308-1312.
[9]GUAN F.Separation and Determination of Ions by High-performance Capillary Electrophoresis[J]. Chinese Journal of Analytical Chemistry,1995,23(1):111-116.
[10]SB/T 10157-1993.茶叶感官评审方法[S].
[11]GB/T 5009.167-2003.饮用天然矿泉水中氟、氯、溴离子和硝酸根、硫酸根含量的反相高效液相色谱法[S].
[12]李卫东,靳燕.离子色谱法测定水中的硝酸盐氮、氯化物、硫酸盐[J]. 石油化工应用,2010,29(12):100-103.
(责任编辑 李婷婷)
Detection on Fluoride in Tea by High Performance Liquid Chromatography
CHEN Xiao-cong,LIU Jia-ling,DUAN Yu-lin,LIU Xing,YANG Li
(Guangxi-ASEAN Food and Drug Safety Inspection and Testing Center,Nanning 530001,China)
A quick and accurate High Performance Liquid Chromatography (HPLC)method was established to detect the fluoride illegally added into tea.After extracted and absorbed by hot water,The sample was determined by HPLC and the background absorption was 1,2-Benzenedicarboxylic acid.The separation of fluoride was performed on a Agilent ZORBAX- ODS column (4.6mm×250mm,5μm)using acetonitrile -0.1mol/L 1,2-Benzenedicarboxylic acid(15∶85,v∶v)as the mobile phase with flow rate of 1.0 mL/min.The temperature was 35℃ and the detection was at 254 nm.The result showed that there is a good linear relation in the range of 0.5~10.0μg/mL with correlation coefficient of 0.9998.The average recovery was 101.0%,RSD= 1.67%.The method is accurate and feasible,suitable for determination of fluoride in the tea.
tea;fluoride;HPLC;1,2-Benzenedicarboxylic acid
陈小聪(1974— ),女,研究生,高级工程师,主要从事食品检验及质量管理。
段玉林(1982— ),高级工程师,研究方向:食品、保健食品及化工产品的分析检测。

