四种口蹄疫病毒非结构蛋白抗体ELISA试剂盒检测猪血清样本的质量评估
史 茜,陈瑞花,王科珂,徐新峰,卢曾军,季新成
(1. 新疆出入境检验检疫局,新疆乌鲁木齐 830063;2. 中国农业科学院兰州兽医研究所,甘肃兰州 730046)
四种口蹄疫病毒非结构蛋白抗体ELISA试剂盒检测猪血清样本的质量评估
史 茜1,陈瑞花1,王科珂1,徐新峰1,卢曾军2,季新成1
(1. 新疆出入境检验检疫局,新疆乌鲁木齐 830063;2. 中国农业科学院兰州兽医研究所,甘肃兰州 730046)
[目的] 对4种口蹄疫病毒非结构蛋白抗体ELISA试剂盒进行质量评估。[方法] 用4种商品化的口蹄疫非结构蛋白抗体ELISA检测试剂盒,对非免疫健康、免疫健康、免疫感染和非免疫人工感染4种类型猪血清样本进行检测,分析试剂盒的诊断敏感性、诊断特异性、分析敏感性、分析特异性及重复性。[结果] 4种试剂盒的诊断敏感性在76.8%~94.4%之间,诊断特异性在97.7%~100%之间,分析敏感性和分析特异性较好。4种检测试剂盒与4种猪常感染疾病的阳性血清不发生反应。试剂盒的批间重复性为(10.545±6.845)%~(37.577±28.626)%;批内重复性为(9.037±6.075)%~ (37.601±27.027)%。[结论] 在实际应用中,需根据检测目的不同,选取相应的试剂盒。
口蹄疫;非结构蛋白抗体;ELISA试剂盒;质量评估
口蹄疫(Foot-and-mouth disease,FMD)是由口蹄疫病毒(FMDV)引起的急性热性高度接触性传染病,一旦发病将严重影响疫情国家和地区的畜牧业发展和对外贸易,造成巨大经济损失,是世界各国高度关注的重大动物疫病,也是我国的一类动物疫病[1]。注射疫苗是防控该病的主要方法。如何区分自然感染动物和疫苗免疫动物在 FMD 防治中具有重要意义。
FMDV蛋白质根据是否存在于病毒颗粒中分为结构蛋白(Structural protein,SP)和非结构蛋白(Non-structural protein,NSP)。现代疫苗在加工过程中会去除非结构蛋白,因此以口蹄疫病毒的非结构蛋白为抗原,检测动物体内的NSP抗体是一种很好的区分感染动物和疫苗免疫动物的诊断方法。目前市售的NSP抗体检测试剂盒种类繁多,质量良莠不齐,对试剂盒进行质量评价的研究报道也较少。本试验选取了4种常用的商品化口蹄疫非结构蛋白抗体检测试剂盒,分别对非免疫无FMD、免疫健康、免疫感染和人工感染4类猪血清进行检测,用以评估试剂盒的灵敏度、特异性、重复性等质量参数,为试剂盒的选用提供技术支持。
1 材料与方法
1.1材料
1.1.1血清。非免疫无口蹄疫猪血清88份,采自加拿大;免疫健康猪血清88份,为田间背景下利用猪口蹄疫O型灭活疫苗(中农威特生物科技股份有限公司生产)免疫60 d后采血获得,采自新疆某猪场;猪水泡病、猪繁殖与呼吸综合征、猪传染性胃肠炎、猪呼吸道冠状病毒病和伪狂犬病毒抗体阳性血清,由新疆出入境检验检疫局技术中心中亚地区动物疫病检测国家重点实验室保存。人工免疫健康猪血清88份,为试验背景下注射1次疫苗后21 d和28 d采血获得;田间采集的免疫后疑似感染猪血清96份;人工感染猪血清108份,攻毒试验后10 d采集,均表现出FMD症状。以上样品由中国农业科学院兰州兽医研究所口蹄疫参考实验室提供。
1.1.2试剂盒。4种商品化的猪口蹄疫非结构蛋白ELISA检测试剂盒。A试剂盒:阻断ELISA,适用于牛、羊、猪血清的检测,国外进口,批号为F130601L、F130901L、F131201L;B试剂盒:间接ELISA,适用于猪血清的检测,国内生产,批号为2014052206F、2014111906F、2013100906F;C试剂盒:阻断ELISA,适用于猪血清的检测,国内生产,批号为20140607e、20141021e、20140910e;D试剂盒:间接ELISA,适用于猪血清的检测,国外进口,批号为20141126、20151114。
1.1.3主要仪器耗材。Spectra max plux 384酶标仪、Eppendorf各型号微量加样器。
1.2方法
分别对试剂盒的诊断敏感性、诊断特异性、分析敏感性、分析特异性及重复性等技术指标进行检测,试验操作及结果判定均按照试剂盒操作说明进行。
1.2.1诊断敏感性及诊断特异性试验。利用上述4种检测试剂盒,分别对88份非免疫无FMD猪血清样品(真阴性血清)和108份人工感染猪血清(真阳性血清)进行检测,按照说明书判定结果,按以下公式计算诊断敏感性和诊断特异性[2]:诊断敏感性=阳性样品检出数/已知阳性样品总数;诊断特异性=阴性样品检出数/已知阴性样品总数。
1.2.2分析敏感性试验。利用4种试剂盒,对108份人工感染猪血清进行检测;选取4种试剂盒检测均为阳性的6份血清,从1:2开始,进行10个梯度倍比稀释(即1:2、1:4、1:8、1:16、1:32、1:64、1:128、1:256、1:512、1:1 024),用4种检测试剂盒,分别对上述6份不同稀释度的样品进行检测,每份样品设复孔,以检出阳性结果的最高稀释倍数作为分析敏感性的检测结果。
1.2.3分析特异性试验。用4种检测试剂盒,分别检测猪繁殖与呼吸综合征、猪传染性胃肠炎、猪呼吸道冠状病毒病和伪狂犬病毒病的抗体阳性血清样品,每个样品设复孔,判断试剂盒检测样品时的分析特异性。
1.2.4重复性试验。每种试剂盒抽取3个批次,每个批次抽取3个试剂盒,分别对6份样品进行检测,每个样品做3个重复,由2个以上操作人员在不同的时间对相同样品进行重复检测。变异系数计算公式为CV=100%×(标准差/平均值),试剂盒的变异系数为6份样品变异系数的平均值±标准差。
1.2.5对免疫血清样品的检测。对免疫3次以上的健康猪血清、免疫健康猪血清和人工免疫21~28 d后采集的猪血清各88份进行检测。同时对96份田间免疫后疑似感染的猪血清进行检测。
2 结果与分析
2.1诊断敏感性和诊断特异性
用4种试剂盒,分别对已知阴性和阳性猪血清样品的检测结果为:4种试剂盒的诊断特异性均较高,在97.7%~100%之间;诊断敏感性在76.8%~94.4%之间;试剂盒D的诊断敏感性最高,试剂盒A、B和C的诊断特异性最高(表1)。

表1 4种试剂盒对已知阳性(诊断敏感性)和阴性(诊断特异性)血清样品的检测结果
2.2分析敏感性
对6个阳性血清倍比稀释样品的检测结果为:对1号样品检出的最高血清稀释度为1/8,2号与3号样品检出的最高稀释度为1/64,4~6号样品检出的最高稀释度稀释度大于1/1 024。试剂盒D对于6个样品的血清稀释度最低为1/8,最高大于1/1 024。试剂盒D具有较高的分析敏感性,试剂盒A次之(表2)。

表2 4种诊断试剂盒分析敏感性试验结果
2.3分析特异性
用4种检测试剂盒,对猪繁殖与呼吸综合征、猪传染性胃肠炎、猪呼吸道冠状病毒病和伪狂犬病毒病抗体阳性血清进行检测,均未检测出阳性。
2.4重复性
变异系数计算结果为:A和B试剂盒的批次内变异系数均小于10%,同时A和B 两种试剂盒的批间重复性小于15%,具有较高的批内和批间重复性;试剂盒D的批内重复性小于15%,批间重复性小于20%,C试剂盒批内、批间重复性均大于30%(表3)。

表3 4种诊断试剂盒重复性试验结果
2.5对免疫猪血清样品的检测
利用4种试剂盒,分别对88份免疫3次以上健康猪血清进行检测,结果除试剂盒D检出2份阳性样品外,其余试剂盒检测结果均为阴性;对88份随机采集的免疫健康猪血清的检测结果显示,试剂盒D检出4份阳性样品,试剂盒B检出1份阳性样品,试剂盒A与C未检出阳性样品;对试验背景下注射1次疫苗后21 d或28 d的猪血清检测结果为,试剂盒D检出3份阳性样品,其余试剂盒均未检出阳性样品。以上结果显示,4个试剂盒对免疫猪血清检测的特异性在96.6%~100%之间(表4)。
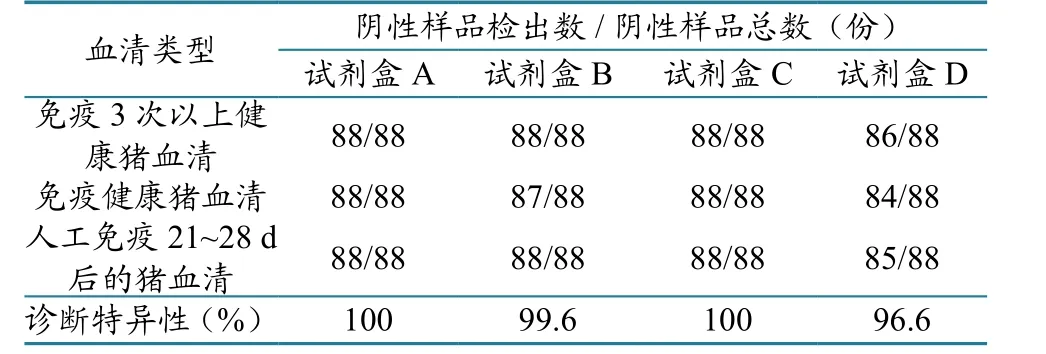
表4 4种诊断试剂盒对免疫后健康猪血清样品的检测结果
用4种试剂盒,对96份免疫后感染FMD的猪血清检测的结果为:试剂盒D检出阳性样品数85份,诊断敏感性为88.5%;试剂盒A检出阳性样品数为59份,诊断敏感性为61.5%;试剂盒B和C的诊断敏感性分别为53.1%和56.3%(表5)。
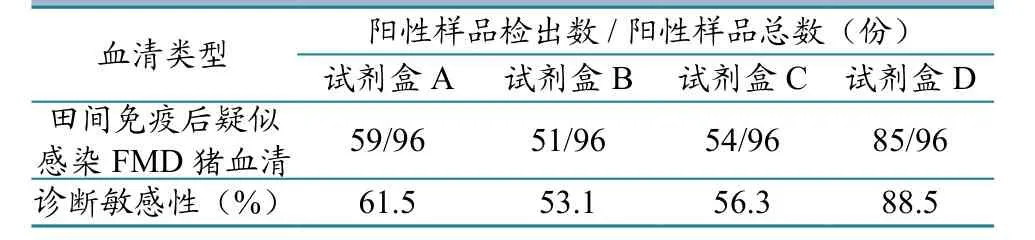
表5 4种诊断试剂盒对免疫后感染猪血清样品检测结果
3 讨论
20世纪90年代以来,研究发现针对3ABC、3B的血清抗体水平可以作为区分免疫动物和感染动物的指标[3-4]。这是因为在现代疫苗加工过程中,2C、3A、3B和3C等非结构蛋白会被去除,因此免疫动物体内不会产生针对NSP的抗体,只会诱导产生针对病毒结构蛋白的抗体。而当动物感染FMDV并出现病毒复制后,无论表现为临床或亚临床症状,动物都会出现2种抗体:一种是针对衣壳蛋白的抗体;另一种是针对NSP的抗体。后者可以用来区分免疫动物和感染动物。1997年在荷兰召开的有关学术研讨会上,与会学者确认以生物工程技术制备的3ABC作为抗原的ELISA方法是区分FMDV自然感染和疫苗免疫动物的理想方法[5]。国内外相继研制了很多检测NSP抗体的ELISA试剂盒,来区分检测免疫动物与感染动物,从而达到对疫病的诊断与防控的目的。目前我国缺乏对商品化试剂盒敏感性、特异性、重复性等指标的质量评估。然而试剂盒的低敏感性会造成假阴性的试验结果,使得感染动物未被检出,增加了该病的传播风险;低特异性又会造成误杀,因此增加了经济损失;重复性较差会造成检测结果不稳定。因此,对试剂盒的质量评估工作意义重大。
本试验通过对未免疫血清和免疫血清检测结果的比较可知,4个试剂盒对未免疫血清和免疫血清的诊断特异性分别在97.7%~100%和96.6%~100%之间,试剂盒D略低。4个试剂盒对上述两类血清的诊断敏感性检测结果差异较大,对未免疫血清的诊断敏感性在76.8%~94.4%之间,对免疫血清的诊断敏感性在53.1%~88.5%之间,未免疫血清的诊断敏感性高于免疫血清。Brocchi等[6]通过NCPanaftosa、IZS-Brescia、Ceditest、Svanova、Switzerland和UBI 6种试剂盒,对牛、羊、猪血清样品共3 551份进行检测,血清分为免疫动物、感染动物、自然发病动物和免疫后感染动物和非免疫感染动物。结果表明,6种试剂盒对未免疫感染动物的敏感性均达100%,对免疫后感染动物,NCPanaftosa、IZS-Brescia、Ceditest 3个试剂盒检测敏感性均在90%以上,特异性在99%以上。本实验的检测结果与Brocchi的结论总体一致,未免疫样品的诊断特异性和诊断敏感性也高于免疫血清。造成差异的原因可能是因为疫苗免疫后限制了病毒的复制,免疫动物NSP抗体的产生较未免疫动物慢,且抗体滴度较低[7]。诊断特异性低的原因可能是在疫苗加工处理过程中,NSP去除不完全,经免疫后也产生NSP抗体。试验结果也说明ELISA试剂盒用于检测未免疫样品检测的准确率更高。本试验评估的4种试剂盒的诊断敏感性较上述报道偏低,其原因可能是由于试验选取的免疫后感染猪血清采自田间疑似感染猪,而人工感染猪血清采自攻毒试验后10 d的猪。通常猪感染病毒1~2周后才开始产生NSP抗体[8-9]。故上述样品虽均表现出口蹄疫症状,但采样时尚未产生或只产生较弱的NSP抗体。通过实验还可看出,4种试剂盒对免疫3次后的健康血清与免疫1次的人工免疫健康猪血清的阴性检出率无明显差异,田间背景下免疫健康猪血清与实验室背景下免疫猪血清的检出率也无明显差异,因此3次以内的免疫次数与免疫条件对检测结果不会产生影响。
具有较高敏感性的试剂盒,不一定具有较高的特异性。综合判断,试剂盒D的诊断敏感性、诊断特异性、分析敏感性和分析特异性较好。实际应用中,应根据不同的检测目的,选取相应的试剂盒,如对于进出境动物检疫,要注重试验的敏感性,相反,对于流行病学监测,则应注重试验的特异性。
[1] World Organization for Animal Health(OIE). Manual of diagnostic tests and vaccines for terrestrial animals:Chapter 2.1.8 Foot and mouth disease [M]. Pairs:OIE,2016.
[2] 季新成,哈森,于学辉,等. 三种ELISA试剂盒对牛新孢子虫血清抗体比较检测[J]. 检验检疫学刊,2012,22(2):24-27.
[3] PABLO J J,COMPAIRED D,TROTTA M,et al. Validation of an r3AB1-FMDV-NSP ELISA to distinguish between cattle infected and vaccinated with foot-and-mouth disease virus[J]. Journal of Virological Methods,2011,178(1/2):191-200.
[4] BERGMANN I E,DE MELLO P A,NEITZERT E,et al. Diagnosis of persistent aphthovirus infection and its differentiation from vaccination response in cattle by use of enzyme-linked immunoelectrotransfer blot analysis with bioengineered non-structural viral antigens [J]. Am. J. Vet. Res,1993,54:825-831.
[5] DE DIEGO M I,BROCCHI E,MACKAY D,et al. The use of the non-structural polyprotein 3ABC of FMD virus as a diagnostic antigen in ELISA to differentiate infected from vaccinated cattle [J]. Arch Viro,1997,142:2021-2033.
[6] BROCCHI E,BERGMANN I E,DEKKER A,et al. Comparative evaluation of six ELISAs for the detection of antibodies to the non-structural proteins of foot-and-mouth disease virus [J]. Vaccine,2006,24(47/48):6966-6979.
[7] CHUNG W B,SORENSEN K J,LIAO P C,et al. Differentiation of foot-and-mouth disease virus-infected from vaccinated pigs by enzyme-linked immunosorbent assay using non-structural protein 3AB as the antigen and applicationto an eradication program [J]. J. Clin. Microbiol,2002,40:2843-2848.
[8] LEE F,LIN Y L,JONG M H. Comparison of ELISA for the detection of porcine serumantibodies to non-structural proteins of foot-and-mouth disease virus [J]. J. Virol. Methods,2004,116:155-159.
[9] CHEN S P,ELLIS T M,LEE M C,et al. Comparison of sensitivity and specif i city in three commercial foot-and-mouth disease virus non-structural proteins ELISA kits with swine sera in Taiwan [J]. Veterinary Microbiology,2007,119:164-172.
(责任编辑:朱迪国)
Evaluation on the Performance of Four ELISA Tests for Antibody against Non-structural Protein of Foot-and-mouth Disease in Swine Sera
Shi Qian1,Chen Ruihua1,Wang Keke1,Xu Xinfeng1,Lun Zengjun2,Ji Xincheng1
(1. Xinjiang Entry-exit Inspection and Quarantine Bureau,Urumqi,Xinjiang 830063;2. Lanzhou Veterinary Research Institute of Chinese Academy of Agriculture Science,Lanzhou,Gansu 730046)
[Objective]To evaluate the quality of four commercialized ELISA kits for the detection of antibodies to the non-structural proteins(NSPs)of Foot-and-mouth disease virus(FMDV). [Methods] The four commercialized ELISA kits were compared. The diagnostic sensitivity and specificity,analytic sensitivity and specificity,and repeatability of FMDV NSP ELISA kits were analyzed by detecting four types of sera from uninfected,vaccinated,naturally infected and challenged swine. [Results] The diagnostic sensitivity of the four ELISA kits were between 76.8% to 94.4%,the relatively high diagnostic specif i city were ranging from 97.7% to 100%,and both analytic sensitivity and specif i city were good. Sera from swine infected with other four different diseases cannot be detected using the kits. The repeatability of intra-assay was between(10.545±6.845)% to(37.577±28.626)%,and the inter-assay was between(9.037±6.075)% to(37.601±27.027)%. [Conclusion] In practice,the different kits could be selected for different detection purpose.
Foot-and-mouth disease;non-structural protein;ELISA kit;quality evaluation
S851.33
B
1005-944X(2017)08-0100-05
10.3969/j.issn.1005-944X.2017.08.026
国家质检总局质检公益专项(201410061)
季新成

