白蛋白结合型紫杉醇治疗晚期乳腺癌患者的临床效果观察
毕大鹏
白蛋白结合型紫杉醇治疗晚期乳腺癌患者的临床效果观察
毕大鹏
目的探讨白蛋白结合型紫杉醇治疗晚期乳腺癌患者的近期疗效以及安全性。方法回顾性分析2013年1月至2015年6月期间收治的45例应用白蛋白结合型紫杉醇治疗的晚期乳腺癌患者的临床资料。白蛋白结合型紫杉醇单药化疗剂量260 mg/m2,静脉滴注30 min,每3周给药1次,无需进行抗过敏预处理。同时给予患者5-羟色胺3(5-HT3)受体拮抗剂以预防化疗药物导致的胃肠道不良反应,并进行补液水化处理。每2个周期评估疗效以及不良反应。结果本组45例患者均顺利完成疗程,平均化疗5.2个周期。所有患者均可评价疗效,其中CR 3例(6.67%),PR 16例(35.56%),SD 24例(53.33%),PD 2例(4.44%),总有效率ORR为42.22%。治疗过程中,主要不良反应包括消化道反应、骨髓抑制、感觉神经异常以及肌肉关节酸痛,Ⅲ~Ⅳ度白细胞减少发生率为53.33%,Ⅲ~Ⅳ度粒细胞减少发生率为40.00%,Ⅲ~Ⅳ度血小板减少(2.22%)以及贫血(8.89%)的发生率较低。结论白蛋白结合型紫杉醇治疗晚期乳腺癌患者可以取得较好的临床效果,且不良反应较少,患者耐受性好,可以推广应用。
白蛋白紫杉醇;晚期乳腺癌;临床疗效;安全性
乳腺癌是女性常见的恶性肿瘤,发病率逐年增高,且发病年龄趋于年轻化,居女性恶性肿瘤发病率的首位,成为严重危害妇女健康的主要恶性肿瘤之一[1-2]。目前,临床上主要采用手术、放疗、化疗、内分泌治疗、靶向治疗以及中药治疗等综合方法治疗乳腺癌。近年来,新辅助化疗在临床上广泛应用于乳腺癌的治疗中,可以显著提高保乳率、手术率以及消除全身微转移灶等[3]。紫杉烷类药物自20世纪90年代广泛应用于临床,被认为是治疗乳腺癌最有效的药物。但是,由于该药物的水溶性极差,常常需要应用助溶剂,而助溶剂可以导致多种不良反应发生,不仅影响了药物的作用,也给患者带来了更大的痛苦。白蛋白结合型紫杉醇(Abraxane)是一种全新的紫杉醇剂型,它改变了助溶剂,以纳米微粒白蛋白为载体,不仅可以明显提高治疗效果,也减轻了药物的不良反应[4]。本研究回顾性分析了45例应用白蛋白结合型紫杉醇治疗的乳腺癌患者的临床资料,观察治疗效果以及药物的不良反应,现报道如下。
1 资料与方法
1.1 一般资料回顾性选取2013年1月至2015年6月期间来我院治疗的晚期乳腺癌45例患者的临床资料。纳入标准:所有患者均经过病理学或细胞学以及影像学确诊为复发性转移性乳腺癌,均为复治,均有客观的肿瘤指标以评价疗效,身体状况评分(ECOG)为0~2分,预计生存时间超过3个月,无其他化疗禁忌证。本组患者年龄33~67岁,中位年龄47岁;其中浸润性导管癌37例,小叶癌3例,髓样癌3例,腺癌2例;按照术后组织病理的受体表达情况分为人类表皮生长因子受体2(HER-2)阳性者5例,三阴型(ER、PR、HER-2均为阴性)者17例,内分泌治疗敏感Luminal型(ER和/或PR阳性,HER-2阴性)者23例;一线化疗16例,二线及以上化疗 29例;既往采用紫杉类药物进行治疗的患者31例,其中发生耐药12例。所有患者均符合本院医学伦理委员会相关要求,均签署了知情同意书。
1.2 治疗方法所有患者均应用白蛋白结合型紫杉醇单药化疗,剂量为260 mg/m2,静脉滴注30 min,每3周给药1次,无需进行抗过敏预处理。在进行化疗的同时,给予5-羟色胺3(5-HT3)受体拮抗剂以预防化疗药物导致的胃肠道不良反应,并进行补液水化处理。化疗结束后 48 h,如果患者白细胞降低超过Ⅱ度,常规皮下注射粒细胞集落刺激因子,150 μg/d,连用5 d,以升高白细胞数量。
1.3 观察指标①疗效评价:根据实体瘤疗效评价标准评价,每完成2个化疗周期评价1次临床疗效。分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)以及疾病进展(PD);有效率(ORR)=(CR+PR)/总例数×100%。②不良反应评价:按照世界卫生组织(WHO)急性标准分为0~Ⅳ共5级[5]。
1.4 统计学分析采用SPSS 17.0统计软件对数据进行分析,采用描述性统计分析评价患者的临床病理特征,计数资料以百分比(%)进行表示,组间比较采用χ2检验,P<0.05认为差异有统计学意义。
2 结果
2.1 近期疗效本组所有患者均完成 2~8个周期的化疗,平均周期数为5.2。所有患者均能够评价临床疗效,其中CR 3例(6.67%),PR 16例(35.56%),SD 24例(53.33%),PD 2例(4.44%),ORR为42.22%。
2.2 不良反应治疗过程中,主要不良反应包括消化道反应、骨髓抑制、感觉神经异常以及肌肉关节酸痛;严重不良反应主要为骨髓抑制,Ⅲ~Ⅳ度白细胞减少发生率为53.33%,Ⅲ~Ⅳ度粒细胞减少发生率为40.00%,Ⅲ~Ⅳ度血小板减少(2.22%)以及贫血(8.89%)的发生率较低。骨髓抑制经 G-CSF治疗后均症状缓解,能够继续接受化疗。见表1。
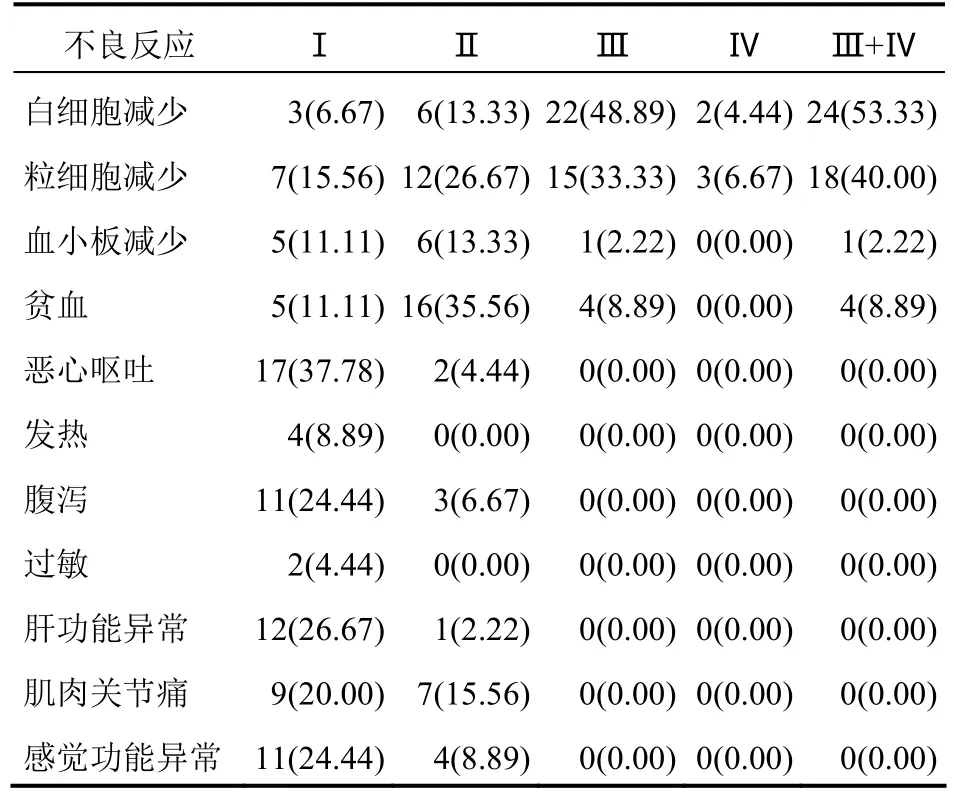
表1 45例晚期乳腺癌患者白蛋白结合型紫杉醇方案的常见不良反应[例(%)]
3 讨论
乳腺癌位居女性肿瘤中新发病例数的第 1位,死亡率位居女性癌症的第 2位,对女性的身体健康及生命安全造成严重影响[6]。晚期乳腺癌的治疗较为困难,一般根据患者的身体情况、转移部位、疾病进展速度、既往治疗疗效以及对不良反应的耐受程度等决定所使用的治疗方案[7]。紫杉烷类抗癌药物属于细胞周期特异性抗微管药物,作用于细胞微管网后,能够结合微管蛋白,致使微管聚合,并使其稳定,使微管网的正常重组受到抑制,细胞周期在 M期和G2期受到阻断;另外,该药物还可以对抗肿瘤血管的形成起到有效的抗肿瘤作用[8-9]。与传统的制剂相比,白蛋白纳米载体制剂可以将紫杉醇迅速清除,并分布至组织,使得对组织的亲和力明显增加。通过与细胞膜上的Gp60结合,白蛋白结合型紫杉醇可以激活细胞膜上窖蛋白1(Caveolin-1),通过血管内皮细胞将紫杉醇转运到组织中,然后转运至肿瘤细胞内,含有药物的纳米微粒可以通过毛细血管壁细胞间隙进入到肿瘤组织中,在肿瘤组织中蓄积后发挥作用[10-11]。
本组45例晚期乳腺癌患者中,治疗总有效率为42.22%。本研究结果提示,对于既往溶剂型紫杉类药物进行治疗且耐药的晚期乳腺癌患者,应用白蛋白结合型紫杉醇进行治疗,仍然可以取得比较满意的疗效。与紫杉醇及多西紫杉醇相比,白蛋白结合型紫杉醇可以显著增加肿瘤细胞内有效药物的浓度,抗肿瘤活性更强。Blum 等[12]报道显示,采用150 mg/m2白蛋白结合型紫杉醇治疗既往应用过紫杉类药物治疗的耐药晚期乳腺癌患者,得到的ORR为 165,中位无进展生存期(PFS)为 3.5个月。Schwartzberg等[13]采用白蛋白结合型紫杉醇联合卡培他滨一线治疗晚期乳腺癌,结果显示ORR为61%,中位PFS为10.6个月。白蛋白结合型紫杉醇的最大耐受剂量(MTD)为300 mg/m2,剂量限制性毒性主要为骨髓抑制、感觉神经病变[14]。本研究结果还显示,在治疗过程中患者的主要不良发应为消化道反应、骨髓抑制、感觉神经异常以及肌肉关节酸痛;Ⅲ~Ⅳ度白细胞和粒细胞减少发生率较高,Ⅲ~Ⅳ度血小板减少及贫血发生率较低。同时,经过相应的对症处理后,本组患者的不良反应均可缓解;Ⅲ~Ⅳ度骨髓抑制发生率较高,考虑可能与本研究中复治患者较多,骨髓造血功能相对较差有关。
综上所述,对于既往紫杉类耐药的、既往接受过多重化疗的晚期乳腺癌患者采用白蛋白结合型紫杉醇为基础的化疗方案,仍然可以取得较好的疗效,且不良反应少,患者耐受性好。但是,由于本研究的病例数较少,观察时间短,因此,应当加大样本量和观察时间以进一步探索该药物的疗效和安全性。
[1] Jemal A,Siegel R,Ward E,et al.Cancer statistics,2008[J].CA Cancer J Clin,2008,58(2):71-96.
[2] 李剑英,季从飞,陈佳,等.卡培他滨维持治疗晚期乳腺癌的临床观察[J].中国癌症杂志,2014,24(5):381-386.
[3] 詹鹏,郭放,葛亚楠,等.白蛋白结合型紫杉醇二线治疗晚期三阴性乳腺癌临床效果[J].临床误诊误治,2015,28(12):55-57.
[4] Ibrahim NK,Samuels B,Page R,et al.Multicenter phase II trial of ABI-007,an albumin-bound paclitaxel, in women with metastatic breast cancer[J].J Clin Oncol,2005,23(25):6019-6026.
[5] 中华医学会.临床诊疗指南-肿瘤分册[M].北京:人民卫生出版社,2005:183-204.
[6] 曾梓涵,赵玫,彭华,等.microRNA-21、microRNAlet-7a在三阴性乳腺癌与 LuminalA型乳腺癌血清中的表达差异.[J].实用医学杂志,2015,31(21):3499-3501.
[7] 梁旭,李惠平,邸立军,等.白蛋白结合型紫杉醇治疗晚期难治性乳腺癌的疗效及安全性分析[J].中国癌症杂志,2014,24(11):836-841.
[8] Sparano JA,Wang M,Martino S,et al.Weekly paclitaxel in the adjuvant treatment of breast cancer[J].N Engl J Med,2008,358(16): 1663-1671.
[9] 龚军,彭春雷,姚卫东,等.白蛋白结合型紫杉醇治疗晚期乳腺癌的临床观察[J].南通大学学报(医学版),2014,34(1):65-66.
[10] 洪熠,陈心华,李娜妮,等.白蛋白结合型紫杉醇治疗转移性乳腺癌的临床疗效与安全性观察[J].中国肿瘤临床,2012,39(6):352-354.
[11] 朱华云,孙小峰,陈嘉,等.曲妥珠单抗联合白蛋白结合型紫杉醇治疗晚期乳腺癌的疗效和安全性[J].徐州医学院学报,2015, 35(11):752-755.
[12] Blum JL,Savin MA,Edelman G,et al.Phase II study of weekly albumin-bound paclitaxel for patients with metastatic breast cancer heavily pretreated with taxanes[J].Clin Breast Cancer,2007,7(11): 850-856.
[13] Schwartzberg LS,Arena FP,Mintzer DM,et al.Phase II multicenter trial of albumin-bound paclitaxel and capecitabine in first-line treatment of patients with metastatic breast cancer[J].Clin Breast Cancer,2012,12(2):87-93.
[14] 刘培延,孙蔚莉,刘德林,等.白蛋白结合型紫杉醇治疗晚期乳腺癌的疗效和安全性[J].中华临床医师杂志(电子版),2013,7(3): 1077-1080.
10.12010/j.issn.1673-5846.2017.02.009
鞍山市肿瘤医院六病区,辽宁鞍山 114036

