遗传性对称性色素异常症ADAR1基因剪切突变一例
汤庄力 王晓鹏 肖生祥
·论著·
遗传性对称性色素异常症ADAR1基因剪切突变一例
汤庄力 王晓鹏 肖生祥
目的: 检测一例遗传性对称性色素异常症散发病例ADAR1基因突变。方法: 提取患者及100名健康对照外周血DNA,采用聚合酶链式反应(PCR)扩增ADAR1基因的全部外显子并测序。结果: 该患者ADAR1基因11号外显子与11号内含子交界处检测到一新的c.3091+1G>T剪切突变,家族成员及100例无关正常人中未发现突变。应用Mutation Taster进行剪切突变蛋白功能预测分析,提示该突变为致病剪切突变,可能导致编码蛋白的催化结构域丢失。结论: 本例患者检测到一个ADAR1基因新的突变位点,丰富了突变谱。
遗传性对称性色素异常症; 剪切突变; ADAR1基因
遗传性对称性色素异常症(dyschromatosis symmetrica hereditaria, DSH, MIM127400)是一种发病率较低的,具有高外显率的常染色体显性遗传疾病。其临床表现为发生在手足伸侧的对称性色素减退及色素沉着斑。部分患者颜面部位亦可受累,表现为雀斑样改变。组织病理示:色斑处表皮棘层下部和基层内黑素增加,其下真皮上部嗜黑素细胞增多及少量淋巴细胞浸润,而白斑处基层色素减少乃至消失[1]。2003年,Zhang等[2]将本病定位在1号染色体1q11~1q21区域内,同年日本学者Miyamura等[3]将致病基因确定为该区域内双链RNA特异性腺苷脱氨酶(adenosine deaminase, RNA specific, ADAR1)基因。本研究运用PCR技术检测1例散发患者ADAR1基因突变位点。
1 材料和方法
1.1 临床资料 患者,男,27岁。父母非近亲婚配。自3岁时手足背部出现散在针尖大小色素减退斑伴色素沉着斑,其间皮肤颜色正常(图1)。皮损随患者年龄增大逐渐增多增大,光照后皮损加剧,冬季有所减轻,患者既往未予重视,否认其他系统疾病史。家族中无类似病史。
1.2 标本收集 向患者及其直系近亲充分阐明本研究目的及意义,获取其知情同意后经肘正中静脉采集外周静脉血2 mL,EDTA抗凝,-80℃深低温保存。募集100名健康志愿者(募集入选条件:男女不限,24~28岁,无系统疾病),获取知情同意后采集外周静脉血2 mL作为对照,血样编号后相同条件下保存。
1.3 DNA提取 冻存外周血样完全融化后用全血基因组DNA提取试剂盒(天根生化科技)提取基因组DNA备用。
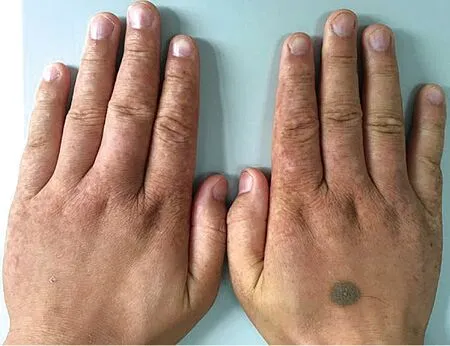
图1 患者手部皮损
1.4 聚合酶链式反应扩增ADAR1基因全部外显子 采用Primer3.0软件设计ADAR1基因15个外显子共17对引物。扩增11号外显子的上游引物为5’- TCCCATGGTAGGCCTTAGAA -3’;下游引物为5’- CTGTGCCCAGTGACTAATGG -3’。扩增目的片段长度约为358 bp。PCR体系为20 μL,上下游引物各1 μL 、DNA模板3 μL、DEPC水5 μL、PCR mix 10 μL,反应条件为预变性95℃,5 min;35个扩增循环,每个循环由变性(94℃,30 s)、复性(56℃,30 s)、延伸(72℃,1 min);72℃延伸5 min。PCR产物经2%琼脂糖凝胶电泳,溴化乙锭/紫外线以了解产物情况。
1.5 DNA序列分析 PCR产物纯化后经ABI3730XL型全自动荧光DNA测序仪(Applied Biosystems, CA, USA)测序。将测序所得序列与Gen Bank中人类ADAR1基因序列进行比对,分析SNP及突变情况。
2 结果
2.1 基因测序结果 该患者基因组DNA经PCR、DNA测序后在第11外显子与第11内含子交界处检测到一新的c.3091+1G>T剪切突变(图2),导致第11号内含子剪切受体发生改变。正常的100人对照及患者直系近亲均未见此剪切突变。其余外显子及内含子均未见突变。
2.2 剪切突变功能预测分析 应用Mutation Taster软件进行剪切突变蛋白功能预测分析[4],以该突变点两侧各6 bp范围的DNA序列为目标序列进行检索,结果提示该突变为致病剪切位点突变,可能影响正常剪切并使得蛋白质功能受到影响。检索序列共有两个限制性内切酶识别位点,分别为c.3091+3位点的GAGT以及c.3091+1位点的GTGA,两者的突变型较野生型对蛋白质功能的影响均显著增加。
对蛋白特征改变进行预测提示,除了下游蛋白质序列可能发生改变外,所编码蛋白的催化结构域可能丢失。通过与ExAC及1000G数据库进行比对,未发现已报道的相关突变。

c.3091+1G>T mutation in Intron11 of ADAR1 gene in the patient
3 讨论
遗传性对称性色素异常症发病率至今少见报道,该病曾被普遍认为是罕见病且仅发生于东亚尤其是日本和中国[5],但近年欧美国家关于该病的报道亦可见诸笔端[6]。一般认为由于色减斑或色沉斑与白种人或黑种人肤色相近,易被患者忽视或错诊、漏诊及误诊。同时该病无碍患者生存,且非增龄性疾病,轻症仅对患者生活质量造成影响,部分患者因此不愿就诊。
该病目前仍无特效疗法,可通过避免日光直接暴晒减慢疾病进展。患者于40岁左右后有自行缓解的趋势,但无法痊愈[1]。
ADAR1基因编码的双链RNA特异性腺苷脱氨酶全长1226个氨基酸,分为6个结构域,分别为2个Z-DNA结合结构域(Zα, Zβ),3个dsRNA结合结构域(DRBM1,DRBM2,DRBM3),1个催化结构域[7]。该酶广泛分布于全身各组织器官,通过将mRNA前体靶位点的腺嘌呤催化为次黄嘌呤完成RNA编辑[8]。当该基因发生剪切突变时,突变位点不能被限制性核酸内切酶正确识别并催化,可能造成片段插入或出现提前终止密码子(premature termination codons),造成基因转录翻译异常进而导致疾病发生[9]。在已报道的可能致病突变中,剪切突变所占比例最小,累计报道12例(T1601+2G,A1935-2G,G2080-1A,T2270+2G,A2271-3G,T2668+2A,G2763-1T,A2886-2C,c.3020-2A>T,G3202+5A,A3203-2G,G 3315+1 A)[10-19],约占现有所有突变报道的7%,且其中仅3例报道通过进一步实验明确了理论的蛋白质改变。
从基因结构上分析,ADAR1基因11号外显子位于催化结构域中,其c.3089位点至c.3090位点是限制性内切酶Psp1406 I的酶切位点(AACGTT),而在其下游c.3091+14至c.3091+15位点是潜在的限制性核酸内切酶Nsp I的酶切位点(ACATGC),当c.3091+1位点发生突变而不能被酶特异性识别时,下游的潜在酶切位点就可能被识别并被剪切,进而造成下游mRNA及蛋白质产物结构和功能的改变。同时由于该位点无法被内切酶识别,继续转录可能会出现提前终止密码子,导致该基因编码的蛋白不完整甚至通过泛素化等细胞自我保护途径降解。本例患者拒绝进一步提供血样以供realtime-PCR明确该突变的具体剪切方式,因而无从得知最终的蛋白改变。蛋白质作为生物功能的执行者,该层面的改变有助于更好地理解该病的生物学行为。
遗传性对称性色素异常症至今机制仍不明,通过基因测序手段获得的大量突变数据有助于为后续的蛋白组学研究、基因型与表型关联、发病机制及治疗等进一步研究提供帮助。
[1] 赵辨.中国临床皮肤病学[M].南京:江苏科学技术出版社,2009.1250.
[2] Zhang XJ, Gao M, Li M, et al. Identification of a locus for dyschromatosissymmetricahereditaria at chromosome 1q11-1q21[J]. J Invest Dermatol,2003,120:776-780.
[3] Miyamura Y, Suzuki T, Kono M, et al. Mutations of the RNA-specific adenosine deaminase gene (DSRAD) are involved in dyschromatosissymmetricahereditaria[J]. Am J Hum Genet,2003,73:693-699.
[4] Schwarz JM, Rödelsperger C, Schuelke M, et al. Mutation Taster evaluates disease-causing potential of sequence alterations[J]. Nat Methods,2010,7(8):575-576.
[5] Hayashi M, Suzuki T. Dyschromatosis symmetrica hereditaria[J]. J Dermatol,2013,40:336-343.
[6] Bilen N, Akturk AS, Kawaguchi M, et al. Dyschromatosis symmetrica hereditaria: a case report from Turkey, a new association and a novel gene mutation[J]. J Dermatol,2012,39:857-858.
[7] Herbert A, Rich A. The role of binding domains for dsRNA and Z-DNA in the in vivo editing of minimal substrates by ADAR1[J]. P Natl Acad Sci USA,2001,98:12132-12137.
[8] Wang Y, Zeng Y, Murray JM, et al. Genomic organization and chromosomal location of the human dsRNA adenosine deaminase gene: the enzyme for glutamate-activated ion channel RNA editing[J]. J Mol Biol,1995,254:184-195.
[9] Liu Y, George CX, Patterson JB, et al. Functionally distinct double-stranded RNA-binding domains associated with alternative splice site variants of the interferon-inducible double-stranded RNA-specific adenosine deaminase[J]. J Biol Chem,1997,272:4419-4428.
[10] Suzuki N, Suzuki T, Inagaki K, et al. Mutation analysis of the ADAR1 gene in dyschromatosis symmetrica hereditaria and genetic differentiation from both dyschromatosis universalis hereditaria and acropigmentatioreticularis[J]. J Invest Dermatol,2005,124:1186-1192.
[11] Murata I, Hozumi Y, Kawaguchi M, et al. Four novel mutations of the ADAR1 gene in dyschromatosis symmetrica hereditaria[J]. J Dermatol Sci,2009,53:76-77.
[12] Li CR, Xu XL, Sun XJ, et al. Two new mutations of the ADAR1 gene associated with dyschromatosis symmetrica hereditaria[J]. Arch Dermatol Res,2010,302:477-480.
[13] Peng CJ, Wikramanayake AH. Differential regulation of disheveled in a novel vegetal cortical domain in sea urchin eggs and embryos: implications for the localized activation of canonical wnt signaling[J]. PloS One,2013,8:e80693.
[14] 王晓鹏,刘艳,肖生祥,等.两个遗传性对称性色素异常症家系的DSRAD基因剪切突变[J].中国皮肤性病学杂志,2010,24(6):502-504,508.
[15] Kono M, Akiyama M, Kondo T, et al. Four novel ADAR1 gene mutations in patients with dyschromatosis symmetrica hereditaria[J]. J Dermatol,2012,39:819-821.
[16] Kantaputra PN, Chinadet W, Ohazama A, et al. Dyschromatosis symmetrica hereditaria with long hair on the forearms, hypo/hyperpigmented hair, and dental anomalies: report of a novel ADAR1 mutation[J]. Am J Med Genet A,2012,158:2258-2265.
[17] Xu XG, Lv Y, Zhai JL, et al. Two novel mutations of the ADAR1 gene in Chinese patients with dyschromatosis symmetrica hereditaria successfully treated with fractional CO2laser[J]. J Eur Acad Dermatol,2016,30:1035-1038.
[18] Zhang XJ, He PP, Li M, et al. Seven novel mutations of the ADAR gene in Chinese families and sporadic patients with dyschromatosis symmetrica hereditaria (DSH)[J]. Hum Mutat,2004,23:629-630.
[19] Okamura K, Abe Y, Fukai K, et al. Mutation analyses of patients with dyschromatosis symmetrica hereditaria: Ten novel mutations of the ADAR1 gene[J]. J Dermatol Sci,2015,79:88-90.
(收稿:2016-10-12 修回:2016-10-26)
Splice-site mutation in ADAR1 gene in a patient with dyschromatosis symmetrica hereditaria
TANGZhuangli,WANGXiaopeng,XIAOShengxiang.
TheSecondAffiliatedHospitalofXi'anJiaotongUniversity,DepartmentofDermatology,Xi'an710004,ChinaCorrespondingauthor:WANGXiaopeng,E-mail:wangdctor@163.com
Objective: To detect the mutations in ARAD1 gene in one sporadic patient with dyschromatosis symmetrica hereditaria. Methods: Genomic DNA was extracted from peripheral blood of patient and 100 healthy controls. All exons of ADAR1 gene were amplified by polymorphism chain reaction (PCR) and the products were purified and directly sequenced to detect mutations. Results: A novel splice-site mutation c.3091+1G>T was identified in the junction of exon 11 and intron 11, which was not detected in controls. Potential protein function changes of the altered DNA sequence was detected by Mutation Taster and the result showed the splice-site mutation was a pathogenic mutation which might lead to the loss of catalytic structural domain. Conclusion: One novel splice-site mutation was identified, which further expand the database of ARAD1 mutations.
dyschromatosis symmetrica hereditaria; splice site mutation; ADAR1 gene
国家自然科学基金(编号:30800991)
西安交通大学第二附属医院,陕西西安,710004
王晓鹏,E-mail: wangdctor@163.com

