姜黄素自微乳化药物递送系统制备及质量评价*
李泽民, 李晓庆, 许小红 , 杨绍杰.成都医学院 药学院·四川省高校结构特异性小分子药物研究重点实验室(成都 60500);2成都市慢性病医院(成都 60083)
·论 著·
姜黄素自微乳化药物递送系统制备及质量评价*
李泽民1, 李晓庆1, 许小红1, 杨绍杰2Δ
1.成都医学院 药学院·四川省高校结构特异性小分子药物研究重点实验室(成都 610500);2成都市慢性病医院(成都 610083)
目的 制备姜黄素自微乳化药物递送系统,并进行初步质量评价。方法 根据姜黄素的溶解性选择辅助乳化剂及油相种类;采用伪三元相图优选乳化剂种类;以纳米乳的粒径为指标,通过单因素实验优化辅料的比例。结果 中链脂肪酸(MCT)为油相,聚乙二醇-400(PEG-400)为助乳化剂,聚氧乙烯菎麻油RH40(Cremophor RH40)为乳化剂,比例为MCT∶PEG-400∶Cremophor RH40=2∶2∶6(w/w),所得自微乳化制剂的乳化能力最大,粒径最小,且稳定性良好。结论 制备的姜黄素自微乳化药物递送系统质量、稳定性符合要求,为姜黄素用于视网膜β-淀粉样蛋白(Aβ)沉积研究提供了制剂学基础。
姜黄素;自微乳化药物递送系统; Aβ沉积
阿尔茨海默病(AD)主要病理改变包括β-淀粉样蛋白(Aβ)沉积、老年斑、神经纤维缠结[1]。现有研究表明, Aβ沉积不仅存在于AD患者脑组织,也出现在视网膜中。有研究使用姜黄素视网膜荧光照相显示小鼠的Aβ沉积,提示视网膜Aβ沉积可以反映脑组织的Aβ沉积,且视网膜沉积早于脑组织出现。AD临床症状发生前15年即可发现视网膜Aβ沉积,且视网膜荧光照相能够更直接和廉价地检测Aβ沉积,对早期发现和筛查AD具有重要意义[2]。
然而,直接口服姜黄素吸收差、生物利用度低,且达不到荧光显示所需要的药物剂量[3-5]。自微乳化药物递送系统(self-micro emulsifying drug delivery systems, SMEDDS )不仅能改善疏水性药物的溶解性,还能自发形成粒径小于100 nm的纳米乳,增加药物的透膜性,从而提高药物吸收程度[6-9]。因此,本研究拟制备姜黄素自微乳化药物递送系统(cur-SMEDDS)制剂,并对其质量进行研究,以期提高姜黄素吸收程度,为后期实现视网膜Aβ沉积的标注提供易吸收的口服制剂。
1 材料与方法
1.1 材料与仪器
姜黄素对照品,中国药品生物制品检定所,批号:110752-201005,纯度>98%;姜黄素原料药,南京泽朗医药科技有限公司,批号:ZL120911,纯度96%;中链脂肪酸(MCT),山东西亚化学工业有限公司,纯度:98%;肉豆蔻酸异丙酯(IPM),山东西亚化学工业有限公司,纯度:98%; Cremophor EL和Cremophor RH40德国 BASF 公司;甲醇、乙腈Sigma色谱级;乙醇、1, 2-丙二醇、吐温 80,聚乙二醇(PEG-400),成都市科龙化工试剂厂,分析纯;水为超纯水。Ultimate 3000型高效液相色谱,美国戴安;BP 211D电子天平,德国赛多利斯,Zetasizer Nano ZS-90型激光粒度仪,英国马尔文,DF-101S磁力搅拌器,巩义市予华仪器公司。
1.2 实验方法
1.2.1 色谱条件与含量测定方法 色谱柱Agilent HC-C18柱 (4.6×250 mm,粒径5 μM),流动相为水(0.1%的甲酸)∶乙腈=50∶50,流速1 mL/min,检测波长428 nm,柱温35 ℃。供试品溶液配制:精密称取cur-SMEDDS 适量置容量瓶中,加入适量甲醇,超声10 min,然后加流动相稀释定容即得。对照品溶液:取姜黄素对照品适量,置容量瓶中,加流动相配制浓度为10 μg/mL溶液即得。测定法:另取供试品溶液与对照品溶液50 μL,注入液相色谱仪测定,外标法计算供试品溶液浓度。
1.2.2 姜黄素在各种辅料中的溶解度测定 称取各辅料约1 g,分别加入500 mg 姜黄素,涡旋5 min后,37 ℃避光震摇48 h。取样品12 000 rpm离心10 min,精密取上清液适量,用流动相稀释后测定姜黄素含量,计算其在不同介质中的溶解度。
1.2.3 乳化剂选择 将选择的油相、乳化剂和辅助乳化剂配制成一系列不同比例(w/w)的自微乳化浓缩液(0.05∶0.05∶0.9、0.05∶0.1∶0.85、0.05∶0.15∶0.8、……、0.9∶0.05∶0.05)。涡旋不同比例的自微乳化浓缩液,使油相、乳化剂、辅助乳化剂混合均匀备用。称取浓缩液1 g,加入100 mL水,37 ℃水浴,50 r/min搅拌30 min,观察溶液是否澄清透明或呈乳白色。根据观察结果绘制伪三元相图[10]。
1.2.4 油相比例筛选 固定乳化剂和辅助乳化剂比例为9∶1(w/w),分别加入不同比例的油相,混合均匀,分别取浓缩液1 g (n=3),加入100 mL 37 ℃水,50 r/min搅拌30 min,使自微乳化浓缩液形成稳定的乳液。取乳液适量,在25 ℃条件下,用激光粒度仪测试乳液的粒径。
1.2.5 乳化剂和辅助乳化剂的比例筛选 固定油相比例为20%,改变乳化剂和辅助乳化剂的比例(w/w)为7∶1、6∶2、5∶3、4∶4、3∶5、2∶6、1∶7,按照上述比例配置成为不同的自微乳化浓缩液。称取混合均匀的自微乳化浓缩液1 g,加入100 mL水,37 ℃水浴,50 r/min搅拌30 min,检测乳液粒径。
1.2.6 稀释介质的pH筛选 按照油相∶乳化剂∶辅助乳化剂为2∶2∶6制备自微乳化浓缩液。称取1 g该浓缩液,分别加入100 mL 水、pH=1.2的盐酸溶液、pH=6.8的磷酸盐缓冲液,37 ℃水浴,50 r/min搅拌30min,检测乳液粒径。
1.2.7 不同载药量对粒径分布的影响 取辅料的质量比为Cremophor RH40∶PEG-400∶MCT=6∶2∶2自微乳化浓缩液1 g(n=3),加入500 mg 姜黄素原料药,涡旋5 min后,37 ℃避光震摇48 h。取出样品12 000 r/min,离心10 min,精密取上清液适量,用甲醇稀释后按照“1.2.1色谱条件”项下要求进行检测,计算药物自微乳化浓缩液中的溶解度,结果为(55.30±2.49) mg/g。1 g自微乳化浓缩液最大能够溶解大约55 mg姜黄素。分别取自微乳化浓缩液1 g,分别加入姜黄素 10、20、30、40、50 mg,涡旋直到姜黄素完全溶解后加入100 mL水,在37 ℃的水浴中,50 r/min搅拌30 min,测试样品的粒径。
1.2.8 cur-SMEDDS制剂的制备 采用溶解法制备cur-SMEDDS制剂。辅料的质量比为Cremophor RH40∶PEG-400∶MCT=6∶2∶2。按照该比例称取各种辅料,涡旋直至混合均匀。按照每1 g辅料加入姜黄素原料药30 mg计,加入所需要的姜黄素原料药,涡旋直至姜黄素完全溶解,得到的浓缩液即为载药量为30 mg/g的cur-SMEDDS。
1.2.9 释放度实验 取cur-SMEDDS 1 g(相当于含有姜黄素30 mg),置溶出杯中。以含有0.1%十二烷基硫酸钠的水溶液900 mL为溶出介质,温度为(37.0±0.5 )℃,浆法50 r/min,分别于5、10、20、30、60、90、120 min取样5 mL,并补足损失的溶出介质,用0.45 μM滤膜过滤,取续滤液备用。另取30 mg姜黄素原料药同法操作。样品照“1.2.1色谱条件”项下规定检测含量,计算累积释放度。
1.2.10 稳定性研究 取已制备的cur-SMEDDS进行稳定性实验。分别取适量样品放在50 mL的离心管中密封,分别放在4 ℃、25 ℃环境中避光保存,分别于7 、14 d取样,照“1.2.1”项下规定测定样品含量,加入100 mL水,37 ℃水浴,50 r/min搅拌30 min,测试样品的粒径。
2 结果
2.1 姜黄素在不同辅料中的溶解度测试结果
根据溶解度结果大小,选择Cremophor EL和Cremophor RH40为主乳化剂进行优选,选择PEG-400为辅助乳化剂,选择MCT为乳剂油相(表1)。

表1 姜黄素在不同介质中的溶解度
2.2 绘制伪三元相图
Cremophor RH40作为乳化剂时,浓缩液的自微乳化区域明显大于Cremophor EL,Cremophor RH40的乳化效率更高,因此选择Cremophor RH40为乳化剂(图1)。
2.3 不同比例的油相微乳的粒径测试结果
体系中随着油相比例的增加,微乳的粒径随之增大,当油相比例超过20%时,出现双峰或三峰,说明该系统不够稳定。为得到粒径<100 nm的微乳,确定油相比例不超过20%为宜(表2)。
2.4 不同比例的乳化剂和辅助乳化剂的粒径测试结果
随着乳化剂与辅助乳化剂的比值减小,微乳的粒径呈逐步增大趋势,且当乳化剂和辅助乳化剂的比值<6∶2时,体系中出现双峰或三峰。通常SMEDDS乳化剂比例在30%~60%,尽管非离子型乳化剂毒性很小,若使用量过高,会对胃肠道有刺激作用。因此从表格中结果分析,确定乳化剂与辅助乳化剂的比例为6∶2(表3)。

图1 不同乳化剂的伪三元相图注:“■”:有效自微乳化区域
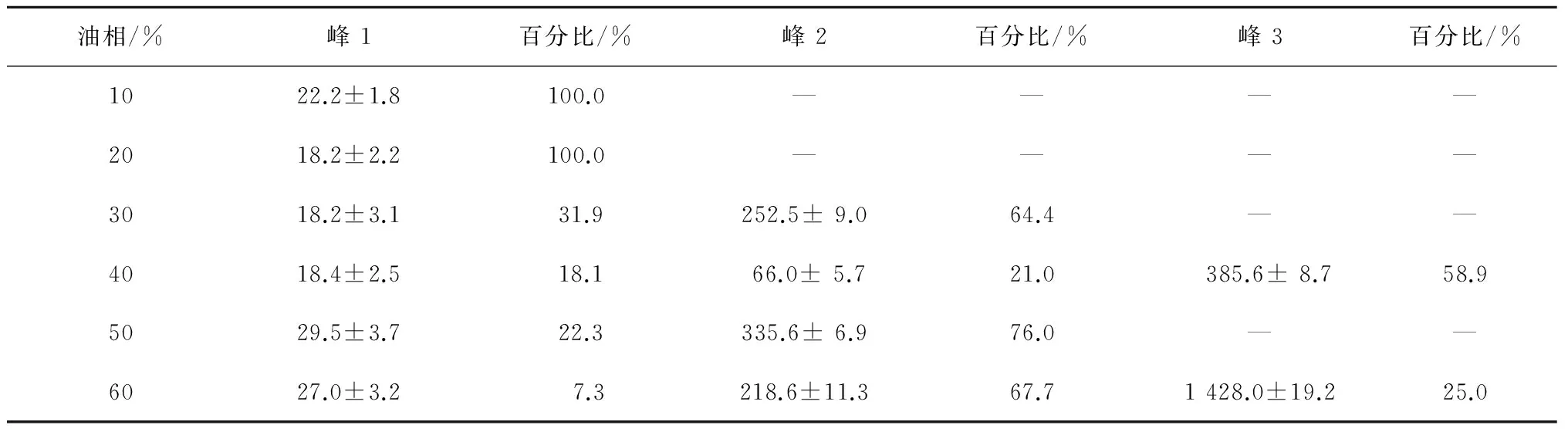
表2 不同油相比例对微乳粒径的影响

表3 乳化剂/辅助乳化剂的比例对于微乳粒径分布的影响
2.5 不同pH介质稀释微乳粒径的测试结果
结果表明,用不同介质稀释自微乳化浓缩液,所得到乳液粒径差别不大,均呈单峰,且粒径<20 nm,说明pH对于乳液粒径影响很小,同时表明自微乳化浓缩液可以在胃液和肠液中形成纳米微乳(表4)。

表4 稀释液pH值对微乳粒径的影响
2.6 不同载药量的微乳粒径分布
结果显示,当载药量超过30 mg/g时,乳液中液滴的粒径出现双峰情况。同时,载药量过大时,SMEDDS不能形成稳定的界面膜,乳液中的液滴就会融合从而使粒径变大,甚至使部分药物析出。为了提高制剂的载药效率,确定每g自微乳化浓缩液载药30 mg为宜(表5)。

表5 不同载药量对粒径分布的影响
2.7 释放度实验结果
cur-SMEDDS在10 min时即释放了90%以上药物;而姜黄素原料药在120 min时,其释放度仍然没有超过40%(图2)。

图2 cur-SMEDDS及原料药累积释放度结果
2.8 稳定性研究结果
结果表明,cur-SMEDDS在2周内,4 ℃和25 ℃储存,姜黄素含量没有明显的变化,同时稀释成为乳剂后,样品的粒径均<20 nm,与0 d无明显差异,说明2周内样品稳定(表6~7)。

表6 cur-SMEDDS 2周内稳定性试验结果

表7 cur-SMEDDS 2周内粒径变化情况
3 讨论
乳化剂与助乳化剂的用量比是影响体系稳定性的主要因素。HLB值较大的非离子型表面活性剂,在遇水的情况下能够迅速自乳化形成微乳,而辅助乳化剂主要作用在于提高界面膜的柔顺性、流动性和牢固性。乳化剂与辅助乳化剂的用量比越大,乳化作用越强,但兼顾体系稳定性及胃肠道刺激性,应适宜减少乳化剂的用量,降低潜在的毒性。
本研究通过初步的体外质量研究评价,发现姜黄素SMEDDS在含有SDS的溶出介质中,10 min即释放出90%以上的药物,姜黄素粉末在同样的介质中120 min释放度还不到40%。稳定性实验也证明样品在常温和低温条件下存储2周质量稳定。本品的制备为下一步将姜黄素用于视网膜Aβ沉积研究提供了制剂基础。
[1]应侠, 吴振, 雷严, 等. 阿尔茨海默病的发病机制及治疗药物研究进展[J]. 中国药房, 2014,25(33):3152-3155.
[2]李剑明, 杨和平, 白中红, 等. 姜黄素水溶性制剂对小鼠黑素瘤自发性转移的抑制作用[J]. 中国肿瘤生物治疗杂志, 2008, 15(3): 286-288.
[3]Jack C R Jr, Albert M S, Knopman D S,etal. Introduction to the recommendations from the National Institute on Aging-Alzheimer's Association workgroups on diagnostic guidelines for Alzheimer's disease [J]. Alzheimers Dement, 2011, 7(3): 257-262.
[4]Loftsson T, Brewster M E. Pharmaceutical applications of cyclodextrins. 1. Drug solubilization and stabilization[J]. J Pharm Sci, 1996, 85(10): 1017-1025.
[5]Lin H S, Chean C S, Ng Y Y,etal. 2-hydroxypropyl-beta-cyclodextrin increases aqueous solubility and photostability of all-trans-retinoic acid[J]. J Clin Pharm Ther, 2000, 25(4): 265-269.
[6]柯秀梅, 杨荣平, 郭响香, 等. 自乳化释药系统(SEDDS)对姜黄素类组分增溶作用的研究[J]. 中草药, 2014, 45(7): 935-941.
[7]彭璇, 陈苹苹, 包强, 等. 水飞蓟宾过饱和自乳化给药系统的制备及性质研究[J]. 中草药, 2010, 41(1): 40-44.
[8]Mamadou G, Charrueau C, Dairou J,etal. Increased intestinal permeation and modulation of presystemic metabolism of resveratrol formulated into self-emulsifying drug delivery systems[J]. Int J Pharm, 2017, 521(1-2): 150-155.
[9]O’Driscoll C M. Lipid-based formulations for intestinal lymphatic delivery[J]. Eur J Pharm Sci, 2002, 15(5): 405-415.
[10] 吴雪梅, 刘茂柏, 方令平, 等. 姜黄素与胡椒碱复方自乳化给药系统的处方优化[J]. 中国医院药学杂志, 2013, 33(12): 933-938.
Preparation and Quality Evaluation of Curcumin Self-microemulsifying Drug Delivery System*
LiZemin1,LiXiaoqing1,XuXiaohong1,YangShaojie2Δ.
1.SchoolofPharmacy,ChengduMedicalCollege&KeyLaboratoryofSmallMoleculeSpecialStructureDrugs,SichuanInstitutionofHigherEducation,Chengdu610500,China;2.ChengduChronicDiseasesHospital,Chengdu610083,China
Objective To develop a self-microemulsifying drug delivery system (SMEDDS) and conduct the preliminary quality evaluation. Methods The types of co-emulsifiers and oils were selected on the basis of the solubility of curcumin. The pseudo-ternary phase diagram was used to select the types of emulsifiers. The single influencing factor experiment was used to determine the optimal excipient ratio by taking the particle size of nano-emulsion as the index. Results By taking MCT as oil, PEG-400 as co-emulsifier, and Cremophor Rh40 as emulsifier respectively, the capacity of self-emulsifying was the optimal with the smallest particle size and greatest stability when the ratio of MCT, PEG-400 and Cremophor RH40 was 2∶2∶6. Conclusion The quality and stability of curcumin SMEDDS conform to the requirements of oral preparation, which provides a pharmaceutical basis for the use of curcumin in the research of Aβ deposition in retina.
Curcumin; Self-microemulsifying drug delivery system; Aβ deposition
*通信作者:四川省卫计委普及应用项目(No:16PJ093)
http://kns.cnki.net/kcms/detail/51.1705.R.20170321.1022.028.html
10.3969/j.issn.1674-2257.2017.02.008
R749.6
A
△通信作者:杨绍杰,E-mail:yldbwdx2005@hotmail.com

