新型苯并二氢呋喃合二酮酸类化合物的合成及其与整合酶分子对接研究
范 晔, 罗 杨, 马 成
(新疆医科大学 药学院,新疆 乌鲁木齐 830011)
·研究论文·
新型苯并二氢呋喃合二酮酸类化合物的合成及其与整合酶分子对接研究
范 晔, 罗 杨, 马 成*
(新疆医科大学 药学院,新疆 乌鲁木齐 830011)
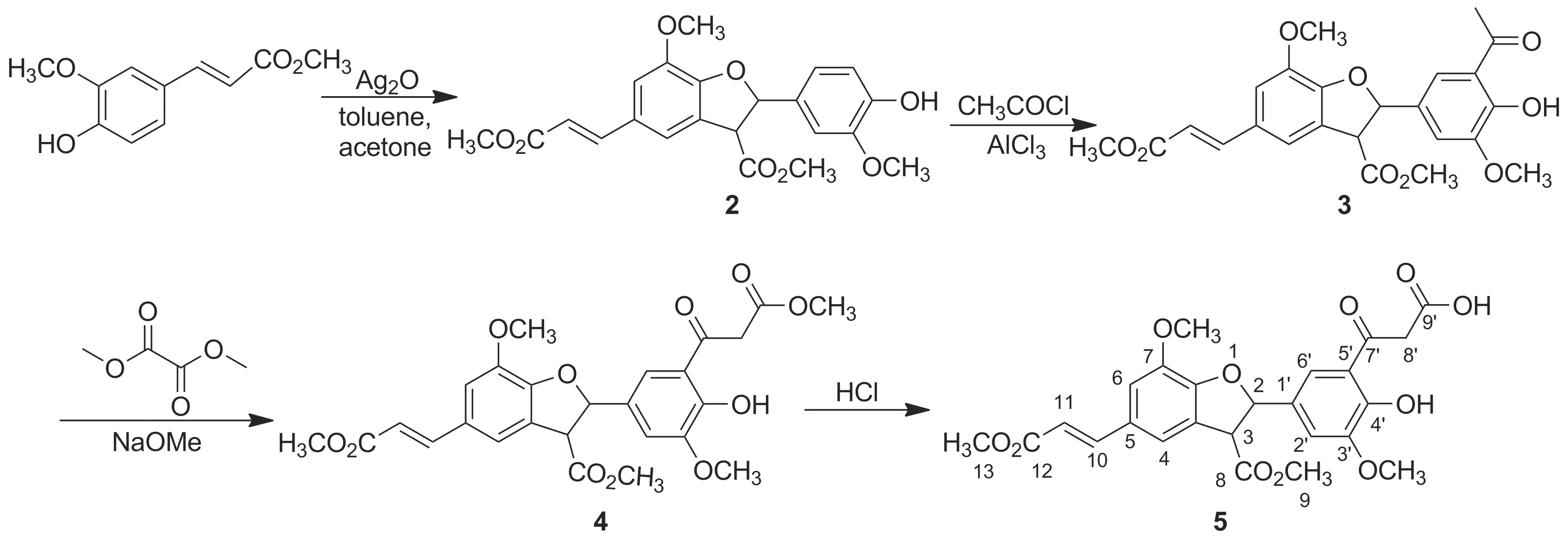
以阿魏酸甲酯为原料,通过氧化偶联构建2-芳基苯并二氢呋喃骨架,再经傅克酰基化和酯缩合反应依次制得(E)-3-[2-(4-羟基-3-甲氧基-5-乙酰基)苯基-3-甲氧羰基-7-甲氧基-2,3-二氢苯[b]并呋喃-5-基]丙烯酸甲酯(3)和(E)-3-[2-(4-羟基-3-甲氧基-5甲氧羰基乙酰基)苯基-3-甲氧羰基-7-甲氧基-2,3二氢苯并[b]呋喃-5-基]丙烯酸甲酯(4); 4经水解反应合成3-【2-羟基-3-甲氧基-5-{5-[2-(甲氧基羰基)乙烯基]-7-甲氧基-3-甲氧羰基-2,3-二氢苯并[b]呋喃-2-}基】苯基-3-氧丙酸(5),化合物3~5未见文献报道,其结构经1H NMR,13C NMR和MS(ESI)表征。采用分子对接软件Autodock vina对化合物2~5与HIV-1整合酶核心部位高度同源的PFV IN(PDB: 3L2V)进行对接,计算结果显示该类化合物能与整合酶形成稳定的复合物,具有1,3-二酮基团的化合物3, 4和5能与整合酶中金属离子产生螯合作用,其中化合物5的结合作用最强。
阿魏酸甲酯; 2-芳基苯并二氢呋喃; 1,3-二酮; 合成; HIV-1整合酶; 分子对接
2-芳基苯并二氢呋喃类化合物是一类在自然界中广泛存在的天然有机化合物,在丹参和百部等药用植物中均有发现,具有抗肿瘤、抗真菌和抗氧化等多种生物活性[1-3]。买尔丹·马合木提[4]等从新疆紫草中发现一种2-芳基苯并二氢呋喃类木脂素(1, Chart 1),对HIV-1感染MT-2细胞的过程具有抑制作用[5],进一步研究显示该化合物对HIV-1整合酶的形成具有抑制作用[6],为2-芳基苯并二氢呋喃的药用研究提供了新的方向。目前已上市的三个HIV-1整合酶抑制剂雷特格韦(Raltegravir, 2007年[7])、埃替格韦(Elvitegravir, 2012年)和多特格韦(Dolutegravir, 2013年)结构中都含有1,3-二酮结构[8-9],该结构可以与整合酶活性位点中的二价镁离子发生螯合作用,能选择性抑制HIV-1整合酶的链转移过程[10]。
本文以阿魏酸甲酯为原料经氧化偶联构建2-芳基苯并二氢呋喃骨架(类似于新疆紫草中木脂素结构)制得(E)-3-[2-(4-羟基-3-甲氧基)苯基-3-甲氧羰基-7-甲氧基-2,3-二氢苯并[b]呋喃-5-基]丙烯酸甲酯(2); 2经傅克酰基化反应制得(E)-3-[2-(4-羟基-3-甲氧基-5-乙酰基)苯基-3-甲氧羰基-7-甲氧基-2,3-二氢苯[b]并呋喃-5-基]丙烯酸甲酯(3); 3经酯缩合反应在2-位苯环中引入1,3-二酮结构制得(E)-3-[2-(4-羟基-3-甲氧基-5甲氧羰基乙酰基)苯基-3-甲氧羰基-7-甲氧基-2,3二氢苯并[b]呋喃-5-基]丙烯酸甲酯(4); 4经水解反应合成3-【2-羟基-3-甲氧基-5-{5-[2-(甲氧基羰基)乙烯基]-7-甲氧基-3-甲氧羰基-2,3-二氢苯并[b]呋喃-2-}基】苯基-3-氧丙酸(5, Scheme 1),化合物3~5未见文献报道,其结构经1H NMR,13C NMR和MS(ESI)表征。采用分子对接软件Autodock vina对2~5与HIV-1整合酶核心区域高度同源的泡沫病毒整合酶(PFV IN, PDB: 3L2V)进行分子对接,分析二者之间的相互作用,为化合物对HIV-1整合酶是否具有抑制作用提供参考,为生物活性筛选奠定基础。
1 实验部分
1.1 仪器与试剂
X-4型显微熔点仪(温度未校正);Varian INOVA-400型核磁共振仪(CDCl3为溶剂,TMS为内标);UPLC-TQD型质谱仪。
阿魏酸甲酯,广州全奥化工产品有限公司;氧化银,天津市光复精细化工研究所;草酸二甲酯,阿拉丁试剂;其余所用试剂均为分析纯。
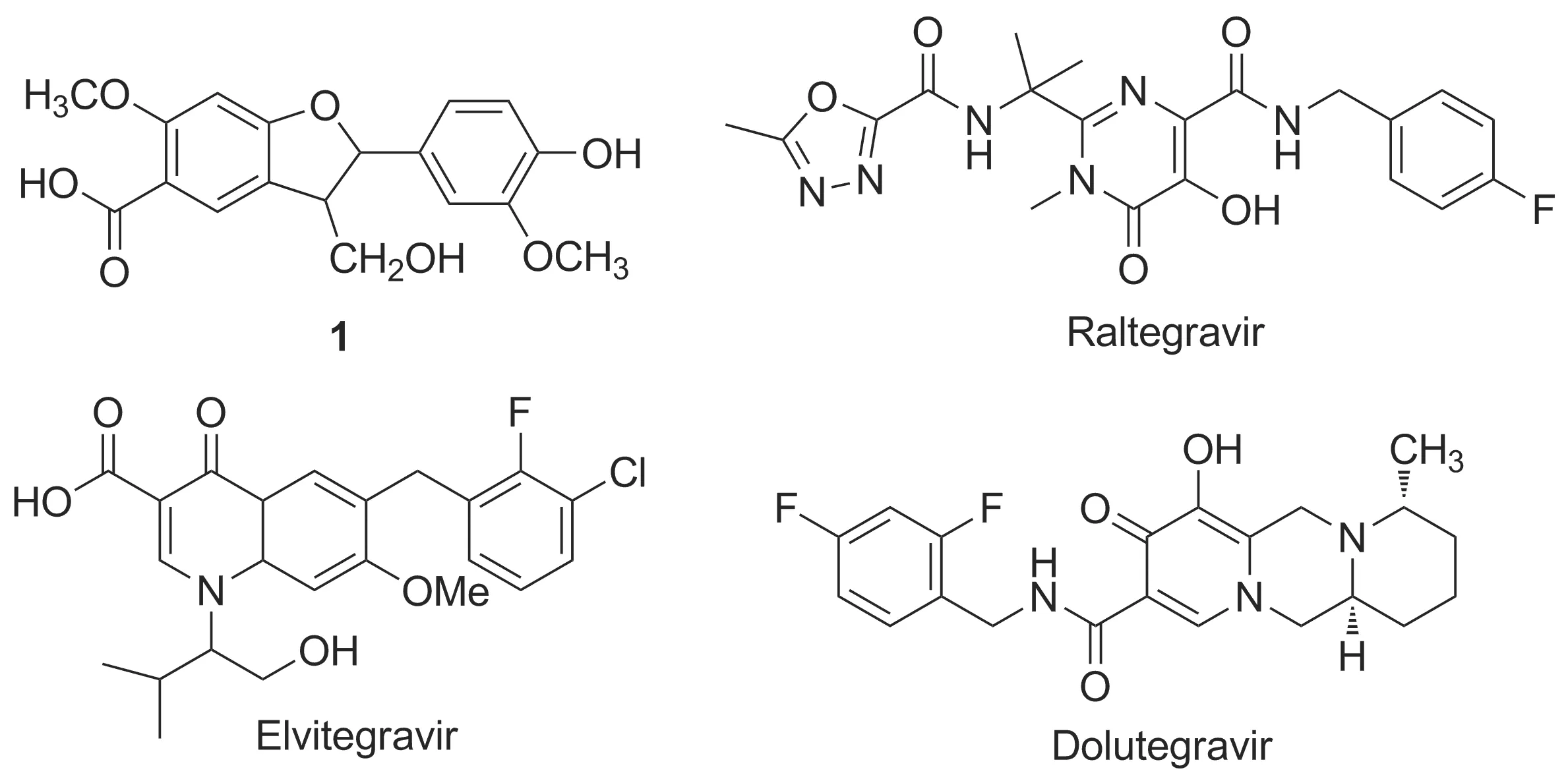
Chart 1
Scheme 1
1.2 合成
(1) 2的合成
将阿魏酸甲酯5.1 g(24.5 mmol)溶于40 mL丙酮和60 mL甲苯的混合液中,N2保护下加入Ag2O 3.5 g(15.1 mmol),于室温反应24 h得黄棕色溶液。抽滤,滤液减压蒸馏得红棕色油状粗产物,经硅胶柱层析[洗脱剂:V(石油醚) ∶V(乙酸乙酯)=5 ∶1]纯化得白色固体粉末2 1.9 g,产率37.2%, m.p.151.2~153.3 ℃;1H NMR(CDCl3)δ: 7.65(d,J=16.2 Hz, 1H, 11-H), 7.39(s, 1H, 6-H), 7.19(s, 1H, 4-H), 7.14(d,J=6.0 Hz, 1H, 6′-H), 7.03(d,J=2.0 Hz, 1H, 2′-H), 6.89(dd,J=6.0 Hz, 2.0 Hz, 1H, 5′-H), 6.33(d,J=16.2 Hz, 1H, 12-H), 6.11(d,J=7.8 Hz, 1H, 2-H), 4.36(d,J=7.8 Hz, 1H, 3-H), 3.91(s, 3H, 6-OCH3), 3.85(s, 3H, 13-OCH3), 3.83(s, 3H, 3′-OCH3), 3.80(s, 3H, 10-OCH3);13C NMR(CDCl3)δ: 170.7(C=O), 167.7(C=O), 149.9, 146.9, 146.1, 144.8, 144.6, 131.1, 128.4, 125.6, 119.3, 117.8, 115.3, 114.6, 112.1, 108.8, 87.4, 56.0, 55.9, 55.3, 52.8, 51.6, 50.4; MS(ESI)m/z: 414.41[M+]。
(2) 3的合成
将2 1.7 g(4.2 mmol)溶于20 mL无水二氯甲烷中,搅拌下加入三氯化铝0.6 g(4.9 mmol),缓慢加入乙酰氯0.5 mL(7.0 mmol),于室温反应3 h得棕红色液体,依次用水(3×20 mL)洗涤,用甲醇重结晶得白色固体3 0.522 1 g,产率33.8%, m.p.135.4~138.3 ℃;1H NMR(acetone-d6)δ: 7.75(s, 1H, 5′-H), 7.62(d,J=16.2 Hz, 1H, 11-H), 7.39(s, 1H, 6-H), 7.28(s, 1H, 4-H), 7.09(s, 1H, 2′-H ), 6.43(d,J=16.2 Hz, 1H, 12-H), 6.04(d,J=7.8 Hz, 1H, 2-H), 4.47(d,J=7.8 Hz, 1H, 4-H), 3.91(s, 3H, 3′-OCH3), 3.83(s, 3H, 7-OCH3), 3.80(s, 3H, 13-OCH3), 3.75(s, 3H, 10-OCH3), 2.05(s, 3H, CH3);13C NMR(acetone-d6)δ: 206.7(C=O), 171.8(C=O), 169.2(C=O), 168.6, 167.8, 153.2, 152.6, 144.8, 141.4, 141.2, 138.4, 134.2, 130.5, 124.0, 121.7, 119.9, 113.6, 112.3, 88.9, 63.1, 57.0, 56.8, 53.2, 52.3, 20.9; MS(ESI)m/z: 456.15[M+]。
(3) 4的合成
依次将3 0.3 g(0.7 mmol)和草酸二甲酯0.2 g(1.5 mmol)加至圆底烧瓶中,加入乙醚10 mL,搅拌使其完全溶解;缓慢滴加新制0.19 mmol·mL-1甲醇钠溶液6 mL,滴毕,于室温反应过夜得橘红色溶液。常压蒸馏除去乙醚,残余物用丙酮重结晶得白色固体4 0.162 8 g,产率44.8%, m.p.157.4~160.2 ℃;1H NMR(CD3OD)δ: 7.65(d,J=15.6 Hz, 1H, 11-H), 7.22(d,J=11.4 Hz, 1H, 6′-H), 6.95(s, 1H, 6-H), 6.81(d,J=15.6 Hz, 1H, 12-H), 6.41(d,J=16.2 Hz, 1H, 4-H), 6.01(s, 1H, 2′-H), 5.34(s, 1H, 2-H), 4.38(d,J=7.2 Hz, 1H, 3-H), 3.92(s, 3H, OCH3), 3.88(s, 3H, OCH3), 3.82(s, 3H, OCH3), 3.77(s, 3H, OCH3), 3.72(s, 3H, OCH3), 3.55(s, 2H, CH2);13C NMR(CD3OD)δ: 208.6(C=O), 171.9(C=O), 169.2(C=O), 165.3(C=O), 153.4, 151.7, 150.5, 145.8, 144.7, 143.6, 134.1, 129.7, 125.4, 123.0, 117.8, 115.1, 114.2, 113.3, 87.4, 56.5, 55.4, 54.9, 52.0, 50.8, 48.2; MS(ESI)m/z: 514.46[M+]。
(4) 5的合成
将4 0.15 g(0.3 mmol)溶于20 mL 1,4-二氧六环中,加入1 mol·L-1盐酸5 mL,搅拌下于室温反应24 h得呈黄色溶液。减压蒸馏得橘黄色固体,用甲醇重结晶得黄色固体5 0.037 8 g,产率25.3%, m.p.180.3~184.3 ℃;1H NMR(CD3OD)δ: 10.31(s, 1H, OH), 7.65(d,J=15.6 Hz, 1H, 12-H), 7.03~6.98(m, 4H, 2′,6′,4,6-H), 6.33(d,J=15.6 Hz, 1H, 13-H), 6.19(d,J=7.8 Hz, 1H, 2-H), 4.35(d,J=7.8 Hz, 1H, 4-H), 3.92(s, 3H, OCH3), 3.85(s, 3H, OCH3), 3.82(s, 3H, OCH3), 3.80(s, 3H, OCH3), 3.51(s, 2H, CH2);13C NMR(CD3OD)δ: 206.7(C=O), 170.5(C=O), 168.8(C=O), 167.5(C=O), 151.2, 149.7, 144.7, 144.6, 139.8, 138.4, 128.7, 125.3, 123.0, 118.1, 117.8, 115.6, 112.1, 110.0, 86.1, 56.5, 55.9, 55.5, 52.9, 51.6; MS(ESI)m/z: 500.46[M+]。
1.3 分子对接方法
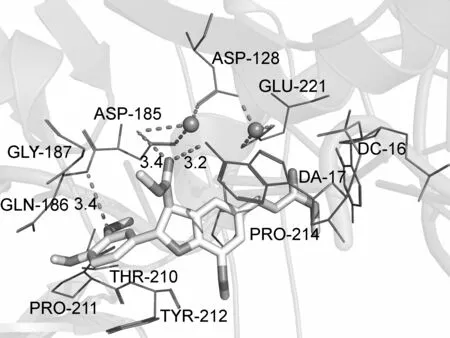
由于HIV-1整合酶(IN)的溶解度差,其完整的三维结构目前尚未被解析,目前只解析了一个小分子(5CITEP)与HIV-1 IN核心区域的复合结构,蛋白质数据库(Protein Data Bank, RCSB)中ID为1QS4[11]。根据张美青等[12]的研究表明,原型泡沫病毒(PFV)IN与HIV-1 IN的高度的同源性,PFV IN与1QS4核心区域经过叠合实验表明,PFV IN与1QS4的核心区域基本叠合,但1QS4由于缺失第二个Mg2+和病毒DNA而使核心区域不完整。而已解析的PFV IN中含有两个金属离子和病毒DNA,很好的弥补了1QS4的缺陷,并且解析的PFV IN蛋白复合晶体3L2V中与蛋白核心区域复合的小分子为Raltegravir,这使得PFV IN成为研究HIV-1 IN抑制剂的有效靶点。
用PyMol提取3L2V整合酶蛋白A链、DNA、小分子配体和金属离子。用AutoDockTools 1.5.6处理受体结构;经AutoDock Vina软件以目标化合物2~5为配体,分别与晶体结构3L2V进行分子对接,通过PyMol软件显示结果图。
2 结果与讨论
2.1 合成
以两分子的阿魏酸甲酯为原料,经过氧化偶联、傅克酰基化、酯缩合和酯水解4步反应合成4个2-芳基苯并二氢呋喃类化合物,其中化合物3~5是具有1,3-二酮基团的化合物。在合成化合物5时发现2-芳基苯并二氢呋喃结构在水解时对碱较敏感,在低浓度碱的催化下可使2-芳基苯并二氢呋喃结构发生裂解开环,而在6 mol·L-1盐酸中则不会开环;因此,2-芳基苯并二氢呋喃结构的化合物不宜在碱性条件下进行化学反应。
2.2 分子对接结果
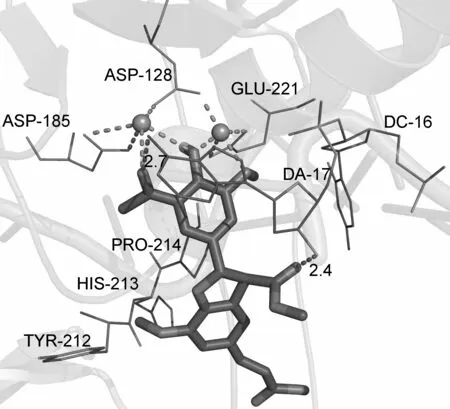
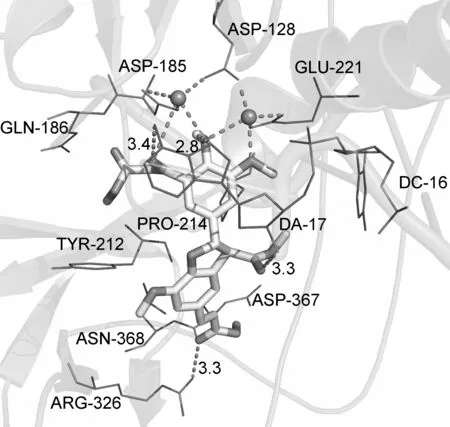
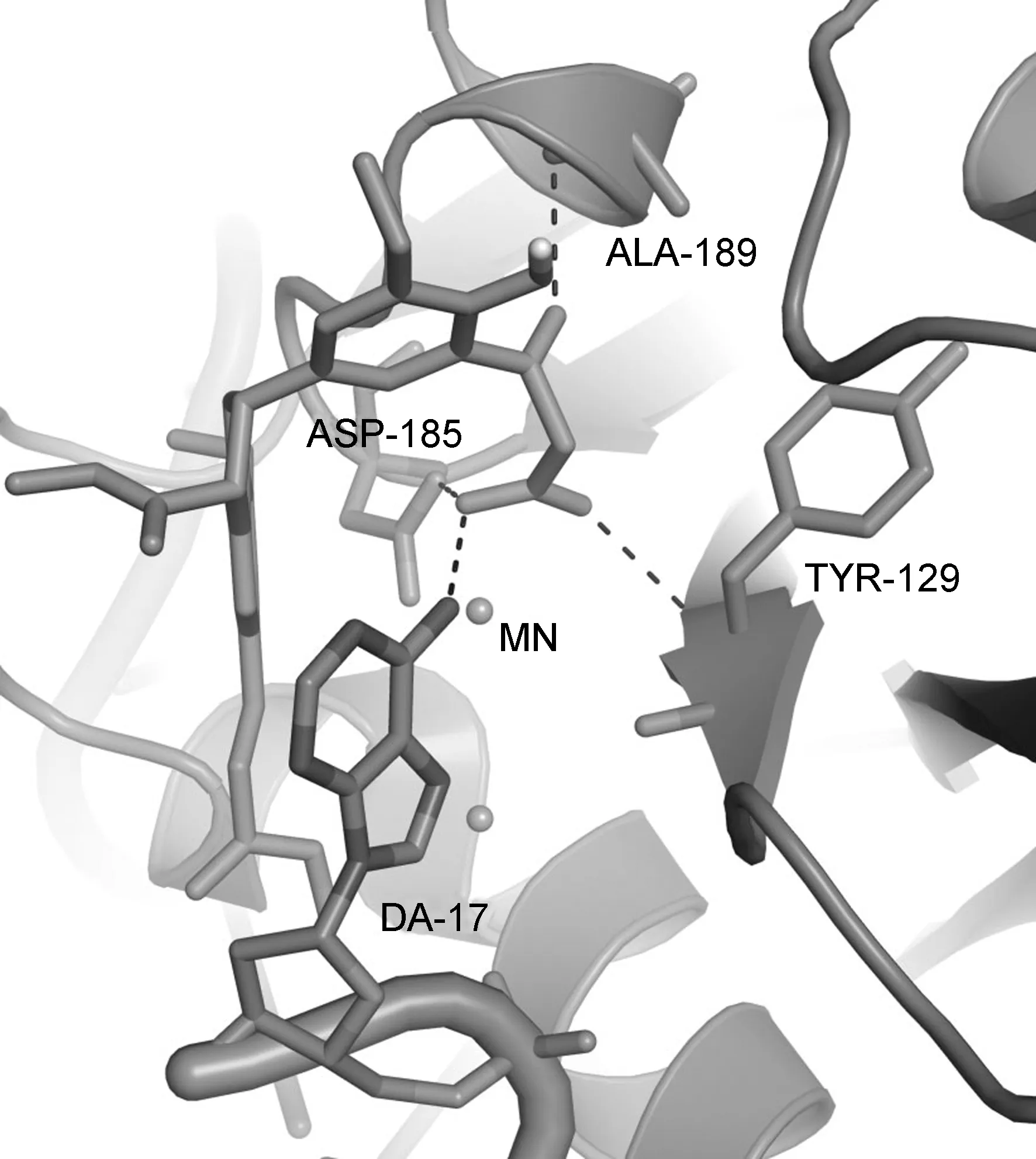
本文对化合物2~5进行了与整合酶蛋白为受体的分子对接处理,结果分别见表一和图1。
由表1可以看出,在化合物2的5′-位酰化后引入1,3-二酮结构(苯环羟基与乙酰羰基)后得到的化合物3,结合能降低;进一步酯化和水解反应得到的化合物4和5(苯环外部1,3-二酮结构),化合物与整合酶活性口袋的结合能进一步降低;化合物与受体蛋白中的残基形成氢键的个数和强度也在增加,根据形成氢键的残基的种类发现4个化合物均与核苷酸DA-17形成氢键,提示整合酶中DNA的存在是该类药物发挥良好活性的重要组成部分;苯并二氢呋喃2-位苯环伸入至活性口袋的底部,与周围的氨基酸残基存在范德华力作用,而5-位丙烯酸甲酯部分位于活性口袋的开口区域,作用力较弱,因此2-位芳环是主要活性部位。化合物3~5中含有的1,3-二酮结构可以和整合酶活性口袋中的两个金属离子螯合在一起,进一步增强复合物的稳定性。
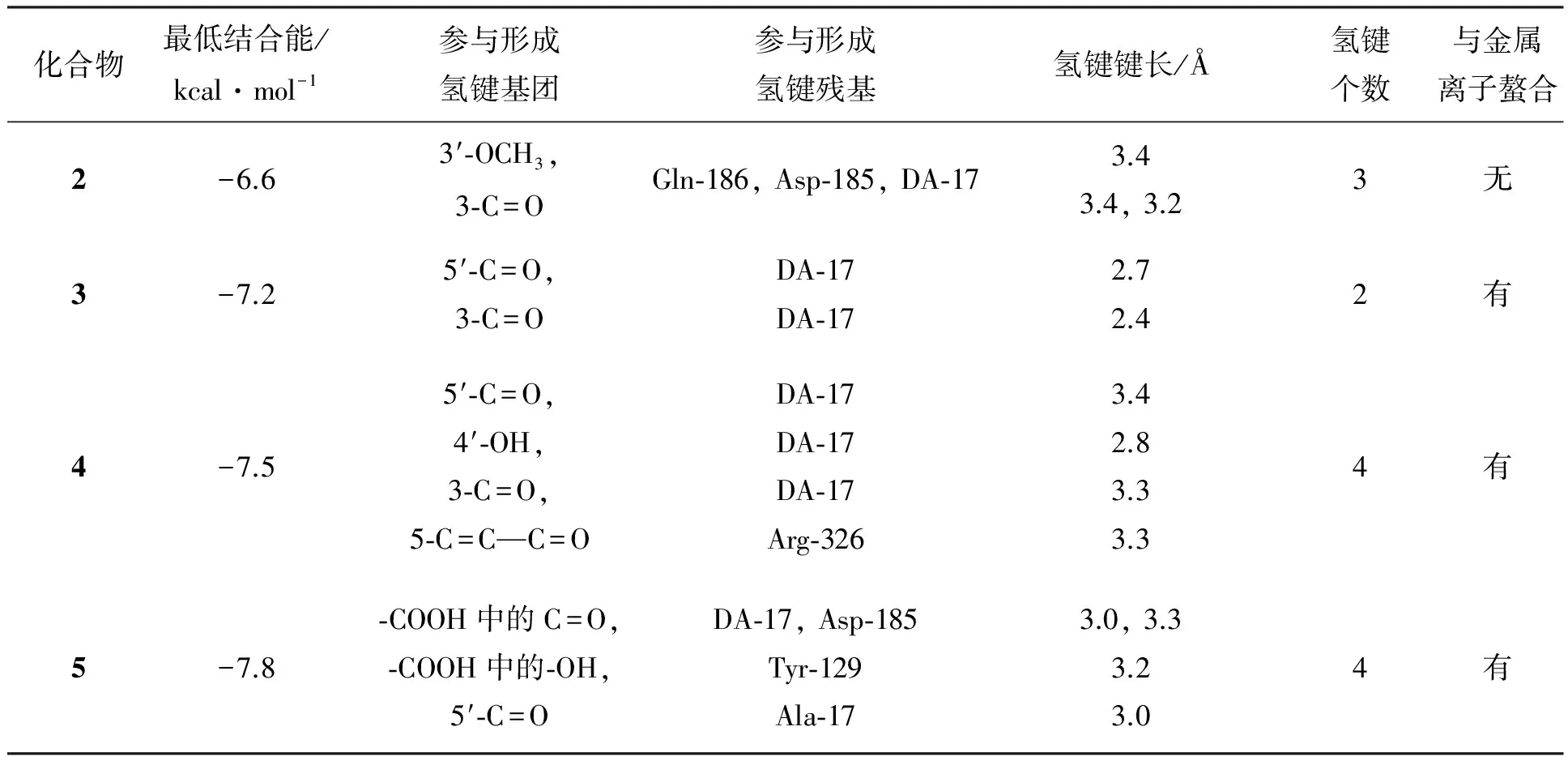
表1 化合物2~5与受体蛋白(3L2V)的分子对接结果
2
3
4
5
计算结果显示,化合物5与整合酶形成复合物的结合能最低,与其形成氢键的整合酶残基种类最多,活性最强,推测其对HIV-1整合酶具有良好的抑制作用。
以阿魏酸甲酯为原料合成了4个2-芳基苯并二氢呋喃类化合物,其中化合物3, 4和5为具有1,3-二酮基团的新化合物,化合物5为1,3-二酮酸。用计算机模拟化合物2~5与整合酶晶体结构(PDB: 3L2V)相结合的分子对接结果显示:该类化合物主要活性部位是苯并二氢呋喃环的2-位芳环,整合酶中的DNA的存在是药物作用的必要部分;该类化合物和整合酶具有良好的结合能力,4个化合物与整合酶残基形成氢键的数量和强调逐渐增强,形成复合物的结合能逐渐降低,其中化合物3, 4和5中的1,3-二酮基团部位可以与整合酶中金属离子发生螯合作用,5可能是4个化合物中活性最强的化合物。预示该类化合物可能具有潜在抑制HIV-1整合酶活性的作用,为进一步测定其生物活性提供了参考依据。
[1] 蒲文飞,王飞,王淳. 2-芳基苯并[b]呋喃衍生物的生物活性与合成策略[J].有机化学,2011,31(2):155-165.
[2] Ngouela S, Tsmao E, Connolly J D. Lignans and other constituents ofZanthoxylumheitzii[J].Phytochemistry,1994,37(3):867-869
[3] 庞冀燕,许遵乐. 2-取代芳基苯并呋喃类化合物生物活性及合成研究进展[J].有机化学,2005,25(1):25-33.
[4] 买尔旦·马合木提,贺金华,堵年生. 软紫草抗HIV的水溶性成分及提取物:CN 200510129949.2[P].2009.
[5] 买尔旦·马合木提,贺金华,古丽仙·胡加. 新疆软紫草提取物抗HIV-1体外活性研究(Ⅰ)[J].新疆医科大学学报,2009,32(4): 374-377.
[6] 买尔旦·马合木提,古丽仙·胡加,秦冬梅. 新疆紫草提取物抗HIV-1体外活性研究(Ⅱ)[J].新疆医科大学学报,2009,32(4): 377-379.
[7] HicksC, Gulick R M. Raltegravir:The first HIV type 1 integrase inhibitor[J].Clinical Infectious Diseases,2009,48(7):931-939.
[8] Serrao E, Odde S, Ramkumar K,etal. Raltegravir,elvitegravir,and metoogravir:The birth of “me-too” HIV-1 integrase inhibitors[J].Retrovirology,2009,6:25-39.
[9] Dow D E, Bartlett J A. Dolutegravir,the second-generation of integrase strand transfer inhibitors(INSTIs) for the treatment of HIV[J].Infectious Diseases Therapy,2014,3(2):83-102.
[10] 石雅玮,刘振明,金宏威,等. 二酮酸类HIV-1整合酶抑制剂的定量构效关系[J].物理化学学报,2007,23(9):1393-1398.
[11] Barreca M L, Lee K W, Chimirri A,etal. Molecular dynamics studies of the wild-type and double mutant HIV-1 integrase complexed with the 5CITEP inhibitor: mechanism for inhibition and drug resistance[J].Biophysical Journal,2003,84(3):1450-1463.
[12] 张美青. 计算机辅助设计二酮酸类HIV-1整合酶抑制剂的研究[D].杭州:浙江大学,2013.
Synthesis of Novel Dihydrobenzofuran Compounds and Molecular Docking of Them with Diketoacid
FAN Ye, LUO Yang, MA Cheng*
(School of Pharmacy, Xinjiang Medical University, Urumqi 830011, China)
2-Aryl dihydrobenzo[b]furan skeleton was constructed from methyl ferulate through oxidative coupling reaction. Friedel-Crafts acetylation and ester condensation were applied to synthesize (E)methyl 3-[2-(4-hydroxy-3-methoxy-5-acetyl)phenyl-3-methoxcarbonyl-7-methoxy-2,3-dihydrobenzo[b]furan-5-yl] arcylate(3) and (E)methyl 3-[2-(4-hydroxy-3-methoxy-5-methoxcarbonacetyl)phenyl-3-methoxcarbonyl-7-methoxy-2,3-dihydrobenzo[b]furan-5-yl]acrylate(4). The compound 4 was hydrolyzed to afford 3-(2-hydroxy-3-methoxy-5-(5-(2-(methoxcarbonyl)vinyl)-7-methoxy-3-methoxcarbonyl-2,3-dihydrobenzo[b]furan-2-)yl)phenyl-3-ox-propanoic acid(5). Among them, 3~5 were new compounds. The structures were characterized by1H NMR,13C NMR and MS(ESI). Autodock vina was applied for molecular docking of compound 2~5 toward prototype foamy virus(PFV) integrase(IN)(PDB: 3L2V), a highly homologous protein of HIV-1 IN. The results showed that the stable complexes could be formed between these compounds and IN. In particular, compound 3~5 with 1,3-diketo moiety can chelate with metal ions in the IN, and affinity of compound 5 is strongest.
methyl ferulate; 2-aryl dihydrobenzofuran; 1,3-diketone; synthesis; HIV-1 integrase; molecular docking
2016-12-26
新疆维吾尔自治区高校科研计划重点项目(XJEDU2016I031); 新疆医科大学研究生创新创业项目(CXCY097)
范晔(1990-),男,满族,辽宁桓仁人,硕士研究生,主要从事天然产物活性成分的结构修饰与合成研究。
马成,博士,副教授, E-mail: mac2008hk@126.com
O621.3; O626.11
A
10.15952/j.cnki.cjsc.1005-1511.2017.04.16326

