以氯气教学为例谈化学教学中自救互救知识的渗透
王希霞
摘 要 本文主要以氯气教学为例,分析了化学教学中自救互救知识的渗透问题。
关键词 氯气教学 化学教学 自救互救
中图分类号:G633.8 文献标识码:A
1根据事故了解氯气的物理性质
创设情境:播放重庆天原化工厂液氯泄露事故的视频短片,启发学生根据有关情境自主总结氯气的物理性质,指导学生闻氯气的气味,掌握闻气体的基本方法,再归纳总结出氯气的物理性质。
2中毒原理看氯气与水的反应,渗透自救知识
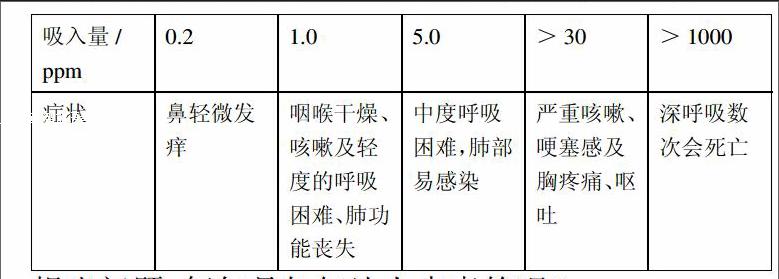
资料卡片:观看氯气吸入量与中毒症状的资料;
提出问题:氯气是如何让人中毒的呢?
演示实验:气体通过呼吸道进入身体,用湿润的蓝色石蕊试纸模拟呼吸道粘膜,将其迅速插入装有氯气的试管中,发现蓝色石蕊试纸先变红后褪色。试纸变红说明有酸生成,后又褪色说明有具有漂白性的物质生成。
原理讲授:氯气通过人的呼吸,进入呼吸道与黏膜中的水分发生反应
生成了盐酸和次氯酸。盐酸有较强的腐蚀性,次氯酸有强烈的氧化性,因而又具有漂白性,二者均能引起呼吸道及支气管黏膜损伤,又因次氯酸的强氧化性,在高浓度下可引起肺水肿,血液浓度增加,呼吸变慢,最终导致心力衰竭而死亡。
提出问题:如果你居住在某化工厂附近,在家中发现氯气泄漏时,如何实现自救呢?
分析问题:引导学生从家中物品和撤离方面考虑,组织学生讨论并回答。
得出结论:当发现氯气泄漏时,首要是在最短时间内尽快撤离毒气现场,利用口罩、游泳眼镜或家中毛巾衣物沾湿水捂住口鼻,使吸入氯气量减少到最低。撤离时,要向侧风向快速撤离。迎风会误入重污染区,吸入高浓度毒气,顺风会导致长时间吸入毒气,增加对人体中毒的伤害。
3错误处理钢瓶泄漏看氯气的强氧化性
提出问题:事故现场液氯钢瓶发生严重泄漏无法封堵时,应如何处理呢?能不能在液氯钢瓶上喷水呢?
分析问题:引导学生回顾氯气与水的反应,补充此反应在生成盐酸和次氯酸的同时放出大量的热能。工作人员吸入盐酸和次氯酸蒸气或烟雾,会引起急性中毒,眼和皮肤接触易被灼伤。追问还有其他原因吗?
分析问题:盐酸还会腐蚀钢瓶,放出氢气。氢气与氯气遇明火易发生爆炸,引出氯气与非金属单质的反应。启发诱导学生迁移应用氧化还原反应原理分析得出氯气具有强氧化性,同时诱导学生从氯原子结构分析氯气为什么具有强氧化性,并演绎出与金属的反应。
实验演示:氯气与铜和铁的反应,学生观察实验现象。
分析问题:除氯气与水反应生成的HCl会与钢瓶发生反应外,另一产物HClO具有不稳定性,受阳光照射又会分解成氯化氢和氧气,氢氧混和也易发生爆炸。
得出结论:如果向泄漏的氯气钢瓶浇水,不仅起不到降温作用,反而促使钢瓶升温,增大爆炸危险,并形成有毒、腐蚀性强的盐酸,使抢险堵漏人员面临更大危险。
4正确处理泄漏钢瓶看氯气的酸性,渗透自救知识
提出问题:那么如何正确地对泄露的液氯钢瓶进行处理呢?
分析问题:氯气溶于水后与水反应得到两种酸,因此可将其与碱性物质反应。
得出结论:工业上将泄漏的钢瓶浸入呈碱性的石灰水中,使其进行中和反应。引出氯气与碱的反应。对扩散的氯气往地面上撒苏打水溶液,这是因为Na2CO3溶液水解后形成NaOH。类比得出Cl2与NaOH的反应。
同时补充次氯酸钙与次氯酸钠分别是漂白粉和消毒液的主要成分,引导学生回顾次氯酸的漂白性,得出二者的原理以及碳酸和次氯酸的酸性强弱。
提出问题:如果顺利撤离出污染区后,出现恶心、呕吐、呼吸困难的症状时,应怎么办?引导学生根据已学知识讨论并回答。
分析问题:生活中的弱碱性物质能够帮助除去衣物和身体上接触到的氯气。
得出结论:撤离出毒气污染区后,用肥皂水和清水清洗衣物、冲洗全身。用净水漱口,喝干净水,服用碱性饮料比如牛奶,寻求治疗。
提出问题:面对险境时,我们不仅要自救也要帮助他人获救。若身边有吸氯过多已中毒的人员,你该如何做?能进行人工呼吸吗?
分析问题:氯气中毒后呼吸道表皮细胞大面积损伤后,会有大量的体液流出造成呼吸受阻。人工呼吸会使肺部循环加快,造成体液的流出,呼吸障碍恶化。再结合已学知识得出具体急救方法。
得出结论:先将吸氯人员迅速撤离事故现场至空气新鲜而安静的地方躺下,解开衣服放松裤带。如果衣服沾染了液氯或氯水,应脱去污染衣物,用肥皂水或清水冲洗皮肤,皮肤酸灼伤用2%~3%碳酸氢钠溶液湿敷,不宜做人工呼吸。
参考文献
[1] 韦佳輝.弹道导弹发射阵地燃气流场数值模拟及人员安全性分析[D].太原:中北大学,2015.
[2] 赵玉泉.从社会生活实际走进化学—新课程理念下氯气一节的课堂教学设计[J].化学教学,2006(4):39-40.
[3] 常见事故分析与防范对策丛书编委会.危险化学品常见事故与防范对策[M].中国劳动社会保障出版社,2005,1.

