线性-树枝状共聚物载药微球的制备、表征及体外释放
杨李影, 郭 睿, 戎宗明
(1.华东理工大学化学与分子工程学院,上海 200237; 2.巴斯夫上海涂料有限公司,上海 201108)
线性-树枝状共聚物载药微球的制备、表征及体外释放
杨李影1, 郭 睿2, 戎宗明1
(1.华东理工大学化学与分子工程学院,上海 200237; 2.巴斯夫上海涂料有限公司,上海 201108)
以自制的生物可降解线性-树枝状两嵌段两亲共聚物材料为药物载体,采用透析法制备了雷帕霉素载药微球。通过扫描电子显微镜(SEM)、动态光散射仪(DLS)、紫外分光光度计对雷帕霉素载药微球的表面形貌、粒径分布、载药量及释放行为进行了研究。结果表明:载药微球的载药量和包封率分别可达到40%和90%以上,与哑铃型三嵌段两亲共聚物载药微球相当,但平均粒径大幅降低(粒径约300 nm),同样具有显著的缓释作用。
线性-树枝状共聚物; 生物可降解; 载药微球; 体外释放; 雷帕霉素
抗肿瘤药物的控制释放是恶性肿瘤化疗的关键,而生物可降解材料成为主要的药物载体[1-4],尤其是聚乙二醇-聚乳酸两亲型嵌段共聚物,由于其独特的自组装等优异功能,成为研究的重点并被广泛地应用到载药体系中[5-7]。
本课题组曾自制了生物可降解的聚L-丙交酯-dendron-聚乙二醇-dendron-聚L-丙交酯哑铃型三嵌段两亲共聚物[8],实验研究发现其在选择性溶剂中能自组装形成规整的空心微球[9],利用其自组装的特点,采用透析法制备了载雷帕霉素微球,得到了载药量和包封率分别可达40%和91%、平均粒径在300~500 nm的载药微球[10];对于在水中具有一定溶解度的替莫唑胺药物,则以替莫唑胺饱和水溶液作选择性溶剂,透析制得了载药量可达40%、平均粒径不大于800 nm的载药微球[11]。这两种载药微球都具有缓释功能,体外缓释时间最长可达到900 h之久。
为了进一步减小载药微球的粒径,又以聚乙二醇单甲醚代替聚乙二醇作为起始剂,通过发散法合成了一系列线性-树枝状两嵌段共聚物,并通过增加亲水链长的方法来提高其所形成的胶束在水溶液中的稳定性[12]。本文将以此类嵌段共聚物为载体,进行包裹免疫抑制药物雷帕霉素(Rapamycin,RAPA)的研究,在确定制备工艺的条件下,探究不同结构的线性-树枝状两嵌段共聚物对其所形成的载药微球的载药性能,如粒径分布、形态、缓释等性能的影响,以获得性能更为优异的药物载体材料。
1 实验部分
1.1 主要原料与仪器
主要原料:雷帕霉素(医用级),上海东方医院提供;透析袋,7 000 Du,VISKASE®公司;线性-树枝状共聚物(mPEG(5 000)-Gx-PLLA(y)n,x为2、3、4,y为2 500、5 000、10 000,n为4、8、16),实验室自制,其结构如图1所示,文中所用线性-树枝状两嵌段共聚物的结构信息见表1。

图1 四代线性-树枝状共聚物结构
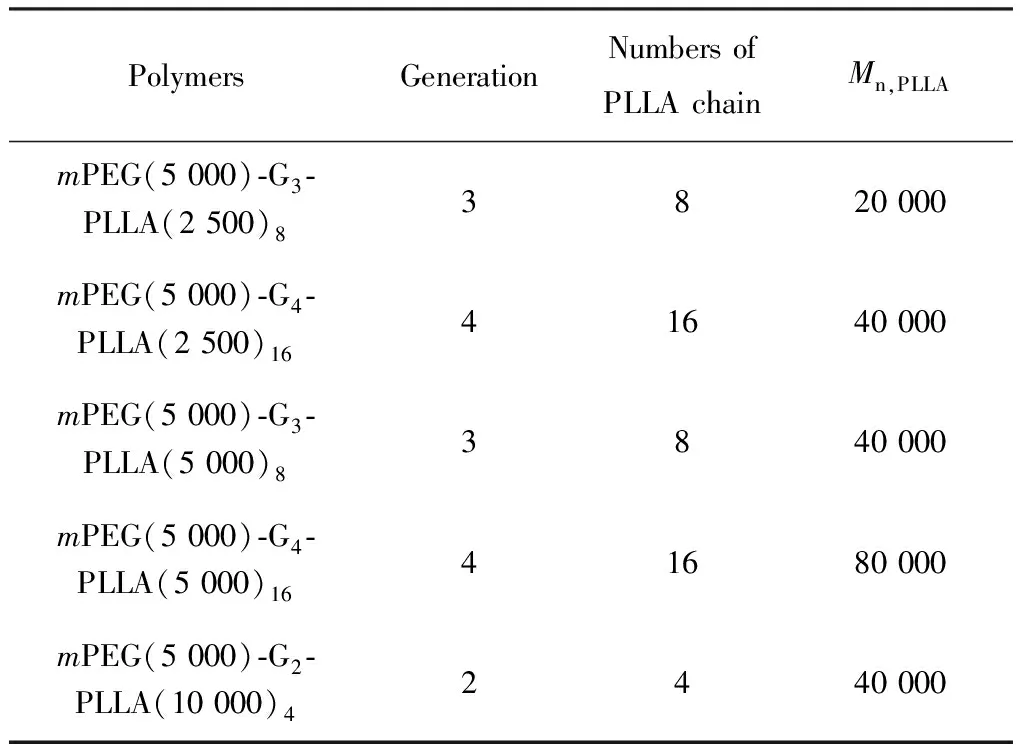
PolymersGenerationNumbersofPLLAchainMn,PLLAmPEG(5000)⁃G3⁃PLLA(2500)83820000mPEG(5000)⁃G4⁃PLLA(2500)1641640000mPEG(5000)⁃G3⁃PLLA(5000)83840000mPEG(5000)⁃G4⁃PLLA(5000)1641680000mPEG(5000)⁃G2⁃PLLA(10000)42440000
扫描电子显微镜(SEM,日本Hitachi S-3400);动态光散射(DLS,Zetasizer Nano,英国马尔文仪器有限公司);紫外分光光度计(UV765,上海精密科技有限公司)。
1.2 雷帕霉素载药微球的制备及表征
采用透析法制备聚合物载药微球。称取一定量的线性-树枝状共聚物及RAPA药物粉末于四氢呋喃中,超声待其完全溶解后,将混合液转入透析袋内。在35 ℃恒温下,在去离子水中透析,低速搅拌,间隔4 h更换外水相,直至溶剂除尽。待透析结束后,将透析袋内溶液高速离心40 min,取出底部白色沉淀,经冷冻干燥后得到固体载药微球。空微球的制备方法与载药微球的制备方法相似,仅在四氢呋喃溶剂中不加入雷帕霉素即可。
采用动态光散射仪(DLS)测量微球的平均粒径及分散系数(PDI)。取一定体积的微球溶液,在25 ℃下,测量样品粒径大小及分布系数,每个样品测量3次。采用扫描电镜(SEM)观察微球形貌特征。将微球溶液样品分散在云母片上,自然干燥,做喷金处理后在扫描电镜下观察微球的形貌及大小。
1.3 载药微球载药量及包封率的测定
称取一定质量冷冻干燥后的载雷帕霉素的微球粉末,使其完全溶解于一定量二氯甲烷中,用紫外分光光度计测得其在波长278 nm处的吸光度A。同时根据RAPA在二氯甲烷中的标准曲线计算得出载药微球中RAPA的含量。载药微球的实测载药量(DL)及包封率(EE)计算公式:
(1)
(2)
式中:ms为包裹进微球的药物质量;m0为总的共聚物投入质量;mt为总的药物投入质量。
1.4 雷帕霉素载药微球体外释放测定方法
称取一定质量的雷帕霉素,用乙醇溶解,按照乙醇与PBS缓冲液体积比1∶9,加入pH=7.4的PBS缓冲液,分别配成一系列不同浓度的溶液,用不含雷帕霉素的PBS与乙醇的混合液作空白参比,用紫外分光光度计测定其在278 nm处的吸光度(A),绘制得到标准曲线,A=51.96c-0.008 6,相关系数R为0.999 1,式中雷帕霉素质量浓度c的单位为mg/mL。
称取一定质量的载雷帕霉素微球粉末分散在pH=7.4的PBS缓冲溶液中。将溶液转移至透析袋内,浸置在37 ℃的PBS溶液中模拟体外释放。每间隔一段时间,取2 mL的缓释溶液,同时补加等量的新鲜PBS缓冲液,保持缓冲液的体积不变。采用紫外分光光度计测得缓释溶液的吸光度,根据标准曲线方程计算出不同时间RAPA的累计释放量,绘制体外RAPA累计释放率-时间曲线。
2 结果与讨论
2.1 载药微球的载药性能
2.1.1 最佳投药质量比的确定 以mPEG(5 000)-G4-PLLA(2 500)16和mPEG(5 000)-G4-PLLA(5 000)16两个共聚物制备载药微球为例,考察了投药质量比对载药微球的载药量、包封率、粒径及形态的影响,实验结果见表2和图2。从表2中可以看出,随投药质量比的增加,两种共聚物的载药微球实测的载药量呈线性增加,但载药微球的平均粒径变化不大;在相同的投药比时,由于mPEG(5 000)-G4-PLLA(5 000)16的疏水链段PLLA较mPEG(5 000)-G4-PLLA(2 500)16增长了1倍,能吸附较多的药物,因此其载药量和包封率也相对较高,相应的微球粒径也较大些。
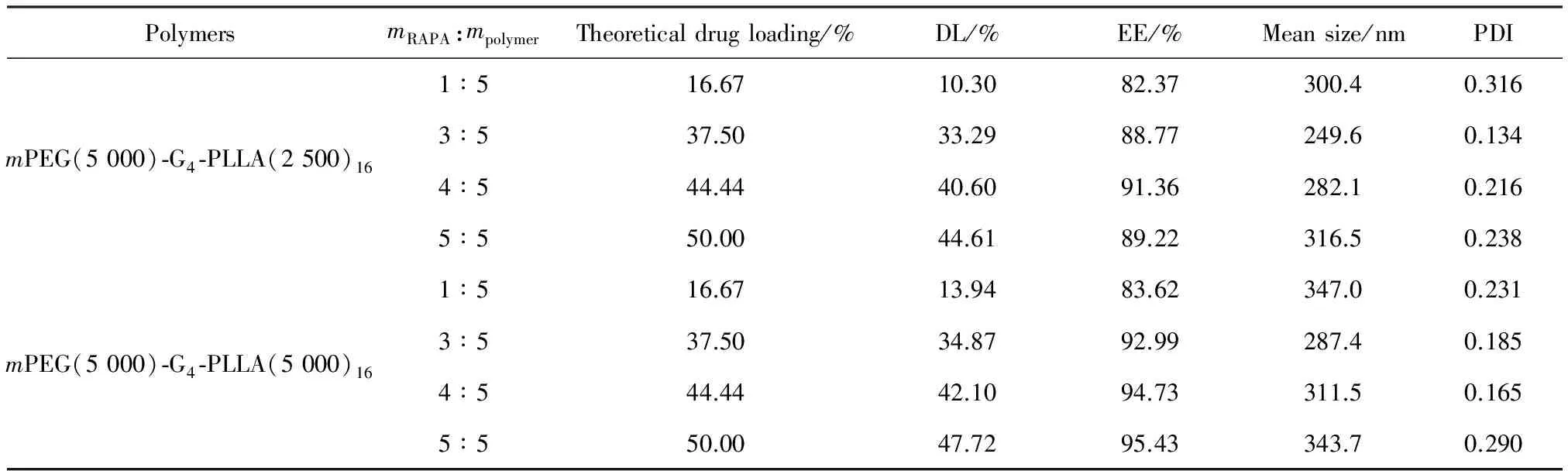
表2 RAPA不同投药质量比对载药微球平均粒径、载药量以及包封率的影响
为了进一步确定药物是否完全被包裹进微球内部,采用扫描电镜(SEM)观察了所制备的载药微球的形貌,结果见图2,从图2中可以看到载药微球本身呈空心球形,且分散良好。对于mPEG(5 000)-G4-PLLA(2 500)16共聚物载药微球,在投药质量比为3∶5时,载药微球表面光滑,见图2(a);但在投药质量比为4∶5(图2(b))和5∶5(图2(c))时,微球表面有类似药物颗粒黏附,外面也可看到零星药物颗粒存在,说明雷帕霉素药物并没有完全被包裹进微球内部,实验测得的载药量和包封率并不真实。因此,其最佳的投药质量比应为3∶5。而mPEG(5 000)-G4-PLLA(5 000)16共聚物的载药微球表面和外面均未见有药物颗粒,见图2(d~f),载药量和包封率也随着投药比的增加而增大。考虑到mPEG(5 000)-G4-PLLA(5 000)16是该系列聚合物中聚乳酸含量最多的,为兼顾低代数的聚合物,其投药质量比选择为4∶5。

图2 不同投药质量比载药微球的SEM图
2.1.2 载药微球的性能与聚合物分子结构间的关系 由于合成线性-树枝状一代共聚物中聚乙二醇的体积分数φEO>0.5,不能形成规整的球形胶束[12],故只考察了2~4代线性-树枝状共聚物的载药微球在确定的投药质量比时,载药微球的载药量、包封率和粒径随代数的变化关系,结果见表3。

表3 不同结构线性-树枝状共聚物载药微球的性能对比
从表3的数据可以看出,当共聚物的代数相同时,单链PLLA相对分子质量小,相应的载药微球的载药量、包封率和粒径也小;mPEG(5 000)-G3-PLLA(5 000)8和mPEG(5 000)-G2-PLLA(10 000)4的PLLA分子总量是一样的,但两者载药量等仍有差别,说明载药量和包封率主要随PLLA链长和代数的增加而增大。
线性-树枝状共聚物载药微球与先前所制备的相同代数和PLLA链长的哑铃型三嵌段两亲共聚物(聚L-丙交酯-dendron-聚乙二醇-dendron-聚L-丙交酯)的载药微球[10]相比,两者的载药量和包封率基本相同,但线性-树枝状共聚物载药微球的平均粒径在300 nm左右,而后者的平均粒径约为400 nm,平均粒径有较明显的减小,分布更均匀,而且聚乙二醇链段在溶液中的自由伸展使其更加稳定[12],在临床应用上也更具优势。
2.2 雷帕霉素载药微球的体外释放研究
以mPEG(5 000)-G4-PLLA(5 000)16共聚物制备的载药微球为例,考察了不同载药量的载药微球在37 ℃、pH=7.4的PBS缓冲液中的药物释放速率P(t)随时间t的变化关系,结果见图3。

图3 不同载药量的载药微球体外释放曲线
聚合物载药微球中的药物释放一般分为3阶段[13]:第1阶段是突释,往往是没有被包裹的药物颗粒或是黏附在微球表面的药物;第2阶段是一个缓慢释放阶段,药物穿过聚合物内核向外扩散,速度较缓慢;第3阶段是快速释放,有时也称2次突释,聚合物的降解或溶蚀加快药物释放。
在药物初始释放的0~3 h时间段内为突释阶段,吸附在载体表层中的药物快速溶出,使得释放率急剧上升,不同载药量微球的释放率相差不大。然后进入缓释阶段,药物释放量减少,速率变缓,或近似于线性变化。由于形成微球的聚合物结构相同,粒径相当,故载药量越低,释放出的药物相对量也越高,所以缓释的速率也越快。从图3中可以看出实验测得的释放率随载药量的增大而降低,且呈较好的递变规律。
图4给出了载药量相近的线性-树枝状共聚物mPEG(5 000)-G3-PLLA(5 000)8和mPEG(5 000)-G4-PLLA(5 000)16两种载药微球释放曲线的比较。线性-树枝状共聚物代数越高,聚乳酸的含量也越高,相应的粒径也稍大些,且微球壁也越致密,使得疏水药物RAPA与聚乳酸间的相互作用也增强[14],造成药物在微球壁中的扩散速率变缓,累计释放量降低。聚乳酸链段长度相同的情况下,代数越高,聚乳酸的含量也越多,释放速率就越慢。
图4给出了与mPEG(5 000)-G3-PLLA(5 000)8和mPEG(5 000)-G4-PLLA(5 000)16结构相对应的哑铃型三嵌段两亲共聚物所制备的载RAPA微球的释放曲线,其聚乳酸含量更高,粒径也相应增大,故缓释阶段的释放速率更慢。而线性-树枝状共聚物载药微球在缓释阶段的缓释速率斜率就大得多,说明其微球致密度低,因而药物向外扩散的速率也较快。
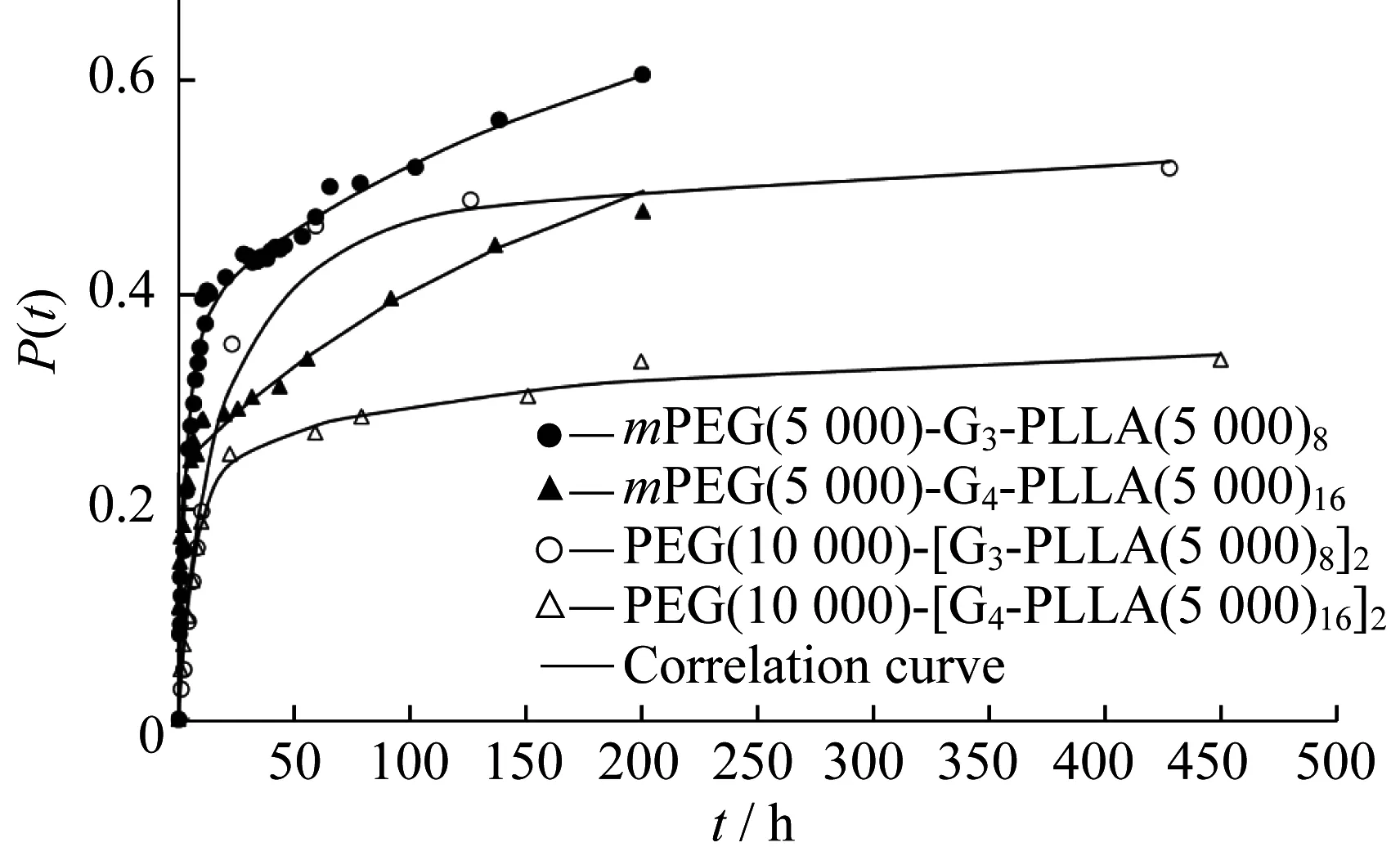
图4 不同结构的共聚物所制备的载药微球体外释放曲线的比较
本课题组曾以Gompertz一级函数作为药物释放动力学模型来描述哑铃型三嵌段两亲共聚物载药释放曲线[10],发现其能较好地描述药物突释阶段,但随着时间的延长,药物仍在释放,Gompertz一级函数模型拟合曲线不再增长,为一水平线,不能真实反映后期药物释放规律。对于此类微球药物释放情况,Gallagher等[15]提出以两个模型的线性组合来拟合,Balcerzak等[16]也采用组合模型来拟合药物释放曲线,并得到了较好的效果。经考察,对于本文的研究体系,可以分别应用Gompertz一级函数和二级释放速率方程来描述突释阶段和扩散释放的释放速率,将两者线性组合的药物释放速率方程的形式为:
(3)
式中:P为药物释放率,0≤P≤1;α1、α2和β1为拟合参数;x为两函数的组合分数;t为时间。
表4列出了采用方程(3) 关联得到的参数、平均绝对误差(AAE)以及平均相对误差(ARE)。从表中可以看出,除了哑铃型三嵌段两亲共聚物PEG(10 000)-[G3-PLLA(5 000)8]2外,拟合的效果都较好。从图3和图4中也可以看到,关联曲线与实验点也能很好地相符,且能反映出其变化趋势。
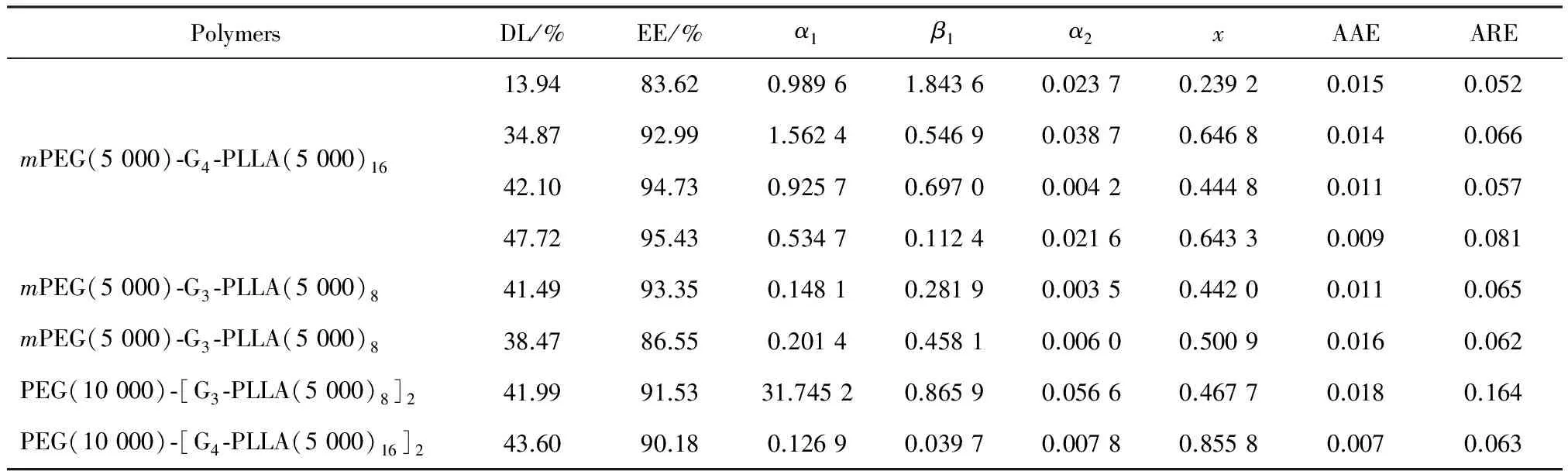
表4 方程(3)的关联结果
3 结 论
以生物可降解的新型线性-树枝状两嵌段共聚物材料作为药物载体,采用透析法制备了RAPA载药微球,与先前的哑铃型三嵌段两亲共聚物载药微球相比,保持了40%以上的高载药量及90%以上的包封率,但平均粒径大大减小,只有300 nm左右。其体外释放行为与载体材料的结构有关。可以通过设计药物载体的结构,来控制RAPA载药微球的释放速率,具有潜在的临床应用价值。
[1]LI Chuan,ZHANG Jia,ZU Yujiao,etal.Biocompatible and biodegradable nanoparticles for enhancement of anti-cancer activities of phytochemicals[J].Chinese Journal of Natural Medicines,2015,13(9):641-652.
[2]KIM J,WILSON D R,ZAMBONI C G,etal.Targeted polymeric nanoparticles for cancer gene therapy[J].Journal of Drug Targeting,2015,23(7-8):627-641.
[3]商宏华,申有青.血清白蛋白纳米药物载体的制备及应用[J].功能高分子学报,2013,26(3):317-324.
[4]娄芳慧,袁金芳,高青雨.Ch-PCL-b-PVP生物可降解胶束的制备及其对布洛芬的控制释放[J].功能高分子学报,2013,26(4):410-416.
[5]ELSABAHY M,WOOLEY K L.Design of polymeric nanoparticles for biomedical delivery applications[J].Chemical Society Reviews,2012,41(7):2545-2561.
[6]HAN Hwa Seung,LEE Jungmin,KIM Hyun Ryoung,etal.Robust PEGylated hyaluronic acid nanoparticles as the carrier of doxorubicin:Mineralization and its effect on tumor targetability in vivo[J].Journal of Controlled Release,2013,168(2):105-114.
[7]李晨晨,龚飞荣,程树军,等.姜黄素缓释胶束的制备、表征及其抗细胞毒类药物的多药耐药性评价[J].华东理工大学学报(自然科学版),2014,40(5):562-567.
[8]WANG Jian,CHENG Shujun,Gong Feirong,etal.Synthesis and study of biomaterials of modified poly(ethylene glyco1) with dendrimers[J].New Chemical Materials,2009,37(9):58-60.
[9]谢威,龚飞荣,江琳,等.树枝状聚L-丙交酯-dendron-聚乙二醇-dendron-聚L-丙交酯的自组装[J].华东理工大学学报(自然科学版),2010,36(4):529-534.
[10]江琳,龚飞荣,范霄宇,等.雷帕霉素缓释胶束的制备及其释放行为[J].华东理工大学学报(自然科学版),2012,38(1):23-27.
[11]郭睿,陈明宇,范霄宇,等.生物可降解哑铃状高分子共聚物替莫唑胺载药微球的制备与表征[J].华东理工大学学报(自然科学版),2014,40(5):555-561.
[12]惠志倩,郭睿,龚飞荣,等.线性-树枝状两亲聚合物及其胶束的制备和聚集行为[J].华东理工大学学报(自然科学版),2016,42(6):800-807.
[13]FREDENBERGA S,WAHLGRENB M,RESLOWC M,etal.The mechanisms of drug release in poly(lactic-co-glycolic acid)-based drug delivery systems:A review[J].International Journal of Pharmaceutics,2011,415(1-2) 34-52.
[14]WU Yan,WANG Tiewei,LI Mingjun,etal.Hyperbranched poly(amine-ester)-poly(ε-caprolactone) copolymer and their nanoparticles as camptothecin delivery system[J].Journal of Polymer Research,2011,18(5):1147-1158.
[15]GALLGHER K M,CORRIGAN O I.Mechanistic aspects of the release of levamisole hydrochloride from biodegradable polymers[J].Journal of Controlled Release,2000,69(2):261-72.
[16]BALCERZAK J,MUCHA M.Analysis of model drug release kinetics from complex matrices of polylactide-chitosan[J].Progress on Chemistry and Application of Chitin and Its Derivatives,2010,15:117-125.
Preparation,Characterization and Release Behavior of Drug-Loaded Microparticles by Linear-Dendritic Diblock Copolymer
YANG Li-ying1, GUO rui2, RONG Zong-ming1
(1.School of Chemisty and Molecular Engineering,East China University of Science and Technology, Shanghai 200237,China;2 BASF Shanghai Coatings Co. Ltd,Shanghai 201108,China)
The rapamycin-loaded spherical microparticle based on biodegradable linear-dendritic diblock copolymer is prepared by dialysis method.Scanning electronic microscope(SEM),dynamic light scattering(DLS) and UV spectrophotometer were used to investigate morphology,size andinvitrorelease behavior of these particles.The results showed that the drug content and encapsulation efficiency of drug-loaded microparticles prepared by diblock copolymer,as well as those prepared by dumbbell-shaped triblock copolymer,could be more than 40% and 90%,respectively.Meanwhile,the mean size of those microparticles reduced significantly and it showed an obvious sustained release as well.
linear-dendritic diblock copolymer; biodegradable; drug-loaded microparticles; druginvitrorelease; rapamycin
1006-3080(2017)01-0050-06
10.14135/j.cnki.1006-3080.2017.01.008
2016-04-27
杨李影(1989-),女,安徽阜阳人,硕士生,研究方向为界面与胶体化学。E-mail:liyingyang2014@126.com
戎宗明,E-mail:rongzm@ecust.edu.cn
O631;R318.08;R944.5
A
——雷帕霉素

