超声提取–离子色谱法测定土壤易溶盐中的氯离子和硫酸根离子
段媛媛,贾亮亮
(河北省地矿局水文工程地质勘查院,石家庄 050021)
超声提取–离子色谱法测定土壤易溶盐中的氯离子和硫酸根离子
段媛媛,贾亮亮
(河北省地矿局水文工程地质勘查院,石家庄 050021)
采用超声提取的方式,以离子色谱法测定土壤易溶盐中的氯离子和硫酸根离子。对实验条件进行了优化,色谱柱为NJ–SA–4A柱 (250 mm×2 mm),保护柱为SI–92G柱(50 mm×4 mm),淋洗液为1.8 mmol/L Na2CO3–1.7 mmol/L NaHCO3,流量为1.0 mL/min;在40℃下,对土壤样品提取10 min。Cl–和SO42–在检测范围内均线性良好,线性相关系数为0.999 8,加标回收率分别为95.0%~99.0%,96.0%~101.0%,测定结果的相对标准偏差分别为1.4%,1.0%(n=4)。与传统的方法相比,该法试剂用量少,操作简单,可用于土壤易溶盐样品的测定。
超声波提取;土壤;氯离子;硫酸根离子;离子色谱法
土壤中的腐蚀性成分会对建筑物的结构及地基产生侵袭,如土壤中的硫酸根离子、氯离子等遇水溶解,达到一定浓度就可能腐蚀混凝土、钢筋等[1–4],对建筑物造成损害。GB/T 50123–1999《 土工试验方法标准》中规定硫酸根的测定采用EDTA络合滴定法或比浊法,但该方法步骤繁琐,且试剂用量大,分析速度慢[5]。硝酸银容量法测定氯根时,所产生的铬酸银能溶于酸中,在pH低于6.6时不能直接用测定氯化物,也不能在极强的碱性反应中进行,因此测定前需调节pH值,操作步骤繁琐。超声波提取法处理样品具有简单、快速、安全等优点,在中药材和各种动、植物中得到了广泛应用[6–9],而用于土壤易溶盐样品的处理未见报道;离子色谱法操作简便,可使多种离子同时分离且快速精确测定。因此笔者采用超声波提取样品,以离子色谱法测定土壤易溶盐浸提液中硫酸根离子和氯离子的含量,提高了工作效率,检测结果准确可靠[10–16]。
1 实验部分
1.1 主要仪器与试剂
离子色谱仪:IC6000型,安徽皖仪科技股份有限公司;
超声波清洗器:KQ–700DE型,昆山市超声仪器有限公司;
高速离心机:TDZ5–WS型,湘仪离心机仪器有限公司;
电子分析天平:MP128型,天津泰斯特仪器有限公司;
SO42–,Cl–标准储备液:1 000 mg/L;
碳酸氢钠、碳酸钠:优级纯,天津市永大化学试剂开发中心;
实验用水为无CO2的去离子蒸馏水。
1.2 色谱条件
色谱柱:NJ–SA–4A柱(250 mm×2 mm,中国农业科学研究院植物保护研究所);保护柱:SI–92G柱(50 mm×4 mm,昭和电工科学仪器有限公司);柱温:30℃;淋洗液:1.8 mmol/L碳酸钠–1.7 mmol/L碳酸氢钠,流量为1.0 mL/min;进样体积:100 µL。
1.3 样品制备
将采集的样品自然风干,风干过程中剔除土壤中的植物残根、石块、锰铁及钙质结核。样品风干后用2 mm孔径的筛子过筛,将筛下样品进行研磨备用。
称取2 mm筛下的风干试样50 g,准确至0.01 g。置于广口瓶中,按水土比5∶1加入纯水,搅匀,放入超声波清洗机中。在水温40℃、功率700 W下,超声10 min后,取出,摇匀,置于离心机高速离心分离。所得的透明滤液即为土壤浸出液,将其贮于细口瓶中,待测。测试前,浸出液用0.45 µm膜过滤,以免堵塞进样系统。
2 结果与讨论
2.1 实验用水
因为空气中的二氧化碳分压大小以及蒸馏水中溶解的二氧化碳均会影响碳酸钙和碳酸镁的溶解度,相应地影响浸出液的盐分数量,所以实验用水必须是无二氧化碳的去离子蒸馏水。
王世君身为鸡东县公路管理站工程师兼农村公路路网改造工程建设指挥部总工程师,自参加工作以来,便一直从事公路与桥梁建设、养护与管理工作。他刻苦钻研业务知识,兢兢业业、务实创新,所负责的各项工作都取得了长足的发展。
2.2 水土比例
用水浸提土壤易溶盐时,应力求将易溶盐完全溶解出来,同时又需尽可能使难溶盐(如碳酸钙)和中溶盐(如硫酸钙)不溶解或少溶解,并避免溶出的离子与土壤胶粒吸附的离子发生交换反应,因此应选择合适的水土比例。由于各种盐类的溶解度不同,故可控制水土比例将易溶盐与中溶盐及难溶盐分离。加水量小的水土比例(如1∶1,2.5∶1),操作困难,不适用于粘土;加水量大的水土比例(如10∶1,20∶1),又易导致溶盐总量偏高。在同一水土比例条件下,浸提时间越长,中溶盐和难溶盐被浸出的可能性愈大,土粒与水溶液之间的离子交换反应亦愈完全,由此产生的误差也愈大。因此必须统一规定制备土壤浸出液时的水土比例和浸提时间,才能使分析结果具有可比性。实验选择行业中普遍选用的5∶1的水土比例。
2.3 淋洗液浓度
用不同浓度的淋洗液对同一Cl–,标准混合离子溶液进行淋洗试验。当淋洗液浓度增大时,色谱峰保留时间减小,总检测时间减小,但分离效果不佳,且峰面积减小;当淋洗液浓度减小时,色谱峰保留时间增长,总检测时间延长。综合考虑选择1.8 mmol/L Na2CO3–1.7 mmol/L NaHCO3为淋洗液,此时色谱峰形最佳,且分离时间适中,样品中其它离子不干扰Cl–,SO42–的测定。
2.4 超声温度
超声温度过高或过低都会对试样分解造成影响,从而导致分析结果偏高或偏低。在超声时间10 min条件下,分别采用30,40,50℃下对土壤易溶盐标准物质GBW(E) 070032样品行超声提取,然后进行测定,结果见表1。

表1 不同超声温度下标准物质的测定结果 mg/kg
2.5 超声时间
超声温度为40℃条件下,选择超声时间5,10,15,20 min,分别对土壤易溶盐标准物质GBW(E) 070032进行超声提取后,测定,结果见表2。
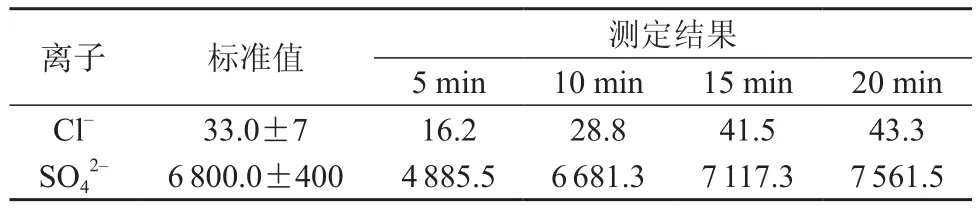
表2 不同超声时间标准物质的测定结果 mg/kg
由表2可以看出,超声温度为40℃时,土壤中硫酸根离子和氯离子的测定值随着超声时间增加而增大,当超声提取10~15 min时,测定值在标准值的范围之内。为了提高工作效率,实验选定超声时间为10 min。
2.6 标准工作曲线及检出限
分别吸取SO42–,Cl–标准储备液配制成系列混合标准工作溶液,SO42–的质量浓度分别为0.0,2.0,5.0,10.0,15.0,20.0,25.0 mg/L在1.2色谱条件下分别测定,以质量浓度为横坐标,峰面积为纵坐标进行线性回归,得到两种阴离子的线性回归方程和相关系数。平行测定10次空白样品,以3倍信噪比计算方法的检出限。线性方程、相关系数和检出限见表3。

表3 线性方程、相关系数和检出限
2.7 精密度试验
将处理好的土壤提取液样品进行5次重复测定,计算测定结果的相对标准偏差,结果见表4。由表4可知,Cl–和SO42–测定结果的相对准偏差分别为1.4%和1.0%,表明该方法的精密度良好。

表4 精密度试验结果
2.8 回收试验
取处理好的土壤滤液,加入一定量的标准离子溶液,进行回收试验,结果见表5。由表5可知,Cl–和SO42–的回收率分别为95.0%~99.0%,96.0%~101.0%,说明该方法具有较高的准确度。土壤样品色谱图与加标样品色谱图见图1和图2。
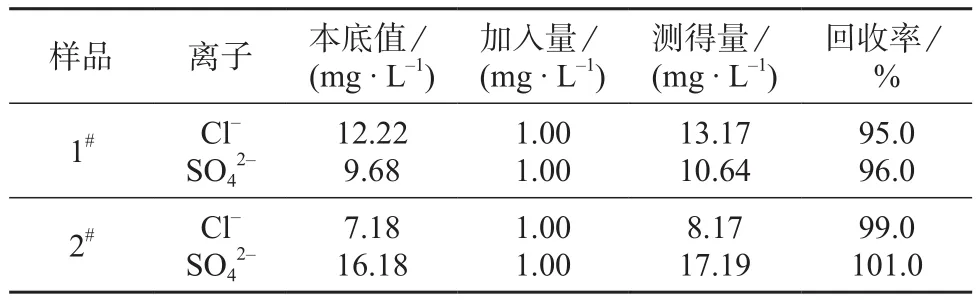
表5 样品加标回收试验结果

图1 土壤样品色谱图

图2 加标样品色谱图
2.9 样品测定
分别称取9个不同地点的土壤样品,按1.3方法处理后,在1.2节色谱条件下测定,结果见表6。由表6可知,XPQK26A样品Cl–含量在400~750 mg/kg之间,其余样品Cl–含量均小于400 mg/kg。根据GB50021–2001《 岩土工程勘察规范》,XPQK26A综合评价为弱腐蚀,其余样品综合评价为微腐蚀。
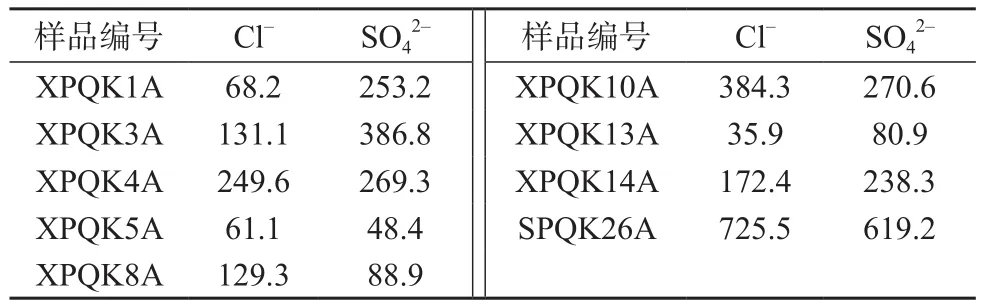
表6 土壤样品中氯根和硫酸根的含量 mg/kg
3 结语
用超声波对土壤易溶盐样品进行预处理,采用离子色谱法测定浸提液中氯根和硫酸根的方法,安全性好、试剂消耗少,灵敏度高,简便快速,在实践中值得参考和应用。
[1] 齐占虎.测定土壤中易溶盐时的注意事项与结果综合评估[J].河北化工,2009,32(12): 69–70.
[2] 朱朝娟,周光明,余娜,等.离子色谱法同时快速测土壤中的F–,Cl–,NO2–,Br–,NO3–,HPO42–,SO42–[J].西南大学学报:自然
科学版,2010,32(9): 54–58.
[3] 历敏宪,龚秋霖.离子色谱法测定电厂炉管垢样中的Cl–、[J].化学分析计量,2002,11(2): 24–25.
[4] 堵小东,戴玄吏.离子色谱法测定土壤样品中的氯离子研究[J].现代科学仪器,2005,24(4): 56–57.
[5] 中华人民共和国水利部. 土工试验方法标准[M].北京:化学工业中国计划出版社,1999.
[6] 张树香.离子色谱测定新疆土壤中C1–,NO3–和SO42–[J].现代科学仪器,2004(5): 60–61.
[7] 顾佳丽,赵刚,徐娜.超声波提取–原子吸收光谱测定油田中土壤中重金属的含量[J].化学研究与应用,2012,24(11): 1 706–1 710.
[8] 查立新,马玲,刘文长,等.振荡提取和超声提取用于土壤样品中元素形态分析[J].岩矿测试,2011,30(4): 393–399.
[9] 杨华,唐邈.超声提取–电感耦合等离子体质谱法分析土壤中重金属化学形态[J].环境监测管理与技术,2015,27(4): 51–53.
[10] 牟世芬,刘克纳,丁晓静.离子色谱方法及应用[M]. 2版.北京:化学工业出版社,2005.
[11] 杨春霞,李彩虹,赵银宝.离子色谱法测定土壤中无机阴阳离子含量[J].理化检验:化学分册,2012(10): 1 199–1 202.
[12] 周晓红,戚荣平,孟琪,等.快速溶剂萃取–离子色谱法测定土壤中的6种阴离子[J].浙江预防医学,2015(7): 754–756.
[13] 徐秀丽,刘文全,徐兴永,等.离子色谱法测定土壤中的Cl–和SO42–[J].化学分析计量,2014(2): 20–22.
[14] 赵春燕.离子色谱法测定东下冯遗址土壤中的无机阴离子[J].中国无机分析化学,2012(3): 22–23.
[15] 张学慧.离子色谱法测定水样中常见阴、阳离子的方法[J].赤峰学院学报:自然科学版,2013(12): 19–20.
[16] 李新峥,王广印.离子色谱法测定新乡市大棚菜田土壤中的阴离子[J].农业科学,2015,5(1): 44–49.
Determination of Chloride and Sulfate Dissolvable Salt in Soil Sample by Ultrasound–Assisted Extraction Ion Chromatography
Duan Yuanyuan,Jia Liangliang
(The Institute of Hydrology and Engineering Geological Prospecting Hebei Geological Mineral Bureau, Shijiazhuang 050021,China)
The method for determination of chloride and sulfate in the soil was developed by ultrasound-assisted extraction and ion chromatography,the sample was extracted by ultrasonic extraction method. The experiment conditions were optimized. The chromatographic column was NJ–SA–4A column (250 mm×2 mm), protective column was SI–92G column (50 mm×4 mm). The mobile phase was 1.8 mmol/L Na2CO3–1.7 mmol/L NaHCO3at fow rate of 1.0 mL/min. The linearity of chloride, sulfate was fne in the detection range, the corelation coeffcient was 0.999 8. The addition recoveries of chloride and sulfate were 95.0%–99.0%,96.0%–101.0%, and relative standar deviation of detection results were 1.4%,1.0%(n=4), resipectively. Compared with traditional method, this method was in low reagent consumption, simple in operation and it is suitable for the determination of dissolvable salt in soil samples.
ultrasonic extraction; soil; chloride; sulfate; ion chromatography
O657.7
:A
:1008–6145(2017)01–0079–03
10.3969/j.issn.1008–6145.2017.01.020
联系人:贾亮亮;E-mail: jialiang0316@163.com
2016–10–06

