鞣酸功能化石墨烯修饰电极上芦丁的电化学行为及灵敏检测
李惠茗,张惠怡,2,赖祥文,2,梁 立,2,刘坤平,2*,苟小军,2*
(1.成都大学 药学与生物工程学院,四川 成都 610106;2.成都大学 药食同源植物资源开发四川省高校重点实验室,四川 成都 610106)
鞣酸功能化石墨烯修饰电极上芦丁的电化学行为及灵敏检测
李惠茗1,张惠怡1,2,赖祥文1,2,梁 立1,2,刘坤平1,2*,苟小军1,2*
(1.成都大学 药学与生物工程学院,四川 成都 610106;2.成都大学 药食同源植物资源开发四川省高校重点实验室,四川 成都 610106)
以双功能化试剂鞣酸一步还原法制备了鞣酸功能化的石墨烯纳米材料(TA-G)。鞣酸不仅起到还原剂的作用,还用作功能化试剂包裹石墨烯纳米片。将所制备的TA-G用于构建芦丁电化学传感器,可实现电化学信号放大并获得较好的检测灵敏度。电极反应动力学结果表明,芦丁在该修饰电极的电化学行为受表面准可逆过程控制。优化后的实验条件为pH 3.0,TA-G(1.0 μg/mL)的电极修饰量为8 μL,扫速为100 mV/s,富集圈数为100圈。在优化条件下,芦丁的还原峰电流在1.0×10-8~1.0×10-5mol·L-1浓度范围内呈现良好的线性关系,检出限(S/N=3)为6.0×10-9mol/L。该传感器具有较高的稳定性、选择性和特异性,可实现实际样品中芦丁的灵敏检测,从而拓宽了石墨烯的应用领域并为药物的快速检测提供了新思路。
鞣酸石墨烯;电化学;修饰电极;芦丁;灵敏检测
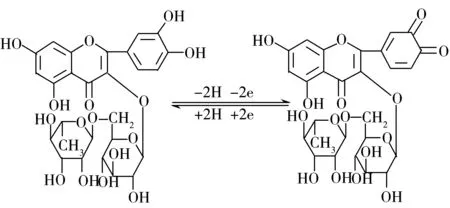
图1 芦丁在电极上的电极反应Fig.1 The electrode-reaction of rutin
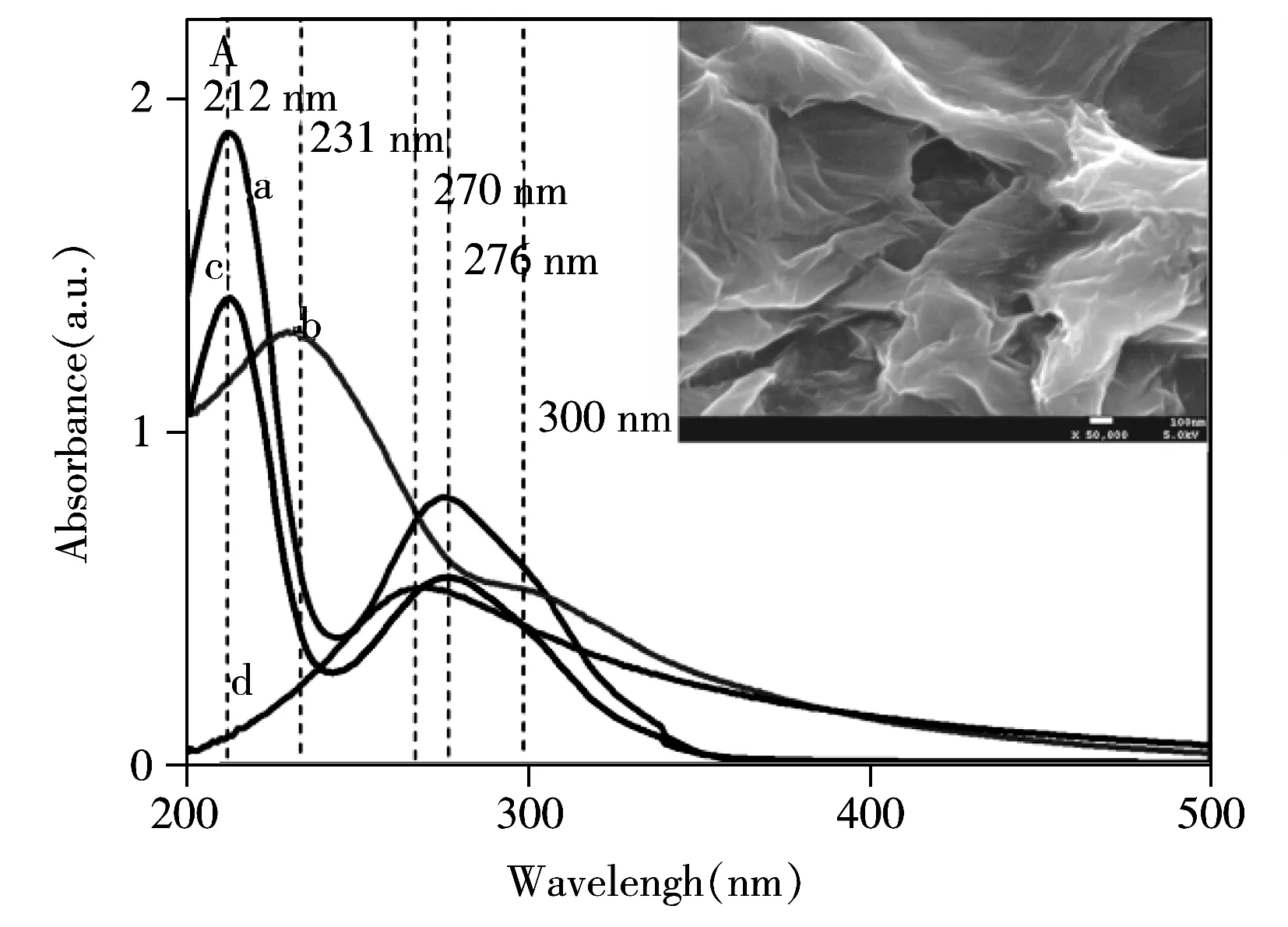
芦丁是一种分布广泛的类黄酮化合物,具有较好的抗氧化性,能降低毛细血管通透性,在心血管疾病的防治中被广泛用作临床治疗药物[1],其快速灵敏检测受到了极大的关注[2]。目前,芦丁的检测方法主要有分光光度法、毛细管电泳法、高效液相色谱法、化学发光法和电化学法[3-7]等。韦湫阳等[4]采用胶束毛细管电泳法测定了中药复方制剂消栓通络片中芦丁的含量,但检出限仅为0.3 mg/L,无法获得较高的灵敏度。陈君等[5]采用高效液相色谱法测定了白花杜鹃叶中的芦丁含量,其检出限虽可达0.006 6 mg/L,但需要复杂的样品前处理且分析时间较长。电化学方法由于具有灵敏度高、方便、快速、成本低等优点,在药物检测领域获得了广泛的关注和应用[8]。芦丁分子有4个酚羟基,相邻的两个酚羟基具有电化学活性,可在电极上发生电极反应(如图1所示),因此通过电化学方法可实现芦丁的灵敏快速检测[9]。为提高检测灵敏度,随着新型纳米材料的发展及其优异的电学性质,多种纳米材料如纳米金[10]、碳纳米管[11]等被引入电化学检测平台。纳米材料独特的物理化学性质,可改善药物与电极间的电子传递效率,从而获得较好的分析性能。
石墨烯是2004年被发现的新型碳基二维纳米材料[12],具有比表面积大、导电性高等优良性质,已在纳米电子器件[13]、传感器[14]及复合物材料[15]等方面得到了广泛应用。但由于纯石墨烯表面官能团较少,不利于进一步应用,因此各种共价和非共价的功能化方法被用于功能化石墨烯的制备。鞣酸是一种高分子量的聚酚类化合物,其结构中包含的儿茶酚和焦没食子酚结构具有一定的还原能力,因此可用于还原氧化石墨烯以制备石墨烯。同时鞣酸结构中包含的大量苯环结构可与石墨烯形成π-π共轭结构以稳定石墨烯。本研究为实现灵敏的芦丁电化学检测,首先以鞣酸为还原剂和保护剂一步法制备了鞣酸功能化的石墨烯(TA-G),然后通过层层组装技术将石墨烯组装到电极表面构建了芦丁电化学传感器,所制备的TA-G一方面具有高的导电性,可加速芦丁在电极表面电子的传递速度。另一方面,TA-G具有大的比表面积,同时,其功能化的鞣酸可与芦丁形成氢键,从而进一步提高芦丁在电极表面的负载量。因此,可实现芦丁电化学传感器信号的放大从而提高芦丁检测的灵敏度。
1 实验部分
1.1 试剂与仪器
芦丁、鳞片石墨购自Sigma-Aldrich公司。氨水和水合肼(80%)购自成都长征试剂有限公司。其它所用化学试剂均为化学纯。芦丁储备液(1.0×10-3mol·L-1)使用甲醇配制,于4 ℃下暗处保存备用。循环伏安测试于CHI 832C电化学工作站(上海辰华)上进行。采用传统的三电极电化学测定体系,工作电极为玻碳电极(GCE)或鞣酸功能化石墨烯(TA-G)修饰的GCE,参比电极为饱和甘汞电极(SCE),对电极为铂丝电极。溶液pH值均采用数字pH计(PHS-3C)测量。实验所用超纯水均取自Milli-Q纯水系统。场发射扫描电子显微镜(FESEM)在Kevex JSM-6701上进行。原子力显微镜(AFM)实验在FP-3D-BIO上以云母片为基底进行测量。
1.2 鞣酸功能化石墨烯的制备
鞣酸功能化的石墨烯采用本课题组之前的方法进行制备[16]。其制备过程简述如下:采用优化的Hummers法以石墨粉为原料制备石墨氧化物(GO)[17]。然后在超声辅助下对GO进行2 h的水相剥离,3 000 r/min转速下离心30 min除去未剥离的GO,即得剥离的氧化石墨烯纳米片(EGO)分散液。将4.0 g鞣酸(TA)加入到100 mL均匀的EGO分散液中,搅拌30 min保证鞣酸完全溶解,然后升温至95 ℃下反应9 h。经过多步的过滤洗涤得到黑色的鞣酸功能化石墨烯(TA-G)固体,于烘箱中烘干备用。同时,不加鞣酸以水合肼为还原剂制备纯石墨烯进行对比实验。
1.3 修饰电极制备
GCE先分别用1.0,0.3,0.05 μm的Al2O3抛光粉进行抛光处理。然后依次用1∶1 HNO3、丙酮和超纯水各超声清洗3~5 min,以得到新鲜干净的电极表面并N2吹干。准确称取1.0 mg上述所制备的TA-G于1.0 mL甲醇中,超声20 min得黑色均匀的TA-G分散液。吸取5 μL TA-G分散液滴涂于干净的GCE表面,并置于干燥器中室温下自然晾干,即得TA-G修饰电极(TA-G/GCE)。
1.4 芦丁测定及实际样品分析
在优化条件下,将制备的修饰电极浸入含有芦丁的PBS缓冲液中(0.1 mol·L-1,pH 3.0)。搅拌下采用循环伏安法(CV)扫描100圈以进行样品富集。然后室温下于0.1~0.8 V电位窗口采用差示脉冲伏安法(DPV)进行测量。测量后的电极浸入PBS缓冲溶液中(0.1 mol·L-1,pH 7.0),CV连续扫描15圈即可实现电极再生。取商品化的芦丁药片(20 mg/片)1片,研磨后加入20 mL甲醇中超声提取20 min,过滤,滤饼用10 mL甲醇冲洗3次,合并各次滤液并用甲醇定容至100 mL备用。
2 结果与讨论
2.1 材料的表征
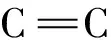
TA-G(c)的FT-IR图(B)
Fig.2 UV-Vis spectra(A) of TA(a),EGO(b),TA-G(c) and pure graphene(d),and FT-IR
spectra(B) of EGO(a),pure graphene(b) and TA-G(c)
insert:SEM of TA-G

采用扫描电子显微镜(SEM)和原子力显微镜(AFM)对TA-G的形貌进行表征。如图2A插图所示,TA-G的SEM照片显示TA-G呈半透明褶皱的轻纱状不规则片状结构。AFM可同时提供样品形态和厚度的直观表征。如图3的AFM图所示,EGO(A)表现出不规则的片状结构,厚度分析(Cross-section analyses)表明EGO的厚度约为1.0 nm。还原后的TA-G(B)同样表现出不规则的片状结构,但TA-G的厚度增加到约为3.0 nm。这也表明鞣酸已成功的功能化到石墨烯表面。
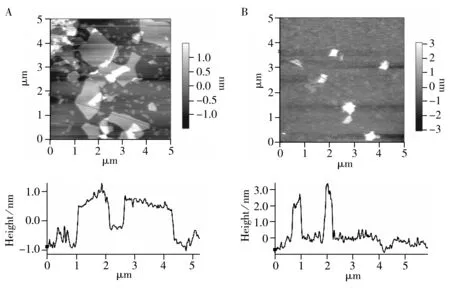
图3 EGO(A)与TA-G(B)的AFM图Fig.3 AFM images of EGO(A) and TA-G(B)
2.2 修饰电极上芦丁的电化学行为
为对比不同电极的电化学性能,以循环伏安法(CV)测试了不同电极上芦丁的电化学行为。如图4A所示,在裸GCE电极上(曲线a),无芦丁的缓冲溶液中,未观察到明显的氧化还原峰。加入芦丁后,芦丁在裸GCE电极(曲线b)上于0.464 V和0.482 V处显示1对强度相对较小的氧化还原峰。然而,对于TA-G修饰的GCE电极(曲线c),芦丁在0.452 V和0.543 V处表现出1对稳定的准可逆氧化还原峰,峰峰分离度为91 mV。这表明芦丁在TA-G/GCE修饰电极表面经历了快速的电子转移过程。与裸GCE电极相比,TA-G/GCE修饰电极上芦丁的电流信号获得了极大的增强。其原因可能是由于TA-G的高导电性以及对芦丁的富集作用,此外,TA-G纳米材料的催化性也是重要因素。多因素的联合作用导致了信号的双重增强。
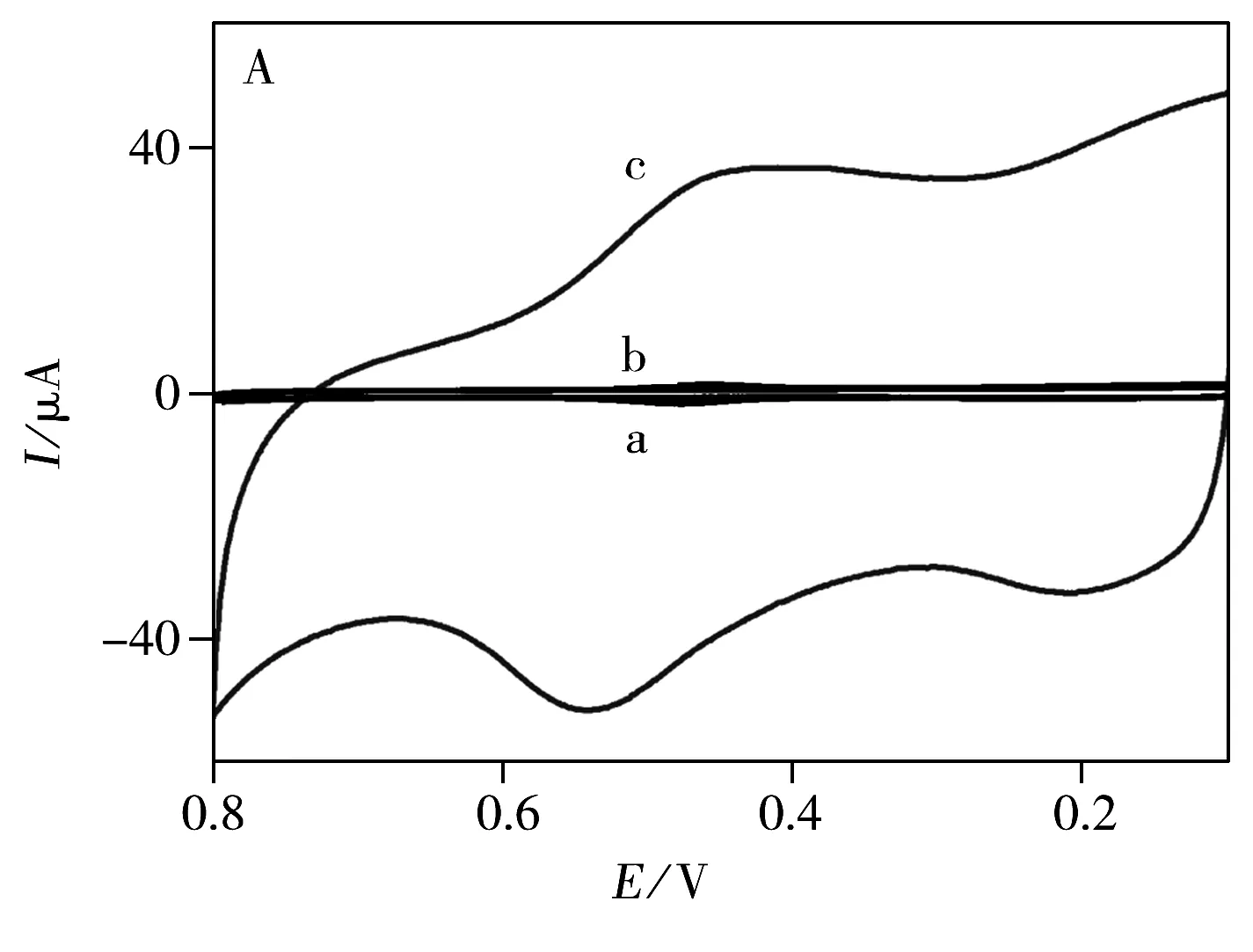
Fig.4 CVs of GCE(a) without rutin in 0.1 mol·L-1pH 3.0 PBS,and bare GCE(b),TA-G/GCE(c) with 1.0×10-6mol·L-1rutin (A) and CVs of TA-G/GCE with the change of scan rate(B)
进一步通过CV法考察了电位扫描速率(v)对芦丁在该修饰电极上电化学信号的影响。如图4B所示,芦丁的氧化还原峰电流值及峰电位差值随扫描速率的增加而增加。当扫描速率从10 mV·s-1增至1 000 mV·s-1时,阳极和阴极电流值均与扫描速率呈线性关系(图5A)。这表明芦丁在TA-G/GCE修饰电极上表现出一个受表面控制的准可逆电化学反应过程。将阳极(Epa)和阴极(Epc)峰电位值与扫描速率的对数(lgv)做图,由图5B可以看出,在高扫描速率范围,Epa和Epc峰电位值均与lgv呈线性关系,其线性方程分别为:Epa=0.542 6+0.069 2lgv;Epc=0.418 6-0.057 4lgv。相关系数分别为0.995 0和0.991 6。根据Laviron模型[20],计算可得电子转移数(n)、电子转移系数(α)及表观速率常数(ks)分别为2,0.56和4.9 s-1。这表明芦丁在该修饰电极上经历了一个快速的电子转移电化学反应。
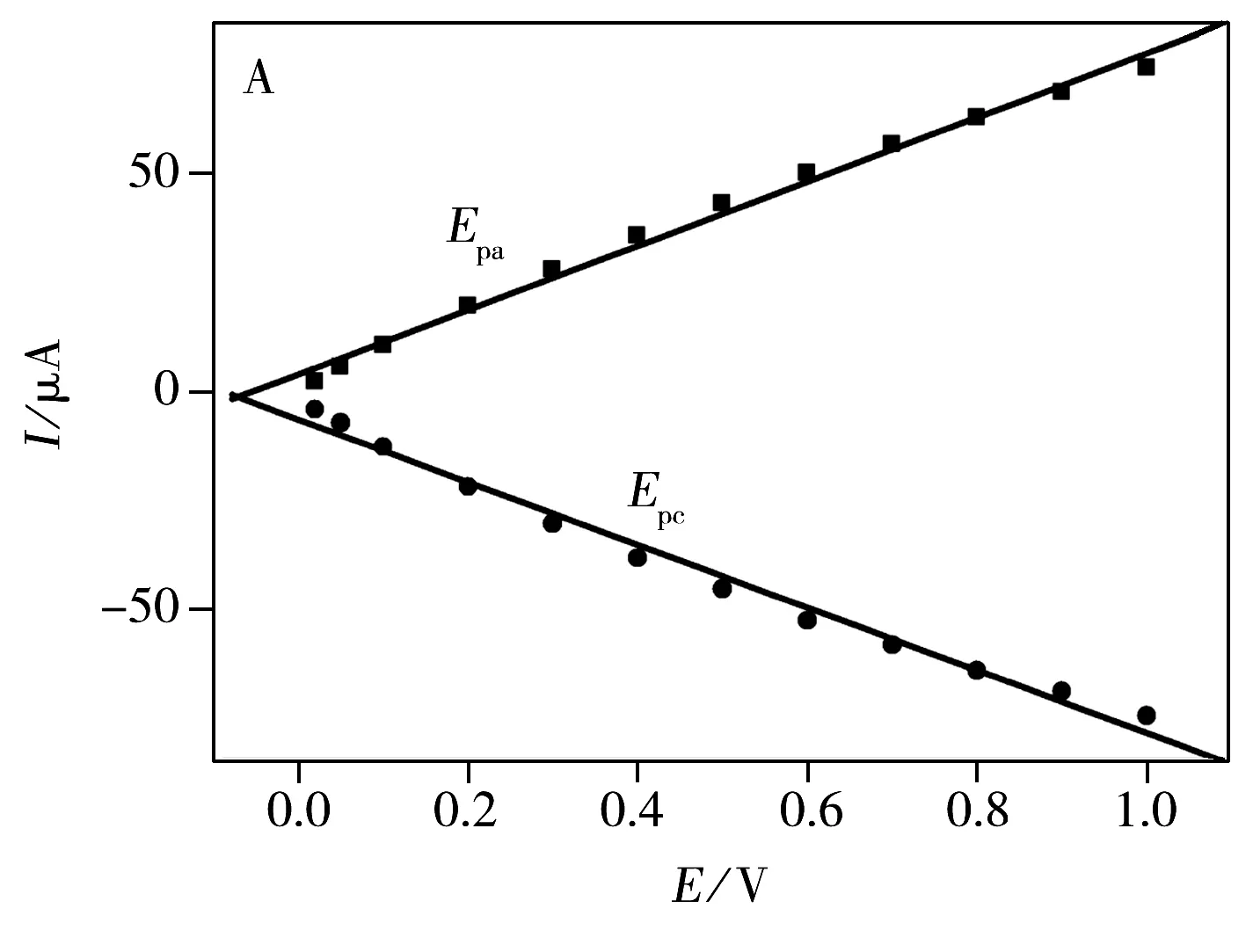
Fig.5 Linear plots of anode and cathode peak currentvs.scan rate(A)and plots of anodic and cathodic potentials against the logarithmic scan rate of TA-G/GCE(B)
2.3 实验条件的优化
对测定芦丁溶液的pH值进行优化,结果如图6A所示。随着测定体系pH值的增大,芦丁CV图中的还原和氧化电流均逐渐增大,pH 3.0时达到最大值,然后又逐步下降。因此,确定最优pH值为3.0。同时,芦丁CV图中的氧化还原峰电位值随pH值的增大而逐渐减小,表明芦丁的电化学氧化还原反应中有H+质子参与反应。将芦丁的还原峰电位对pH值作图,如图6B所示,在pH 2.2~6.0范围内pH值与电位呈线性关系,其线性方程为:Epa=0.713 7-0.068 5×pH,相关系数(r)为0.997 7,斜率为68.5 mV,接近理论值59 mV。这表明芦丁电化学反应中参与反应的电子数等于质子数[21]。结合Laviron模型的计算结果,说明在TA-G/GCE修饰电极上芦丁表现为两质子两电子的电化学反应。此结果与文献结果一致[22]。
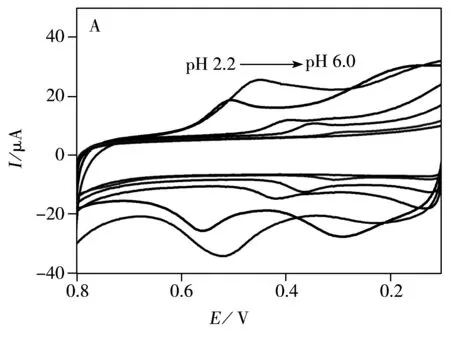
Fig.6 Effect of pH values for CVs of rutin at TA-G/GCE(A)and plot of equilibrium potentialvs.pH value(B)
为在电极上获得最大的芦丁富集量以提高信号强度,对芦丁的CV富集圈数进行了优化(如图7A)。结果表明,随富集圈数的增大,芦丁的还原峰电流值(I)逐渐增大,在100圈时达到最大值并保持稳定。这表明在1.0×10-6mol·L-1浓度下,富集100圈时,芦丁在TA-G/GCE修饰电极的信号达到最大值。因此,选定100圈为优化的芦丁CV富集圈数。
修饰电极上修饰的TA-G分散液体积会影响修饰膜的厚度,从而影响最终测定的电流信号强度。因此对膜厚进行了优化,结果见图7B。由图可知,随着TA-G体积的增加,电流值逐渐增大,在8 μL时达到最大值,然后逐步降低。最终选择TA-G分散液体积为8 μL。
2.4 芦丁检测
在上述优化条件下,采用差示脉冲伏安法(DPV)对不同浓度的芦丁溶液进行测定(如图8)。结果显示,DPV电流值(I)与芦丁浓度(c,mol·L-1)在1.0×10-8~1.0×10-5mol·L-1范围内呈良好的线性关系,其线性方程为I(μA)=0.250 9+2.887 1×cRutin,相关系数(r)为0.992 9,检出限(S/N=3)为6.0×10-9mol·L-1。
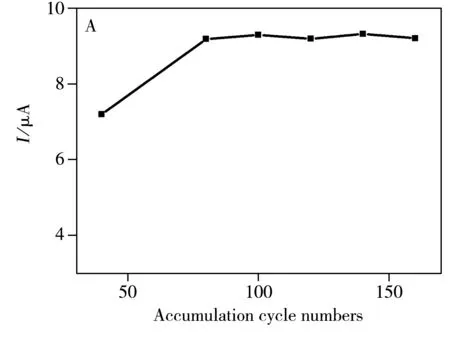
Fig.7 Effect of CV accumulation cycle numbers(A) and film thickness of TA-G/GCE(B) on peak current of 1.0×10-6mol·L-1rutin
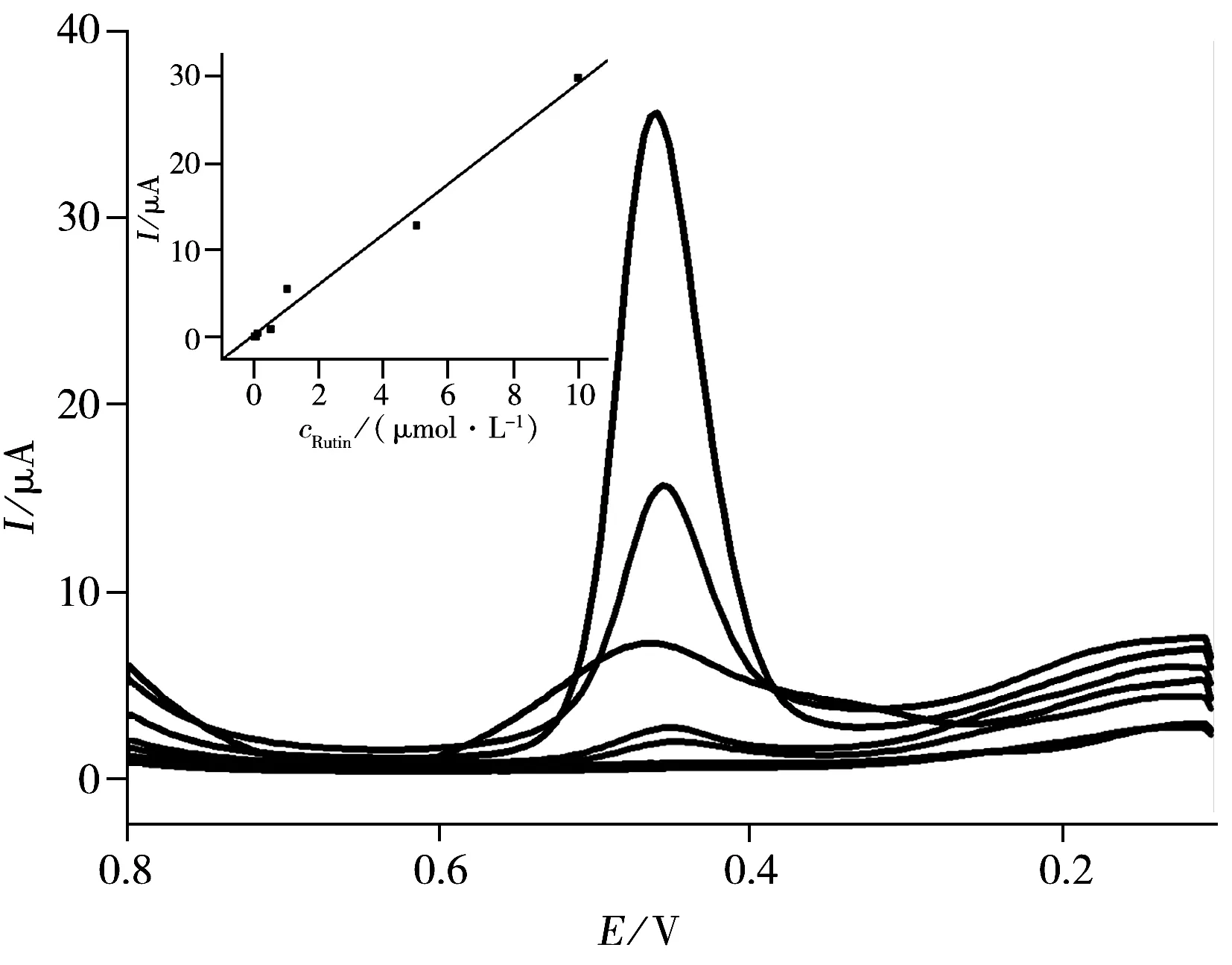
图8 不同浓度芦丁在TA-G/GCE电极上的DPV响应Fig.8 DPV curves of different rutin concentrations on TA-G/GCE rutin concentration(from low to high):1.0,5.0,10,50,100,500,1 000(×10-8 mol·L-1);bufffer:pH 3.0 0.1 mol·L-1 PBS;insert:linear curve of DPV current response for rutin concentration
Table 1 Determination of commercial rutin tablets
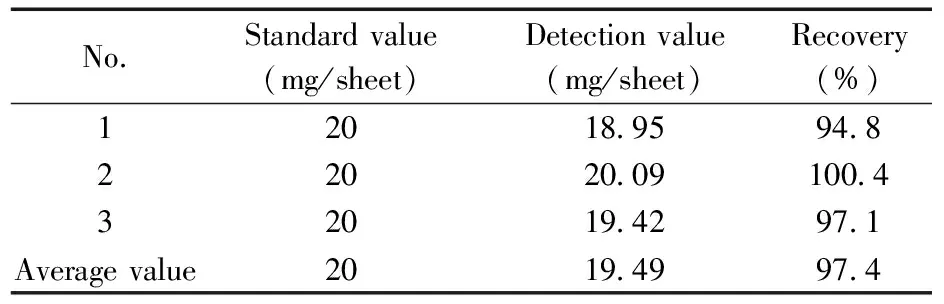
No.Standardvalue(mg/sheet)Detectionvalue(mg/sheet)Recovery(%)1201895948220200910043201942971Averagevalue201949974
2.5 稳定性与精密度
在优化条件下,用同一支修饰电极对同一芦丁溶液(1.0×10-6mol/L)进行6次平行测定,相对标准偏差(RSD)为3.9%;用6支修饰电极测定同一芦丁溶液,RSD为4.7%;将修饰电极在室温下放置2周后重新测定,RSD为4.9%。表明该修饰电极具有良好的稳定性和重复性。同时,考察了常见干扰物质如多巴胺(0.001 mol/L)、抗坏血酸(0.001 mol/L)及血红蛋白(0.001 mol/L)对芦丁测定的影响,结果表明在这3种共存干扰物存在的情况下,芦丁的回收率均可达到95%以上,表明这3种共存物不干扰对芦丁的测定。
2.6 实际样品分析
在优化测定条件下,采用本方法对芦丁药片提取液进行测定。由表1可见,该方法测得芦丁药片中芦丁含量的平均值为19.49 mg/片,与标称值(20 mg/片)接近,3次实验的回收率为94.8%~100.4%,这表明所构建的芦丁电化学传感器可实现实际样品中芦丁的灵敏测定。
3 结 论
本文以双功能化试剂鞣酸还原制备了鞣酸功能化的石墨烯(TA-G),并通过层层组装构建了基于TA-G的芦丁电化学传感器。利用该传感器可在较宽的线性范围内实现芦丁的快速、灵敏检测,并具有较低的检出限。同时,该传感器具有较高的稳定性、选择性和特异性,可实现实际样品中芦丁的灵敏检测。方法拓宽了石墨烯的应用领域并为药物快速检测提供了新思路。
[1] Liao J Q,Qu B D,Liu D,Zheng N Q.Ultrason.Sonochem.,2015,27:110-116.
[2] Yang S L,Li G,Wang G F,Zhao J H,Qiao Z H,Qu L B.Sens.ActuatorsB,2015,206:126-132.
[3] Gong A Q,Ping W H,Wang J,Zhu X S.Spectrochim.ActaA,2014,122:331-336.
[4] Wei Q Y,Zhu P C,Xue Y,Xu Y J.J.Instrum.Anal.(韦湫阳,朱平川,薛莹,徐远金.分析测试学报),2012,31(8):992-995.
[5] Chen J,Zhou G M,Yang Y G,Qin H Y,Dou W H.J.Instrum.Anal.(陈君,周光明,杨远高,秦红英,窦文虎.分析测试学报),2013,32(3):341-345.
[6] Song Z H,Hou S.Talanta,2002,57:59-67.
[7] Feng L B,Qi W,Song R X,He Z M.J.Instrum.Anal.(冯利彬,齐崴,苏荣欣,何志敏.分析测试学报),2014,33(9):1019-1025.
[8] Guo X L,Wang Q,Li J L,Cui J W,Zhou S,Hao S,Wu D M.Biosens.Bioelectron.,2015,64:594-596.
[9] Yang S L,Li G,Zhao J H,Zhu H M,Qu L B.J.Electroanal.Chem.,2014,717/718:225-230.
[10] Pang S N,Wu T L,Liang Y,Su L,Bai Y.J.Instrum.Anal.(庞书南,吴天良,梁毅,苏丽,白杨.分析测试学报),2014,33(12):1404-1409.
[11] Yu H,Jin J,Wang F,Huang L L,Qi G C.J.Instrum.Anal.(于浩,金君,王飞,黄玲玲,齐广才.分析测试学报),2014,33(5):572-577.
[12] Kim H,Abdala A A,Macosko C W.Macromolecules,2010,43:6515-6530.
[13] Yue W W,Jiang S Z,Xu S C,Ma Y,Bai C J.Sens.ActuatorsB,2015,214:204-210.
[14] Yu X W,Sheng K X,Chen J,Li C,Shi G Q.ActaChim.Sin.(于小雯,盛凯旋,陈骥,李春,石高全.化学学报),2014,72:319-332.
[15] Kuang D,Hu W B.J.Inorg.Mater.(匡达,胡文彬.无机材料学报),2013,28(3):235-246.
[16] Liu K P,Li H M,Wang Y M,Gou X J,Duan Y X.ColloidSurf.A,2015,477:35-41.
[17] Hummers W S,Offeman R E.J.Am.Chem.Soc.,1958,80:1339.
[18] Zhou Y,Bao Q L,Tang L A L,Zhong Y L,Loh K P.Chem.Mater.,2009,21:2950-2956.
[19] Shan C S,Yang H F,Han D X,Zhang Q X,Ivaska A,Niu L.Langmuir,2009,25:12030-12033.
[20] Laviron E.J.Electroanal.Chem.,1979,101:19-28.
[21] Zare H R,Sobhani Z,Mazloum-Ardakani M.Sens.ActuatorsB,2007,126:641-647.
[22] An J,Bi Y Y,Yang C X,Hu F D,Wang C M.J.Pharm.Anal.,2013,3(2):102-108.
Electrochemical Behavior and Sensitive Detection of Rutin on Tannic Acid Functionalized Graphene Modified Electrode
LI Hui-ming1,ZHANG Hui-yi1,2,LAI Xiang-wen1,2,LIANG Li1,2,LIU Kun-ping1,2*,GOU Xiao-jun1,2*
(1.School of Bioengineering,Chengdu University,Chengdu 610106,China;2.The Key Laboratory of Medicinal and Edible Plants Resources Exploitation of Higher Education Institutes of Sichuan Province,Chengdu University, Chengdu 610106,China)
In this study,tannic acid(TA) functionalized graphene nano sheets(TA-G) was facilely synthesized through a one-step green reduction method using tannic acid as dual function agent,in which tannic acid acted as not only a reduction reagent to reduce oxided graphene(EGO) but also a capping reagent to functionalize graphene.The as-prepared TA-G was used to construct a graphene based rutin electrochemical sensor,and the modified electrode had a high sensitivity for rutin detection.The results of electrode reaction kinetics of rutin on TA-G modified electeochemical sensor indicated that the electeochemical reaction of rutin on the modified electrode undergone a surface-controlled quasi-reversible electrochemical process.The optimal conditions were as follows:pH value:3.0,TA-G amount(1.0 μg/mL) on TA-G modified electrochemical sensor:8 μL,scan rate:100 mV/s,cycles of enrichment:100. Under the optimal conditions,the fabricated sensor displayed an excellent analytical performance for rutin detection,with a linear range of 1.0×10-8-1.0×10-5mol·L-1and a low detection limit of 6.0×10-9mol·L-1at 3σ.Meanwhile,the fabricated rutin electrochemical sensor also exhibited good selectivity,specificity and stability,and could be used for rutin detection in real samples.The proposed method broadened the application field of graphene and offered a new idea for rapid detection of drug.
tannic acid functionalized graphene;electrochemistry;modified electrode;rutin;sensitive detection
2015-07-05;
2015-08-15
四川省中医药管理局中医药科学技术研究专项(2014F002);四川省教育厅科研项目(15ZB0374);成都大学大学生创新性实验计划项目(CDU_CX_2015104)
10.3969/j.issn.1004-4957.2016.03.006
O657.1;TQ460.72
A
1004-4957(2016)03-0292-07
*通讯作者:苟小军,博士,教授,研究方向:药物分析,Tel:028-84616301,E-mail:26118008@qq.com 刘坤平,博士,副教授,研究方向:药物分析,Tel:028-84616301,E-mail:liukunping@cdu.edu.cn

