高效液相色谱法测定祛风止痛片中乌头碱的含量
曹稳根,翟科峰,段 红,董 增
宿州学院生物与食品工程学院,安徽宿州,234000
高效液相色谱法测定祛风止痛片中乌头碱的含量
曹稳根,翟科峰,段 红,董 增
宿州学院生物与食品工程学院,安徽宿州,234000
建立祛风止痛片中乌头碱的高效液相色谱测定方法。色谱柱为Skim-pack vp-ODS(4.6 mm×250 mm,5 μm)柱;流动相为甲醇-0.1%三乙胺(65∶35,v/v);流速0.8 mL/min;检测波长235 nm;柱温35℃。乌头碱在0.1504~0.3384 μg范围内峰面积与进样量有良好的线性关系(r=0.9991),平均回收率为98.62%,RSD为1.19%。本方法简便可行,准确可靠,重复性好,可用于祛风止痛片制剂的质量控制。
祛风止痛片;乌头碱;高效液相色谱法;甲醇-0.1%三乙胺
祛风止痛片为国家发明专利品种,也是国家中药保护品种,主要由老鹳草、槲寄生、续断、威灵仙、独活、制草乌和红花七味药复方组成,具有祛风止痛、舒筋活血、强壮筋骨等功效,临床用于治疗四肢麻木、腰膝疼痛、风寒湿痹等症,是治疗风湿、类风湿关节炎的理想药物,疗效确切[1-6]。制剂中制草乌辛、苦、热,有毒,具有祛风除湿、温经止痛的作用,用于风寒湿痹、关节疼痛、心腹冷痛、寒疝作痛等疾病的治疗,其中乌头碱既是其药效成分,又是毒性成分,使用不慎极易引起中毒[7-8]。为保证临床用药安全有效,控制祛风止痛片制剂质量,本文建立了祛风止痛片中乌头碱的高效液相色谱测定方法,为祛风止痛片制剂的质量控制提供一定的依据。
1 实验部分
1.1 仪器与试药
LC-20AT岛津高效液相色谱仪(日本岛津公司);U-3310紫外分光光度计(日本Hitachi公司);BP211型电子天平(德国赛多利斯公司);Millipore simplicity -185型超纯水器(美国密里博公司);KQ5200DB型数控超声波清洗器(昆山超声仪器有限公司)。
乌头碱(批号:720-9807,中国药品生物制品检定所);祛风止痛片(批号20080702,20090707,20100103,安徽雪枫药业有限公司);甲醇为色谱纯(美国Fisher公司);其他试剂均为分析纯。实验用水为超纯水。
1.2 色谱条件
色谱柱:Skim-pack vp-ODS(4.6 mm × 250 mm,5 μm);流动相:甲醇-0.1%三乙胺溶液(65∶35,v/v);流速:0.8 mL/min;检测波长:235 nm;柱温:35℃;进样量:10 μL。
1.3 溶液的制备
1.3.1 对照品溶液
精密称取乌头碱对照品0.0047g,用甲醇溶解并定容于25 mL容量瓶中,配制成188 μg/mL的乌头碱母液。用时稀释10倍,即移取1 mL母液用甲醇定容到10 mL容量瓶中,稀释成浓度为18.8 μg/mL的对照品溶液。
1.3.2 样品溶液
取同一批号的祛风止痛片,去除包衣研成粉末,精密称取一定量粉末状样品置入250 mL具塞三角烧瓶中,加入浓氨水12 mL,放置30 min,加乙醚70 mL,超声处理30 min,微孔滤膜滤过,取续滤液,再放在50℃水浴锅中将乙醚挥发干,最后用甲醇溶解,定容于5 mL容量瓶中,摇匀,即得。
1.4 方法专属性考察
按“1.2”色谱条件,记录对照品溶液和样品溶液色谱图,结果见图1。从图1可以看出,在该条件下样品溶液乌头碱的峰与其对照品溶液的峰保留时间一致,且分离良好,无其他干扰。
1.5 线性关系考察
分别准确移取浓度为18.8 μg/mL的对照品溶液 8、10、12、14、16、18 μL注入液相色谱仪,记录色谱图,测定其峰面积。以乌头碱对照品进样量为横坐标,峰面积值为纵坐标,绘制标准曲线,得回归方程y=27950x-60698,r=0.9991。结果表明,乌头碱对照品的峰面积与进样量在0.1504~0.3384 μg范围内有良好的线性关系。
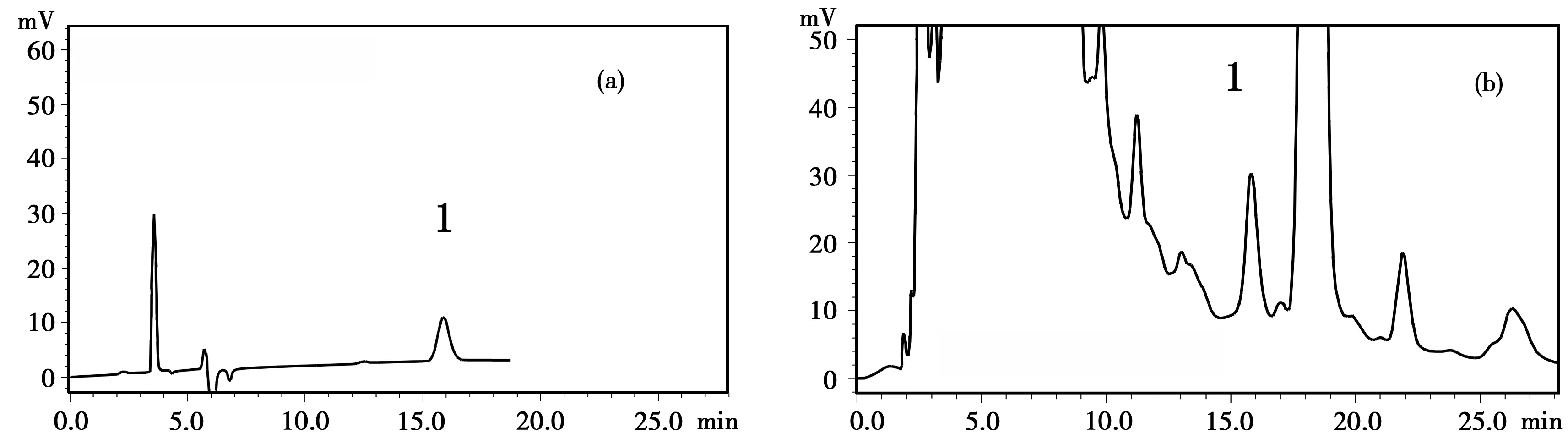
图1 对照品乌头碱(a)和样品(b)的色谱图
2 结果与讨论
2.1 检测波长的选择
文献报道乌头类生物碱在230~240 nm下有较大的吸收峰,如粟贵[9]等报道检测波长为230 nm,辛杨[10]等报道检测波长为235 nm。本实验对乌头碱的甲醇溶液进行了紫外吸收光谱扫描。结果表明,乌头碱在235 nm 处有最大吸收峰,在此波长下测定时,峰面积大,检测灵敏度高,故选择235 nm为检测波长。
2.2 流动相的选择
试验考察了不同比例的甲醇-0.1%三乙胺(60∶40,65∶35,70∶30,75∶25)流动相对峰形和保留时间的影响。结果表明,甲醇∶0.1%三乙胺流动相为65∶35时,分离最好,峰形好,保留时间为15.75 min;60∶40时,保留时间长,虽然分离好,但峰形较宽;70∶30和75∶25时,保留时间短,峰形尖锐,但分离不好。因此,最终确定甲醇-0.1%三乙胺(65∶35,v/v)为流动相。
2.3 精密度试验
准确移取浓度为18.8 μg/mL的对照品溶液10 μL,连续进样6次,记录乌头碱峰面积。结果峰面积的RSD为0.27%,表明仪器精密度良好。
2.4 稳定性试验
取批号为20100103的同一样品溶液10 μL,分别在1、2、4、6、8、24 h后进样,记录峰面积。结果峰面积的RSD为0.67%,表明样品溶液在24 h内保持稳定。
2.5 重复性试验
准确称取批号为20100103样品6份,按“1.3.2”的方法制备样品溶液。按照“1.2”的色谱条件下进样,外标法计算乌头碱的含量。结果乌头碱含量RSD为0.76%,表明重复性好。
2.6 加样回收试验
准确称取批号为20100103样品6份,分别准确加入浓度为18.8 μg/mL的对照品溶液1 mL,按“1.3.2”的方法制备样品溶液,按上述色谱条件测定含量并计算加样回收率。结果测得样品乌头碱平均回收率为98.62%,RSD为1.19%,结果见表1。
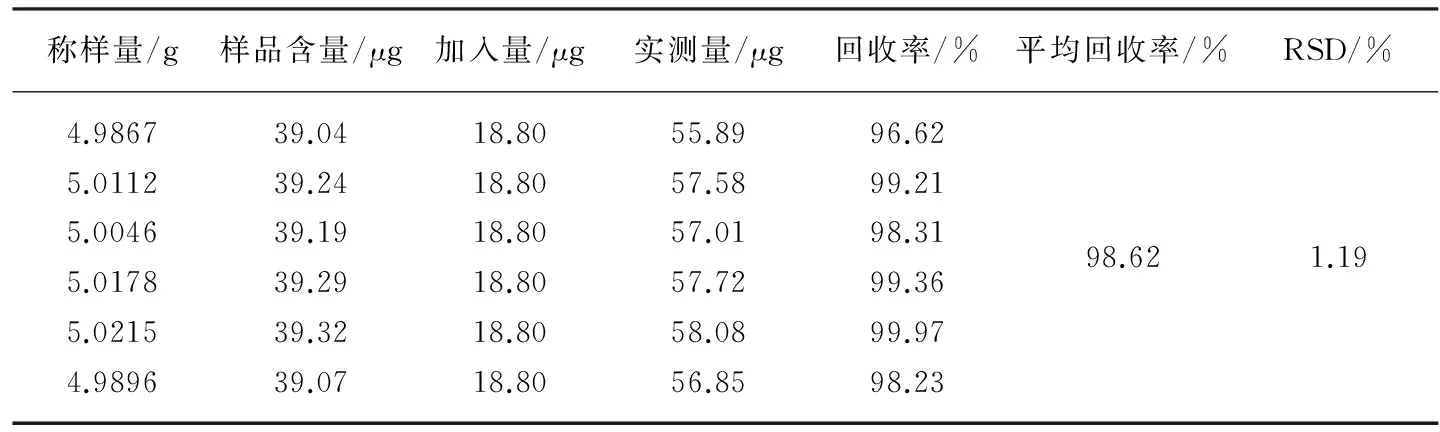
表1 乌头碱加样回收率试验结果
2.7 样品含量测定
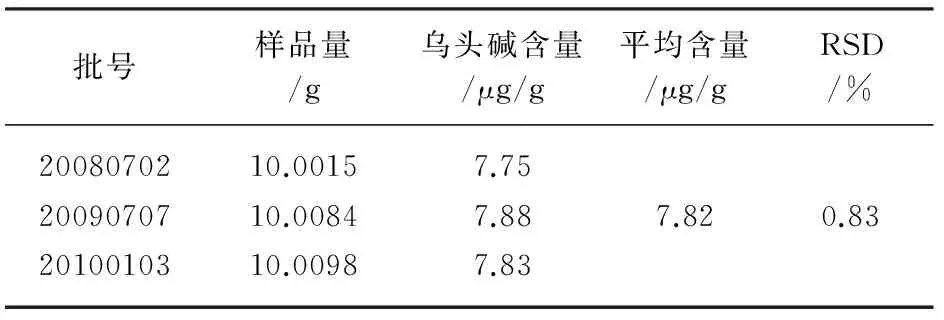
表2 祛风止痛片中乌头碱含量测定结果 n=3
取3批不同批号的祛风止痛片样品,按“1.3.2”项下的方法制备样品溶液,按同样的色谱条件下记录峰面积并计算乌头碱的含量,结果见表2。
3 结 论
本实验建立的HPLC测定方法简便可行,准确可靠,稳定性好,在0.1504~0.3384 μg范围内峰面积与进样量有良好的线性关系,可用于祛风止痛片制剂中乌头碱的检测。
[1]张道荣,郭永振,张琦.祛风止痛片的制剂药物及其制备方法、质量控制方法:ZL200510097337.X[P].2009-05-13
[2]国家药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2010:968
[3]赵向阳.HPLC法测定祛风止痛片中蛇床子素和二氢欧芹醇当归酸酯[J].中国医院用药评价与分析,2016,16(1):112-113
[4]李志浩,瞿京红,郑芳,等.RP-HPLC测定祛风止痛片中原儿茶酸和原儿茶醛的含量[J].辽宁中医药大学学报,2010,12(10):187-189
[5]段红,翟科峰,曹稳根,等.正交试验法优选祛风止痛片中续断、威灵仙和槲寄生的合提工艺[J].中国医院药学杂志,2010,30(17):1439-1442
[6]段红,翟科峰,曹稳根,等.正交试验法优选祛风止痛片中制草乌、独活的合提工艺[J].中成药,2010,32(8):1421-1424
[7]李明梅.高效液相色谱法测定麝香风湿片中乌头碱的含量[J].中国生化药物杂志,2012,33(6):836-838
[8]张宇洁,高苏亚,韩汾汾.反相高效液相色谱法同时测定乌头不同部位中新乌头碱和乌头碱含量[J].中南药学,11(7):551-553
[9]粟贵,廖林川,颜有仪,等.HPLC同时测定生物样品中新乌头碱、乌头碱、次乌头碱的含量[J].中国药学杂志,2009,44(12):946-950
[10]辛杨,王淑敏,刘志强.高效液相色谱法测定草乌叶中新乌头碱、乌头碱和次乌头碱[J].国外医药:植物药分册,2008,23(4):170
(责任编辑:刘小阳)
2016-08-20
安徽省教育厅自然科学研究重点项目(KJ2012A264)。
曹稳根(1964-),安徽东至人,硕士,教授,主要研究方向:生化药物分析。
10.3969/j.issn.1673-2006.2016.11.032
R284.2
A
1673-2006(2016)11-0122-03

