分级多孔结构聚乳酸支架的制备与性能研究*
薄冬营,郭振招,李 红,李启艳,周长忍,赵要武
(1. 暨南大学 理工学院材料科学与工程系, 广州 510632;2. 云南省第一人民医院/昆明理工大学附属医院牙周种植科, 昆明 650032;3. 暨南大学医学院 口腔系, 广州 510632)
分级多孔结构聚乳酸支架的制备与性能研究*
薄冬营1,郭振招1,李 红1,李启艳2,周长忍1,赵要武3
(1. 暨南大学 理工学院材料科学与工程系, 广州 510632;2. 云南省第一人民医院/昆明理工大学附属医院牙周种植科, 昆明 650032;3. 暨南大学医学院 口腔系, 广州 510632)
以左旋聚乳酸为原料,1,4-二氧六环/水为溶剂,采用热致相分离法制备了具有分级多孔结构的组织工程支架。研究了溶剂配比、粗化时间对支架结构和性能的影响。溶剂比为87/13(1,4-二氧六环/水),PLLA浓度5%,粗化1 h时,制备出大孔孔径达300 μm,小孔嵌在大孔孔壁上且孔径在10 μm以下的高连通分级多孔支架。粗化时间的延长使大孔孔径有所增大。细胞实验表明分级多孔支架有助于细胞长入支架内部,促进细胞的增殖。
左旋聚乳酸;热致相分离;分级;支架
0 引 言
组织工程是当今组织再生、修复和重建领域的重要技术和手段[1]。作为细胞载体,组织工程支架需要有一定的机械强度和高连通的多孔结构,以便支撑细胞的粘附增殖以及营养物质和代谢产物的传递[2]。组织工程支架的制备方法较多,如热致相分离法,粒子沥滤法,气体发泡法,快速成型法等,均可制备出孔径在100~500 μm的多孔支架;但往往存在支架结构单一、孔的连通性不高,细胞难以长入(ingrowth)支架内部及物质传递不充分的问题[3-4]。热致相分离法可以制备不同形貌的支架材料,如纳米纤维结构、双连通结构及多孔蜂窝状等,且孔径大小可调、连通性好,可从不用角度满足组织修复的需要[5-7]。从支架材料的设计上,大孔(约300 μm)利于细胞长入支架内部增殖;小孔易于细胞的粘附和组织的代谢[8]。本研究采用热致相分离法制备了具有分级多孔结构的聚乳酸(PLLA)组织工程支架,研究了制备工艺对支架材料微观结构、机械性能以及细胞粘附增殖的影响。
1 实 验
1.1 原料及试剂
聚乳酸(PLLA),Mw= 1.0×105(济南岱罡生物科技有限公司);1,4-二氧六环(A.R级,天津市永大化学试剂有限公司),去离子水,CCK-8试剂盒(同仁化学研究所,上海)。
1.2 支架的制备
按5%(w/v)将PLLA颗粒溶于不同溶剂中,溶剂配比为90/10,87/13,83/17(1,4-二氧六环/水,v/v),恒温搅拌3 h至均相透明溶液。然后加入一定比例的去离子水,继续恒温搅拌2 h,加热温度保持在浊点以上至少5 ℃。分别缓慢降温至凝胶点温度90/10(2 ℃),87/13(25 ℃),83/17(55 ℃)保持1,10,30 min,1 h,1.5,2 h进行粗化。随后将澄清溶液移至特制的聚四氟乙烯模具中,迅速转移至液氮-196 ℃中冷冻1 h。最后将冷冻样品进行冷冻干燥24 h。具体工艺路径如图1所示。

图1 PLLA支架的制备工艺流程图
1.3 样品的表征
支架的孔隙率测定采用体积法,按照下面的公式计算孔隙率
式中ν1为酒精溶液的初始体积,ν2为置入材料24 h后的酒精溶液体积,r,h为圆柱材料的半径和高。将试样材料切成直径为Ø8.5 mm×(10±2 mm)的圆柱形,至少3个平行样品被测量。
支架的形貌采用扫面电镜(TM3030,日立高新技术公司)进行观察。孔径分布根据断面的SEM图进行统计,采用Nano Measurer软件进行断面孔直径测量和统计之后进行非线性拟合,每组样品至少3个平行样品不同位置的断面SEM图被统计,每个样品至少300个孔。
材料的压缩性能采用万能实验机(AG-1,日本津岛公司)在室温下进行实验。样品切割成Ø8.5 mm×5 mm的圆柱,每组至少3个平行样品。压缩速率5 mm/min至试样高度的80%,压缩强度取应力-应变曲线的80%处的强度。
1.4 细胞实验
将支架切割成Ø15 mm×(1 mm±0.5 mm)规格,60Co灭菌后置于24孔板内。细胞采用MC3T3-E1前成骨细胞,细胞接种密度1×106个/mL,分别培养至1,3和5 d时,进行CCK-8检测细胞活性。用酶标仪于490 nm波长检测吸光度,每组3个平行样。复合培养3 d后样品经固定,梯度脱水干燥后,SEM观察形貌。
2 结果与讨论
2.1 支架材料的显微结构
图2是采用不同溶剂比制备的PLLA多孔支架的SEM图;图3是对应的孔径分布图。不同的溶剂比对支架的形貌结构有十分显著的影响。90/10支架形成了类纤维状结构,孔的大小在10 μm以下(如图3(a));在溶剂比为87/13时,形成了显著的分级多孔结构,小孔在10 μm以下,大孔孔径则高达300 μm,连通性好。小孔在大孔的孔壁上形成。随着水比例的进一步增大(83/17),形成了规整的微米级孔结构,孔径为20~30 μm,孔壁多为片层状。

图2 不同溶剂比的PLLA支架形貌图,1,4-二氧六环/水(v/v)
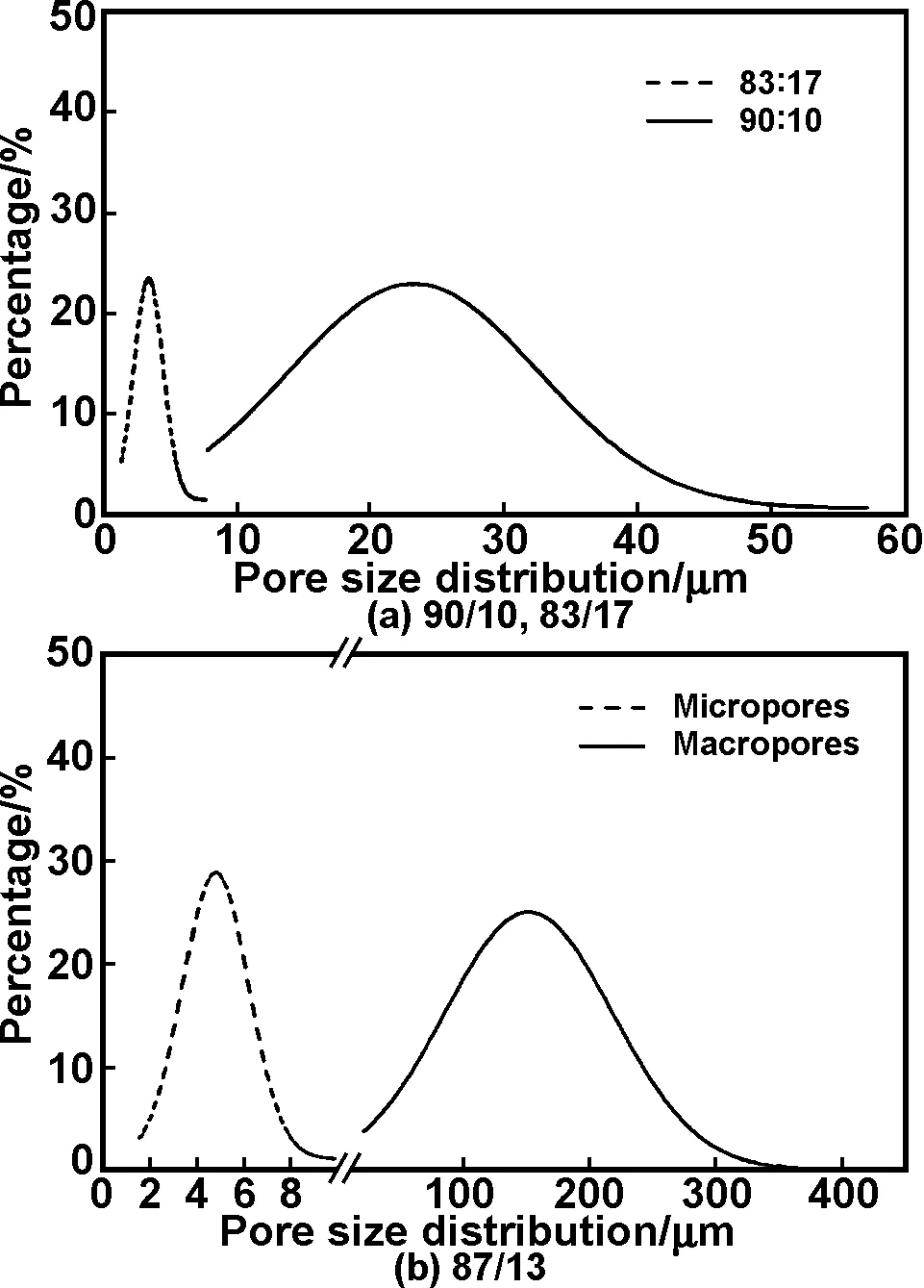
图3 不同溶剂比的PLLA支架孔径分布曲线,1,4-二氧六环/水(v/v)
Fig 3 Pores distribution of PLLA scaffolds according to the ratio of 1, 4-dioxane/water (v/v)
在稀溶液中,高分子链是互相分离的,非溶剂(水)比例的增大相对增大了聚合物的浓度,孤立的高分子链相互靠近,互相穿插交叠,高分子链的互相缠绕产生了富聚合物相和富溶剂相。冷冻干燥过程中,溶剂相挥发形成多孔结构。因此,孔的形态大小与相分离过程密切相关。在溶剂比较高的状态下,相分离区域较小,亲溶剂的高分子链易形成图2(a)的类似纤维的结构,与文献报道相似[9]。随着溶剂中水比例的提高,相分离驱动力大,相分离过程进行的范围宽,易形成范围较大的富溶剂区域。在冷冻干燥后形成大孔结构(如图2(b)所示)。在降温过程中富溶剂相中的溶剂还会经历二次相分离,生成了大孔孔壁上的微孔结构,最后形成了大孔嵌套小孔的分级多孔结构[10]。随着溶剂中水比例的进一步提高,相分离驱动力又减小,富溶剂相中的高分子聚集,形成以图2(c)所示的多孔结构。
按照这种方法制备的支架材料的孔隙率接近90%(表1),随着溶剂比的降低,孔隙率略有下降。

表1 PLLA支架的孔隙率
2.2 粗化时间对支架微观形貌的影响
粗化时间是调节支架微观形貌的工艺因素重要依据。图4是在不同粗化时间下制备的分级多孔支架的SEM图。可以看出,随着粗化时间的增加,PLLA支架材料的大孔孔径在一定程度上有所增加。在粗化时间为30 min时,材料的孔径为150 μm;粗化时间为1 h时,孔径可达300 μm(图2(b))。这是因为随着粗化过程的延长,高聚物富相的高分子链能够充分地相互结合成核长大,从而增大了相分离的驱动作用,同时在搅拌过程中形成的高分子贫相小液滴,在粗化过程中为了减小表面张力而聚集,也为形成大孔提供了条件。但是从图5可以看出,当粗化时间达到一定值(>1 h),支架的孔径几乎上没有什么变化。

图4 不同粗化时间的PLLA支架形貌图 ,1,4-二氧六环/水:87/13(v/v)
Fig 4 SEM images of PLLA scaffolds prepared from 1,4-dioxane/water (87/13) (v/v) system with different coarsening time
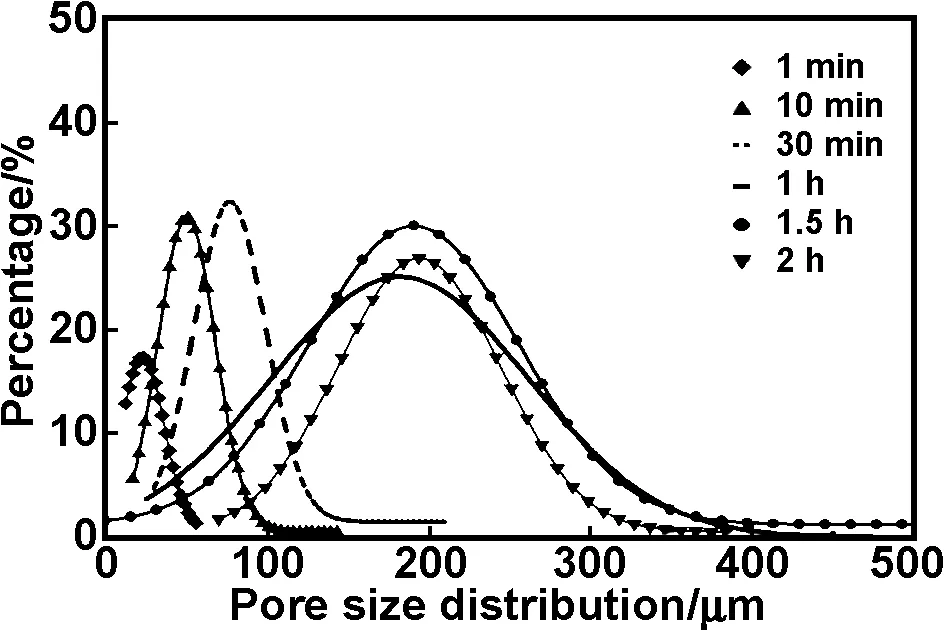
图5 不同粗化时间的PLLA支架孔径分布曲线,1,4-二氧六环/水:87/13(v/v)
Fig 5 Pore size distribution of PLLA scaffolds prepared from 1,4-dioxane/water (87/13) (v/v) system with different coarsening time
2.3 支架材料的力学性能
图6不同溶剂比的PLLA支架的力学性能。

图6 不同溶剂比的PLLA支架的力学性能,粗化时间:1 h
Fig 6 Compressive strength of PLLA scaffolds prepared from 1, 4-dioxane/water system, coarsening time: 1 h
如图6所示,支架材料的压缩强度随溶剂配比降低和浓度增大而增大,这是因为材料孔隙率随溶剂配比的增大而减小(表1所示)。需要注意的是,当溶剂比为87/13,虽然材料的大孔孔径很大,但是机械强度和模量并没有显著下降,故具有分级多孔结构没有导致支架力学性能的下降。
2.4 支架材料的体外细胞培养
不同支架的细胞体外复合培养的CCK-8的检测结果见表2和图8。
表2 PLLA支架的细胞粘附率,粗化时间:1 h
Table 2 Adhesion rate of PLLA scaffolds, Coarsening time:1 h

1,4-二氧六环/水:(v/v)粗化时间粘附率/%90∶101h85.287∶131h71.083∶171h90.987∶131min83.287∶1310min79.487∶1330min76.2
具有单一孔径形貌的支架(溶剂比为90/10、83/17)的细胞粘附率要大于具有分级多孔结构的支架(溶剂比为87/13);但是分级多孔结构的支架上细胞增殖明显高于另外两组。这是因为双孔支架的大孔孔径较大,在细胞植入时,会有部分细胞直接渗透,穿过支架,而未被粘附。材料的孔径以及孔隙率和细胞的粘附有一定的关系,支架的微孔使表面的粗糙度增大,利于细胞粘附,大孔则利于细胞长入支架,从而实现组织的三维空间重建和再生修复。
图7为细胞与支架体外共培养3 d的SEM图。可明显看出细胞粘附在支架的微孔上,并且伸入大孔内部生长,说明细胞可穿入支架材料内部增殖生长。
图8为PLLA支架MC3T3-E1细胞体外培养的CCK-8实验,粗化时间为1 h。

图7 体外培养3 d的MC3T3-E1形貌图,粗化时间:1 h
Fig 7 SEM images of MC3T3-E1 in vitro co-culture with the scaffolds for 3 days: 1,4-dixoane/water: 87/13 (v/v), Coarsening time:1 h
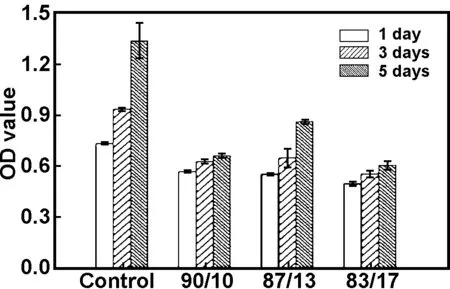
图8 PLLA支架MC3T3-E1细胞体外培养的CCK-8实验,粗化时间:1 h
Fig 8 CCK-8 assay of cell viability from MC3T3-E1 cultured on PLLA scaffolds, Coarsening time:1 h
3 结 论
用热致相分离法制备了分级多孔结构的PLLA支架,大孔孔径可达300 μm,连通性强;小孔10 μm以下,镶嵌于大孔孔壁。研究表明,分级多孔结构的形成与体系的二次相分离过程相关。这种分级多孔PLLA支架具有良好的力学性能,细胞能够长入支架内部,利于组织的再生和修复。
[1] Lisa E F, George C E, Jr Jeffrey T B, et al. Advanced material strategies for tissue engineering scaffolds [J]. Advanced Materials, 2009, 21(32-33): 3410-3418.
[2] Joshua R P, Timothy T R, Ketul C P. Bone tissue engineering: a review in bone biomimetics and drug delivery strategies [J]. Biotechnology Progress, 2009, 25:1539-1560.
[3] Naznin S, Mohd L H, Mim M L. Composite synthetic scaffolds for tissue engineering and regenerative medicine [M]. Berlin:Springer Briefs in Materials, 2015: 1-69.
[4] Hao Y M, Xin J, Lih S T. Fabrication of porous synthetic polymer scaffolds for tissue engineering [J].Journal of Cellular Plastics, 2014, 0(0): 1-32.
[5] Zheng Xiongfei, Zhai Wenjie, et al. 3D nanofibrous poly(L-lactic acid) scaffolds wih large pores fabricated with a single thermally induced phase separation method [J]. Journal of Functional Materials, 2010, 41(1): 184-188.
郑雄飞, 翟文杰,等. 单一热致相分离法制备聚乳酸纳米纤维支架 [J].功能材料, 2010, 41(1): 184-188.
[6] Mannellan G A, Conoscenti G, Carfì Pavia F, et al. Preparation of polymeric foams with a pore size gradient via thermally induced phase separation(TIPS) [J]. Materials Letters, 2015, 160: 31-33.
[7] Xue Li, Nie Taotao, Ma Haiyun. Precise structural regulation of poly(L-lactide) acid tissue engineering scaffolds[J]. Chemical Journal of Chinese Universities, 2015, 36(7): 1409-1415.
薛 丽, 聂涛涛, 马海云. 聚乳酸组织工程支架结构的精密调控 [J]. 高等学校化学学报, 2015, 36(7): 1409-1415.
[8] Zhao Mingyan, Li Lihua. Three-dimensional honeycomb-patterned chitosan/poly(L-lactic acid) scaffolds with improved mechanical and cell compatibility [J]. Society for Biomaterials, 2011, 98A: 434-431.
[9] Liu Shuqiong, Xiao Xiufeng, et al. Fabrication of poly(L-lactic acid) nanofibrous scaffolds by thermally induced phase separation [J]. Chemical Journal of Chinese Universities, 2011, 32(2): 372-378.
刘淑琼, 肖秀峰,等. 热致相分离制备聚乳酸纳米纤维支架 [J].高等学校化学学报,2011, 32(2): 372-378.
[10] Akbarzadeh R, Yousefi A M. Effects of processing parameters in thermally induced phase separation technique on porous architecture of scaffolds for bone tissue engineering [J]. Appllied Biomaterials, 2014, 102B: 1304-1315.
Fabrication of PLLA scaffolds with hierarchical porous structure
BO Dongying1, GUO Zhenzhao1, LI Hong1, LI Qiyan2, ZHOU Changren1, ZHAO Yaowu3
(1. Department of Materials Science and Engineering, Jinan University, Guangzhou 510632, China;2. Department of Periodontology and Implant Dentistry, The First People’s Hospital of Yunnan Province/Affiliated Hospital of Kunming University of Science and Technology, Kunming 650032, China;3. Department of Stomatology of Medical College, Jinan University, Guangzhou 510632, China)
PLLA scaffolds with hierarchical porous structure were fabricated via a thermal induced phase separation in a 1,4-dioxane/water system. The effects of coarsening and the ratio of solvent/non-solvent on scaffold structure and properties were studied. Results indicated that the ratio of solvent/non-solvent affected the morphology of scaffolds. The scaffolds with interconnected and hierarchical porous structure presented macropores up to 300 μm and micropores below 10 μm embeded in the wall of macropores, when the ratio of 87/13 (1,4-dioxane/water) was applied via coarsening for 1h. The macropore size increased with the extension of the coarsening time. Cell culture results showed that the hierarchical scaffolds were beneficial to the cell’s ingrowth and cell proliferation.
PLLA; TIPS;hierarchical; scaffold
1001-9731(2016)04-04210-04
国家自然科学基金资助项目(31571008,81171459,81160134);广东省医学基金资助项目(A2013334)
2015-10-15
2015-12-10 通讯作者:李 红,E-mail: tlihong@jnu.edu.cn
薄冬营 (1990-),女,河南鹤壁人,硕士,师承李红教授,从事生物医用材料研究。
R318.08
A
10.3969/j.issn.1001-9731.2016.04.043

