康艾注射液辅助替吉奥治疗晚期非小细胞肺癌疗效及对血清VEGF、P53及抗Survivin抗体表达的影响
杨 君,韩 莹,郭晓辉,王爱辉,李明宇
康艾注射液辅助替吉奥治疗晚期非小细胞肺癌疗效及对血清VEGF、P53及抗Survivin抗体表达的影响
杨 君1,韩 莹1,郭晓辉1,王爱辉2,李明宇1
(1. 河北港口集团有限公司港口医院,河北 秦皇岛 066000;2. 河北省秦皇岛市第三医院,河北 秦皇岛 066000)

目的 探讨康艾注射液辅助替吉奥治疗一、二线化疗方案治疗后复发或出现药物抵抗的晚期非小细胞肺癌的近期疗效及对血清VEGF、P53抗体及抗survivin抗体表达的影响。方法 将60例晚期非小细胞肺癌患者随机分为观察组和对照组,对照组给予替吉奥单药治疗,观察组加用康艾注射液治疗,观察2组治疗前后血清VEGF、P53抗体、抗Survivin抗体水平及阳性表达情况,统计2组近期疗效、临床受益率及毒副反应发生情况。结果 治疗后,观察组血清VEGF、P53及抗Survivin抗体水平及对照组血清VEGF、抗Survivin抗体水平均明显低于治疗前(P均<0.05),且观察组血清VEGF水平明显低于对照组(P<0.05),2组P53及抗Survivin抗体水平比较差异均无统计学意义(P均>0.05);2组治疗前后各指标阳性率比较差异均无统计学意义(P均>0.05)。疗程结束后,2组疗效比较差异无统计学意义(P>0.05);治疗结束后4周进行随访,观察组临床受益率有高于对照组的趋势,但差异无统计学意义(P>0.05)。治疗过程中,观察组严重毒副反应总发生率明显低于对照组(P<0.05)。结论 替吉奥联合康艾注射液治疗一、二线化疗方案治疗后复发或出现药物抵抗的晚期非小细胞肺癌患者,虽然不能明显提高近期疗效,但能明显改善血清VEGF、P53抗体及抗Survivin抗体水平,降低不良反应发生率,有利于提高患者治疗的依从性,改善生存质量。
康艾注射液;替吉奥;非小细胞肺癌;VEGF;P53抗体;抗Survivin抗体
The curative effect of Kang’ai injection combined with S-1 in the treatment of advanced non-small cell
Key words: Kang’ai injection; S-1; non-small cell lung cancer; vascular endothelial growth factor; P53 antibody; anti-Survivin antibody
肺癌是临床最常见的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)约占肺癌的80%[1],大多数晚期肺癌患者经过一线、二线治疗后常会出现不同程度的药物抵抗,系统化疗已无益于疗效的提高及生存质量的改善,而强化治疗只会增加细胞毒性。替吉奥是一种新型抗肿瘤药物,其单药作为三线治疗方案治疗晚期非小细胞肺癌能取得较好的肿瘤控制效果,并在一定程度上改善患者的生存质量,但在治疗过程中骨髓抑制等严重毒副作用发生率仍较高[2]。随着中药辅助治疗肿瘤研究的不断深入,发现中药不仅能在一定程度上提高临床疗效,而且具有良好的减毒作用。2013年6月—2015年6月,笔者观察比较了替吉奥联合康艾注射液和替吉奥单药治疗一、二线化疗方案治疗后复发或出现药物抵抗晚期非小细胞肺癌患者的临床效果,现将结果报道如下。
1 临床资料
1.1 一般资料 选择上述时期河北港口集团有限公司港口医院收治的60例晚期非小细胞肺癌患者,均签订知情同意书自愿参与本次研究,并已经院伦理委员会批准。患者均有明确的可测量病灶;均为手术和/或一、二线化疗方案治疗后复发或出现药物抵抗者;TNM分期为ⅢB~Ⅳ期;入院时距上次化疗结束超过1个月,且预计生存期>3个月。排除有严重心肝肾功能异常及3个月内使用过康艾注射液或替吉奥治疗者。采用随机数字表法分为2组:观察组30例,男19例,女11例;年龄39~78(61.81±12.63)岁;TNM分期为ⅢB期 14例,Ⅳ期16例;鳞癌9例,腺癌15例,大细胞癌2例,腺鳞癌4例。对照组30例,男18例,女12例;年龄38~76(60.64±12.89)岁;TNM分期为ⅢB期 16例,Ⅳ期14例;鳞癌8例,腺癌18例,大细胞癌1例,腺鳞癌3例。2组性别、年龄、肿瘤分期、分型比较差异均无统计学意义(P均>0.05),具有可比性。
1.2 治疗方法 对照组予替吉奥(维康达,山东新时代药业有限公司生产,批号:20121024)80 mg/(m2·d),分早晚2次口服,连用4周后休息2周,6周为1个疗程,共治疗2个疗程。观察组在对照组治疗基础上给予康艾注射液(白云山制药股份有限公司生产,批号:20121108)60 mL加入0.9%氯化钠注射液250 mL中静脉滴注,1次/d,连用4周后休息2周,6周为1个疗程,共治疗2个疗程。
1.3 观察指标
1.3.1 2组治疗前后血清VEGF、P53抗体、抗Survivin抗体水平及阳性表达情况 分别于治疗前1 d及末次治疗后1 d晨空腹取静脉血5 mL,常规分离血清后,-20 ℃保存待检。标本缓慢解冻,实验前平衡室温。采用双抗体夹心酶联免疫吸附法进行定量检测,试剂盒均为深圳晶美生物公司提供,严格按照试剂盒操作说明书进行操作。
1.3.2 2组近期疗效 于末次治疗次日根据实体瘤疗效评价标准(RECIST)[3]评价近期疗效。完全缓解(CR):目标病灶全部消失;部分缓解(PR):基线病灶长径总和缩小≥30%;稳定(SD):基线病灶长径总和缩小<30%或增加<20%,未出现新病灶;进展(PD):基线病灶长径总和增加≥20%或出现新病灶。CR+PR为总有效,CR+PR+SD为疾病控制。
1.3.3 临床受益率 在治疗结束后4周进行随访并根据患者体力状况、体质量改变及疼痛变化情况对临床受益情况进行评价,以体力状况评分(KPS评分)增加≥10分;食欲好转,体质量增加;止痛药物使用量及疼痛程度降低≥50%3项指标中至少有1项获得连续4周的改善,且其他指标无持续恶化为临床受益[4]。
1.3.4 毒副反应情况 根据WHO抗肿瘤药物毒性分级标准对治疗过程中的毒副反应进行评价和记录,严重程度由轻到重分为0~Ⅳ级[5],本研究仅对Ⅲ~Ⅳ级的严重毒副反应的发生情况进行对比分析。
1.4 统计学方法 应用SPSS13.0统计学软件对数据进行处理。计数资料比较采用卡方检验,等级资料比较采用秩和检验;计量资料用均数±标准差表示,方差齐时采用t检验,方差不齐时采用t检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 2组治疗前后血清VEGF、P53及抗Survivin抗体水平比较 2组治疗前血清VEGF、P53抗体及抗Survivin抗体水平比较差异均无统计学意义(P均>0.05)。治疗后,观察组血清VEGF、P53及抗Survivin抗体水平及对照组血清VEGF、抗Survivin抗体水平均明显低于治疗前(P均<0.05),且观察组血清VEGF水平明显低于对照组(P<0.05),2组P53抗体及抗Survivin抗体水平比较差异均无统计学意义(P均<0.05)。见表1。
2.2 2组血清VEGF、P53及抗Survivin抗体阳性率比较 2组治疗前血清VEGF、P53及抗Survivin抗体阳性率比较差异均无统计学意义(P均>0.05);2组治疗后各指标阳性率有降低趋势,但2组比较差异均无统计学意义(P均>0.05)。见表2。
2.3 2组近期疗效比较 疗程结束后2组均无CR者,2组总有效率及疾病控制率比较差异均无统计学意义(P均>0.05)。见表3。
2.4 2组临床受益率比较 治疗结束后4周进行随访,2组均无失访及死亡者,观察组临床受益率为63.33%(19/30),对照组为43.33%(13/30),2组临床受益率比较差异无统计学意义(2=2.411,P=0.121)。
2.5 2组毒副反应发生情况 治疗过程中,2组患者出现的Ⅲ~Ⅳ级严重毒副反应主要为厌食、恶心呕吐、白细胞降低,2组各严重毒副反应发生率比较差异均无统计学意义(P均>0.05),而观察组严重毒副反应总发生率明显低于对照组(P<0.05)。见表4。

表1 2组治疗前后血清VEGF、P53抗体及抗Survivin抗体水平比较

表2 2组治疗前后血清VEGF、P53及抗Survivin抗体阳性表达情况 例(%)

表3 2组近期疗效比较 例(%)
注:①与对照组比较,2=0.417,P=0.519;②与对照组比较,2=1.071,P=0.301。
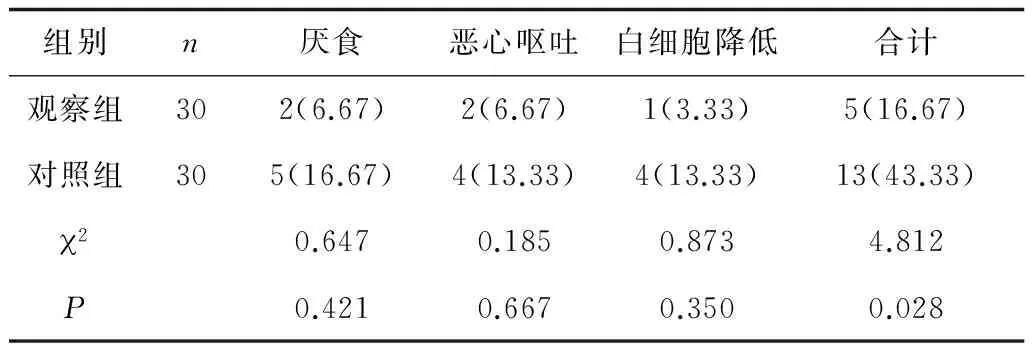
表4 2组Ⅲ~Ⅳ级毒副反应情况 例(%)
3 讨 论
肺癌属于二氢嘧啶脱氢酶(DPD)高活性肿瘤,肺组织中DPD活性明显高于胃、肠、乳腺等其他器官[6]。替吉奥是一种DPD抑制类口服氟尿嘧啶类抗肿瘤药,主要由替加氟(FT)、吉美嘧啶(CDHP)、奥替拉西钾(Oxo)组成。其中FT能在体内转化成5-Fu而发挥抗肿瘤作用。CDHP和Oxo为生化调节剂[2],CDHP可以选择性可逆地抑制DPD作用下5-Fu的分解,提高FT转化的5-Fu浓度,从而保持稳定的血药浓度,增强抗肿瘤的活跃性及疗效;Oxo可选择性可逆地抑制乳清酸磷酸核糖转移酶,抑制5-Fu向5-氟核苷酸转化,从而减轻胃肠道毒副反应,同时又不影响5-Fu抗肿瘤活性[7]。Totani等[8]关于替吉奥单药用于进展期非小细胞肺癌二线治疗的Ⅱ期临床研究结果显示,对于既往至少接受过一种铂类方案化疗的ⅢB~Ⅳ期进展期非小细胞肺癌患者,连用替吉奥 28 d,休息14 d为1个周期,部分缓解率为12.5%,疾病控制率为39.6%,中位生存时间为8.2个月。Ono等[9]应用替吉奥作为三线或三线以上治疗晚期非小细胞肺癌的研究结果显示,总缓解率和疾病控制率分别为5.7%和40%,中位生存期为208 d,毒副反应相对较温和。储建华等[2]应用单药替吉奥三线治疗ⅢB~Ⅳ期非小细胞肺癌的研究结果显示,治疗2个疗程后,总有效率和疾病控制率分别为15%和55%,而严重毒副反应(Ⅲ~Ⅳ级)主要以恶心呕吐(5%)、厌食(10%)、皮肤色素沉着(15%)、白细胞下降(10%)为主。本研究中,替吉奥单药治疗的晚期非小细胞肺癌患者,治疗2个疗程后,总有效率为16.67%,肿瘤控制率为46.67%,毒副反应以厌食、恶心呕吐、白细胞降低为主,与以上研究结论基本一致,表明对于一、二线化疗方案治疗失败或效果欠佳的晚期非小细胞肺癌患者,替吉奥单药治疗对肿瘤具有一定的缓解和控制作用,但严重的骨髓抑制及胃肠道反应发生率仍较高,可能导致患者难以耐受而影响治疗的顺利进行。中医中药的治疗特点为整体观念和辨证论治,作为肿瘤化疗的辅助用药,具有杀伤和抑制肿瘤细胞、提高机体免疫功能等作用。康艾注射液是一种新型中药复方抗肿瘤制剂,其主要有效成分包括人参、黄芪及苦参。人参有补脾益肺、固脱生津、安神增智之功效;黄芪补脾益肺、补气升阳、益气固表、脱毒生肌、利水消肿;苦参具有清热燥湿之功效。现代药理学研究发现,人参能兴奋中枢神经系统,提高反应能力,并有抗疲劳作用,能提高机体免疫功能,增强机体对各种有害刺激及损伤的非特异性抵抗力,同时人参提取物能促进骨髓造血功能,使血液中红细胞、白细胞、血红蛋白等数量明显增加。黄芪能增强机体非特异性免疫功能,同时促进骨髓细胞的分裂分化,促进白细胞和红细胞等的生成[10]。苦参是活性抗癌成分之一,能抑制肿瘤细胞增殖,诱导肿瘤细胞周期阻滞和凋亡;还能降低癌细胞的黏附性和管道内皮细胞的通透性,从而减少肿瘤的转移;还能有效激活以细胞毒性T细胞为免疫效应因子的免疫反应,从而发挥促进抗肿瘤免疫反应的作用,改善预后;还可降低耐药因子P-gp的表达,从而增强肿瘤对化疗药物的敏感性,提高诱导凋亡作用[11];另外苦参碱还具有减轻化疗所致的骨髓抑制,缓解胃肠道反应的作用,可改善患者食欲,减轻疼痛,从而提高患者化疗的耐受性[12]。基于康艾注射液各成分的减毒增效作用,其已广泛地应用于恶性肿瘤的治疗,并取得了较好的临床效果。郎万吉等[13]分析发现,无论联合化疗还是放疗,康艾组CR、PR都高于对照组,白细胞下降及生活质量也优于对照组。秦宇芬等[14]对国内应用康艾注射液联合化疗治疗非小细胞肺癌的13项随机对照研究进行Meta分析显示,康艾注射液联合化疗可提高近期疗效,改善患者生存质量。但对于一、二线化疗方案治疗后复发或出现药物抵抗的患者应用康艾注射液治疗效果的研究甚少。本研究对此类患者分别应用替吉奥及替吉奥联合康艾注射液治疗,疗程结束后,2组整体疗效、总有效率及疾病控制率、临床受益率比较虽然差异无统计学意义,但辅助康艾注射液的观察组有增高的趋势;且治疗过程中观察组严重毒副反应总发生率明显低于对照组。表明对于一、二线化疗方案治疗后复发或出现药物抵抗的患者,在替吉奥治疗基础上加用康艾注射液治疗,能在一定程度上提高肿瘤控制率及临床受益率,但差异并不显著,这可能与本研究样本量较小、治疗时间较短等因素有关,但明显减轻了治疗的毒副反应。
VEGF是肿瘤诱导血管生成过程中的主要调节因子,能使血管通透性增加,促进血管内皮细胞增生及血管形成,与肿瘤的生长及转移密切相关。VEGF在多种恶性肿瘤中高表达,其表达越强提示新生血管越丰富,肿瘤进展越快,转移部位越多[15]。秦建文等[16]报道,非小细胞肺癌患者血清VEGF水平明显高于健康对照组,且与非小细胞肺癌的临床分期有关。王小侠等[17]的研究发现,化疗后肺癌患者血清VEGF的表达明显下降,认为VEGF可作为肺癌近期疗效、复发及转移判断的重要指标。P53基因是重要的抗癌基因之一,P53基因突变会使其失去对肿瘤的抑制作用而具有致癌作用,导致突变型P53蛋白高表达,同时上调VEGF的表达,与肿瘤的发生及转移具有明显的相关性[18],但由于P53蛋白检出率较低而不具备肿瘤标志物的特性,临床常通过检测外周血P53抗体水平对肿瘤的分期、化疗疗效、肿瘤复发及预后进行判断。王巍等[19]认为晚期非小细胞肺癌患者血清P53抗体水平较健康人群明显升高,且与化疗效果呈负相关。王晓彬等[20]的研究结果显示,Ⅲ期非小细胞肺癌患者血清P53抗体阳性率明显高于肺良性疾病组及正常组,且P53抗体阳性滴度与肿瘤大小具有相关性。Survivin是新发现的一种凋亡抑制蛋白,不仅参与凋亡控制,而且还特异性地在细胞周期G2/M期表达,参与对细胞基因转录的调节,肿瘤细胞的Survivin过表达可导致抗Survivin抗体及细胞毒性T淋巴细胞抗癌反应[21],与肿瘤细胞的生长、浸润及转移密切相关,目前临床上多采用抗Survivin抗体的检测对Survivin基因表达进行评价。已有大量研究结果显示,非小细胞肺癌患者血清抗Survivin抗体水平及阳性率均明显高于健康人群,且非小细胞肺癌患者治疗后抗Survivin抗体水平较治疗前明显降低,抗Survivin抗体检测对非小细胞肺癌的诊断及疗效判断均具有重要价值[21-22]。本研究结果显示,治疗后,观察组血清VEGF、P53及抗Survivin抗体水平及对照组血清VEGF、抗Survivin抗体水平均明显低于治疗前,且观察组血清VEGF水平明显低于对照组,2组P53及抗Survivin抗体水平比较差异均无统计学意义;2组各指标阳性率治疗前后比较差异均无统计学意义。提示替吉奥和康艾注射液联用有良好的抗肿瘤作用,可明显降低血清VEGF、P53抗体及抗Survivin抗体水平,这可能与康艾注射液抑制肿瘤细胞增殖、诱导肿瘤细胞周期阻滞和凋亡,抑制肿瘤新生血管形成,促进肿瘤宿主的抗肿瘤免疫反应,增强肿瘤耐药细胞对化疗药物的敏感性等多重抗肿瘤机制有关。
综上所述,替吉奥联合康艾注射液治疗一、二线化疗方案治疗后复发或出现药物抵抗的晚期非小细胞肺癌患者,虽然不能明显提高近期疗效,但能明显降低血清VEGF、P53抗体及抗Survivin抗体水平及不良反应发生率,有利于提高患者治疗的依从性,改善生存质量。但由于本研究样本量较小,并未对不同组织分型、不同分化程度的晚期非小细胞肺癌患者治疗效果进行分析,且未对远期疗效及生存期进行评价,因此,对于康艾注射液治疗晚期非小细胞肺癌的疗效是否与患者的组织分型、分化程度存在相关性,延长康艾注射液疗程是否会对患者的远期疗效及生存期带来有利影响等,仍有待大样本、多中心研究及长期随访加以证实。
[1] Pearson FG. Non-small cell lung cancer:role of surgery for stages Ⅰ-Ⅲ[J]. Chest,1999,116(6 Suppl):500-503
[2] 储建华,刘地发,吉浩明. 单药替吉奥三线治疗晚期非小细胞肺癌40例临床观察[J]. 交通医学,2013,27(5):507-508
[3] 王宏羽,张湘茹. 脂质体紫杉醇联合卡铂与紫杉醇联合卡铂一线治疗晚期非小细胞肺癌的疗效和安全性的比较[J]. 中国医学科学院学报,2014,36(3):305-308
[4] 孙宝信,白璐,李青山,等. 替吉奥联合奥沙利铂与FOLFOX6方案治疗晚期胃癌的疗效对比[J]. 中国老年学杂志,2013,33(14):3306-3308
[5] 孙燕. 内科肿瘤学[M]. 6版. 北京:人民卫生出版社,2001:105-108
[6] Fukushima M,Morita M,Ikeda K,et al. Population study of expression of thymidylate synthase and dihydropyrimidine dehydrogenase in patients with solid tumors[J]. Int J Mol Med,2003,12(6):839-844
[7] 王帅兵,刘红波,刘威威,等. 替吉奥胶囊单药用于老年胃癌患者术后辅助化疗的前瞻性对照研究[J]. 临床肿瘤学杂志,2013,18(6):535-538
[8] TotaniY,SaitoY,HayashiM,etal.AphaseIIstudyofS-1monotherapyassecond-linetreatmentforadvancednon-smallcelllungcancer[J].CancerChemotherPharmacol,2009,64(6):1181-1185
[9] Ono A,Naito T,Murakami H,et al. Evaluation of S-1 as third-or further-line chemotherapy in advanced non-small-cell lung cancer[J]. Int J Clin Oncol,2010,15(2):161-165
[10] 章跃平,徐安,王鹰,等. 康艾注射液在恶性肿瘤化疗中的减毒作用[J]. 航空航天医药,2010,21(1):20-21
[11] 张鸣杰,黄建. 苦参碱类抗肿瘤作用机制研究的新进展[J]. 中国中药杂志,2004,29(2):115-118
[12] 施林花, 裘友好. 苦参碱加化疗治疗中晚期恶性肿瘤的临床观察[J]. 肿瘤学杂志,2001,7(2):95-97
[13] 郎万吉,曾利群,向万明. 康艾注射液治疗肿瘤临床应用文献调查[J]. 云南中医中药杂志,2010,31(6):92-93
[14] 秦宇芬,嵇宏亮,留永咏. 非小细胞肺癌康艾注射液联合化疗的系统评价[J]. 中华肿瘤防治杂志,2012,19(12):921-924
[15] 马广耀,陈铭伍,冯旭,等. Survivin和血管内皮生长因子与肺癌关系的研究进展[J]. 微创医学,2010,5(1):58-62
[16] 秦建文,周静敏,马淑萍. 非小细胞肺癌血清VEGF和PDGF测定的临床意义[J]. 天津医药,2007,35(12):897-899
[17] 王小侠,石怡珍,周剑影. 恶性肿瘤患者血清VEGF、IL-8水平与化疗疗效关系的研究[J]. 标记免疫分析与临床,2007,14(3):131-134
[18] Ecke TH,Schlechte HH,Schiemenz K,et al. TP53 gene mutations in prostate cancer progression[J]. Anticancer Res,2010,30(5):1579-1586
[19] 王巍,林耀东,陈泽程,等. 定量检测血清p53抗体预测晚期非小细胞肺癌预后[J]. 实用肿瘤杂志,2011,26(1):46-49
[20] 王晓彬,靳海龙,韩毅. 血清P53蛋白、P53抗体在Ⅲ期非小细胞肺癌患者的检测[J]. 中国医刊,2013,48(3):45-47
[21] 邹亚峰,王国臣. 化疗对非小细胞肺癌患者血清抗Survivin抗体水平的临床研究[J]. 河北医药,2010,32(1):11-13
[22] 董德琼,杨渝浩,薛东鹰. 非小细胞肺癌患者血清抗Survivin抗体、p53抗体水平的研究[J]. 贵州医药,2005,29(11):969-970
lung cancer and its influence on the expression of serum VEGF, P53 and anti-survivin antibody
YANG Jun1, HAN Ying1, GUO Xiaohui1, WANG Aihui2, LI Mingyu1
(1. Port Hospital of Hebei Port Group Company Limited, Qinhuangdao 066000, Hebei, China; 2. The Third Hospital of Qinhuangdao, Qinhuangdao 066000, Hebei, China)
Objective It is to investigate the curative effect of Kang’ai injection combined with S-1 in the treatment of advanced non-small cell lung cancer (NSCLC) patients which relapse or drug resistance after one-, second-line chemotherapy regimen, and observe its influence on the expression of serum VEGF, P53 antibody and anti-survivin antibody. Methods 60 cases of advanced NSCLC patients were randomly divided into observation group and control group. The patients were treated with S-1 monotherapy in the control group, and with Kang’ai injection in the observation group combined with S-1. The levels of serum vascular endothelial growth factor (VEGF), P53 antibody and anti-survivin antibody and their positive expression were observed in the 2 groups before and after treatment, and the recently curative effect, clinical benefit rate and adverse reaction were recorded. Results After treatment, the serum levels of VEGF, P53 and anti-survivin antibody of the observation group and the levels of VEGF, anti-survivin antibody of the control group were significantly lower than those before treatment (allP<0.05), and the serum VEGF level of the observation group was significantly lower than that of the control group (P<0.05), there was no significant difference in the levels of P53 and anti-survivin antibody between the two groups (allP>0.05); there was no significant difference in positive rate of various index of the two groups before and after treatment (allP>0.05). After the end of treatment, there was no significant difference in curative effect between the two groups (P>0.05); the end of treatment after 4 weeks of follow-up, the clinical benefit rate of the observation group were higher than those of the control group, but there was no significant difference (P>0.05). During the course of treatment, the total incidence of severe toxicity in the observation group was significantly lower than that in the control group (P<0.05). Conclusion The treatment of Kang’ai injection combined with S-1 in the treatment of advanced NSCLC patients which relapse or drug resistance after one-, second-line chemotherapy regimen cannot significantly improve the curative effect in the near future, but can significantly improve the levels of serum VEGF, P53 antibody and anti-survivin antibody, reduce the incidence of adverse reactions, is helpful to improve the compliance of patients and improve quality of life.
杨君,女,主治医师,研究方向为晚期肺癌的临床治疗。
10.3969/j.issn.1008-8849.2016.18.010
R734.2
A
1008-8849(2016)18-1970-05
2016-01-25

