普洱茶茶褐素的分离研究
王天禄,杜丽平,刘 艳,马立娟,肖冬光
(天津科技大学生物工程学院,天津 300457)
普洱茶茶褐素的分离研究
王天禄,杜丽平*,刘艳,马立娟,肖冬光
(天津科技大学生物工程学院,天津 300457)
为了了解普洱茶茶褐素的组成,对从普洱茶中提取的茶褐素进行了分离。通过比较不同树脂对茶褐素的吸附与解吸能力,选择AB-8大孔树脂对普洱茶茶褐素进行分离,得到TBsP1和TBsP2两个组分;进一步利用DEAE-52纤维素柱对TBsP1组分进行分离,得到6个组分;对茶褐素组分TBsP1、TBsP2以及TBsP1分离得到的6个组分的总糖、总酚和蛋白质的含量进行了分析,并进一步对各组分的单糖组成进行了分析。结果表明:不同组分的茶褐素其总糖、总酚和蛋白质的含量有一定的区别,TBsP1分离得到的4个主要组分单糖组成相似,含量不同,与从普洱茶生产原料晒青毛茶中提取的水溶性色素的单糖组成和含量有较大的差异。
普洱茶,茶褐素,AB-8大孔树脂,DEAE-52,单糖组成
普洱茶是我国特有的,采用云南大叶种晒青毛茶经渥堆发酵制成,渥堆发酵过程中,茶多酚在微生物作用及湿热作用下被氧化成茶黄素、茶红素,茶黄素和茶红素进一步氧化聚合[1],并结合多糖、蛋白质、脂质[2]等化合物形成茶褐素。茶褐素能溶于水而不溶于乙酸乙酯和正丁醇,是一类十分复杂的化合物,具有抗癌[3]、减肥降脂[4]、抗疲劳[5]等活性功能,化学组成及结构有待探明。
目前关于茶黄素的研究最为深入,已制备得到多种茶黄素单体[6],茶红素的研究也取得一定进展[7],茶褐素则由于其组成、结构复杂,极性很大,分离纯化的难度高,其研究进展缓慢。谭超[8]等利用原子力显微镜对不同分子量的茶褐素进行观察,发现不同分子量的茶褐素粒子形貌并不均一。杨大鹏[9]利用硅胶层析对茶褐素进行分离,发现茶褐素为多羟基物质,含有烷基、羧基及苯环,主要的糖单位为葡萄糖。杨新河[10]等利用sephadex-LH20对茶褐素进行分级,得到六个级分,这些级分由儿茶素以外的多酚、蛋白质及多糖组成,但是各组分中总酚、总糖和蛋白质含量不同。
本研究从普洱茶中提取茶褐素,采用大孔树脂将茶褐素分离成两个不同极性的组分,再通过DEAE-52阴离子交换树脂对极性较高,酚类含量低的组分按离子强度的差异进行分离,以期获得数种不同性质的茶褐素部分,进一步对各部分的总糖、总酚和蛋白质的含量以及单糖糖组成进行研究,为研究茶褐素类物质组成、结构、功能提供参考。
1 材料与方法
1.1材料与仪器
普洱茶天士力机采茶叶生产;阳离子交换树脂001X7、D72、D61、D151,阴离子交换树脂D280、D201、D301T,大孔吸附树脂AB-8、D4006、NKA-9、D3520南开大学化工厂;DEAE-52阴离子交换树脂北京华迈科生物技术有限公司;1-苯基-3-甲基-5-吡唑啉酮(PMP)上海思域化工;三氟乙酸、乙酸乙酯、二氯甲烷、正丁醇、无水乙醇、硫酸、碳酸氢钠、氯化钠天津市光复科技有限公司,分析纯;重蒸酚索莱宝;考马斯亮蓝G250、福林酚北京鼎国昌盛生物技术有限责任公司。
N-1100旋转蒸发仪日本东京理化;UV5200紫外可见分光光度计上海元析;Agilent 100高效液相色谱仪美国Agilent。
1.2实验方法
1.2.1茶褐素的制备[9]普洱茶粉碎后,用95%乙醇浸提,每次8 h,浸提三次,至浸提液基本无色,除去醇溶性物质;剩余的茶粉用60 ℃热水,按1∶20(w/v)的加水比浸提三次,合并三次浸提的茶汤,滤纸抽滤除去悬浮颗粒,60 ℃旋蒸浓缩,至浓缩液体积为浓缩前的1/10,依次用乙酸乙酯、二氯甲烷和正丁醇按1∶1(v/v)的比例对浓缩液进行萃取,每种有机溶剂萃取三次,得到剩余水层,60 ℃旋转蒸发除去有机溶剂,冻干得到茶褐素粉末,复溶后4 ℃保存,备用。
1.2.2茶褐素化学成分测定总酚测定用福林酚法[11];总糖测定采用苯酚硫酸法[12];蛋白质的测定采用考马斯亮蓝法[13]。
1.2.3树脂的选择通过比较11种大孔树脂对茶褐素的吸附和解吸情况,选择合适的树脂用于茶褐素的分离。
1.2.3.1树脂的吸附率分别准确称取2.0 g经过预处理后的各型号树脂,置于50 mL广口试剂瓶中,精确加入10 mL浓度为2 mg/mL的茶褐素溶液,以100 r/min速度于25 ℃恒温摇床振荡至吸附饱和后过滤,测定滤液中总酚、总糖的浓度,按式(1)计算树脂的吸附率。
吸附率(%)=[(C0-Ce)/C0]×100
式(1)
式中:C0为吸附前茶褐素溶液中总酚(或总糖)浓度(mg/mL);Ce为吸附后茶褐素溶液中总酚(或总糖)浓度(mg/mL)。
1.2.3.2树脂的解吸率用50%(v/v)乙醇溶液对吸附饱和的树脂,于25 ℃下进行解吸,达到平衡后过滤,测定解吸液中总酚、总糖的浓度,按式(2)计算解吸率。
解吸率(%)=[Cr×Vr/(C0-Ce)×V0]×100
式(2)
式中:Cr为解吸液中的总酚(或总糖)浓度(mg/mL);Vr为解吸液的体积(mL);C0、Ce见式(1);V0为茶褐素溶液的体积(mL)。
1.2.4AB-8树脂的静态吸附研究
1.2.4.1静态吸附曲线准确称取经过预处理后的AB-8树脂2.0 g分别置于18个30 mL广口试剂瓶中,分别精确加入10 mL总酚浓度约0.4 mg/mL的茶褐素溶液,于25 ℃下进行静态吸附,于30 min、1、2、4、6和8 h取一组(3瓶),过滤后测定溶液中总酚和总糖浓度,按公式(1)计算不同时间的吸附率。
1.2.4.2饱和吸附实验准确称取经过预处理后的AB-8树脂2.0 g置于30 mL广口试剂瓶中,分别精确加入10 mL总酚浓度为1.0、2.5、5.0、7.5、10.0、15.0、20.0 mg/mL的茶褐素溶液,25 ℃静态吸附8 h,测定溶液中茶褐素溶液的总酚浓度,按公式(3)计算树脂的吸附量。
Q=(C0-Ce)×V0/W
式(3)
式中:Q为吸附量(mg/g);W为湿树脂质量(g);C0、Ce见式(1);V0为茶褐素溶液的体积(mL)。
1.2.4.3pH对AB-8树脂吸附的影响准确称取经过预处理后的AB-8树脂2.0 g,用1 mol/L HCl溶液和1 mol/L NaOH溶液将总酚浓度0.4 mg/mL的茶褐素溶液的pH调为2.0、4.0、6.0、8.0和10.0,于25 ℃进行静态吸附实验,吸附饱和后,测定茶褐素溶液中总酚、总糖的浓度,并按式(1)计算树脂的吸附率。
1.2.4.4乙醇浓度对AB-8树脂解吸的影响配制浓度(v/v)为10%、20%、30%、40%、50%、60%、70%的乙醇水溶液,分别对茶褐素饱和吸附的AB-8树脂25 ℃下进行解吸,测定解吸液中的总酚浓度,并按式(2)计算解吸率。
1.2.5AB-8树脂的动态吸附研究动态吸附在装有AB-8树脂的玻璃层析柱(1.6 cm×5 cm)中进行,树脂体积约为10 mL(相当于6 g树脂)。
1.2.5.1上样浓度对AB-8树脂动态吸附的影响准备总酚浓度分别为2.0、3.0、4.0、5.0、6.0 mg/mL的茶褐素溶液,用1 mol/L HCl溶液调pH至4.0,准确取50 mL于25 ℃恒温上样,流速1 BV/h,上样结束后用50 mL、pH4.0的去离子水冲树脂柱,合并两侧的流出液,测定流出液中总酚和总糖的浓度,按式(1)计算吸附率。
1.2.5.2上样流速对AB-8树脂动态吸附的影响准确取50 mL总酚浓度为4.0 mg/mL的茶褐素溶液,用1 mol/L HCl溶液调pH至4.0,以流速为1、2、3、4、5、6 BV/h,25 ℃恒温分别上样,上样结束后用等体积pH4.0的去离子水冲洗层析柱,收集流出液,并按式(1)计算其吸附率。
1.2.5.3上样次数对茶褐素吸附的影响将上样与冲洗的流出液合并,浓缩至约50 mL,测定浓缩流出液中的总酚和总糖浓度,重复上样操作四次,计算每一次的吸附率。
1.2.5.4AB-8树脂分离组分TBsP1与TBsP2AB-8树脂通过重复上样和洗脱收集未被吸附的组分TBsP1和被AB-8树脂吸附后洗脱的组分TBsP2。
1.2.6DEAE-52阴离子交换树脂对TBsP1组分进行分离
1.2.6.1DEAE-52线性洗脱准确称取50.0 mg TBsP1溶解在1 mL去离子水中,在规格为1.6 cm×10 cm的DEAE-52层析柱中上样,用1 mol/L NaCl溶液,于25 ℃进行线性梯度洗脱,流速3 BV/h,每5 mL收集一管洗脱液,用苯酚硫酸法测定490 nm下的吸光值,绘制线性洗脱曲线,确定梯度洗脱浓度。
1.2.6.2DEAE-52梯度洗脱准确称取200.0 mg TBsP1溶于5 mL去离子水,上样,用线性梯度洗脱中确定的NaCl浓度溶液于25 ℃洗脱,洗脱流速3 BV/h,最后用0.5 mol/L NaOH溶液对层析柱上的残留物进行洗脱,用苯酚硫酸法测定490 nm下的吸光值,绘制洗脱曲线。收集各个洗脱组分,透析除盐,冻干得到TBsP1的各分离组分。
1.2.7茶褐素的主要组分的单糖组成
1.2.7.1样品处理根据Yuan等的方法对茶褐素主要组分的单糖组成进行分析[14]。准确称取5.0 mg样品溶于4 mL浓度为2 mol/L三氟乙酸中,充入氮气封管,110 ℃水解4 h,加入4 mL甲醇后用氮气吹干,重复3次,去除三氟乙酸;加入1 mL去离子水复溶,离心取上清,之后进行PMP衍生操作,得待检测样品。
1.2.7.2色谱条件色谱柱Agilent ZORBAX Eclipse Plus C18,4.6 mm× 250 mm i.d.,5 μm;流动相:0.1 mol/L磷酸盐(pH6.7)缓冲液-乙腈(83∶17);柱温:30 ℃;检测波长:250 nm;流速:1 mL/min;进样体积20 μL。
1.3数据处理
实验中每个处理重复三次,Origin 8.1软件作图。
2 结果与分析
2.1树脂的筛选
为了考察不同型号树脂对茶褐素中酚类物质和糖类物质的吸附能力,按照1.2.3对11种型号的树脂进行比较,实验结果如图1,由图可知,11种树脂对茶褐素的酚类和糖类的吸附能力明显不同,001X7、D61、D72、D151和D4006树脂对茶褐素的吸附能力较弱,其他类型的树脂对茶褐素有较好的吸附,D301T对糖类和酚类的吸附能力都强,达不到将糖类和酚类分离的效果,D201和D280对茶褐素总酚和总糖吸附很强,解吸附发现:即使用2%(w/v)的NaOH溶液也难以解吸,说明其与茶褐素结合强度高,造成了死吸附,不适合对茶褐素进行分离。所以选择NKA-9、D3520和AB-8树脂进一步研究其解吸能力,结果如表1所示。

图1 不同型号树脂对茶褐素中总糖和总酚的吸附率Fig.1 Adsorption rate of different resins for total sugarand total phenol from puerh tea theabrownins
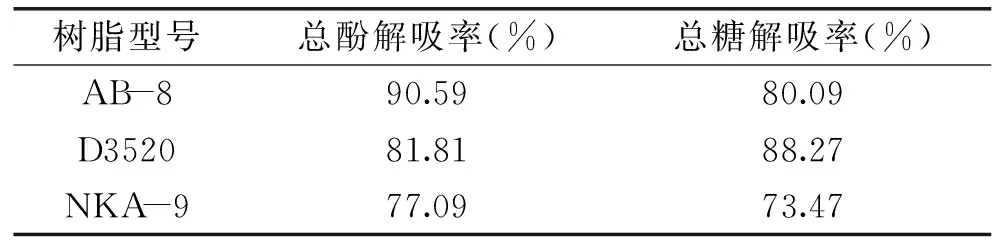
树脂型号总酚解吸率(%)总糖解吸率(%)AB-890.5980.09D352081.8188.27NKA-977.0973.47
由表1可知,AB-8树脂吸附茶褐素总酚的解吸率高达90%以上,是三种树脂中解吸率最高的,而且对总糖的解吸率比较高,故选择AB-8树脂进行茶褐素的分离。
2.2AB-8树脂对茶褐素的分离研究
2.2.1AB-8树脂的静态吸附与解析
2.2.1.1AB-8树脂的茶褐素吸静态附曲线由图2可知,AB-8树脂在吸附30 min时,总酚的吸附率就达62.95%,总糖吸附率达到19.34%,吸附1 h,总酚的吸附率达到了70.80%,总糖吸附率为30.97%,随后吸附率变化不大。

图2 AB-8树脂静态吸附曲线Fig.2 Static adsorption curve of AB-8 resin
2.2.1.2茶褐素总酚浓度对AB-8树脂吸附的影响由图3可知,当茶褐素中总酚浓度小于10 mg/mL时,AB-8树脂的吸附量和浓度呈正比关系,当总酚浓度超过10 mg/mL时,AB-8树脂对茶褐素中总酚的吸附量增加不大,AB-8树脂对茶褐素中总酚的吸附量约为55 mg/g。

图3 茶褐素总酚浓度对AB-8树脂吸附的影响Fig.3 Effect of polyphenol concentration on adsorptioncapacity of AB-8 resin
2.2.1.3pH对AB-8树脂吸附茶褐素的影响由图4可知,pH对AB-8树脂的吸附性能有一定的影响。粗提茶褐素溶液的pH大约为6.2~6.8,pH的变化会影响茶褐素中的酚羟基的解离,AB-8树脂在pH为4.0时对总酚的吸附量达到最大,AB-8树脂对总糖的吸附率随着pH的上升而下降。pH过低或者过高都会影响氢键的形成,选择pH4.0作为AB-8树脂的最佳吸附pH。

图4 pH对AB-8树脂吸附率的影响Fig.4 Effect of pH on adsorption rates of AB-8 resin
2.2.1.4乙醇浓度对AB-8树脂的茶褐素解吸影响由图5可以看出,随着乙醇浓度的提高茶褐素的解吸率逐渐上升,当乙醇浓度为60%时总酚的解吸率达91.64%,总糖的解吸率也达到了91.41%。当乙醇浓度达到70%时,总酚的解吸率开始降低,总糖的解吸率基本不变。推测茶褐素的极性较强,当乙醇浓度过高时可能会导致部分茶褐素的析出,从而使得解吸率下降。

图5 乙醇浓度对解吸率的影响Fig.5 Effect of ethanol concentration on desorption rates of AB-8 resin
2.2.2AB-8树脂的动态吸附
2.2.2.1上样浓度对AB-8树脂动态吸附的影响由图6可知,当总酚浓度在小于4 mg/mL,总酚吸附率均在67%左右,当浓度高于4 mg/mL时吸附率迅速下降。可能是由于浓度过高会导致溶液中的茶褐素无法与树脂充分接触,达不到理想的吸附效果。

图6 茶褐素浓度对吸附率的影响Fig.6 Effect of theabrwonin concentration on dynamic rates of AB-8 resin
2.2.2.2上样流速对AB-8树脂动态吸附的影响由图7可知,当上样流速小于4 BV/h时,吸附率都维持在65%,而流速高于4 BV/h时,吸附率大幅度降低。可能由于流速过高导致茶褐素与树脂的接触时间不够,从而降低了吸附率。

图7 上样流速对吸附率的影响Fig.7 Effect of flow rates on dynamicadsorption rates of AB-8 resin
2.2.2.3重复上样次数对吸附率的影响通过重复上样和洗脱收集到未被吸附的组分TBsP1和被AB-8树脂吸附后洗脱的组分TBsP2,由图8可知,重复上样3次和4次,AB-8树脂对茶褐素中总酚和总糖的吸附率基本相同,选择重复上样3次。茶褐素经分离得到TBsP1和TBsP2,两个组分的总糖、总酚和蛋白质含量如表2所示。

图8 重复上样次数对吸附率的影响Fig.8 Effect of sample-loading times on dynamic adsorption rates of AB-8 resin

组分总糖含量(%)总酚含量(%)蛋白质含量(%)TBs23.6925.539.53TBsP127.1817.104.44TBsP219.3328.9612.55
由表2可知,TBsP1组分中糖含量最高,达到27.18%,蛋白含量仅为4.44%,TBsP2中酚含量最高,为28.96%。选择DEAE-52阴离子交换树脂对TBsP1进一步分离,并对其单糖组成进行研究。
2.3DEAE-52阴离子交换树脂分离TBsP1
按照1.2.6方法,绘制线性洗脱曲线如图4a,确定洗脱用NaCl的浓度。根据图9a中的出峰状况,选择去离子水、0.06、0.13、0.17、0.5 mol/L的NaCl进行洗脱,对未被洗脱的部分用0.5 mol/L的NaOH进行洗脱。
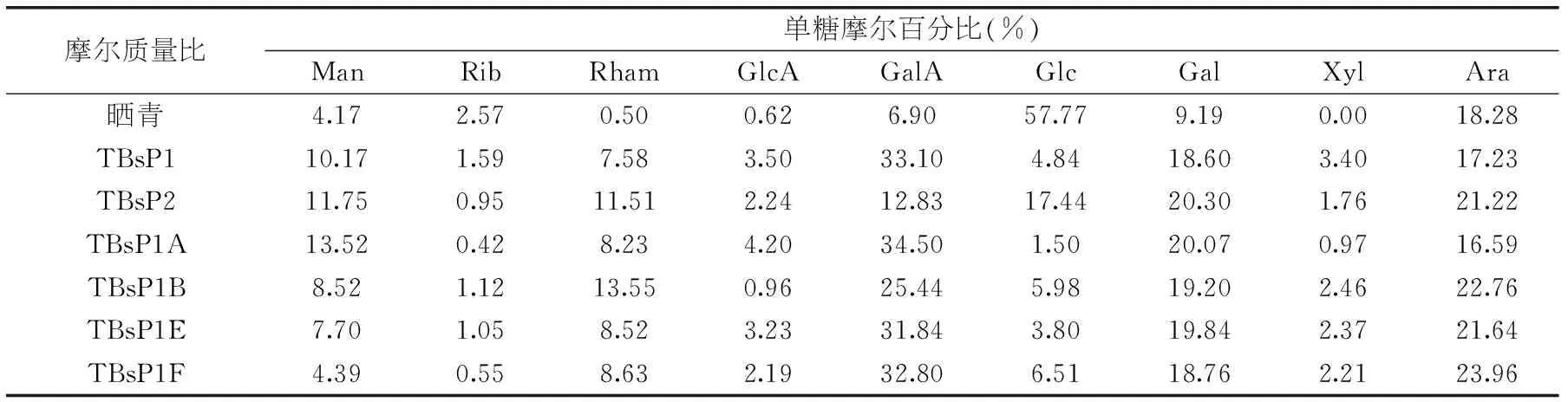
表4 茶褐素的主要分离组分的单糖组成
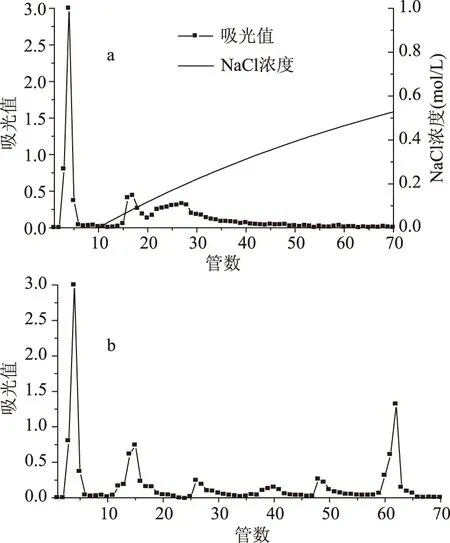
图9 DEAE-52树脂洗脱曲线Fig.9 DEAE-52 chromatography eluting curve注:a为DEAE-52树脂线性洗脱曲线,b为DEAE-52树脂梯度洗脱曲线。
由图9b可知,经DEAE-52阴离子交换树脂梯度洗脱峰较为对称,可以认为各个茶褐素组分得到较好分离且组分性质较为单一,收集各个茶褐素组分,旋蒸浓缩,蒸馏水透析除去NaCl,冻干得到各个组分。按洗脱顺序将各组分分别命名为TBsP1A、TBsP1B、TBsP1C、TBsP1D、TBsP1E、TBsP1F。各组分的得率分别为27.40%、9.56%、4.40%、3.08%、9.36%、19.76%。其总糖、总酚和蛋白质的含量如表3。
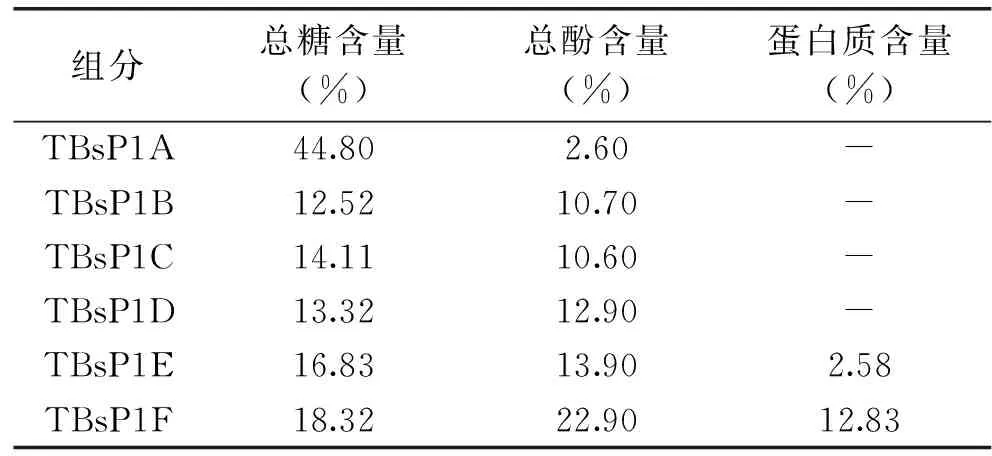
表3 DEAE-52阴离子交换柱分离的
由表3可知,经DEAE-52阴离子交换树脂梯度洗脱得到的各个茶褐素组分的总糖,总酚以及蛋白含量均有区别。TBsP1A的总糖含量最高,为44.80%,总酚含量为2.60%;TBsP1B、TBsP1C、TBsP1D、TBsP1E中总糖和总酚的含量相近,TBsP1E中含有2.58%的蛋白质;TBsP1F中总酚含量要高于其他组分,蛋白质的含量也较高。
2.4茶褐素的主要分离组分的单糖分析
按照1.2.7用高效液相色谱对茶褐素分离所得单糖组分分析结果如表4所示。普洱茶生产原料晒青毛茶中提取的色素中Glc含量最高,摩尔百分比为57.77%,其次为Ara,摩尔百分比为18.28%。晒青毛茶经微生物作用后,茶褐素分离所得组分中单糖组成差异较大,其中Gal、Man、Rham、两种酸性多糖有所增加,Glc的含量明显变少。普洱茶茶褐素的不同分离组分的单糖摩尔百分比有差异,茶褐素的两个粗分离组分中TBsP1中的GalA比例高于TBsP2,Glc比例低于TBsP2。TBsP1分离所得的几个主要组分中,单糖的种类相似,摩尔百分比有区别,其主要单糖为GalA、Gal和Ara,另外两个组分TBsP1C、TBsP1D量太少,未进行单糖组分分析。
3 结论
本文通过利用AB-8树脂将茶褐素分离成两种不同的极性的组分,两个组分总糖、总酚、蛋白质含量不同,TBsP1中多糖含量较高,TBsP2中总酚含量最高。两组分的单糖组成上也有区别,尤其是GalA和Glc的摩尔百分比差异较大。TBs-P1组分经DEAE-52分离后得到六种不同性质的组分,各个组分总糖、总酚和蛋白质含量均有区别,说明经过AB-8树脂和DEAE-52树脂分步层析分离,可以将不同性质的茶褐素组分进行分离。不同组分中多糖、多酚和蛋白质的结合程度也有所不同。茶褐素的主要分离组分单糖组成相似,各种单糖的摩尔百分比有差别,但与晒青毛茶相比差异较大,说明普洱茶发酵过程中,原料的糖类物质经微生物作用发生变化,并与多酚和蛋白质结合形成了茶褐素。有关普洱茶发酵过程中茶褐素形成方式、单糖组成的变化,各组分的结构特定、生理活性等还有待研究。
[1]谭超,郭刚军,李宝才,等.普洱茶茶褐素理化性质与光谱学性质研究[J].林产化学与工业,2010,30(4):53-58.[2]Jiashun Gong,Qin Zhang,Chunxiu Peng,et al. Curie-point pyrolysis-gas chromatography-mass spectroscopic analysis of theabrownins from fermented Zijuan tea [J]. Journal of Analytical and Applied Pyrolysis,2012,97:171-180.
[3]Steel V E,Kelloff G J,Balentine D,et al. Comparative chemopreventive mechanisms of green tea,black tea and selected polyphenol extracts measured byinvitrobioassays[J]. Carinogenesis,2000,21(1):63-67.
[4]姜波,田维熙,齐桂年.四川边茶提取物对脂肪酸合酶的抑制作用[J].中国科学院研究生院学报,2007,24(3):291-299.
[5]龚加顺,陈文品,周红杰,等.云南普洱茶特征成分的功能与毒理学评价[J].茶叶科学,2007,27(3):201-210.
[6]Wang Kunbo,Liu Zhonghua,Huang Jianan,et al.Preparative isolation and purification of theaflavins and catechins by high-speed countercurrent chromatography[J]. Journal of Chromatography B,2008,867(2):282-286.
[7]Rajesh Krishnan,Girish BMaru. Isolation and analyses of polymeric polyphenol fractions from black tea[J]. Food Chemistry,2006,94(3):331-340.
[8]谭超,彭春秀,高斌,等.普洱茶茶褐素类主要组分特征及光谱学性质研究[J].光谱学与光谱学分析,2012,32(4):1051-1056.
[9] 杨大鹏.云南普洱茶茶褐素主要化学成分的分离及结构鉴定[D].昆明:云南农业大学,2009.
[10]杨新河,王丽丽,黄建安,等.普洱茶茶褐素的分级及相关性质初步研究[J].茶叶科学,2011,31(3):187-194.
[11]GB/T 8313-2008. 茶叶中茶多酚和儿茶素类含量的检测方法[S].北京:中国标准出版社,2008.
[12]杨勇杰,姜瑞芝,陈英红,等.苯酚-硫酸法测定杂多糖含量的研究[J].2005,27(6):706-708.
[13]安志强,孙新顺,乔文庆.考马斯亮蓝法测定青霉素发酵液中可溶性蛋白质含量[J].河北化工,2010,33(9):60-61.
[14]Qingxia Yuan,Longyan Zhao,Qianqian Cha,et al. Structural Characterization and Immunostimulatory Activity of a Homogeneous Polysaccharide fromSinonovaculaconstricta[J]. Journal of Agricultural and Food Chemistry,2015,63(36):7986-7994.
Study on fractionation of theabrownins in Puerh tea
WANG Tian-lu,DU Li-ping*,LIU Yan,MA Li-juan,XIAO Dong-guang
(College of Biotechnology,Tianjin University of Science & Technology,Tianjin 300457,China)
In this paper,the adsorption and desorption properties of different macroporous resins for Puerh tea theabrownins was investigated,and AB-8 macroporous resins was selected for fraction. Two fractions,TBsP1 and TBsP2 were obtained from the separation of Puerh tea theabrownins by AB-8 macroporous resin. With using DEAE-52 cellulose chromatography for grading TBsP1,six theabrownins fractions were obtained. The monosaccharide compositions of TBsP1,TBsP2 and four major fractions of TBsP1 were analysised. The fractions of theabrownins were different in the contents of total sugar,total phenol and protein. The monosaccharides compositions of four major fractions were similar,and different in contents. Comparing with the water soluble pigments extracting from Puerh crude tea,the compositions and content of monosaccharides were significantly different.
Puerh tea;theabrownins;AB-8 macroporous resin;DEAE-52;monosaccharide composition
2015-12-29
王天禄(1990-),男,硕士研究生,研究方向:生物分离及现代酿造技术,E-mail:wangtianlu1990@126.com。
杜丽平(1967-),女,博士,副教授,主要从事发酵工艺及分离分析方面的研究,E-mail:dlp123@tust.edu.cn。
教育部“长江学者和创新团队发展计划”项目(IRT1166)。
TS272.2
A
1002-0306(2016)16-0136-06
10.13386/j.issn1002-0306.2016.16.019

