负载虾青素淀粉纳米粒的表征与稳定性能研究
刘占军,崔成龙,2,李志威,耿旭芳,赵琳琳,赵 宁
(1.华北理工大学,河北唐山 063009;2.中国药科大学,江苏南京 211198)
负载虾青素淀粉纳米粒的表征与稳定性能研究
刘占军1,崔成龙1,2,李志威1,耿旭芳1,赵琳琳1,赵宁1
(1.华北理工大学,河北唐山 063009;2.中国药科大学,江苏南京 211198)
为了提高虾青素的稳定性,制备了淀粉接枝聚甲基丙烯酸甲酯纳米粒,然后采用透析法,将虾青素与纳米粒混合制成虾青素纳米粒。测定了淀粉及接枝共聚物的红外光谱、纳米粒的平均粒径、粒径分布、纳米粒形态,并以虾青素的丙酮溶液作为比较,对虾青素纳米粒的稳定性进行了测定。结果表明,虾青素纳米粒的平均粒径为(208.1±26.4) nm,分散系数为0.284±0.035;4 h光照后,虾青素纳米粒保留率为26.34%;30 ℃和50 ℃恒温避光下,贮存8 d时虾青素纳米粒的保留率分别为91.81%和83.44%;在pH=1、3、5、7、9或11条件下,虾青素纳米粒的保留率平均值为86.18%。
虾青素,纳米粒,淀粉,聚甲基丙烯酸甲酯
人们越来越认识到食品与人类健康的密切关系,各种保健食品及食品添加剂正以迅猛之势发展。近年来,人们对虾青素的重视程度越来越高。虾青素(Astaxanthin),是一种类胡萝卜素,具有很强的抗氧化活性,具有多种保健功能,如增强免疫反应,预防癌症、心血管疾病,延缓白内障发展、黄斑退化,抵抗炎症和幽门螺杆菌感染[1-2],所以,虾青素广泛应用于食品、饮料和医药等领域[3]。但是,由于其生物利用度低,水溶性差,性质不稳定,易受光、氧、温度、pH等外界因素的影响而发生变化,使其应用受到了一定的限制[4]。
淀粉因来源丰富、价格低廉、可再生、可完全被生物降解[5],被广泛用作食品及食品添加剂,但制备成纳米粒[6]用于添加剂的文献并不多见。将淀粉与聚甲基丙烯酸甲酯接枝得到纳米粒,负载虾青素,可以提高其稳定性,延长保存时间,扩大其应用范围。虾青素纳米粒具有较小的粒径和表面积,增加溶解度和稳定性,而提高生物利用度,易于在广泛的产品中应用。
红外光谱法是化合物的结构分析及定性判断的基本方法,可以推测化合物的结构、类别、基团组成等信息[7]。利用透射电子显微镜(TEM)表征材料的形貌、成分、晶体结构等,具有直观、分辨率高、放大倍率宽等特点,尤其对于纳米粒等超细微粒更是不可缺少的测量手段[8]。激光粒度测量方法的理论依据是Fraunhofer衍射理论和完全的米氏光散射理论。该测量方法具有实际分辨率高,检测速度快,智能化程度较高,输出结果是连续的粒径分布,使用方便,重复性好[9]。
本文采用二羟基二过碘酸合镍(IV)钾为引发剂[10],制备淀粉接枝聚甲基丙烯酸甲酯纳米粒,用于负载虾青素,对负载虾青素淀粉纳米粒进行了红外光谱、透射电子显微镜、激光粒度等表征,并以虾青素的丙酮溶液作为比较,对虾青素纳米粒的稳定性进行评价。
1 材料与方法
1.1材料与仪器
虾青素(含量≥95%)Sigma公司;可溶性淀粉分析纯,天津市凯通化学试剂有限公司;引发剂二羟基二过碘酸合镍(IV)钾本课题组实验室自制;甲基丙烯酸甲酯(≥99.5%)分析纯,天津致远化学试剂有限公司,重蒸后使用;丙酮(≥99.5%)分析纯,天津致远化学试剂有限公司,重蒸后使用;二甲基亚砜(DMSO)分析纯,用氢化钙加热回流,然后在氮气保护下减压蒸馏[11]。
Brookhaven 90Plus激光粒度/Zeta电位分析仪美国Brookhaven公司;H600透射电子显微镜日本Hitachi公司;1100型高效液相色谱仪(四元梯度泵,手动进样,Angilent工作站)美国Angilent公司;BK30低温高速离心机德国Sigma公司;FTIR-8400傅里叶变换红外光谱仪日本Shimadzu公司;AE240十万分之一电子天平瑞士Mettler公司;KQ-100超声波清洗机昆山超声仪器厂;LS-3000光照实验仪北京天星科仪科技公司;集热式磁力搅拌器(水浴油浴两用锅)力辰仪器科技有限公司;MD10透析袋截留相对分子量14000,北京瑞达恒辉科技发展有限公司。
1.2实验方法
1.2.1淀粉接枝共聚物的制备制备方法参照文献[12]略改进,一个500 mL的三颈烧瓶,配备温度计、磁力搅拌器和通氮气装置,在水浴中进行温度控制。先加入淀粉2.88 g,170 mL蒸馏水,在搅拌下加热到90 ℃保持30 min,然后冷却到35 ℃,并用N2吹泡30 min,以去除体系中的氧气。加入甲基丙烯酸甲酯1 mL后滴加2 mL引发剂,反应在35 ℃条件下持续5 h,确保反应完全。得到的产物反复用去离子水洗3次除去未反应的淀粉,将干燥后的产物放入索氏提取器中,用丙酮室温条件下提取48 h,以完全除去其中的均聚物聚甲基丙烯酸甲酯。真空冷冻干燥后的产物备用。
1.2.2空白纳米粒的制备用透析法制备淀粉纳米粒[13]。精密称取接枝聚合物2.3 mg溶解在1.65 mL DMSO中,持续搅拌,使之溶解,加入透析膜,用去离子水进行透析。透析介质在开始后3 h,每小时换一次,之后每5 h更换一次,共透析24 h。得到的纳米粒溶液,滴加0.1%三聚磷酸钠溶液0.25 mL,保持15 min,以使纳米粒稳定,真空冷冻干燥,备用。
1.2.3虾青素纳米粒的制备[13]精密称取淀粉纳米粒23 mg溶解在16.5 mL DMSO中,持续搅拌,使之溶解。将虾青素0.17 mg溶于4 mL丙酮中,混合后加入透析膜,用去离子水进行透析。透析介质前3 h,每小时换一次,之后每5 h更换一次,共透析24 h,得到虾青素纳米粒溶液。
1.2.4纳米粒的红外光谱采用溴化钾压片法制备样品,室温扫描测定,扫描范围400~4000 cm-1。
1.2.5纳米粒的粒径分布室温条件下,将空白纳米粒和虾青素纳米粒的混悬液,分别加入去离子水稀释10倍,置激光粒度分析仪中测定纳米粒的粒径,测定条件:散射角为90°,测定温度为室温。
1.2.6透射电子显微镜(TEM)取少量纳米粒混悬液滴至铺有碳膜的铜网上,静置5 min后滴加2%磷钨酸染色,自然晾干后,于透射电子显微镜下观察纳米粒形态。
1.2.7虾青素的测定虾青素的含量测定按文献[14]方法进行:0.5 mL的样品加入到2 mL(50∶50 v/v)二氯甲烷和甲醇的混合液。密闭条件下搅拌15 min,之后在室温下离心5 min(800×g)。此提取程序重复2次,合并提取液,然后用滤膜过滤(4 mm,0.45 μm),取上清液进样测定。色谱条件:色谱柱:Extend-C18柱(4.6 mm×150 mm,5 μm);流动相:甲醇∶二氯甲烷∶乙腈∶水(85∶5∶5∶5);检测波长480 nm;流速1.0 mL/min;柱温为室温;进样量为20 μL,以虾青素浓度c为横坐标,峰面积A为纵坐标进行线性回归,得到回归方程A=156.38c-41.72,r=0.9998,线性范围0.6~19 μg/mL。
1.2.8光照条件下虾青素纳米粒的稳定性参照文献方法[15]并进行改进,取10 mL虾青素纳米粒溶液及虾青素丙酮溶液,浓度均为20 μg/mL,分别置于具塞比色管中,置于LS-3000光照实验仪,在室温条件下测定,调节照度为4000 LX,分别在20、40、60、80、100、120、140、160、180、200、240 min,进行取样,按1.2.7方法测定,每个样品平行3次。
1.2.9温度对虾青素纳米粒稳定性的影响[15]将虾青素的丙酮溶液及虾青素纳米粒溶液10 mL分装于具塞比色管中,分别置于30 ℃和50 ℃温度下避光水浴,分别在1、2、3、4、5、6、7、8 d取样,按1.2.7方法测吸光值。每个样品平行3次。
1.2.10pH对虾青素纳米粒稳定性的影响将6份虾青素的丙酮溶液及虾青素纳米粒溶液10 mL分装于具塞比色管中,调节其pH分别为1、3、5、7、9、11,室温避光静置24 h,按1.2.7方法测吸光值。每个样品平行3次。
1.2.11稳定性评价用虾青素保留率表示纳米粒的稳定性,虾青素保留率(%)=实验条件下虾青素的含量/实验开始时虾青素的含量。
1.2.12数据处理采用Orogin8.5及IBM SPSS 20数据分析软件对数据进行处理,运用Duncan检验进行显著性分析(p<0.05)。
2 结果与分析
2.1红外光谱
淀粉、聚甲基丙烯酸甲酯和淀粉接枝共聚物的红外光谱如图1。聚甲基丙烯酸甲酯和淀粉接枝共聚物的谱图上,在1200~1000 cm-1范围都有一个宽峰,在淀粉的详图上没有。-C=O的特征振动吸收峰1726 cm-1可以明显地在聚甲基丙烯酸甲酯和淀粉接枝共聚物的红外光谱中观察到。在约3411 cm-1处的宽峰,为淀粉上葡萄糖单元的羟基伸缩振动吸收峰。在845和755 cm-1是CH2-CH2的伸缩振动吸收峰。另外2994 cm-1和2949 cm-1处两个小峰是-OCH3和-CH两脂肪族基团吸收峰。在淀粉接枝共聚物的谱图上出现的上述新出现的吸收峰说明产物为接枝共聚物。[10]
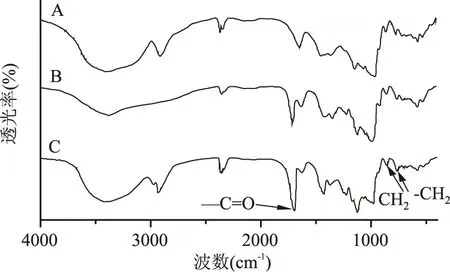
图1 红外光谱Fig.1 FTIR of starch and starch copolymer注:A:淀粉,B:聚甲基丙烯酸甲酯,C:淀粉接枝共聚物。
2.2纳米粒形态
纳米粒的透射电镜照片见图2、图3,表明制得的空白纳米粒呈现球形或类球形,形态比较均匀圆整,大小基本均一,应用软件Image J进行计算,得平均粒径为(121.5±16.8) nm;虾青素纳米粒的形态基本规整,呈球形,均匀程度要差,粒径大小差别较大,平均粒径为(208.1±26.4) nm,主要因为在负载虾青素的过程中,每个空白纳米粒与虾青素的接触机会不同,导致负载量不同,出现粒径上的差异[16]。另外从图3上可以看到电镜照片的背景有灰色斑块,是由溶液在铜网碳膜上干燥后造成,含有游离虾青素及淀粉降解产物[17]。

图2 空白纳米粒的透射电镜图(80000×)Fig.2 Transmission electron micrographs of nanoparticles(80000×)

图3 虾青素纳米粒的透射电镜图(60000×)Fig.3 Transmission electron micrographs of nanoparticles(60000×)
2.3纳米粒的粒径分布
激光粒度分析仪测得分布图见图4、图5,空白纳米粒,平均粒径为(161.8±21.8) nm,分散系数为0.112±0.016,可见分布大多集中在平均粒径附近,极少部分比较小粒径的纳米粒使分散程度变大;虾青素纳米粒的平均粒径为(296.7±29.6) nm,分散系数为0.284±0.035,分布图上816 nm附近出现的小峰,可能是由于纳米粒低程度聚集或是不均匀形成,导致分散程度加大,这和透射电镜照片看到的情况相符合。纳米粒负载后分布变宽,在其它的载体也是普遍存在的。另外,粒径分布图比电镜照片得到的尺寸更大,是由于不同的测定条件导致的[18]。
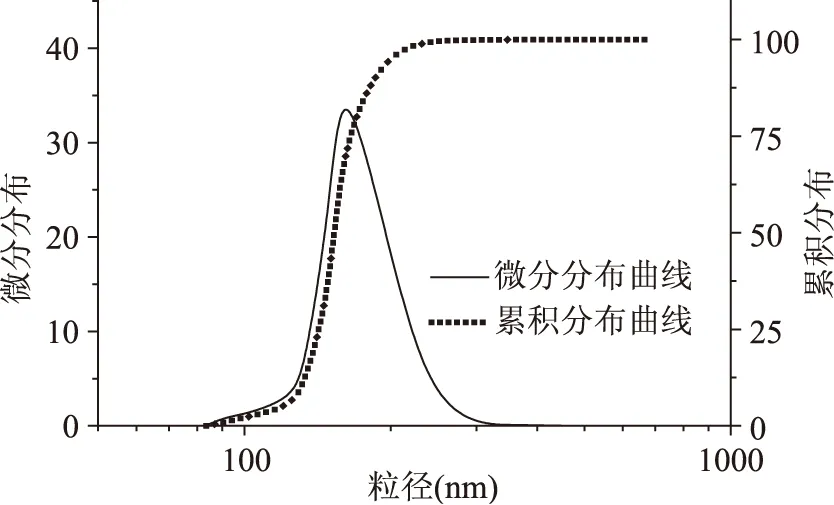
图4 空白纳米粒的粒径分布Fig.4 The size distributions of blank nanoparticles
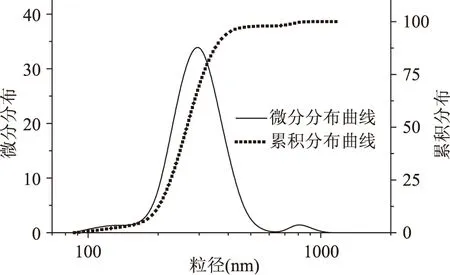
图5 虾青素纳米粒的粒径分布Fig.5 The size distributions of nanoparticles
2.4光照条件下虾青素纳米粒的稳定性
由图6可见,在光射条件下,虾青素溶液受光照影响较大,大量发生反应而降解,随时间的延长,含量逐步下降,在4 h后样品中的虾青素保留率低至16.66%。主要原因是虾青素在光直射条件下,分子很容易被激发,发生脱氢反应,生成类胡萝卜自由基阳离子,而自由其生成后很容易诱发其他的虾青素分子发生降解[19]。纳米粒中虾青素保留率的变化趋势与在丙酮溶液中相同,时间越长,分解的虾青素越多,但程度比虾青素丙酮溶液低,4 h后虾青素保留率为26.34%,提高了58.1%。这主要由于纳米粒具有表面与界面效应,具有吸收光子能量及吸收部分自由基的特性,减弱了光化学反应[20]。
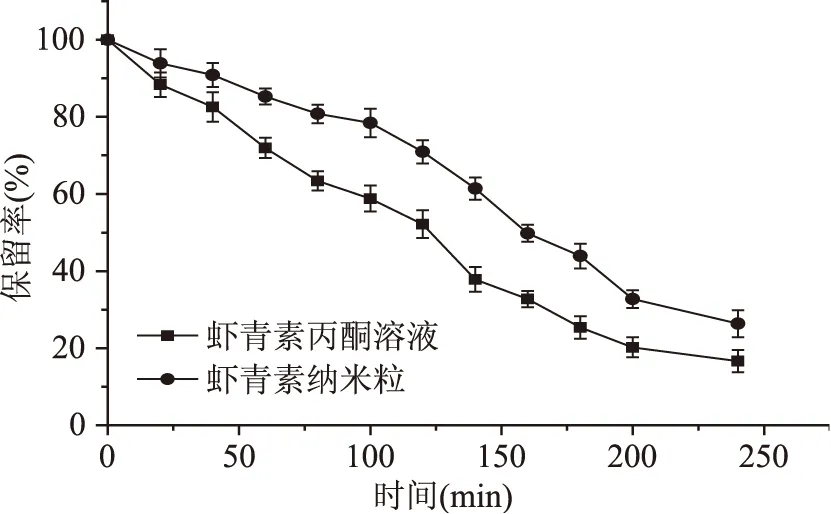
图6 光照对稳定性的影响Fig.6 Effect of light on the stability
2.5温度对虾青素稳定性的影响
图7为虾青素的丙酮溶液和虾青素纳米粒的避光条件下的耐热曲线。由图7可知,随着贮藏时间的延长,虾青素丙酮溶液中含量逐渐下降,30 ℃和50 ℃恒温避光下,贮存8 d时虾青素保留率分别为87.55%和75.35%;温度越高,含量越低,表明温度对虾青素的稳定性影响较大,温度增加促进虾青素的分解[21]。虾青素受热分解是一个复杂的过程,但有两个主要的反应:异构化和氧化[22],温度升高使其异构化和氧化加剧。在相同的条件下纳米粒中的虾青素贮存8 d时保留率分别为91.81%和83.44%,分别比丙酮溶液的保留率提高了4.87%和10.7%。其稳定性得到显著改善(p<0.05),主要是纳米粒所具有的纳米效应,使虾青素得到了有效的保护[21]。
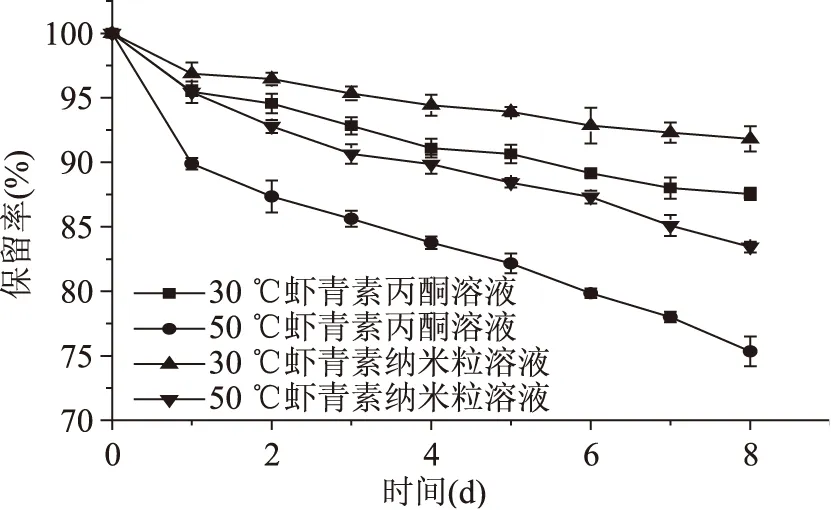
图7 温度对稳定性的影响Fig.7 Effect of temperature on the stability
2.6pH对虾青素稳定性的影响
图8为虾青素的丙酮溶液和虾青素纳米粒的避光条件下的pH曲线。由图8可见,虾青素的丙酮溶液和虾青素纳米粒溶液,都显示出在较低的pH条件下更稳定,但由于酸度过大,稳定性有下降的趋势。这是由于在过于酸性或碱性条件下,容易导致虾青素分子中双键异构化,而使虾青素功能基团失效[23]。在各pH条件下虾青素负载于纳米粒,保留率平均值为86.18%,稳定性虽有提高,但保留率仅平均提高5.86%,主要是因为在溶液中,H+和OH-会向纳米粒内扩散,扩散平衡后,对于纳米粒内的虾青素的影响与在丙酮溶液中虾青素基本相同。
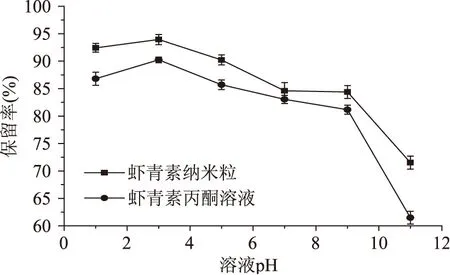
图8 pH对稳定性的影响Fig.8 Effect of pH on the stability
3 结论
红外光谱表明,利用二羟基二过碘酸合镍(IV)钾为引发剂,制备得到的产物为淀粉接枝聚甲基丙烯酸甲酯,该方法具有反应条件温和的特点,同样适用于其它的天然高分子材料用于制备纳米粒。
空白纳米粒及虾青素纳米粒的形态都基本规整,呈球形,粒径分别为(121.5±16.8) nm和(208.1±26.4) nm,纳米粒负载虾青素后,粒度虽比空白纳米粒大,但仍在纳米级别;粒径分散系数分别为0.112±0.016和0.284±0.035,虾青素纳米粒的分布也明显变宽。
纳米粒具有更大的比表面积,对包载其中的虾青素具有保护作用,所以虾青素纳米粒在各种条件下,都比虾青素丙酮溶液稳定。尤其在光照条件下最为明显,4 h光照后,虾青素纳米粒保留率26.34%,比虾青素丙酮溶液的保留率16.66%提高了58.1%;30 ℃和50 ℃恒温避光下,贮存8 d时虾青素纳米粒的保留率91.81%和83.44%,比丙酮溶液保留率87.55%和75.35%,分别提高了4.87%和10.7%;在不同的pH条件下,保留率平均提高了5.86%。
淀粉资源丰富,成本低,有利于开发制备虾青素相关产品,延长其存贮时间及提高产品的质量,具有较好的应用前景。
[1]Zhang L,Wang H. Multiple Mechanisms of Anti-Cancer Effects Exerted by Astaxanthin[J]. Marine Drugs,2015,13(7):4310-4330.
[2]Wu H,Niu H,Shao A,et al. Astaxanthin as a Potential Neuroprotective Agent for Neurological Diseases[J]. Marine Drugs,2015,13(9):5750-5766.
[3]Wan B,Li J,Zhao Y,et al. Applications of micro/nano-encapsulation technology on improving the solubility and stability of astaxanthin[J]. Science & Technology of Food Industry,2014,35(23):382-386.
[4]Bustamante A,Masson L,Velasco J,et al. Microencapsulation of H. pluvialis oleoresins with different fatty acid composition:Kinetic stability of astaxanthin and alpha-tocopherol[J]. Food Chemistry,2016,190:1013-1021.
[5]石佳,辛嘉英,王艳,等. 酯化改性淀粉研究进展[J]. 食品工业科技,2014,35(2):395-399.
[6]Pagels RF,Prud’homme RK. Polymeric nanoparticles and microparticles for the delivery of peptides,biologics,and soluble therapeutics[J]. Journal of Controlled Release,2015,219:519-535.
[7]Liu YH,Zhang AQ,Li JB,et al. Graft copolymerization of methyl acrylate onto cellulose by potassium diperiodatonickelate(IV)initiating system[J]. Journal of Polymer Materials,2004,21(2):189-195.
[8]祖国胤,丁桦. 材料现代研究方法实验指导书[M]. 北京:冶金工业出版社,2012.
[9]李文凯,吴玉新,黄志民,等,激光粒度分析和筛分法测粒径分布的比较[J]. 中国粉体技术,2007,22(5):10-13.
[10]Liu YG,Liu XH,Deng KL,et al. Graft copolymerization of methyl acrylate onto poly(vinyl alcohol)initiated by potassium diperiodatonickelate(IV)[J]. Journal of Applied Polymer Science,2003,87(3):529-534.
[11]程能林. 溶剂手册[M]. 北京:北京化工出版社,1994:37-40.
[12]Shalviri A,Chan HK,Raval G,et al. Design of pH-responsive nanoparticles of terpolymer of poly(methacrylic acid),polysorbate 80 and starch for delivery of doxorubicin[J]. Colloids and Surfaces B-Biointerfaces,2013,101:405-413.
[13]Simi CK,Emilia Abraham T. Hydrophobic grafted and cross-linked starch nanoparticles for drug delivery[J]. Bioprocess Biosyst Eng,2007,30(3):173-180.
[14]Anarjan N,Tan CP. Developing a three component stabilizer system for producing astaxanthin nanodispersions[J]. Food Hydrocolloids,2013,30(1):437-447.
[15]宋素梅,刘富俊,姜启兴,等. 南极磷虾虾壳中虾青素稳定性的研究[J]. 食品工业科技,2012,33(18):96-98,102.
[16]Steichen SD,Caldorera-Moore M,Peppas NA. A review of current nanoparticle and targeting moieties for the delivery of cancer therapeutics[J]. European Journal of Pharmaceutical Sciences,2013,48(3):416-427.
[17]Bodnar M,Hartmann JF,Borbely J. Preparation and Characterization of Chitosan-Based Nanoparticles[J]. Biomacromolecules,2005,6(5):2521-2527.
[18]Jiang X,Xin H,Gu J,et al. Enhanced Antitumor Efficacy by D-Glucosamine-Functionalized and Paclitaxel-Loaded Poly(Ethylene Glycol)-Co-Poly(Trimethylene Carbonate)Polymer Nanoparticles[J]. Journal of Pharmaceutical Sciences,2014,103(5):1487-1496.
[19]Anarjan N,Tan CP. Effects of Storage Temperature,Atmosphere and Light on Chemical Stability of Astaxanthin Nanodispersions[J]. Journal of the American Oil Chemists Society,2013,90(8):1223-1227.
[20]Zhang WT,Yu SX,Liu W,et al. "Pulling" pi-conjugated polyene biomolecules into water:enhancement of light-thermal stability and bioactivity by a facile graphene oxide-based phase-transfer approach[J]. Rsc Advances,2014,4(90):48765-48769.
[21]Ambati RR,Phang SM,Ravi S,et al. Astaxanthin:Sources,Extraction,Stability,Biological Activities and Its Commercial Applications-A Review[J]. Marine Drugs,2014,12(1):128-152.
[22]Bustos-Garza C,Yanez-Fernandez J,Barragan-Huerta BE. Thermal and pH stability of spray-dried encapsulated astaxanthin oleoresin from Haematococcus pluvialis using several encapsulation wall materials[J]. Food Research International,2013,54(1):641-649.
[23]Villalobos-Castillejos F,Cerezal-Mezquita P,Hernandez-De Jesus ML,et al. Production and stability of water-dispersible astaxanthin oleoresin from Phaffia rhodozyma[J]. International Journal of Food Science and Technology,2013,48(6):1243-1251.
Characterization and stability of the starch nanoparticles loaded with astaxanthin
LIU Zhan-jun1,CUI Cheng-long1,2,LI Zhi-wei1,GENG Xu-fang1,ZHAO Lin-lin1,ZHAO Ning1
(1.North China University of Science and Technology,Tangshan 063009,China;2.China Pharmaceutical University,Nanjing 211198,China)
In order to improve the stability of astaxanthin,the starch-graft-poly(methyl methacrylate)nanoparticles were synthesized,and then nanoparticles loaded with astaxanthin were prepared by the dialysis method. IR spectra of the starch and the graft copolymer,the average particle size,particle size distribution,and morphology of the nanoparticles loaded with astaxanthin were measured. The stability of nanoparticles loaded with astaxanthin was determined with an acetone solution of astaxanthin as a comparison. The results showed that the average particle size and polydispersity indexof staxanthin nanoparticles were(208.1±26.4) nm and 0.284±0.035 respectively. The astaxanthin retention rate of nanoparticles was 26.34% after 4 h under artificial lighting.It was 91.81% and 83.44% after storage 8 days at 30 ℃ and 50 ℃ respectively,in the dark under same temperature conditions.It was 86.18% on average at pH1,3,5,7,9 or 11 conditions.
astaxanthin;nanoparticles;starch;poly methyl methacrylate(PMMA)
2016-02-22
刘占军(1967-),男,博士,副教授,研究方向:药用辅料制备及天然高分子材料改性,E-mail:liuzhanjun815@163.com。
河北省自然科学基金(H2013209192)。
TS201.1
A
1002-0306(2016)16-0084-05
10.13386/j.issn1002-0306.2016.16.008

