铵盐钙盐除杂制备高纯二氧化硅
刘晓红,张 琪
(南昌大学资源环境与化工学院,南昌 330031)
铵盐钙盐除杂制备高纯二氧化硅
刘晓红,张琪
(南昌大学资源环境与化工学院,南昌330031)
以磷肥生产过程中的副产物氟硅酸为原料制备高纯二氧化硅。氟硅酸与氨水反应,得到氟硅酸铵溶液,加入铵盐沉淀钙镁离子,再加入钙盐沉淀铝铁离子,静置后过滤得到净化的氟硅酸铵溶液;将净化液氟硅酸铵与氨水反应生成二氧化硅沉淀,经过滤、热洗、干燥、煅烧,得到高纯二氧化硅。样品SiO2符合国标要求。实验表明,以氟硅酸制备高纯二氧化硅工艺可行。工艺特点是将低附加值的氟硅酸转化为高附加值的高纯SiO2,铵盐钙盐除杂适宜,反应步骤少、过程简单、操作条件温和。
氟硅酸;氨水;铵盐;钙盐;高纯SiO2
.
1 引 言
高纯二氧化硅(SiO2)是一种纯度极高、杂质极少,耐高温、耐酸碱、电绝缘性良好的精细化工产品,是国防军工、宇航、电子、光学仪器、光纤通讯、激光等高科技领域的一种基础原材料。用途不同,对高纯SiO2质量要求也不同。
磷肥生产过程中产生副产品氟硅酸,浓度8wt%~12wt%、16wt%~25wt%不等。低浓度的氟硅酸,多数工厂直接排放;较高浓度的氟硅酸用来制备氟硅酸钠、氟化铝等,但未给企业带来较高的经济效益。氟硅酸的排放,造成生态危害、水体污染,还浪费了氟、硅资源。回收利用氟硅酸制备SiO2的方法[1]有:氟硅酸氨化法,氟硅酸盐法,氟硅酸浓硫酸法,氟硅酸碳酸氢铵法[2]。氟硅酸氨化法是氟硅酸先经过脱色、脱砷、除磷、除硼以及过滤等除杂纯化,后与氨反应得到高纯二氧化硅。优点是工艺比较简单,产物品质较好。氟硅酸盐法是H2SiF6经过一系列除杂精制后与NaCl反应、NaOH反应,得SiO2。优点是成本较低,得到了SiO2和NaF,缺点是使用的盐等原料会降低SiO2品质。氟硅酸浓硫酸法得到的二氧化硅品质较低。氟硅酸碳酸氢铵法是氟硅酸氨化净化,碳酸氢铵重结晶净化,得到高纯二氧化硅。
本文以氟硅酸和氨水为原料,铵盐钙盐除杂制备高纯SiO2。工艺特点:铵盐钙盐除杂,是一种新的净化方法;产物SiO2纯度高;除杂过程简单,易操作;能处理磷肥工业杂质含量高的氟硅酸;制备高附加值的高纯SiO2或高纯氟硅酸铵产品。
2 实 验
2.1原料、试剂和仪器
原料氟硅酸取自某磷肥生产的副产物,氟硅酸中含H2SiF6=23.1wt%,P2O5=122 μg·g-1,密度1.21 g/cm3,主要杂质含量见表1。

表1 氟硅酸主要杂质含量
试剂:氨水、铵盐、钙盐规格均是AR、天津市大茂化学试剂厂。自制蒸馏水。
仪器:恒温水浴装置,BILON-CX-101型,金坛市富华仪器有限公司;搅拌器,JJ-1型,江苏姜堰市银河仪表厂;循环水真空泵,SHZ-D型,巩义市英峪予华仪器厂;pH计,PHS-3E,上海精密科学仪器有限公司;数显鼓风干燥箱,GZX-9140MBE型,上海博迅实业有限公司;马弗炉,SRJX-4-13型,天津电炉厂。
2.2基本原理
氟硅酸和氨水中和反应生成氟硅酸铵:
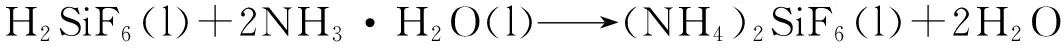
(1)
搅拌下,在氟硅酸铵溶液中加入铵盐、钙盐除杂,有白色沉淀生成,过滤得净化的氟硅酸铵溶液。
氟硅酸铵再和氨水反应,生成SiO2沉淀和氟化铵:
(2)
2.3工艺流程和实验步骤

图1 制备高纯二氧化硅工艺流程Fig.1 Process flow chart of high-purity silicon dioxide
氨水既是原料,也是调节料液pH值的碱液。
中和反应:塑料烧杯中,加蒸馏水稀释H2SiF6至一定浓度,置于恒温水浴,搅拌,常温下滴加NH3·H2O反应,测浆液pH值,至pH=3.5~4.0为反应终点,停止加氨水。得到(NH4)2SiF6溶液。
除杂:搅拌条件下,在(NH4)2SiF6溶液中加入铵盐,至溶液pH=6.0~6.5;后加入一定量钙盐,搅拌30 min后静置,滤去碱渣,得到净化的(NH4)2SiF6溶液。
制备高纯SiO2:塑料烧杯中加入部分净化的(NH4)2SiF6溶液作底液(以浸没搅拌桨叶为准),置于恒温水浴中,搅拌下加热至一定温度,分别滴入余下的(NH4)2SiF6净化液和NH3·H2O,至pH=9~10后停止加NH3·H2O,再搅拌反应40 min,过滤,滤饼洗涤3次。滤液收集。将滤饼放入烧杯中,加蒸馏水,加热,搅拌热洗1 h,趁热真空抽滤分离、干燥、煅烧。
2.4分析检测
用P-E3030 原子吸收分光光度计检测金属杂质含量。
2.5红外光谱分析
采用美国热电尼高力公司Nicolet380型傅立叶变换红外光谱仪分析SiO2样品,KBr制片,扫描范围4000~400 cm-1。
3 结果与讨论
原料H2SiF6是磷肥工业的副产物,带有杂质。中和反应后,对氟硅酸铵溶液除杂,否则杂质进入产品SiO2中,采用铵盐、钙盐除杂。选择除杂物质的原则是既能去除杂质,又不能引入新的杂质。
3.1铵盐除杂
为了考察铵盐的除杂效果,在中和反应后的氟硅酸铵溶液中加入铵盐,不加入钙盐。H2SiF6浓度稀释至8.5wt%,加25%氨水反应至料液的pH=3.7。室温下,在反应液中加入一定量的铵盐,静置后过滤,去滤渣。检测未加铵盐和加了铵盐的氟硅酸铵溶液中的杂质含量,结果如下。

表2 铵盐对氟硅酸铵溶液的除杂效果
从表2可知,加入铵盐m(铵盐)∶m(H2SiF6折100%计)=25wt%,氟硅酸铵溶液中Ca离子从50.4 μg·g-1下降到小于1 μg·g-1,钙净化率98%;Mg离子从4.2 μg·g-1下降到小于1 μg·g-1,镁净化率>76%;钙镁离子生成沉淀,氟硅酸铵溶液中钙镁金属杂质被除去。
加入铵盐(碳酸铵、或硫酸铵、或磷酸铵、或氟化铵等),pH=6.0~6.5,铵盐中的碳酸根、或硫酸根、或磷酸根、或氟离子和溶液中的钙、镁离子生成难溶性的钙盐、镁盐,从而除去了溶液中的钙镁离子。25℃下,部分钙、镁盐的溶度积如下:CaCO3的溶度积8.7×10-9;CaSO4的溶度积4.93×10-5;Ca3(PO4)2的溶度积2.07×10-33;CaF2的溶度积2.6×10-5;MgF2的溶度积6.4×10-9。这些钙镁盐的溶度积很小,属难溶盐,故溶解度很小,所以溶液中钙镁离子被除去。铵盐除杂去除钙镁。
3.2钙盐除杂
在中和反应后的氟硅酸铵溶液中先加入铵盐,不过滤,再加入钙盐除杂,实验研究了加钙盐对氟硅酸铵溶液纯度的影响。实验条件:H2SiF6浓度8.5wt%,m(铵盐)∶m(H2SiF6折100%计)=25wt%。

表3 钙盐对氟硅酸铵溶液的除杂效果
在氟硅酸铵溶液中加入钙盐,溶液呈乳白色,有白色碱渣生成。加入m(钙盐):m(H2SiF6折100%计)=7.5wt%时,氟硅酸铵溶液中的Fe、Al生成沉淀,过滤后,滤液中的Fe=2 μg·g-1,Al<1 μg·g-1,钙盐除杂,铝铁净化率96%。pH=6.0~6.5,添加钙盐(硫酸钙、或氢氧化钙等),形成了难溶的氟化钙为主的沉淀物质,氟硅酸铵溶液中溶解的Al、Fe络盐成分,也形成了难溶的金属化合物,与氟化钙及铵盐除杂形成的钙镁难溶盐一起共沉,生成吸附状的淤泥。固液分离后,得到了精制的氟硅酸铵溶液。钙盐除杂去除铝铁。
3.3 H2SiF6浓度对SiO2纯度的影响
实验条件:m(铵盐)∶m(H2SiF6折100%计)=25wt%,m(铵盐)∶m(H2SiF6折100%计) = 7.5wt%。加蒸馏水稀释H2SiF6,不同氟硅酸浓度下实验,氟硅酸浓度对样品SiO2纯度的影响如下。

表4 氟硅酸浓度对样品SiO2品质的影响
表4,H2SiF6浓度8.5wt%时,SiO2中杂质含量<1.5μg·g-1,得率95.6%;H2SiF6浓度17wt%时,SiO2中杂质含量2.9 μg·g-1,得率94.1%。这是因为,氟硅酸浓度高,夹带的杂质密集,铵盐钙盐除杂时,净化效果差些,致使高纯SiO2夹带杂质含量相应高一点。氟硅酸经蒸馏水稀释后浓度低,带入的杂质分散大,与铵盐钙盐接触充分,除杂效果好些,得到的SiO2纯度高些。
3.4样品SiO2纯度
实验得到的样品SiO2质量如表5。

表5 SiO2中主要杂质含量

图2 样品SiO2的IR光谱图Fig.2 IR pattern of sample SiO2
所得样品SiO2金属杂质含量小于2 μg·g-1,达到国标GB/T 20020-2005要求。
3.5SiO2的红外表征
图2为样品SiO2的红外光谱图。
图2,波数3438.51 cm-1是SiO2中所含水分子、表面吸附水及结晶水的吸收峰;SiO2特征吸收峰出现在1629.58 cm-1、1105.03 cm-1、808.88 cm-1和470.55 cm-1处,1105.03 cm-1处为Si-O-Si键反对称伸缩振动峰,470.55 cm-1为Si-O键弯曲振动峰。经红外光谱检测确定样品是SiO2。
综上所述,该工艺过程简单,原料易得,反应条件温和,能耗较低,成本低,具有良好的经济效益。
4 结 论
以磷肥工业副产H2SiF6为原料,加NH3·H2O两步反应,采用铵盐钙盐除杂,得到了高纯SiO2,高纯SiO2达国标GB/T 20020-2005要求。表明铵盐、钙盐选择正确,加入量适宜,未带入新的杂质。铵盐加入量m(铵盐)∶m(H2SiF6折100%计)=25wt%,钙净化率98%,镁净化率>76%;钙盐加入量m(铵盐)∶m(H2SiF6折100%计)=7.5wt%,铝铁净化率96%。
[1]应盛荣,姜战.以氟硅酸制备高纯石英砂的技术与工艺[J].化工生产与技术,2013,20(4):27-30.
[2]刘晓红,卢爱军,刘燕燕,等.用氟硅酸制备高纯二氧化硅[J].化工时刊,2002,(1):32-34.
Producing High Purity Silicon Dioxide Using Ammonium Salt and Calcium Salt to Remove Impurities
LIU Xiao-hong,ZHANG Qi
(School of Resource Environmental and Chemical Engineering,Nanchang University,Nanchang 330031,China)
High purity SiO2was prepared with Fluosilicic acid as the raw material,which is the by-product of the production of phosphate fertilizer. Fluosilicic acid reacts with ammonia to obtain Ammonium fluosilicate solution,and add ammonium salt in it to precipitate calcium and magnesium ions,and calcium salt to precipitate iron and aluminum ions,after standing for a while,filter it to obtain purified ammonium fluorosilicate solution. It reacts with ammonia to form SiO2precipitate. High purity SiO2will be obtained after filtration,hot washing,drying and calcination. The SiO2precipitate meets the national standard. The experiment result shows that it is feasible to use Fluosilicic acid to get high-purity silicon dioxide. The characteristics of this process are as follows,first it can convert low value-added fluorine acid to high value-added high-purity SiO2,then it is appropriate to remove impurities by ammonium salt and calcium salt; at last,there are just few steps,simple process and mild reaction condition.
fluorosilicic acid;ammonia;ammonium salt;calcium salt;high-purity silicon dioxide
刘晓红(1963-),女,教授.主要从事化工过程新工艺、新技术开发方面的研究.
TQ173
A
1001-1625(2016)02-0651-04

