伴有肾脏损伤及其高危风险的慢性乙型肝炎患者抗病毒治疗专家共识
中华医学会肝病学分会
伴有肾脏损伤及其高危风险的慢性乙型肝炎患者抗病毒治疗专家共识
中华医学会肝病学分会
1 前言
*2015年版多个乙型肝炎防治指南推荐慢性乙型肝炎患者在抗病毒治疗前后应监测肾脏功能相关指标。
*对于具有肾脏损伤风险以及合并肾脏损伤的慢性乙型肝炎患者提出了推荐治疗方案的意见和药物。
2015年版亚太肝脏研究协会(Asian Pacific Association for the Study of the Liver,APASL)《亚太乙型肝炎临床管理指南》、2015年版中国《慢性乙型肝炎防治指南》以及2015年版世界卫生组织(World Health Organization,WHO)《慢性乙型肝炎感染预防、管理和治疗指南》均提出慢性乙型肝炎(chronic hepatitis B,CHB)患者在治疗前后应定期监测肾脏功能相关指标,同时对于具有肾脏损伤风险以及合并肾脏损伤的CHB患者提出了推荐治疗方案的意见和药物。2015年版中国慢性乙型肝炎防治指南在特殊人群抗病毒治疗推荐意见部分,关注了存在肾脏损伤的特殊患者,提出对于已经存在肾脏疾患及其高危风险的CHB患者,应尽可能避免应用阿德福韦酯(Adefovir dipivoxil,ADV)或替诺福韦酯(Tenofovir dipivoxil,TDF);对于存在肾脏损伤风险的CHB患者,推荐使用恩替卡韦或替比夫定治疗。本共识旨在为合并肾脏损伤及其高危风险的中国CHB患者,提供基于循证医学的推荐意见,以更好地指导临床实践。
2 流行病学
*CHB患者发生肾脏损伤的风险较普通患者高。
*存在肾脏损伤及高危风险的CHB患者若未能及时进行有效治疗,部分患者最终可发展为终末期肾病。
*长期ADV或TDF治疗可能导致低血磷、肾功能不全和骨软化症。
根据2006年全国流行病学调查数据,1~59岁一般人群HBsAg携带率为7.18%,CHB患者约2 000万例。我国成人慢性肾脏病(chronic kidney disease,CKD)患病率约为10.2%~11.3%,推算成人CKD患者超过1.2亿人[1]。
CHB患者发生肾脏损伤的风险较普通患者更高,临床医生应对CHB患者的肾脏损伤情况给予特别关注。伴ALT升高的HBV感染者发生肾小球滤过率(glomerular filtration rate,GFR)下降或CKD几率高于正常人。Cai J[2]开展的一项大型横断面研究,纳入6 854例中国成人,评估HBV感染与肾功能和蛋白尿的相关性,伴ALT升高的HBV感染患者估算肾小球滤过率(estimate glomerular filtration rate,eGFR)下降(eGFR<60 ml/min/1.73m2)约为无HBV感染患者的4.07倍。在台湾进行的一项队列研究[3],纳入慢性HBV感染且未使用核苷(酸)类似物治疗的17 758例成人患者和未感染HBV的71 032例成年人,结果HBV感染者CKD的发生率显著高于未感染HBV者。
存在慢性肾脏损伤及高危风险的CHB患者若未能及时进行有效治疗,部分患者最终可发展为终末期肾病(end stage renal disease,ESRD)。ESRD的高致残率和高病死率不仅危害大,而且其治疗费用高昂[4]。流行病学调查显示[5],40岁以上人群CKD患病率达9.4%,据此推算我国40岁以上人群CKD患者达4 400万,如果其中1%发展为ESRD而需要血液净化治疗,则每年需要医疗费用达500亿元人民币。
来自中国乙型肝炎随访与临床科研平台(CR-HepB)2014年12月的数据显示:由于上市时间、价格等原因,在口服核苷(酸)类似物抗病毒治疗的CHB患者中,31.66%接受ADV治疗,接受恩替卡韦(Entecavir,ETV)、拉米夫定(Lamivudine,LAM)、替比夫定(Telbivudine,LdT)、TDF治疗的比例分别为30.56%、6.71%、10.57%和0.45%[6]。而长期ADV或TDF治疗有的会导致近端肾小管损伤,可能引起低血磷、骨软化症等[7,8,9]。ADV或TDF治疗2~9年,约15%患者发生肾小管损伤[10]。接受ADV单药治疗5年的CHB患者(51.4%为代偿性肝硬化)肾脏损伤(eGFR的下降程度大于20%以上)累计发病率可达34.7%[11]。对TDF临床3期试验纳入患者的8年研究结果显示[12],患者出现血肌酐较基线升高≥0.5 mg/dL的发生率为2.2%,血磷<2.0 mg/dL的发生率为1.7%。
3 治疗前评估
*CHB患者接受核苷(酸)类抗病毒药物之前,应评估肾小球和肾小管功能。
*eGFR和蛋白尿是普通人群死亡危险的独立预测因素。
临床医生应当在CHB患者接受核苷(酸)类抗病毒药物之前,评估肾小球和肾小管功能,以便更加安全合理地制定治疗方案和随访计划。
常见肾小球功能筛查指标包括:GFR、尿蛋白/肌酐比值、24h尿蛋白定量等。GFR是指单位时间(通常为1 min)内两肾生成滤液的量。作为评估肾功能的敏感和实用指标,GFR通常通过eGFR来估算,目前主要采用CKD-EPI公式和MDRD公式计算eGFR[13]。GFR正常参考值>90 ml/min,但可随着年龄、性别、体表面积和生理状态及检测方法变化而有所不同,青年男性平均GFR为130 ml/min/1.73 m2,青年女性平均为120 ml/min/1.73 m2,波动范围在14%~18%[14]。
CKD-EPI公式:eGFR=141×选小值(血清肌酐SCr/k,1)a×选大值(SCr/k,1)-1.209×0.993年龄×1.018(若是女性)×1.159(若是黑色人种)。k在女性为0.7,在男性为0.9,a值在女性为-0.329,男性为-0.411;选小值代表选择SCr/k或1中的最小值,选大值代表选择SCr/k或1中的最大值。MDRD公式:eGFR=186x(血清肌酐)1.154x(年龄)0.203x0.742(女性)。值得注意的是,上述公式中肌酐的检测方法是不一样的,MDRD公式中肌酐是用苦味酸法检测的,而CKD-EPI则是用酶法检测的。
尿蛋白与肌酐比值测定是用于监测尿蛋白排出情况的一种新的可靠方法,这是因为尿蛋白与肌酐比值的测定,能够较为可靠地反映24小时尿蛋白量,具有快速、简便、精确的特点,可作为临床上较为理想的定性、定量诊断蛋白尿和随访的指标。用B型超声波检查肾脏,已被临床广泛应用。肾脏本身的解剖结构为B超检查提供了良好的条件,肾脏的被膜、实质、肾盂等组织结构的层次,都能用B超显示出来。B超能准确地测定肾脏的大小、位置和形态,鉴别肾脏内肿物是囊性还是实性病变,测量移植肾脏的大小和连续观察移植肾脏的变化。B超显示皮质回声增强,常常提示肾小球、肾间质或肾血管疾病,肾脏容积缩小、皮质回声增强、皮髓质分界不清常提示慢性肾脏病。
肾小管功能的检查包括尿比重、尿渗透压、尿电解质(磷、钙、钾等)、尿中小分子蛋白(微球蛋白、视黄醇结合蛋白等)、尿酶[N-乙酰-β-D-氨基葡萄糖苷酶(NAG)等]及尿糖定性检查。正常新鲜尿液呈弱酸性,pH波动于5.0~7.0,若酸中毒出现碱性尿,提示有近端肾小管性酸中毒[14]。
一项荟萃分析[15]包括检测了尿蛋白/肌酐比的14项研究共105 872例受试者,以及检测了尿蛋白的7项研究共1128 310例受试者,采用Cox比例危险模型估算与eGFR和蛋白尿相关的全因和心血管死亡危险比。结果表明eGFR和蛋白尿是普通人群中死亡危险的独立预测因素。
4 肾脏损伤高危因素
*肾脏损伤高危因素包括:慢性HBV感染、高龄、肾毒性药物、合并症。
目前,已知肾脏损伤高危因素包括:糖尿病、高血压、代谢综合征(高脂血症、高尿酸血症、肥胖等)、高龄(≥50岁)、肾脏病家族史、慢性HBV感染、肾毒性药物(抗生素、非甾体抗炎药、中草药、造影剂及化疗药物)等。我国一项纳入13 925例CKD患者(eGFR<60 ml/min/1.73m2或存在肾脏损伤标志物)的横断面研究结果表明[16]:高龄、使用过肾毒性药物、农村生活、心血管病史、高密度脂蛋白水平低于40 mg/dL、高血压是肾脏功能损伤的独立危险因素。单因素分析表明:糖尿病和腹型肥胖与eGFR<60 ml/min/1.73 m2相关,年龄越大,eGFR<60 ml/min/1.73m2的人群比率越高。随着年龄增长,GFR下降,40岁以后,年龄每增长10岁,GFR下降近10 ml/min/1.73 m2,80岁时GFR平均值几乎是青年成人的一半。对于基线eGFR<90 ml/min/1.73m2的患者,eGFR越低,发生全因及心血管死亡风险越高,发生ESRD的风险比也越高[17,18],而患者一旦发展为ESRD则后果十分严重,致残率和病死率明显增加。
5 初治C H B患者
*对于存在潜在肾脏损伤的高危风险的CHB人群建议优先选择ETV或LdT进行初始抗病毒治疗。
*初治CHB合并基线肾脏损伤的患者(eGFR<90 ml/min/1.73m2),根据现有循证医学的数据,推荐选用ETV或LdT抗病毒治疗,选用LdT时还可通过路线图管理减少远期耐药情况的发生。
*凡具有上述之一者,应避免初始使用ADV和TDF治疗。
对于存在潜在肾脏损伤高危风险的CHB人群,虽然GFR没有明显的下降,但长期治疗可能导致这类患者比普通CHB患者更容易出现GFR下降[19]。2015年版中国指南和国际指南均推荐延长CHB的治疗疗程,意味着CHB患者需要接受长期抗病毒治疗,而长期治疗对患者的肾功能有更高的要求。为了保障患者能够接受足够疗程的治疗,对于伴有明显高危风险肾脏损伤的患者应当追求更高的肾脏安全性,推荐ETV或LdT作为初始抗病毒治疗药物[20]。
我国2015年CHB防治指南及国际CHB防治指南都肯定了LdT在肾功能改善方面的获益,提出LdT可能具有改善eGFR的作用。2015年APASL指南同样提出LdT具有潜在肌酐清除率改善作用[21]。ETV对CHB患者的肾功能无显著影响[22,23,24]。因此,对于初治CHB合并基线肾脏损伤的患者(eGFR<90 ml/min/1.73m2),推荐选用ETV或LdT进行抗病毒治疗。选用LdT抗病毒治疗时还可通过路线图管理减少耐药的发生。基于中国人群的一项前瞻性多中心临床试验EFFORT研究[25],根据路线图进行优化治疗,其2年结果表明,对于LdT治疗早期应答良好的患者(24周HBV DNA<300拷贝/毫升)继续单药治疗,2年耐药率为5.5%;对于LdT治疗早期应答不佳的患者(24周HBV DNA≥300拷贝/毫升),加用ADV优化治疗,2年耐药率为0.5%。应用优化治疗方案治疗,整体试验人群2年HBV DNA<300拷贝/毫升者为76.7%,耐药率为2.7%。
长期ADV或TDF治疗有的会引起近端肾小管损伤,可能导致低血磷、肾功能不全和骨软化症。因此,对于已经存在肾脏损伤及其高危风险的CHB患者,应尽可能避免初始使用ADV或TDF单药治疗。
6 经治患者
*ADV或TDF经治CHB患者若出现eGFR<90 ml/min/1.73m2或血磷、血钙进行性下降,可根据患者GFR调整抗病毒药物剂量,推荐换用LdT、ETV或联合LdT治疗,并定期监测患者HBV DNA水平。
核苷(酸)类药物在肾小管上皮细胞质内的累积可以导致线粒体细胞氧耗竭和氧化呼吸链功能障碍,从而导致肾小管上皮细胞凋亡,而且ADV的作用较TDF更强。药物导致的持续肾小管损伤可以导致肾小管细胞减少,GFR降低和肾衰竭。由核苷酸类似物导致的早期肾小管损伤,常表现为肾小管重吸收功能障碍,血磷、血钙下降,尿磷、尿钙排泄异常,尿液酸化功能异常,伴或不伴有微量蛋白尿。因此,长期接受ADV或TDF治疗的患者在治疗中应定期监测肾脏相关指标,若出现肾小球或肾小管指标异常,应综合考虑患者现状,决定应对策略。可根据GFR调整核苷(酸)类药物剂量:当GFR为30~49 ml/min时,应将药物剂量减半或隔天服药;当GFR为10~29 ml/min时,隔2天服药[26]。
对于ADV单药治疗的患者,虽发生病毒学应答,但当出现eGFR<90 ml/min/1.73m2伴或不伴有血磷、血钙降低时,建议换用ETV或LdT继续治疗;对于联合ADV治疗发生病毒学应答的患者,当出现eGFR<90ml/min/1.73m2或血磷、血钙下降时,推荐选择ADV联合LdT方案;对于TDF经治患者,推荐换用LdT、ETV或联合LdT继续治疗。Qi X[27]的一项回顾性对照研究,纳入195例ADV单药治疗且eGFR较基线下降约20 ml/min,调整为联合治疗后评估eGFR的变化。在治疗24个月时,LAM联合ADV治疗组eGFR进一步降低了10.41 ml/min,ETV联合ADV治疗组eGFR进一步降低了9.03 ml/min,而LdT联合ADV治疗组eGFR增加至15.99 ml/min,且最终eGFR水平与未接受ADV治疗组相当。结果显示无论是ETV联合ADV还是LAM联合ADV方案,均无法逆转ADV导致的eGFR下降,仅LdT联合ADV方案可逆转ADV导致的eGFR下降。一项在我国开展的前瞻性队列研究[28],共纳入275例慢性HBV感染者,接受LAM、ADV、LdT、ETV治疗,随访平均23个月结果显示:LdT较其他核苷(酸)类药物显著改善了CHB患者的eGFR,而ETV治疗组eGFR较未治疗组未发生显著的改善。
7 乙型肝炎肝硬化患者
*乙型肝炎肝硬化合并eGFR<90 ml/min/1.73m2的患者,推荐选择基于ETV或LdT的单药或联合治疗方案。
*对于年龄大于50岁的肝硬化患者,考虑到LdT对于老年患者肾脏指标的改善有效,推荐选择基于LdT或ETV的单药或联合治疗方案。
*对急性肝衰竭,亚急性肝衰竭、慢加急性肝衰竭和慢性肝衰竭患者,如果出现eGFR<90 ml/min/1.73m2或者血肌酐、尿素氮异常,可以短期换用LdT,等待患者肾功能指标平稳恢复后再酌情评估是否需要改变抗病毒治疗方案。
肝硬化和慢性HBV感染都是导致肾脏损伤的危险因素,基线GFR越低的肝硬化患者死亡风险越高,所以应该更加关注乙型肝炎肝硬化患者使用药物的肾脏毒性[29,30]。由于肝硬化人群需要长期治疗,为保障长期治疗的可行性,需要追求更高的药物肾脏安全性[20,31]。此外,乙型肝炎肝硬化患者一旦出现肾脏不良事件,危害严重,如发生肝肾综合征,预后极差,病死率极高,5 a病死率可达100%[32]。
肝硬化患者常应用袢利尿剂缓解腹水等水钠潴留症状,但是袢利尿剂常可以加重肾功能异常患者的肾脏损伤。对于必须使用这类药物的患者,在选择抗病毒治疗药物时,需要特别关注其对肾功能的影响,权衡利弊。当乙型肝炎肝硬化患者合并eGFR<90 ml/min/1.73m2时建议选择ETV或LdT治疗,以保证长期治疗的可行性和肾脏的安全性。
对于HBeAg阳性和HBeAg阴性的血清HBV DNA水平分别<1×108IU/mL或1×<106IU/mL的乙型肝炎肝硬化合并eGFR<90ml/min/1.73m2或年龄>50岁的患者,推荐选择基于LdT的单药或联合治疗方案,但应特别注意耐药的发生[33]。Lee S[34]的一项临床队列研究,纳入116例CHB患者(平均年龄54岁)接受LdT治疗,578例患者(平均年龄53岁)接受ETV治疗,至少治疗18个月。与ETV治疗组比,LdT治疗的肝硬化患者eGFR得到显著改善。一项2年随机双盲试验结果表明[35]:LdT治疗也可改善成人失代偿期乙型肝炎肝硬化患者eGFR,经LdT治疗2年后,40.7%基线eGFR 60~90 ml/min/1.73m2的患者转为eGFR>90 ml/min/1.73m2。
8 肝/肾移植患者
*接受肝移植术前,HBsAg阳性,HBV DNA检测不到的CHB患者,在术后接受激素/免疫抑制剂治疗,推荐使用ETV或LdT预防性抗病毒治疗,同时应密切监测HBV DNA水平。
*接受肾移植术前,HBsAg阳性,HBV DNA检测不到的CHB患者,在术后接受激素/免疫抑制剂治疗,考虑到患者肾功能水平,以及钙调离子抑制剂(他克莫司、环孢素A等)具有一定的肾毒性,推荐使用LdT或ETV预防性抗病毒治疗,同时应密切监测患者HBV DNA水平。
肝/肾移植患者,接受激素/免疫抑制剂治疗易出现HBV再激活,通常表现为ALT>2×ULN,HBV DNA载量上升1 log10或病毒载量大于20 000IU/ml[36,37]。HBV再激活可能引起严重肝炎,重者可为暴发型肝衰竭,导致死亡[37]。因此,推荐HBsAg阳性接受肝/肾移植患者应接受预防性核苷(酸)类似物治疗,防止HBV再激活[20,31]。
肝肾移植患者常应用钙调离子抑制剂抗排异反应,但是长期使用一线钙调离子抑制剂(他克莫司、环孢素A等)对于肾功能异常的患者可以进一步加重肾脏损伤,表现为肾小管间质损伤。多数慢性中毒者累及血管、间质,表现为血管壁结节性蛋白沉积、血管内膜增厚、管腔变窄或阻滞,因缺血而致肾小管萎缩,间质纤维化。研究显示,环孢素A肾毒性发生率可以达到30%~74%。所以,对于必须使用这类药物的患者,在选择抗病毒药物时,需要特别关注其对肾功能的影响。
ETV可预防肝移植术后CHB复发[38,39]。LdT除可用于预防肝肾移植术后CHB复发,对肝/肾移植受体具有更好的肾脏保护作用。Perrella A et al[40]选用LdT作为肝移植患者的预防性抗病毒药物,结果显示LdT预防HBV再激活安全有效,且对肾脏无任何显著有害作用,在肝移植18个月内LdT似乎具有改善患者肾功能的作用。Cholongitas E et al[41]的研究结果也显示了LdT用于肝移植受体对肾功能的改善作用。Yap DY et al[42]的研究显示LdT用于HBsAg阳性肾移植受体也具有良好的疗效和肾脏安全性。对于接受肝/肾移植术前,HBsAg阳性且HBV DNA检测不到的CHB患者,在术后接受激素/免疫抑制剂治疗,可选用LdT或ETV预防性抗病毒治疗。HBsAg阴性、抗HBc阳性受者接受HBsAg阳性供肝时,术后也应立刻进行预防性抗病毒治疗[43]。
9 肝细胞癌(hepat ocel l ul ar carci nom a,H C C)患者
*对于血清HBV DNA<1×105IU/mL的HCC患者,若同时出现eGFR<90 ml/min/1.73m2或存在肾脏损伤高危风险,推荐接受ETV或LdT治疗,并定期检测患者HBV DNA水平。
*对于年龄大于50岁的HCC患者,考虑到LdT对于老年患者肾脏指标的改善有效,推荐单药或者联合ETV或LdT治疗,并定期检测患者HBV DNA水平。
抗病毒治疗可抑制HBV复制、改善患者肝功能,减少或延缓HCC复发,延长患者生存时间[44,45]。HBV相关HCC患者只要HBV DNA可检测到,均应接受抗病毒治疗[46]。对于HBV DNA<1×105IU/mL的HCC患者,若同时出现eGFR<90 ml/min/1.73m2,推荐ETV或LdT治疗[43,47,48,49]。Wu[45]报道了台湾大型队列随访研究,评估HCC患者接受手术切除后肿瘤的复发情况,结果表明接受核苷(酸)类似物抗病毒治疗患者6年肿瘤复发率显著低于未接受核苷(酸)类似物治疗患者。Kim YW[49]的一项研究,中晚期(TNM 3/4期)且肝功能差(Child-Pugh B级/C级)的HCC患者接受LdT和ETV治疗12周和24周,LdT组病毒学应答率分别为25%和42.8%,ETV组分别为33.3%和33.3%,LdT治疗的短期疗效和ETV相当。
10 乙型肝炎相关性肾炎患者
*乙型肝炎相关性肾炎患者,由于HBV感染可导致肾脏损伤,推荐进行抗病毒治疗以缓解患者肾脏病变。乙型肝炎相关性肾炎患者不需要接受激素/免疫制剂治疗的情况下,可以参照CHB防治指南,推荐使用ETV或LdT进行抗病毒治疗。
乙型肝炎相关性肾炎是常见的继发性肾脏疾病,由HBV感染诱导的免疫反应引起。对于基线DNA>1×105IU/ml的CHB患者抗病毒治疗,可缓解乙型肝炎相关性肾炎患者的肾脏损伤。此类患者的抗病毒治疗可参考我国或APASL指南相关推荐意见,选用ETV或LdT进行抗病毒治疗。但考虑到乙型肝炎相关性肾炎已经出现了肾脏损伤,可考虑选用LdT抗病毒治疗,以保护患者的肾脏功能。
11 乙型肝炎合并其他肾脏疾病患者
*基于中国CHB防治指南和APASL指南,对于乙型肝炎合并其他肾脏疾病患者,推荐ETV或LdT治疗。肾脏疾病进展快、中度以上肾脏损伤或存在其他疑问时,应转诊到肾内科。
由于乙型肝炎合并其他肾脏疾病的患者已经出现肾脏损伤,治疗时应考虑药物对肾脏的安全性。目前,尚无循证医学证据显示ETV抗病毒治疗存在肾脏安全性问题。在临床上,有相对更多的数据支持LdT能改善eGFR[50,51]。在3期LdT临床研究中[51],评估LdT长期治疗对eGFR的作用,结果从基线到治疗4年,eGFR(MDRD公式)增加了14.9 ml/min/1.73 m2。一项临床队列研究[34],纳入116例CHB患者,分别给予LdT和ETV治疗,分析基线eGFR<90 ml/min/1. 73 m2亚组患者,结果显示LdT治疗组较ETV治疗组eGFR显著升高。因此,对于乙型肝炎合并其他肾脏疾病的患者,推荐ETV或LdT治疗。如果出现肾脏疾病进展速度快、呈中度以上肾脏损伤或存在其他疑问的情况,应及时转诊到肾内科进行诊治。
12 治疗监测
*在CHB患者接受抗病毒药物之后,临床医生应该至少每三个月对患者的肾功能进行复查和随访,尤其是对于既往接受过核苷酸类似物治疗的患者。
对于无肾脏损伤和低风险的患者,其肾功能监测的频率推荐为治疗第1年至少每3个月监测一次,此后至少每6个月复查一次,而对于具有肾脏损伤的高危因素的患者,其肾功能监测的频率推荐为每3个月监测一次。如肌酐清除率<60 ml/min或血清磷酸盐水平<2 mg/dl,则应在原有基础上增加监测频率(表1)[52]。
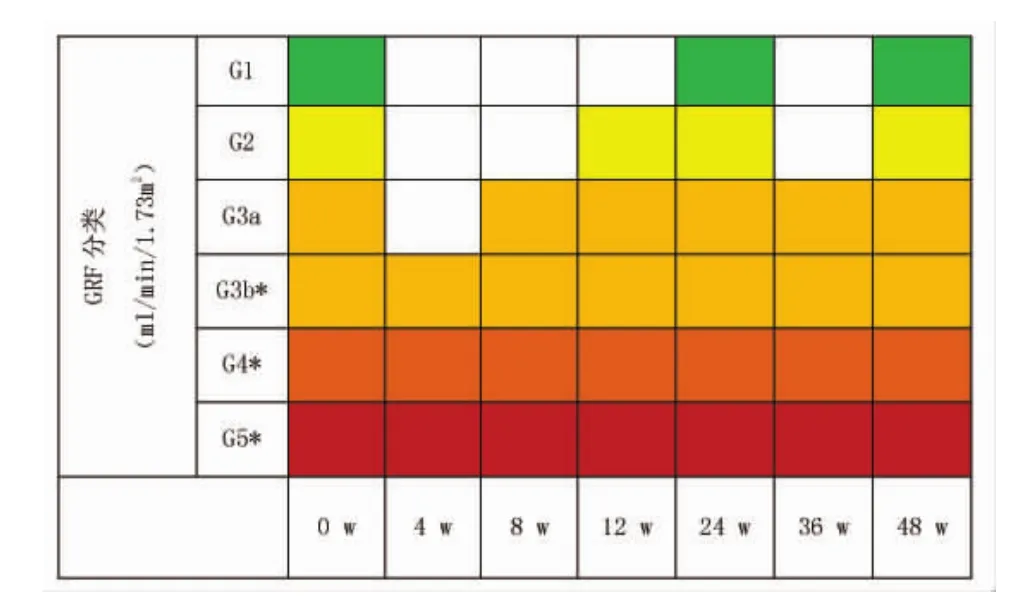
表1 依据肾功能水平推荐监测C H B患者肾功能指标的随访频率
[1]Zhang L,Wang F,Wang L,et al.Prevalence of chronic kidney disease in China:a cross-sectional survey.Lancet,2012,379 (9818):815-822.
[2]CaiJ,FanX,MouL,etal.Associationofreducedrenal function with hepatitis B virus infection and elevated alanine aminotransferase.ClinJAmSocNephrol,2012,7(10):1561-1566.
[3]Chen YC.13-year nationwide cohort study of chronic kidney diseaseriskamongtreatment-naivepatientswithchronic hepatitis B in Taiwan.BMC Nephrol,2015,16:110.
[4]陈香美,孙雪峰,蔡广研.我国慢性肾脏病防治的公共健康政策思考.中华医学杂志,2014.94(4):241-243.
[5]张路霞,左力,徐国宾,等.北京市石景山地区中老年人群中慢性肾脏病的流行病学研究.中华肾脏病杂志,2006,22:67-71.
[6]http://www.cfhpc.org/upload/ppt/20150525223338670.pdf.
[7]Fernandez-FernandezB1,Montoya-FerrerA,SanzAB,etal. Tenofovirnephrotoxicity:2011update.AIDS ResTreat,2011;2011:354908.
[8]Girgis CM,Wong T,Ngu MC,et al.Hypophosphataemic osteomalacia in patients on adefovir dipivoxil.J Clin Gastroenterol,2011,45:468-473.
[9]Hall AM,Hendry BM,Nitsch D,et al.Tenofovir-associated kidney toxicity in HIV-infected patients:a review of the evidence. Am J Kidney Dis,2011,57:773-780.
[10]Gara N,Zhao X,Collins MT,et al.Renal tubular dysfunction duringlong-termadefovirortenofovirtherapyinchronic hepatitis B.Aliment Pharmacol Ther,2012,35(11):1317-1325.
[11]Kim YJ,Cho HC,Sinn DH,et al.Frequency and risk factors of renal impairment during long-term adefovir dipivoxil treatment inchronichepatitisBpatients.JGastroenterolHepatol,2012,27(2):306-312.
[12]Marcellin P GE,Flisiak R,Trinh H,et al.Long-term treatment withtenofovirdisoproxilfumarateforchronichepatitisB infection is safe and well tolerated and associated with durable virologic response with no detectable resistance:8 year results from two phase 3 trials.Hepatology,2014,60:313A-314A.
[13]KDIGO.Chapter 1:Definition and classification of CKD.Kidney Int Suppl(2011),2013,3(1):19-62.
[14]黎磊石.中国肾脏病学.人民军医出版社,2008:14-16.
[15]Chronic Kidney Disease Prognosis Consortium,Matsushita K,van der Velde M,et al.Association of estimated glomerular filtration rateandalbuminuriawithall-causeandcardiovascular mortalityingeneralpopulationcohorts:acollaborative meta-analysis.Lancet,2010,375(9731):2073-2081.
[16]Wen CP,Matsushita K,Coresh J,et al.Relative risks of chronic kidney disease for mortality and end-stage renal disease across races are similar.Kidney Int,2014,86(4):819-827.
[17]Shin JH,Kwon HJ,Jang HR,et al.Risk Factors for renal functional decline in chronic hepatitis B patients receiving oral antiviral agents.Medicine(Baltimore),2016,95(1):e2400.
[18]Wen CP,Matsushita K,Coresh J,et al.Relative risks of chronic kidney disease for mortality and end-stage renal disease across races are similar.Kidney Int,2014,86(4):819-827.
[19]ShinJH,KwonHJ,Jang HR,etal.Riskfactorsforrenal functional decline in chronic hepatitis B patients receiving oral antiviral agents.Medicine(Baltimore),2016,95(1):e2400.delete [20]中华医学会肝病学分会和感染病学分会.慢性乙型肝炎防治指南(2015年版).实用肝脏病杂志,2016,19(3):Ⅴ-ⅩⅩⅢ.
[21]SarinSK,KumarM,LauGK,etal.Asian-Pacificclinical practice guidelines on the management of hepatitis B:a 2015 update.Hepatol Int,2016,10(1):1-98.
[22]Wu X,Cai S,2,Li Z,et al.Potential effects of telbivudine and entecavir on renal function:a systematic review and meta-analysis.Virol J,2016,13(1):64.
[23]Saadah OI,Sindi HH,Bin-Talib Y,et al.Entecavir treatment of children 2-16 years of age with chronic hepatitis B infection. Arab J Gastroenterol,2012,13:41-44.
[24]Jonas MM,Chang MH,Sokal E,et al.Randomized controlled trial of entecavir versus placebo in children with HBeAg-positive chronic hepatitis B.Hepatology,2015.doi:10.1002/hep.28015.
[25]Sun J,Xie Q,Tan D,et al.The 104-week efficacy and safety of telbivudine-based optimization strategy in chronic hepatitis B patients:arandomized,controlledstudy.Hepatology,2014,59:1283-1292.
[26 Liaw YF,Kao JH,Piratvisuth T,et al.Asian-Pacific consensus statement on the management of chronic hepatitis B:a 2012 update.Hepatol Int,2012,6(3):531-561.
[27]Qi X,Wang J,Chen L,et al.Impact of nucleos(t)ide analogue combination therapy on the estimated glomerular filtration rate in patients with chronic hepatitis B.Medicine(Baltimore),2015,94(15):e646.
[28]QiX,WangJY,MaoRC,etal.Impactofnucleos(t)ide analogues on the estimated glomerular filtration rate in patients with chronic hepatitis B:a prospective cohort study in China.J Viral Hepat,2015,22(1):46-54.
[29]蔡建芳,窦晓丽,文煜冰,等.乙型肝炎病毒相关性肾炎的相关因素分析.中华肾脏病杂志,2011,27(2):96-99.
[30]Lim YS,Larson TS,BensonJT,et al.Serum sodium,renal function,and survival of patients with end-stage liver disease.J Hepatol,2010,52(4):523-528.
[31]WHO Guidelines Approved by the Guidelines Review Committee.Guidelines for the prevention,care and treatment of persons with chronic hepatitis B infection.Geneva:World Health Organization,2015 Mar[ahead of print].
[32高宝秀,贺勇,李贵星,等.慢性重型肝炎并发肝肾综合征的相关因素分析.临床肝胆病杂志,2011,27(7):749-751.
[33]Pipili C,Cholongitas E,Papatheodoridis G.Review article:nucleos (t)ide analogues in patients with chronic hepatitis B virus infection and chronic kidney disease.Aliment Pharmacol Ther,2014,39(1):35-46.
[34]Lee S,Park JY,Song K,et al.Comparison of the effects of telbivudineandentecavirtreatmentonestimatedglomerular filtration rate in patients with chronic hepatitis B.Gut Liver,2015 May 13[ahead of print].
[35]Chan HL,Chen YC,Gane EJ,et al.Randomized clinical trial:efficacyandsafetyoftelbivudineandlamivudinein treatment-naivepatientswithHBV-relateddecompensated cirrhosis.J Viral Hepat,2012,19(10):732-743.
[36]Shouval D,Shibolet O.Immunosuppression and HBV reactivation.Semin Liver Dis,2013,33(2),167-177.
[37]MandalàM,FagiuoliS,FrancisciD,etal.HepatitisB in immunosuppressedcancerpatients:pathogenesis,incidenceand prophylaxis.Crit Rev Oncol Hematol,2013,87(1):12-27.
[38]Cholongitas E,Papatheodoridis GV.High genetic barrier nucleos (t)ide analogue(s)forprophylaxis from hepatitisB virus recurrence after liver transplantation:a systematic review.Am J Transplant,2013,13:353-362.
[39]Yi NJ,Choi JY,Suh KS,et al.Post-transplantation sequential entecavir monotherapy following 1-year combination therapy with hepatitis B immunoglobulin.J Gastroenterol,2013,48:1401-1410. [40]Perrella A,Lanza AG,Pisaniello D,et al.Telbivudine prophylaxis for hepatitis B virus recurrence after liver transplantation improves renal function.Transplant Proc,2014,46(7):2319-2321.
[41]CholongitasE,VasiliadisT,GoulisI,etal.Telbivudineis associatedwithimprovementofrenalfunctioninpatients transplanted for HBV liver disease.J Viral Hepat,2015,22(7):574-580.
[42]Yap DY,Chan TM.The use of telbivudine in kidney transplant recipients with chronic hepatitis b virus infection-A preliminary experience.Nephrology(Carlton),2015 Oct 20[ahead of print].
[43]European Association for the Study of the Liver.EASL Clinical Practice Guidelines:Liver transplantation.J Hepatol,2016,64(2):433-485.
[44]中华医学会肝病学分会肝癌学组.HBV/HCV相关性肝细胞癌抗病毒治疗专家建议.中华实验和临床感染病杂志(电子版),2012,6:651-655.
[45]Wu CY,Chen YJ,Ho HJ,et al.Association between nucleoside analogues and risk of hepatitis B virus-related hepatocellular carcinoma recurrence following liver resection.JAMA,2012,308:1906-1913.
[46]中华人民共和国卫生部.原发性肝癌诊疗规范(2011年版)摘要.中华肝脏病杂志,2012,20:419-426.
[47]Sun P,Dong X,Cheng X,et al.Nucleot(s)ide analogues for hepatitis B virus-related hepatocellular carcinoma after curative treatment:a systematic review and meta-analysis.PLoS One,2014,9:e102761.
[48]Yin J,Li N,Han Y,et al.Effect of antiviral treatment with nucleotide/nucleosideanalogsonpostoperativeprognosisof hepatitis B virus related hepatocellular carcinoma:a two-stage longitudinal clinical study.J Clin Oncol,2013,31:3647-3655.
[49]Kim YW,Kwon JH,Chung E,et al.Short term virologic efficacies of telbivudine versus entecavir against hepatitis B-related hepatocellular carcinoma.Gastroenterol Res Pract,2015,2015:181065. [50]Gane EJ,Deray G,Liaw YF,et al.Telbivudine improves renal function in patients with chronic hepatitis B.Gastroenterology,2014,146:138-146,e5.
[51]Wang Y,Thongsawat S,Gane EJ,et al.Efficacy and safety of continuous 4-year telbivudine treatment in patients with chronic hepatitis B.J Viral Hepat,2013,20(4):e37-46.
[52]EuropeanAssociationForThe Study Of The Liver.EASL clinical practice guidelines:Management of chronic hepatitis B virus infection.J Hepatol,2012,57(1):167-185.
参编专家(以拼音首字母先后排序)
陈从新,陈良,陈楠,陈新月,陈永平,窦晓光,段钟平,范建高,高志良,韩英,洪富源,江家骥,江建宁,李文歌,李旭,李智伟,娄探奇,梅长林,潘晨,潘红英,孙永涛,田德英,万谟彬,王悦,巫善明,谢青,邢昌赢,邢卉春,徐小元,袁伟杰,张鸿飞,张欣欣,周伯平
(收稿:2016-06-05)
(本文编辑:陈从新)
10.3969/j.issn.1672-5069.2016.04.037
袁伟杰,上海市第一人民医院肾内科,E-mail:ywj4169@163.com;万谟彬,第二军医大学长海医院感染病科,E-mail:mobinwan@aliyun.com

