他达那非固体分散体的制备和性质研究
于超峰,单兴杰,闫占宽,李传筠
(江苏恒瑞医药股份有限公司,连云港 222047)
他达那非固体分散体的制备和性质研究
于超峰,单兴杰,闫占宽*,李传筠
(江苏恒瑞医药股份有限公司,连云港222047)
目的 制备他达那非(tadalafil,TD)固体分散体并进行性质研究。方法利用喷雾干燥法制备固体分散体,以表观溶解度和溶出度为指标筛选处方,采用差示扫描量热(DSC)、粉末X-射线衍射(PXRD)和接触角测定等技术研究药物的存在状态和润湿性等理化性质。结果固体分散体将他达那非的表观溶解度提高22.6倍;20min内药物的累积溶出超过90%;固体分散体药物以分子或无定形状态存在;接触角减小,润湿性增大。结论采用十二烷基硫酸钠(SDS)和介孔硅为载体制备的他达那非固体分散体,能明显提高药物的表观溶解度和溶出度。
他达那非;介孔硅;固体分散体;溶出度
他达那非(tadalafil,TD) 是一种口服的新型磷酸二酯酶5(PDE-5)的特异抑制剂,主要治疗男性勃起功能障碍[1]。由德国拜耳 (Bayer) 与葛兰素史克(GlaxoSmithKline) 公司经过多年研制开发而成。他达那非属低溶解度(7.78μg·mL-1)和高渗透性的药物,即BCSⅡ类药物,在胃肠道中的低溶出度直接导致其低生物利用度和较大的个体差异,进而限制了临床应用。因此采取各种方法提高该药物的溶解度和溶出度是有必要的,如采用包合技术[2]和微乳化[3]技术提高他达那非的溶出速率。固体分散技术能增加难溶性药物的溶出度,提高生物利用度。近年来常用的固体分散体载体材料有高分子聚合物、表面活性剂类、糖、有机酸及吸附性载体类[4]。泊洛沙姆既可作表面活性剂使用,又常用作固体分散体的载体[5],制备的固体分散体能明显改善他达那非的溶出度[6],少有研究报道采用无机多孔载体制备他达那非的固体分散体,改变其物理存在状态,从而提高药物溶出度。本研究采用介孔硅为载体制备他达那非的固体分散体,研究其对他达那非溶解度和溶出度的改善及机制。
1 仪器与材料
1.1仪器DL-360超声波清洗仪(浙江象山县石浦海天电子仪器厂);RC-8D溶出度测试仪(天津市国铭医药设备有限公司);JA1003分析天平(北京光学仪器厂);高效液相色谱泵(L-7100,日立公司);高效液相检测器(L-7400,日立公司);高速离心机(上海科学仪器厂);电子天平(奥豪斯公司);JY-82接触角仪(河北承德鼎盛测试仪器有限公司);B-190型小型喷雾干燥仪(瑞士步琪有限公司)。
1.2试药他达那非(湖北鸿运隆生物有限公司,质量分数≥99%);球形介孔硅(粒径约为300nm,比表面积为600~800m2·g-1,孔径为10~20nm,孔容为1.00~1.30m3·g-1);十二烷基硫酸钠(SDS)(中国禹王化工有限公司);甲醇、二氯甲烷、乙腈及其他试剂,均为分析纯 (天津市恒兴化学试剂制造有限公司)。
2 方法与结果
2.1他达那非/介孔硅固体分散体的制备
2.1.1含十二烷基硫酸钠的固体分散体将十二烷基硫酸钠溶解在水中制成质量浓度为40g·L-1的溶液。将他达那非溶于乙腈,制成质量浓度为3g·L-1的溶液,再加入不同比例的硅载体,搅拌均匀。将100mL的他达那非溶液逐渐加入300mL的十二烷基硫酸钠溶液中,室温下密封搅拌8h,采用喷雾干燥法干燥获得固体分散体。喷雾干燥工艺参数为:进口温度:120~125 ℃;出口温度:70~75 ℃;进风温度:60 ℃;喷气压力:4kg·m2;干燥气流流速:600L·h-1;料液流速:3.0~4.0g·min-1。收集干颗粒,整粒,得含十二烷基硫酸钠的固体分散体。
2.1.2不含十二烷基硫酸钠的固体分散体将他达那非溶于乙腈,制成质量浓度为3g·L-1的溶液,加入适量硅载体,拌匀。将100mL他达那非溶液逐渐加入300mL水中。其他操作同2.1.1项下方法,收集干颗粒,整粒,得不含十二烷基硫酸钠的固体分散体。
2.2分析方法采用高效液相色谱法(HPLC)分析定量他达那非。色谱条件:色谱柱:KromasilC18(250mm×4.6mm5μm,Sweden);流动相:乙腈-pH值为6.0的磷酸盐缓冲液(PBS) (55/45);流速:1.2mL·min-1;柱温:37±0.2 ℃;检测波长:220nm[7];进样量:20μL。
精密称取10.00mg他达那非,置于小烧杯中,用适量乙腈溶解,转移至100mL量瓶中,制成质量浓度为0.10mg·mL-1的储备液。取储备液适量,稀释后配制成质量浓度为0.50,2.00,8.00,20.00和40.00μg·mL-1的系列溶液。分别取20μL注入色谱仪,测定峰面积A。以质量浓度C为横坐标、峰面积A为纵坐标,进行线性回归,回归方程为A=26 751 C+889,r=0.999 8。结果表明,质量浓度在0.50~40.00mg·mL-1范围内,A与C呈良好线性关系。精密度和回收率考察符合方法学要求。
2.3固体分散体理化性质考察
2.3.1表观溶解度取一定量的他达那非原料药和各固体分散体(过100目筛),分别置于10mL具塞瓶中,加蒸馏水5mL,置于37±0.3 ℃恒温摇床中,以100r·min-1振荡,于10,20,30,60,80,120,180和240min取对应样品约0.6mL,用0.45μm微孔滤膜(预先在37 ℃下保温)过滤,取续滤液20μL注入色谱仪,计算表观溶解度,每个样品重复操作3次以上,结果见图1。
2.3.2体外溶出精密称取10.0mg他达那非和相当于10.0mg他达那非的各固体分散体,以900mLpH值为1.2的盐酸、pH值为4.5的磷酸盐缓冲液和pH值为6.8的磷酸盐缓冲液为溶出介质,参照《中国药典》2010年版二部附录ⅩC第2法,温度为37.0±0.1 ℃,转速为50r·min-1,分别于5,10,15,20,30,45和60min取溶出介质5mL(并立即补加等体积空白溶出介质),用0.45μm微孔滤膜过滤。取续滤液20μL注入色谱仪,测定峰面积A。按照回归方程计算他达那非的质量浓度。不同药物与载体比例制得的含十二烷基硫酸钠的固体分散体在pH值为6.8的磷酸盐缓冲液中溶出度曲线见图2。他达那非原料药和固体分散体(1∶4)在不同介质中的溶出曲线见图3。
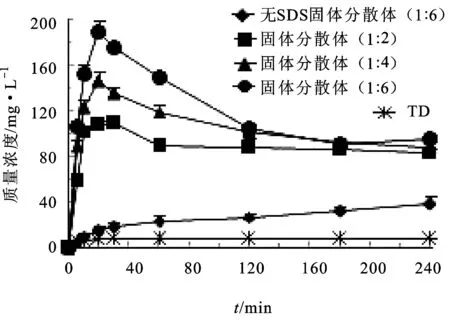
图1他达那非原料药和不同固体分散体在水中的表观溶解度
Fig.1Apparentsolubilityoftadalafilandsoliddispersions
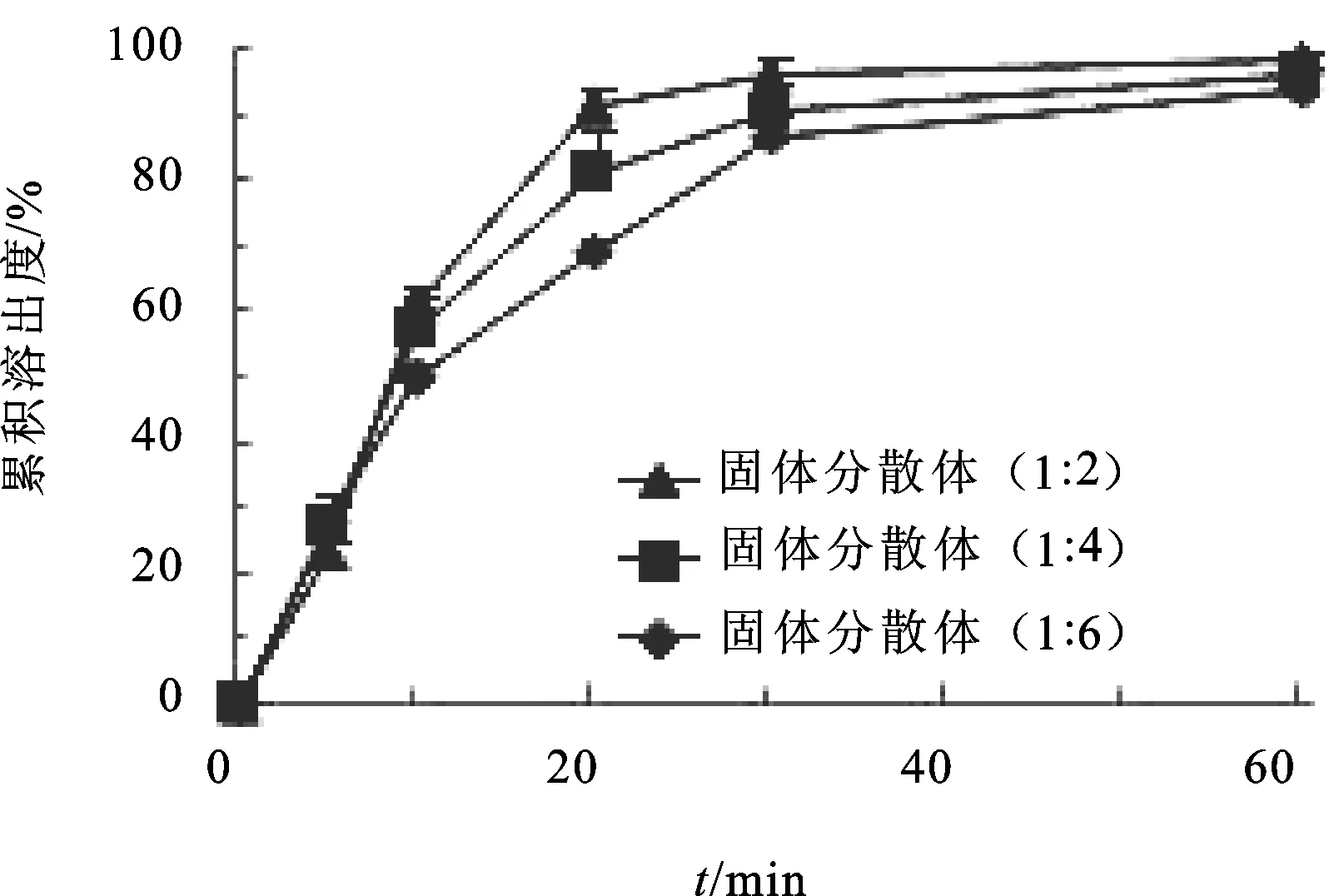
图2不同药物与载体比例制得的含十二烷基硫酸钠的固体分散体在pH值为6.8的磷酸盐缓冲液中的溶出曲线
Fig.2 In vitrodissolutionprofilesoftadalafilsoliddispersionscontainingSDSwithdifferentratiosofdrugtocarrierinpH6.8PBS
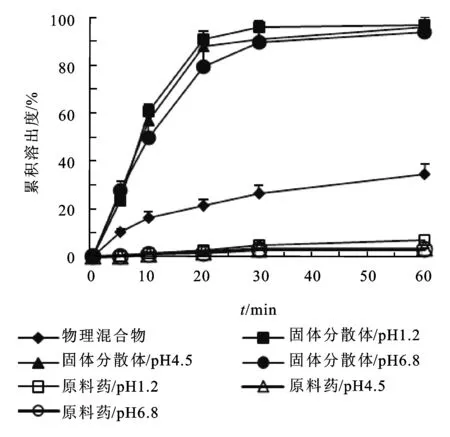
图3他达那非原料药和含十二烷基硫酸钠的固体分散体(1∶4)在不同介质中的溶出曲线
Fig.3 In vitrodissolutionprofilesoftadalafilandtadalafilsoliddispersioncontainingSDS(1∶4)indifferentmedia
2.3.3差示扫描量热准确称量2.0mg的他达那非原料药(过100目筛)、硅载体、十二烷基硫酸钠和相当于他达那非2.0mg的含十二烷基硫酸钠的各固体分散体样品(过100目筛),置于氮气保护的铝锅中,温度范围:30~350 ℃,升温速率:10 ℃·min-1,进行差示扫描量热测定,结果见图4。
2.3.4粉末X-射线衍射分析取他达那非原料药(过100目筛)、硅载体、他达那非与硅载体按照质量比例1∶6的物理混合物(过100目筛)和固体分散体(他达那非与载体比例为1∶6,过100目筛),采用X-射线衍射仪进行扫描测定。采用Cu-Ka辐射在2θ角为5°~40°内以4°·min-1的扫描速度进行分析,步宽0.02°,管电压40kV,管电流30mA,结果见图5。
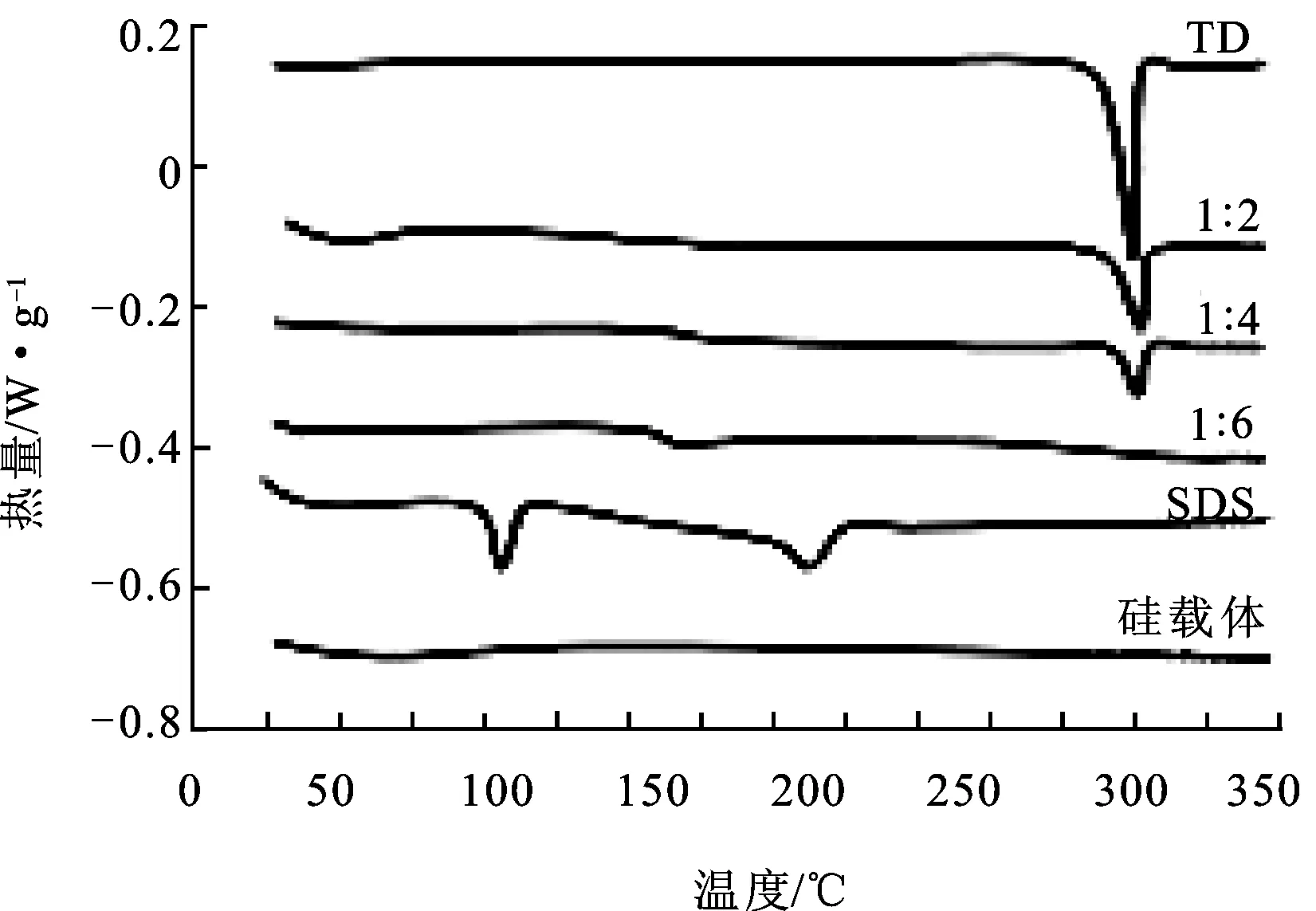
图4他达那非原料药和含十二烷基硫酸钠固体分散体的差示扫描量热曲线
Fig.4DSCcurvesofTDrawdrugandsoliddispersionscontainingSDS
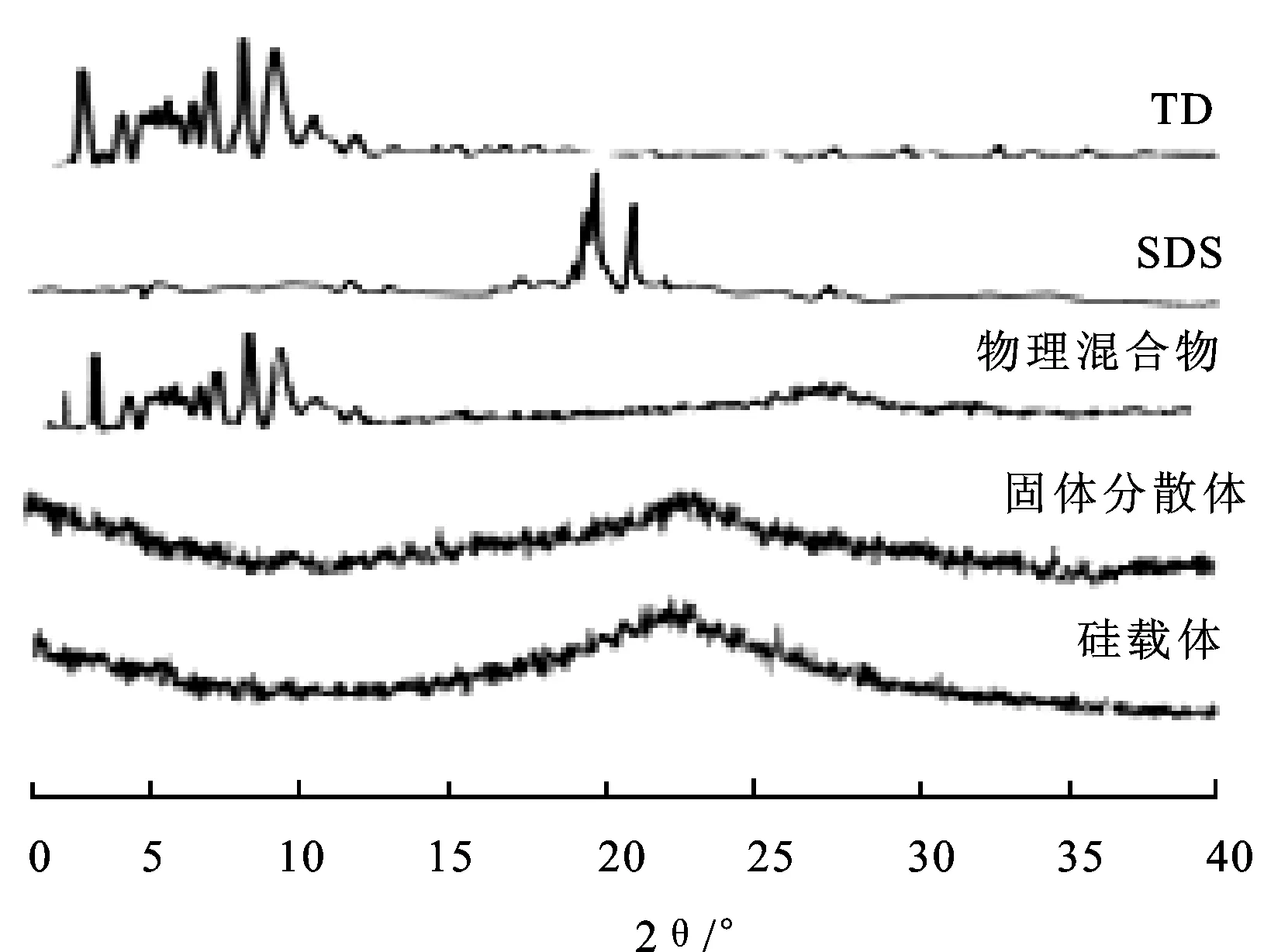
图5他达那非、十二烷基硫酸钠、硅载体、物理混合物(1∶6)、含十二烷基硫酸钠的固体分散体(1∶6)的粉末X-射线衍射谱图
Fig.5PowderX-raydiffractionpatternsofTD,SDS,silicacarrier,physicalmixture(1∶6),soliddispersion(1∶6)containingSDS
2.3.5扫描电镜(SEM)分别将载药前的他达那非原料药和他达那非/介孔硅固体分散体黏在导电胶上,喷金后用扫描电镜观察,结果见图6。
2.4接触角将他达那非、他达那非和硅载体的物理混合物(1∶6)、无十二烷基硫酸钠的固体分散体(1∶6)和含十二烷基硫酸钠的固体分散体(1∶6)各300mg,在压片机上用6mm平冲压片。用微量加液器滴一滴水(约2μL)置于片平面上,采用数码相机,计算结果见表1。

图6扫描电镜照片
A.他达那非;B.硅固体分散体
Fig.6SEMimages
A.TD;B.TD/mesoporoussilicadispersion
表1接触角测定结果
Tab.1Theresultsofcontactangle

样品接触角/°他达那非66.49±0.58物理混合物(1∶6)48.42±0.37无十二烷基硫酸钠的固体分散体(1∶6)34.42±1.27含十二烷基硫酸钠的固体分散体(1∶6)18.32±0.79
3 讨论
美国药典规定他达那非为水不溶性药物,本研究在37 ℃下测定原料药在4h内的表观溶解度小于8.97μg·mL-1。各固体分散体的表观溶解度均高于原料药,主要原因是:硅载体的孔道为20nm左右,药物分散其中,主要以分子状态或小于20nm的聚集体形式存在,分散度极高,使其表观溶解度增大,而药物巨大的比表面积也加速了药物溶解。在制备固体分散体中加入十二烷基硫酸钠,各比例的固体分散体表观溶解度显著增大,固体分散体(1∶6)的表观溶解度与他达那非相比提高22.6倍。各表观溶解度在20min时最大,然后逐渐降低,表明固体分散体溶解存在过饱和现象。此外,20~30min时的表观溶解度随着载体比例的增大而增大,但是在3h之后各溶解度趋于一致。由此可见,表观溶解度迅速提高主要归因于载体的高度分散作用、十二烷基硫酸钠的润湿和增溶作用,而载体比例主要影响药物溶解速率。
20min内,固体分散体(1∶2)的溶出量约为70%,而固体分散体(1∶6)的溶出量为90%。随着药物和载体比例的增大,药物的溶出速率提高。由此可见,药物与载体比例是影响溶解速率和溶出速率的一个主要因素。原料药在pH值为1.2的介质中溶出度较大,具有一定的pH依赖性,但溶出度不足10%。无十二烷基硫酸钠的物理混合物溶出度约为35%。固体分散体在各pH值介质中的溶出度差异不明显,主要是由于显著提高的表观溶解度和极大的表面积克服了原料药本身溶出的pH依赖性。
他达那非原料药在294.4 ℃处有一尖锐的吸热峰,为他达那非熔点峰,说明他达那非原料药为晶体。十二烷基硫酸钠的差示扫描量热曲线有2处吸热峰。以他达那非、十二烷基硫酸钠和硅载体制备的固体分散体随着硅载体比例的增加,他达那非对应的吸热峰减小,说明以晶态存在的他达那非量逐渐减少,而以非晶态存在的他达那非增多。在1∶4和1∶6的固体分散体的差示扫描量热曲线中,在149 ℃处出现一很小的吸热峰,应归于无定形态他达那非的玻璃化转变温度。因此,推测固体分散体以无定形或分子状态存在。硅载体具有较大的表面积和较强的吸附性,抑制他达那非分子聚集,使他达那非以分子或无定形态高度分散。
在粉末X-射线衍射图谱中,他达那非和十二烷基硫酸钠呈现尖锐的晶体衍射峰,他达那非和硅载体的物理混合物呈现两者的衍射峰,说明物理混合没有改变他达那非的存在状态。而硅载体和固体分散体呈现宽而钝的衍射峰,进一步说明药物在固体分散体中以非晶态存在。
扫描电镜显示,他达那非为长度约100μm左右的棒状晶体,而固体分散体为300~400nm左右、与载体形貌相似的类球形体,且载体表面没有明显的药物晶体吸附,说明药物主要分布在介孔孔道中。差示扫描量热、粉末X-射线衍射和扫描电镜的结果一致,说明在固体分散体中药物被高度分散,存在状态发生变化,主要以分子或无定形态存在。
他达那非原料药的接触角为56.49°,具有较高的疏水性,而含十二烷基硫酸钠的固体分散体(1∶6)的接触角为18.32°,润湿性显著提高。含十二烷基硫酸钠比不含十二烷基硫酸钠的固体分散体接触角小,说明在制备固体分散体中加入十二烷基硫酸钠有助于改善药物的润湿性。
他达那非、十二烷基硫酸钠和介孔硅载体制备的固体分散体药物溶出迅速,主要因为药物以分子或无定形态高度分散,表面积和表观溶解度显著增大,润湿性得到改善。
[1]CarsonCC,ShabsighR,SegalS,etal.Efficacy,safety,andtreatmentsatisfactionoftadalafilversusplaceboinpatientswitherectiledysfunctionevaluatedattertiary-careacademiccenters[J].Urology,2005,65(2): 353-359.
[2]Badr-EldinSM,ElkheshenSA,GhorabMM.Inclusioncomplexesoftadalafilwithnaturalandchemicallymodifiedbeta-cyclodextrins.I:preparationandin-vitroevaluation[J].EurJPharmBiopharm,2008,70(3): 819-827.
[3]EI-BadryM,HaqN,FetihG,etal.Solubilityanddissolutionenhancementoftadalafilusingself-nanoemulsifyingdrugdeliverysystem[J].JOleoSci,2014, 63 (6): 567-576.
[4]潘西海,赵丽.固体分散体中常用的载体[J].西北药学杂志,1997,12(6): 277-278.
[5]彭霞,何江梅,黄兴亮,等.泊洛沙姆固体分散体对辛伐他汀溶出特性的影响[J].西北药学杂志,2013,28(2): 178-180.
[6]MehannaMM,MotawaaAM,SamahaMW.Insightintotadalafil-blockcopolymerbinarysoliddispersion:Mechanistic:investigationofdissolutionenhancement[J].IntJPharm,2010,402(1/2): 78-88.
[7]WlodarskiK,SawickiW,PaluchKJ,etal.Theinfluenceofamorphizationmethodsontheapparentsolubilityanddissolutionrateoftadalafil[J].EurJPharmSci, 2014, 62: 132-140.
Preparation and characteristics of tadalafil solid dispersions
YUChaofeng,SHANXingjie,YANZhankuan*,LIChuanjun
(JiangsuHengruiMedicineLimitedCompany,Lianyungang222047,China)
ObjectiveTopreparetadalafil(TD)soliddispersionsandinvestigatethebasiccharacteristicsofthesoliddispersion.MethodsThesoliddispersionwaspreparedbyspraydryingtechnology,andanoptimalformulationofthesoliddispersionwasscreenedbyusingapparentsolubilityanddissolutionexperimentsasindexes.ThecharacteristicsincludingdrugstateinthedispersionandwettabilityofthedispersionwereinvestigatedbyDSC,PXRDandcontacttangleexaminingtechnology.ResultsThroughpreparingthesoliddispersionsofTD,theapparentsolubilityofTDwasenhancedupto22.6times;thedrugreleasewithin20minexceeded90%;thedrugstateindispersionwasmolecularstateoramorphousform;thecontactangledecreasedandthewettabilityofsoliddispersionincreased.ConclusionTheapparentsolubilityandthedissolutionofTDwereimprovedbysoliddispersionbyusingSDSandmesoporoussilicaascarriers.
tadalafil;mesoporoussilica;soliddispersion;dissolution
于超峰,男,工程师
闫占宽,男,工程师
10.3969/j.issn.1004-2407.2016.05.018
R944
A
1004-2407(2016)05-0500-05
2015-11-28)

