基于原位生成的铜纳米颗粒修饰的羧基化多壁碳纳米管构建同时检测抗坏血酸、多巴胺、尿酸的电化学传感器
王思远,钟 霞,柴雅琴,袁 若
(发光与实时分析化学教育部重点实验室,西南大学化学化工学院,重庆400715)
基于原位生成的铜纳米颗粒修饰的羧基化多壁碳纳米管构建同时检测抗坏血酸、多巴胺、尿酸的电化学传感器
王思远,钟霞,柴雅琴*,袁若*
(发光与实时分析化学教育部重点实验室,西南大学化学化工学院,重庆400715)
一些传统的生化小分子多组分同时检测电化学传感器多是利用贵金属纳米材料在电化学中的催化活性,但是往往都是合成制备成本较高限制了其实用前景。该工作用比较廉价的铜纳米颗粒(CuNPs)修饰酸化的多壁碳纳米管(MWCNTs)制备纳米复合物(CuNPs@MWCNTs),代替贵金属纳米颗粒修饰碳材料,用比较低廉的成本构建了抗坏血酸 (AA)、多巴胺 (DA)和尿酸 (UA)多组分同时检测的电化学传感器。CuNPs@MWCNTs修饰的电极对AA,DA和UA的氧化有很好的识别区分性,达到而且有些性能超过贵金属材料制备的传感器。在pH4.0的条件下用差分脉冲伏安法(DPV)传感器在三组分共存体系中检测抗坏血酸、多巴胺和尿酸的线性范围分别为:10 μmol/L~1430 μmol/L,0.3 μmol/L~48.0 μmol/L,0.1 μmol/L~86.7 μmol/L,AA、DA、UA的检测限依次是3.3 μmol/L,0.1 μmol/L,0.03 μmol/L。因此,CuNPs@MWCNTs构建的传感器提供了一个比贵金属纳米颗粒成本较为低廉的进行灵敏快速有选择性的抗坏血酸、多巴胺和尿酸多组分同时检测的装置,在生物科学、临床医学等领域有很好的应用发展前景。
抗坏血酸;多巴胺;尿酸;铜纳米颗粒;同时检测
0 引言
多巴胺(DA)、抗坏血酸(AA)和尿酸(UA)是很多生理过程中重要的生化分子[1]。其中,多巴胺是一种儿茶酚的衍生物,作为一种神经传递素,与一些物质成瘾有很大关系。它可以影响大脑控制运动、情感的过程,也能让人感受到愉快和疼痛[2]。抗坏血酸是一种水溶性维生素,是人体必需的营养成分。在生物体内,它作为抗氧化物可以保护身体免受氧化应激的攻击[3]。尿酸是嘌呤代谢主要最终产物,已经被证明可以导致高尿酸血症和痛风[4]。通常这些功能性的生物分子共存在生理体液中。因此,在卫生保健、临床诊断、生物分析和病理研究等很多领域,急需发展一种高效的有选择性的灵敏的可以对这几种重要生物分子同时检测的方法。
因为AA,DA和UA都是电活性物质,电化学技术以其快速的响应、良好的选择性和灵敏度还有易于在有机体内分离等优点,引起很多关注用来对生化小分子同时检测[5-6]。 然而,AA,DA 和UA因为有很近的氧化电位,所以很难实现在常用的裸电极上用伏安法同时检测这三种分子[7]。所以为了达到这个目的,电极必须修饰上带有分开这些分析物氧化峰的结构。很多修饰电极被用来设计构建电化学生物传感器,尤其基于纳米材料的,特别是金属纳米颗粒和碳纳米材料(例如碳纳米管)[8]。其中贵金属(金、铂等)纳米颗粒因为其形貌使其具有电催化活性和介导快速电子传递到电极表面的能力[8]。但是贵金属制备的纳米复合物的成本高昂,如果能有成本较为低廉的金属复合碳纳米材料制备纳米复合物构建电化学生物传感器,将会在相关领域中有很大的应用前景。铜,作为一种良好的导电材料,得到研究者的关注,其不同的纳米结构可以使其具有应用于电化学的特性。有报道高密度的铜纳米线可以催化二氧化碳的低电位还原[9]。还有将铜和铂制成多孔的合金可以催化甲醇和乙醇的氧化[10]。在生化小分子检测方面,已有研究者将铜纳米颗粒(CuNPs)固载到双联DNA上用荧光的方法检测多巴胺[11]。
综合前面的阐述,设计用酸化带有羧基的多壁碳纳米管(MWCNTs-COOH)在水相中依靠正负电荷吸附硫酸铜中的Cu2+,用AA将Cu2+还原成铜纳米颗粒(CuNPs),得到CuNPs修饰MWCNTs制备的纳米复合物(CuNPs@MWCNTs)。碳纳米管较高的比表面积和良好的电化学催化性能,还有羧基基团提供有选择性的氢键结合位点来区别连接AA,DA,UA的提供质子的基团,有助于区分AA,DA,UA的氧化峰。此外,CuNPs有助于氧化反应中的电子传递,也具有电化学催化活性。因此,该章设计的CuNPs@MWCNTs纳米复合物构建的电化学传感器可以对多巴胺、抗坏血酸和尿酸三种生化小分子进行多组分电化学同时检测,为生化小分子传感装置提供了一个选择性好、成本低廉有应用前景的选择。
1 实验部分
1.1化学试剂
多壁碳纳米管(MWCNTs,纯度95%)从中科院成都有机化学品有限公司(中国,成都)购买。硫酸铜(CuSO4·5H2O)采购自天津市瑞金特化学品有限公司(中国,天津)。多巴胺从Sigma化学试剂公司 (St.Louis,MO,USA)购买。抗坏血酸(AA)和尿酸(UA,纯度99%)购于阿拉丁试剂有限公司(中国,成都)。聚(酰胺-胺)分子(PAMAM,G5.0-NH2)采购于威海晨源分子新材料有限公司(中国,威海)。其他化学试剂盒溶剂都是分析纯级别,该实验用水为超纯水 (电阻率18.2 MΩ· cm)。不同pH的磷酸盐缓冲溶液(PBS 0.1 mol/L)用0.10 mol/L Na2HPO4和0.10 mol/L NaH2PO4溶液配制,支持电解质是0.10 mol/L KCl溶液。
1.2实验仪器
电化学的相关实验在电化学分析测试系统(CHI660C,上海辰华仪器公司)上进行。实验用三电极体系包括:玻碳电极(GCE Φ=4 mm)作为工作电极;饱和甘汞电极(SCE)作为参比电极;辅助电极是铂丝电极。所有的检测实验都在室温下进行。
1.3CuNPs@MWCNTs纳米材料的合成
此复合材料按照如下方法制备:称取3.0 mg羧基化的MWCNTs,超声0.5 h分散在3 mL超纯水中,加入4.6 mmol/L CuSO4溶液300 μL,搅拌4 h。将悬浊液超声均匀后,滴加11.2 mg的AA溶液(2 mL),80℃下水浴加热搅拌12 h。待冷却后,超声分散均匀,用去离子水离心洗涤2次。最终得到的离心固体,中超声2 h在1 mL水中分散均匀,在4℃下冷藏储存待后续试验使用。
1.4传感器的构建
玻碳电极 (GCE)分别用粒径为0.3和0.05 μm的氧化铝粉末依次打磨抛光,再按照水-乙醇-水的顺序依次超声洗涤。洗好的玻碳电极在室温下干燥。待电极干燥后,用移液枪滴加7 μL上述CuNPs@MWCNTs复合纳米材料的分散液于电极表面。在室温下,空气中干燥静置8 h,即可得到CuNPs@MWCNTs/GCE的传感器。
2 结果与讨论
2.1纳米复合物的SEM表征
用扫描投射电镜(SEM)表征了此部分合成的纳米材料的形态学和微观结构 (图1)。通过SEM可以很明显地看到MWCNTs的管状线条结构,同时上面的明亮的部分是大量固载铜纳米颗粒的位置,这主要是因为铜有良好的导电性,所以大量CuNPs固载到MWCNTs上的一段在扫描电镜下会显示出在碳纳米管上明亮的一段结构。因此,这说明上述设计的纳米复合物被成功的合成。
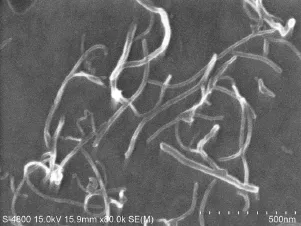
图1 CuNPs@MWCNTs纳米复合物的SEM图Fig.1 SEM images of CuNPs@MWCNTs hybrids
2.2检测条件的pH优化
同前两章一样,因为检测的生化小分子电化学氧化有质子的参与,所以选择的PBS缓存溶液的pH对AA,DA和UA的多组分检测有很大影响。因此差分脉冲伏安法(DPV)被用来考察了pH对AA (0.2 mmol/L),DA (4 μmol/L)和UA(2 μmol/L)检测的影响(图2)。首先抗坏血酸、多巴胺和尿酸的氧化峰电位都伴随着pH值的增大而向负电位方向移动,所以在pH6.0和pH7.0的考察电位范围改到-0.4 V~+0.8 V。在近中性的pH下(pH5.0~pH7.0),抗坏血酸和尿酸的氧化峰电流会逐渐降低,多巴胺的氧化电流会增大,这说明在pH5.0~pH7.0的范围多巴胺有很好的感应信号,而抗坏血酸和尿酸的响应没有很明显。而在pH4.0,相对于电极的背景电流,AA,DA和UA都会有较好的氧化峰可以被观察到,并且峰电位的间距也足够大,克服了三种生化小分子电化学氧化峰重叠的情况。而在pH3.0条件下,虽然AA 和UA的峰电流要大于在pH4.0的,但是考虑到背景电流和三者的氧化峰电位的因素,DA和AA的氧化峰间距不够大,使得两个峰有部分重叠。综上所述,pH4.0是最理想的在CuNPs@MWCNTs传感器上抗坏血酸、多巴胺和尿酸多组分同时检测的条件,后续的实验采用 0.1 mol/L PBS (pH4.0)作为缓冲溶液。
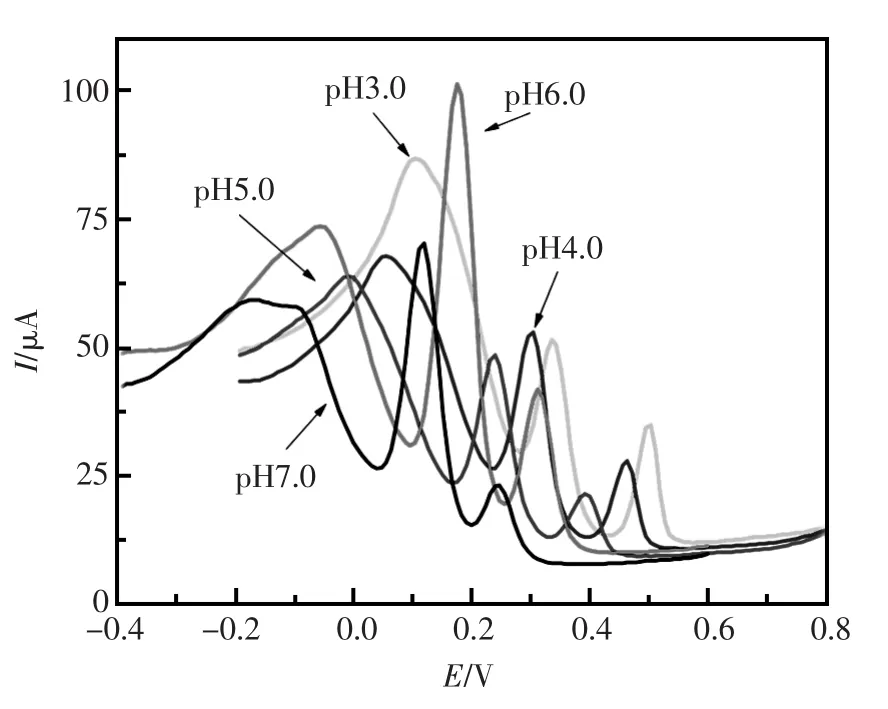
图2 在CuNPs@MWCNTs/GCE上AA(0.2 mmol/L),DA (20 μmol/L)and UA(20 μmol/L)处于不同pH的0.1 mol/L PBS中的DPV曲线Fig.2 DPVs of the CuNPs@MWCNTs modified GCE in 0.1 mol/L PBS containing AA(0.2 mmol/L),DA(20 μmol/L)and UA(20 μmol/L)at different pH value
2.3对抗坏血酸、多巴胺和尿酸的同时检测
该文的主要目标就是用CuNPs@MWCNTs材料构建的电化学传感器也能达到其他贵金属材料构建的传感器用来对共存的抗坏血酸、多巴胺和尿酸多组分同时检测的目的。用CuNPs@MWCNTs修饰的电极构建传感器对AA,DA和UA加入不同浓度进行了DPV研究(图3)。可以看到在0.1mol/L PBS(pH4.0)中,抗坏血酸、多巴胺和尿酸的氧化峰完全分开,并且每种小分子的浓度增加对应的氧化电流都在增加。在CuNPs@MWCNTs/ GCE上,抗坏血酸、多巴胺和尿酸的氧化峰电位分别是+0.068 V,+0.316 V和+0.460 V。在0.1 V左右有个材料的背景电流增大现象,不过抗坏血酸加入后会在背景电流基础上显示出氧化电流,说明对AA的检测并无影响。这个实验结果说明CuNPs@MWCNTs传感器可以实现良好的AA,DA和UA多组分的同时检测。
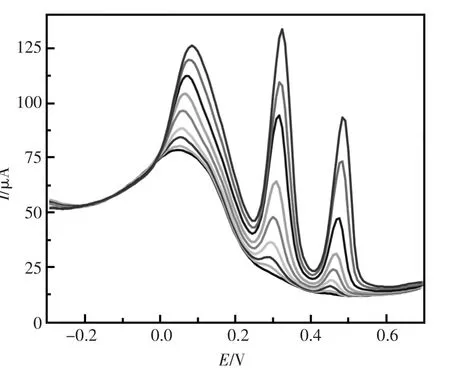
图3 在0.1 mol/L PBS(pH4.0)中加入不同的浓度的AA,DA和UA的传感器DPV曲线,由下到上浓度依次为:[AA]:0.02,0.06,0.16,0.26,0.46,0.66,0.96,1.36,1.05 mmol/L.[DA]:0.5,1.5,2.5,4.5,8.5,13.5,23.5,33.5 and 53.5 μmol/L.[UA]:0.5,1.5,2.5,4.5,8.5,14.5,24.5,44.5 and 74.5 μmol/LFig.3 DPV curves of the sensor in 0.1 mol/L PBS(pH4.0)containing individual concentration of AA,DA and UA mixture.[AA]:0.02,0.06,0.16,0.26,0.46,0.66,0.96,1.36 and 1.05 mmol/L.[DA]:0.5,1.5,2.5,4.5,8.5,13.5,23.5,33.5 and 53.5 μmol/L.[UA]:0.5,1.5,2.5,4.5,8.5,14.5,24.5,44.5 and 74.5 μmol/L
2.4传感器对抗坏血酸、多巴胺和尿酸的线性考察
此外,为了定量地检测这三种分子,还做了每种分子在三组分中传感器DPV线性响应。固定两种物质的浓度,改变另一种分析物的浓度用传感器对其进行检测(图4)。AA,DA和UA的具体DPV曲线分别一次在图4a,b,c中。图4a中说明了在DA(10 μmol/L)和UA(20 μmol/L)存在下不同浓度的AA的DPV相应,得到的抗坏血酸线性方程为I(μA)=67.64+0.0489cAA(μmol/L),线性相关系数rAA=0.9995,抗坏血酸的线性范围是10 μmol/L~1430 μmol/L。图4b中,多巴胺的峰电流随DA浓度从0.3 μmol/L到48 μmol/L增加而增加,其中AA浓度0.2 mmol/L,UA浓度10 μmol/L。多巴胺的线性方程是 I(μA)=41.97+3.27cDA(μmol/L),相关系数rDA=0.9899。图4c展示的是在0.2 mmol/L抗坏血酸和 10 μmol/L多巴胺存在下,尿酸的DPV随浓度变化的相应。其线性范围是0.1 μmol/L~86.7 μmol/L,线性方程是I(μA)= 15.57+1.03cUA(μmol/L)与线性相关系数 rUA= 0.9930。此外,抗坏血酸、多巴胺和尿酸的检测下线分别是3.3 μmol/L,0.1 μmol/L,0.03 μmol/L (S/N=3)。此结果说明CuNPs@MWCNTs传感器可以实现对抗坏血酸、多巴胺和尿酸在共存条件下的定量检测,并且比一些贵金属材料构建的传感器有更好的检测限和灵敏度。其中的原因可能归因于以下几点:(1)多壁碳纳米管有大的电化学活性表面积、良好的稳定性、良好的催化活性;(2)酸化的多壁碳纳米管带有很多羧基基团,这些功能化的基团可以提供有选择性的氢键结合位点来区别连接AA,DA,UA的提供质子的基团,从而达到区分几种小分子的氧化电位目的;(3)CuNPs有良好的导电性,有助于氧化反应是电子的传递过程,提高了传感器的灵敏度。归纳起来,CuNPs@MWCNTs传感器在抗坏血酸、多巴胺和尿酸多组分同时检测方面有很好的灵敏度、选择性和高的催化活性。
3 结论
在此项工作中,将CuSO4原位还原在酸化的MWCNTs上制备纳米复合物来修饰电极,构建了一个可以对抗坏血酸、多巴胺和尿酸多组分同时检测的传感器。CuNPs@MWCNTs所修饰的电极解决了AA,DA和UA三种生化小分子氧化峰重叠问题,通过DPV的方法把三者的氧化峰良好地区分开来。CuNPs@MWCNTs传感器具对抗坏血酸、多巴胺和尿酸具有良好的选择性和灵敏度。与一些贵金属材料制备纳米材料所构建的传感器相比,CuNPs@MWCNTs纳米复合材料在生化小分子多组分电化学同时检测方面提供了一个有前景、成本更低廉、同样有效的选择。
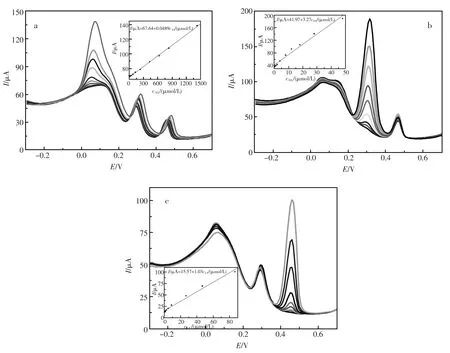
图4 在0.1 mol/L PBS(pH4.0)中,(a)含有10 μmol/L DA,20 μmol/L UA,不同浓度AA的DPV曲线(从低到高依次为):10,40,80,130,230,430,630,830,1430 μmol/L;(b)含有0.2 mmol/L AA,10 μmol/L UA,不同浓度DA的DPV曲线(从低到高依次为):0.3,1,2,4,8,12,18,38,48 μmol/L;(c)含有0.2 mmol/L AA,10 μmol/L DA,不同浓度UA的DPV曲线(从低到高依次为):0.1,0.7,1.7,2.7,4.7,8.7,26.7,46.7,86.7 μmol/L。(插图分别为AA,DA,UA的线性拟合)Fig.4 DPV curves at the sensor in 0.1 mol/L PBS(pH4.0)(a)containing 10 μmol/L DA,20 μmol/L UA and different concentrations of AA(from inner to outer):10,40,80,130,230,430,630,830,1430 μmol/L;(b)containing 0.2 mmol/L AA,10 μmol/L UA and different concentrations of DA(from inner to outer):0.3,1,2,4,8,12,18,38,48 μmol/L;(c)containing 0.2 mmol/L AA,10 μmol/L DA and different concentrations of UA(from inner to outer):0.1,0.7,1.7,2.7,4.7,8.7,26.7,46.7,86.7 μmol/L,respectively
[1]Zhang X,Ma L X,Zhang Y C.Electrodeposition of platinum nanosheets on C60decorated glassy carbon electrode as a stable electrochemical biosensor for simultaneous detection of ascorbic acid,dopamine and uric acid [J].Electrochim.Acta,2015,177:118-127.
[2]Daneshinejad H,Chamjangali M A,Goudarzi N,et al. Application of a thin film of poly(solochrome black T)as a redox mediator for the electro-catalytic simultaneous determination of dopamine and acetaminophen in the pharmaceutical and biological samples[J].Mater.Sci. Eng.,C,2016,58:532-540.
[3]Wang C,Zou X,Zhao X,et al.Cu-nanoparticles incorporated overoxidized-poly(3-amino-5-mercapto-1,2,4-triazole)film modified electrode for the simultaneous determination of ascorbic acid,dopamine,uric acid and tryptophan[J].J.Electroanal.Chem.,2015,741:36-41.
[4]Dutt V V S E,Mottola H A.Determination of uric acid at the microgram level by a kinetic procedure based on a pseudo-induction period[J].Anal.Chem.,1974,46: 1777-1781.
[5]Ronkainen N J,Halsall H B,Heineman W R.Electro-chemical biosensors[J].Chem.Soc.Rev.,2010,39: 1747-1763.
[6]Kimmel D W,LeBlanc G,Meschievitz M E,et al.Electrochemical sensors and biosensors[J].Anal.Chem.,2011,84:685-707.
[7]Zen J M,Chen P J.A selective voltammetric method for uric acid and dopamine detection using clay-modified electrodes[J].Anal.Chem.,1997,69:5087-5093.
[8]Chen A C,Chatterjee S.Nanomaterials based electrochemical sensors for biomedical applications[J].Chem. Soc.Rev.,2013,42:5425-5438.
[9]Raciti D,Livi K J,Wang C.Highly dense Cu nanowires for low-overpotential CO2Reduction[J].Nano letters,2015,15:6829-6835.
[10]Fan Y,Liu P F,Zhang Z W,et al.Three-dimensional hierarchical porous platinum-copper alloy networks with enhanced catalytic activity towards methanol and ethanol electro-oxidation[J].J.Power Sources,2015,296:282-289.
[11]Wang H B,Zhang H D,Chen Y,et al.A label-free and ultrasensitive fluorescent sensor for dopamine detection based on double-stranded DNA templated copper nanoparticles[J].Sens.Actuators,B:Chem.,2015,220: 146-153.
A eletrochemical sensor based on MWCNTs immobilized Cu nanoparticles for simultaneous determination AA,DA and UA
Wang Si-yuan,Zhong Xia,Chai Ya-qin*,Yuan Ruo*
(Key Laboratory of Luminescent and Real-Time Analytical Chemistry,Ministry of Education(Southwest University),College of Chemistry and Chemical Engineering,Southwest University,Chongqing 400715,China)
Some conventional eletrochemical sensor for simultaneous determination AA,DA and UA often use noble metal material owing to its electrocatalytic activity in eletrochemistry,but the cost of synthesis is too high,which limits its practical prospects.A nanohybrid based on multi-walled carbon nanotubes(MWCNTs)immobilized Cu nanoparticles(CuNPs@MWCNTs)for simultaneous electrochemical determination of ascorbic acid(AA),dopamine (DA)and uric acid(UA)was reported in this work.The CuNPs@MWCNTs-modified electrode showed a high selectivity towards the oxidation of AA,DA,and UA,and resolve their overlapped oxidation peaks into three well-defined peaks.Several important parameters that control the performance of the electrochemical sensor were investigated and optimized.Under pH4.0 phosphate buffered saline(PBS)with differential pulse voltammetry(DPV)method,the linear response ranges for the determination of AA,DA,and UA are 10 μmol/L~1430 μmol/L,0.3 μmol/L~48.0 μmol/L,0.1 μmol/L~86.7 μmol/L in the co-existence systems,respectively,with the corresponding detection limits 3.3 μmol/L,0.1 μmol/L,0.03 μmol/L(S/N=3),respectively.In addition,the proposed sensors provide an efficient and promising for simultaneous determination of AA,DA and UA selectively and sensitively and it cost much lower than those using noble metal nanoparticles,which has a good application development prospects in the biological sciences,clinical medicine and other fields.
ascorbic acid;dopamine;uric acid;Cu nanoparticles;simultaneous determination
*通信联系人,E-mail:yqchai@swu.edu.cn,yuanruo@swu.edu.cn

