I-125粒子植入联合化疗和单纯化疗对胰腺癌疗效的荟萃分析
宁 峥, 李宏宇, 郭晓钟, 崔忠敏, 祁兴顺, 侯飞飞
1.沈阳军区总医院消化内科,辽宁 沈阳 110016; 2.大连医科大学研究生院
I-125粒子植入联合化疗和单纯化疗对胰腺癌疗效的荟萃分析
宁 峥1,2, 李宏宇1,2, 郭晓钟1, 崔忠敏1, 祁兴顺1, 侯飞飞1
1.沈阳军区总医院消化内科,辽宁 沈阳 110016; 2.大连医科大学研究生院
目的 分析评价I-125粒子植入联合化疗和单纯化疗对胰腺癌的疗效。方法 通过万方数据库、VIP、CNKI和PubMed数据库收集有关文献。比较两种方法的有效率、临床受益率和生存率。结果 纳入14篇研究文献,共859例患者,分为实验组:I-125粒子植入联合化疗组,共411例;对照组:单纯化疗组,共448例。实验组有效率较对照组提高24%(95%CI: 0.16~0.32,P<0.00001)。实验组临床受益率较对照组提高23%(95%CI: 0.17~0.30,P<0.00001)。实验组与对照组相比,实验组的6个月生存率可提高22%(95%CI: 0.10~0.34,P<0.00001),实验组的12个月生存率可提高27%(95%CI: 0.15~0.39,P<0.00001)。结论 与单纯化疗相比,I-125粒子植入联合化疗能有效地提高胰腺癌治疗的有效率、临床受益率、生存率。
胰腺癌;I-125粒子植入;化疗;有效率;临床受益率;生存率
胰腺癌具有高转移性,大多数胰腺癌患者丧失了手术切除的机会,而选择其他治疗方法,包括放疗和化疗。当前,在局部进展期胰腺癌无法手术切除的患者中,主要治疗手段是联合放化疗。传统全身放疗毒副作用较大,联合化疗毒性相应增加。20世纪初,国外学者率先提出了一种内放疗模式,即在肿瘤体内或周围行微型放射性粒子源植入,通过放射源发出持续低能γ射线,使肿瘤组织受到最大程度的杀伤,同时使正常组织不损伤或仅有轻微损伤,从而控制肿瘤复发并保护正常组织[1]。近几年兴起的I-125放射性粒子源具有体积小、持续辐射、毒副反应轻微等特点,在临床上已有应用,因此有必要对I-125粒子植入联合化疗的疗效进行荟萃分析,为临床提供更加明确的应用依据。
1 资料与方法
1.1 检索策略 查询万方数据库、VIP、CNKI和PubMed数据库收集相关文献。中文检索词为“胰腺癌”、“化疗”、“I-125粒子植入”。英文检索词为:pancreatic cancer,I-125 particles implantation,chemotherapy。
1.2 纳入标准 (1)所有患者均经病理或影像学诊断为胰腺癌,已失去根治手术的机会,但可行姑息手术(胆管或十二指肠支架植入或胆肠吻合、胃空肠吻合等);(2)Karnofsky评分[2](KPS)>60分,预计生存期>3个月。心、肝、肾功能及血常规基本正常。均为初治患者,未接受过放化疗;(3)实验组为I-125粒子联合化疗,对照组为单纯化疗;(4)原始文献包含有疗效评价指标:有效率、临床受益率和生存率。排除标准:胰腺癌以外的肿瘤;无对照组;重复报道;数据描述不详;动物实验。
1.3 观察指标
1.3.1 有效率:应用世界卫生组织(WHO)实体瘤疗效标准[3]。完全缓解(CR):肉眼所见肿瘤完全消失;部分缓解(PR):肿瘤体积减小50%以上;稳定(SD):肿瘤体积减小或增大不足25%;病变进展(PD):肿瘤体积增大超过25%,或出现新病灶。所有患者均以CT影像作为介入治疗后评估依据。有效率(%)=(PR+CR)/样本数×100%。
1.3.2 临床受益率:应用Burris等[4]制定的临床受益疗效评估标准,包括KPS体力评分、疼痛评分、体质量变化3个方面。临床受益标准:(1)疼痛强度减轻≥50%或镇痛药物用量减少≥50%;(2)体力状况按KPS体力评分标准改善≥20分;(3)如果疼痛程度及体力状况均稳定,则非水肿或体腔积液的体质量增加≥7%。以上任何一项指标好转且持续4周以上,无其他任何1项恶化,定义为有效。受益率(%)=有效例数/样本数×100%。
1.3.3 生存率:主要为6个月及12个月生存率。
1.4 资料提取和分析 对纳入文献汇总建立数据库。采用Cochrane协作网提供的Review Manager 5.2软件对资料进行分析。本文主要比较胰腺癌的粒子植入联合化疗方案是否优于单纯化疗方案,评价目标是有效率、临床受益率和生存率,其结局变量为接受粒子植入联合化疗患者和接受单纯化疗患者的差值,即治疗优势(risk difference,RD)。
1.5 文献质量评分 采用2002年改良后的Jadad量表[5],内容包括:随机序列的产生:(1)恰当:计算机产生的随机数字或类似方法(2分);(2) 不清楚:随机试验但未描述随机分配的方法(1分);(3)不恰当:采用交替分配的方法如单双号(0分)。随机化隐藏:(1)恰当:中心或药房控制分配方案、或用序列编号一致的容器、现场计算机控制、密封不透光的信封或其他使临床医生和受试者无法预知分配序列的方法(2分);(2)不清楚:只表明使用随机数字表或其他随机分配方案(1分);(3)不恰当:交替分配、病例号、星期日数、开放式随机号码表、系列编码信封以及任何不能防止分组的可预测性的措施(0分)。盲法:(1)恰当:采用了完全一致的安慰剂片或类似方法(2分);(2)不清楚:试验陈述为盲法,但未描述方法(1分);(3)不恰当:未采用双盲或双盲的方法不恰当,如片剂和注射剂比较(0分);(4)未使用(0分)。撤出与退出:(1)描述了撤出或退出的数目和理由(1分);(2)未描述撤出或退出的数目或理由(0分)。1~3分视为低质量,4~7分视为高质量。
2 结果
2.1 文献基本情况 万方数据库共检索出89篇,VIP数据库检索出58篇,CNKI数据库检索出59篇,PubMed数据库检索出1篇,手动检索1篇。其中重复的文章共98篇,和本研究无关的共42篇,动物实验共6篇,无对照组的文献共32篇,综述共15篇,对照组为I-125粒子植入而非化疗的文献共1篇。最终符合入选标准的文献共14篇。其中,中文文献13篇,外文文献1篇(见表1)。
表1 相关文献基本情况
Tab 1 Characteristics of relevant articles

作者 年份实验组对照组文献类型治疗用药粒子植入方式曹智刚等[6]20093030前瞻性5-Fu+EPI+MMC(5-Fu:1000mg,EPI:80mg,MMC:10~20mg),动脉灌注,1次/dCT引导江月萍等[7]20082122回顾性GEM:1000mg/m2,静滴,1次/周×3周,休息1周,1次/1周,连用3周,共1个疗程超声引导胡智强等[8]20073232前瞻性GEM:1000mg/m2,静滴,1次/周×3周,间隔1周,连续3周,共3个疗程CT引导高飞等[9]20081211前瞻性GEM+P(GEM:1000mg/m2;P:30mg/m2),动脉灌注,GEM:第1、8和15天;P:第1、3、5天;4周1个疗程,共3个疗程CT引导张峰等[10]20092224前瞻性GEM:1000mg/m2,静滴,1次/周×3周,休息1周,连用3周,1个疗程CT引导李玉亮等[11]20071825前瞻性GEM:1000mg/m2,动脉灌注,1次/4周,连续3个疗程CT引导
(续表1)

作者 年份实验组对照组文献类型治疗用药粒子植入方式孙勇等[12]20092522回顾性GEM+P(GEM:1000mg/m2,P:30mg/m2),静滴,GEM:第1、8和15天;P:第4~6天;28d为1个疗程CT引导李凯等[13]20071241回顾性GEM:1000mg/m2,静滴,1次/周×3周,间隔1周,连续3个疗程CT引导沈俊杰等[14]20103027前瞻性GEM+OX(GEM:1000mg/m2,OX:100mg/m2,动脉灌注,4周后重复1次GEM:第1、8天使用,每21天为1个疗程,共2个疗程;OX:第1天使用,每21天为1个疗程,共2个疗程。CT引导彭晓赤等[15]20136045前瞻性GEM+P(GEM:1000m/m2,P:40mg/m2),动脉灌注,45d1个疗程CT引导吴汉青等[16]20096287回顾性GEM:1000mg/m2,静滴,1次/周×3周,休息1周,每4周重复1次术中直视YU等[17]20141515前瞻性GEM:1000mg/m2,静滴,1次/周,共2个疗程CT引导杨文魁等[18]20144543前瞻性GEM+P(GEM:1000m/m2,P:75mg/m2,静滴,GEM:1次/周×2周,第1天、第8天分1~4天应用,P:75mg/m2,分4天使用。21d为1个疗程,共4个疗程。CT引导李帅等[19]20152724前瞻性S-1:80mg/m2,口服,2次/天,连用3周停药1周,4周为1个疗程,共4个疗程CT引导
注: GEM:吉西他滨;P:顺铂;OX:奥沙利铂;5-Fu:5-氟尿嘧啶;EPI:表阿霉素;MMC:丝裂霉素;S-1:替吉奥胶囊。
2.2 文献质量的评价 采用改良后的Jadad量表对每篇文献的研究方法进行质量评价,10篇前瞻性文章均为低质量文章(1~3分),评价过程详见表2。
表2 文献质量分析
Tab 2 Literature quality analysis
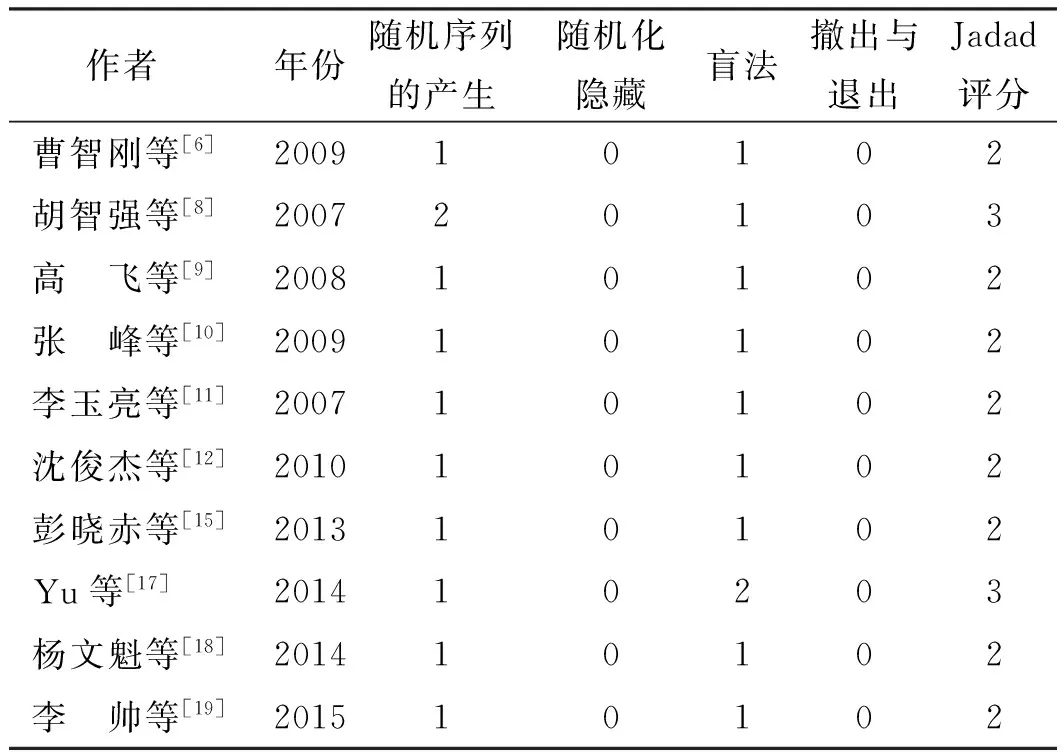
作者 年份随机序列的产生随机化隐藏盲法撤出与退出Jadad评分曹智刚等[6]200910102胡智强等[8]200720103高 飞等[9]200810102张 峰等[10]200910102李玉亮等[11]200710102沈俊杰等[12]201010102彭晓赤等[15]201310102Yu等[17]201410203杨文魁等[18]201410102李 帅等[19]201510102
2.3 结果分析
2.3.1 有效率:结果显示实验组比对照组相比可以提高有效率24%,差异有统计学意义(95%CI:0.16~0.32,P<0.00001)。各项研究间无显著异质性(P=0.11;I2=33%,见图1)。
2.3.2 临床受益率:有11篇提到了临床受益疗效。实验组较对照组可以提高临床受益率23%,差异有统计学意义(95%CI:0.17~0.30,P<0.00001,见图2)。各项研究间无显著异质性(P=0.66;I2=0%,见图2)。
2.3.3 生存率:分析入组的14篇文章,有4篇提到了生存率,实验组与对照组相比,实验组6个月的生存率可提高22%,差异有统计学意义(95%CI:0.10~0.34,P<0.00001),,各项研究间无显著异质性(P=0.74;I2=0%,见图3)。实验组12个月的生存率可提高27%(95%CI:0.15~0.39,P<0.00001),各项研究间无显著异质性(P=0.47;I2=0%,见图4)。

图1 有效率荟萃分析

图2 临床受益率荟萃分析

图3 6个月生存率荟萃分析
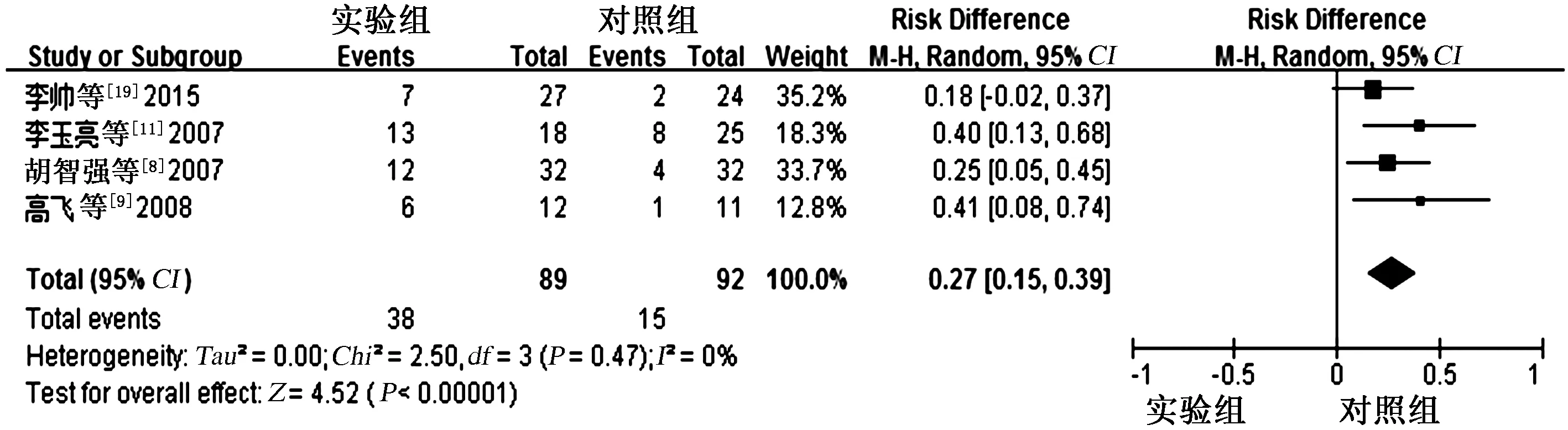
图4 12个月生存率荟萃分析
2.3.4 偏倚结果分析:漏斗图显示对称性尚可,偏倚性较小(见图5~6)。
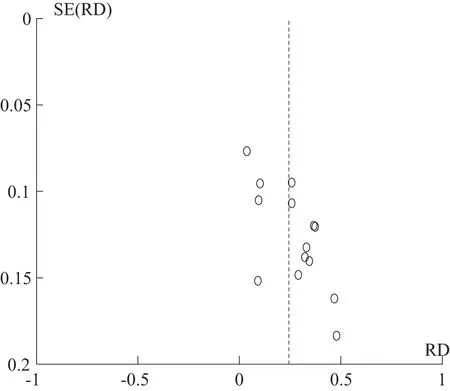
图5 有效率漏斗图
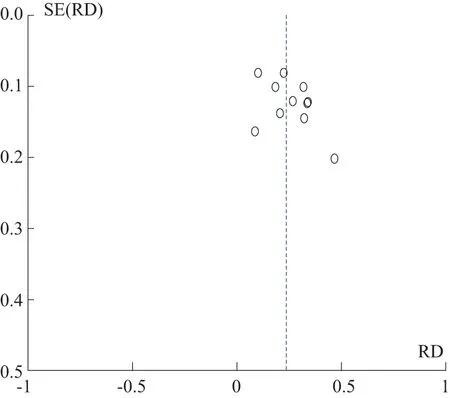
图6 临床受益率漏斗图
3 讨论
胰腺癌预后差,初诊时只有10%~15%的患者可行十二指肠部分或全切除的手术治疗。术后复发和转移风险仍较高,约80%的患者术后出现局部复发,因此术后辅助治疗很关键,主要治疗方法是单纯化疗或联合放化疗。目前,尚无胰腺癌辅助治疗的规范流程。北美学者根据胃肠道肿瘤协作组(GI Tumor Study Group,GITSG)及美国肿瘤放射治疗协作组(Radiation Therapy Oncology,RTOG)的多项随机临床研究结果,推荐联合放化疗;而欧洲学者根据ESPAC-1和CONKO-001的研究结果,推荐采用单纯化疗[20]。
胰腺位置较深,胰腺癌外照射剂量通常在40~60 Gy会引起严重的毒副反应,因此限制了放疗的应用。1934年,Handley在世界上首先运用镭针插植成功治疗胰腺癌。自此拉开了肿瘤内植入放射性粒子治疗肿瘤的序幕[21]。目前出现了在肿瘤体内植入放射性I-125粒子的方法。其半衰期可达59.6 天,可以对靶区进行高剂量、长时间、近距离积累式照射,提高对肿瘤的杀伤效果,而对周围正常组织损伤较小。本研究结果显示,I-125粒子植入联合化疗的疗效优于单纯化疗。这主要可能在于I-125粒子产生的γ射线在低剂量时即能破坏肿瘤细胞的DNA双链,协同细胞毒性药物,促使肿瘤细胞凋亡,同时也可以破坏腹膜后神经丛,减轻疼痛。当然,粒子植入也有不良反应,主要为恶心、呕吐等消化道症状、白细胞和血小板下降、放射性肠炎、腹腔感染等。然而,实验组与对照组之间的并发症发病率差异无统计学意义。14篇文献中有1篇[13]提到了粒子丢失和移位,但未发现有脏器功能受损。这些均说明粒子植入具有较好的安全性。
就化疗方案来说,2011年《NCCN胰腺癌临床实践指南》[22]指出若考虑行同步放化疗,建议选择基于5-Fu或吉西他滨的同步放化疗;放化疗前或后行5-Fu+亚叶酸钙或吉西他滨全身化疗。本研究纳入文献的化疗方案虽然不完全相同,但基本上都是符合指南的化疗方案。国内有研究[23]提示,GEMOX、GEMCAP联合化疗方案治疗胰腺癌,有较好的应用前景,值得进一步临床试验。国外Yoshitomi等[24]发现,胰腺癌术后辅助吉西他滨联合顺铂为基础的化疗方案安全有效。
本研究的主要不足之处在于化疗药物给药途径不尽相同。有5篇文章使用了动脉灌注的方法,1篇文章使用口服化疗药物,其余均使用静脉滴注。有学者发现[25],与外周静脉化疗相比,动脉灌注能显著提高中晚期胰腺癌患者的临床受益率,其不良反应轻微,患者耐受良好。但尚缺少大规模临床随机对照研究来比较两者之间的差异。
本研究初步表明,放射性I-125粒子植入联合化疗的方案在有效率、临床受益率和生存率方面均较单纯化疗方案有所提高,对以后开展大规模临床随机对照研究有一定的参考意义。
[1]Wang JJ,Tang JT, Li G. Brachytherapy for tumor [M]. Beijing: Beijing Medical University Press, 2001: 200. 王俊杰, 唐劲天, 黎功. 放射性粒子近距离治疗肿瘤[M]. 北京:北京医科大学出版社, 2001: 200.
[2]Zhou JC. Practical medical oncology [M]. Beijing: People’s Medical Publishing House, 2003: 45-46. 周际昌. 实用肿瘤内科学[M]. 北京: 人民卫生出版社, 2003: 45-46.
[3]Liu Y, Cheng Y. Reaserch on response evaluation criteria in solid tumors [J]. Pract Oncol J, 2004, 18(2): 149-152. 柳影, 程颖. 实体肿瘤疗效评价标准的研究[J]. 实用肿瘤学, 2004, 18(2): 149-152.
[4]Burris HA 3rd, Moore MJ, Andersen J, et al. Improvements in survival and clinical benefit with gemcitabine as first line therapy for patients with advanced pancreas cancer:a randomized trial [J]. J Clin Oncol, 1997, 15(6): 2403-2413.
[5]Jadad AR, Moore RA, Caoroll D, et al. Assessing the quality of reports of randomized clinical trials is blinding necessary [J]. Controoed Clin Trials, 1996, 17(1): 1-12.
[6]Cao ZG, Wang HH, Bai B, et al. Short-term curative effect of125I seed combined with intra-arterial infusion chemotherapy for pancreatic cancer [J]. J Pract Radiol, 2009, 5(11): 1649-1651. 曹智刚, 王宏辉, 白彬, 等.125I粒子联合动脉化疗治疗胰腺癌的近期疗效[J]. 实用放射学杂志, 2009, 25(11): 1649-1651.
[7]Jiang YP, Jin ZD, Li ZS, et al. The clinical benefit response in treatment of unresectable pancreatic carcinoma by endoscopic ultrasongraphy-guided interstitial implantation of iodine-125 seeds combined with gemcitabine chemotherapy [J]. Chin J Pancreatol, 2008, 8(5): 289-291. 江月萍, 金震东, 李兆申, 等.125I粒子植入联合吉西他滨治疗胰腺癌临床受益疗效评价[J]. 中华胰腺病杂志, 2008, 8(5): 289-291.
[8]Hu ZQ, Qian LY, Wei YS, et al. I-125 particles implanted into tumor combined with gemcitabine to treat extended local pancreas cancer [J]. China Medical Engineering, 2007, 15(1): 87-89. 胡智强, 钱立元, 魏源水, 等.125I放射性粒子术中植入联合吉西他滨治疗局部进展期胰腺癌的临床研究 [J].中国医学工程, 2007, 15(1): 87-89.
[9]Gao H, Fan WJ, Gu YK, et al. Effect of radioiodine-125 seed implantation combined with regional infusion chemotherapy on pancreatic cancer of intermediate and advanced stage [J]. Journal of Sun Yat-Sen University (Medical Science), 2008, 29(4): 459-464. 高飞, 范卫君, 顾仰葵, 等.125I放射性粒子植入联合区域性动脉灌注化疗对中晚期胰腺癌的作用[J].中山大学学报(医学科学版), 2008, 29(4): 459-464.
[10]Zhang F, Zhang CB, Tian JM, et al. Response evaluation of CT guided125I particles implantation and chemotherapy alone in the treatment of pancreatic cancer [J]. J Intervent Radiol, 2009, 18(9): 673-675. 张峰, 张长宝, 田建明, 等. CT引导下125I放射性粒子植入和单纯化疗治疗胰腺癌的疗效评价[J]. 介入放射学杂志, 2009, 18(9): 673-675.
[11]Li YL, Wang YZ, Wang XH, et al.125I implantation combined with gemcitabine in the treatment of advanced pancreatic cancer [J]. Journal of Shandong University (Health Science), 2007, 45(4): 393-396. 李玉亮, 王永正, 王晓华, 等. 动脉灌注吉西他滨联合125I粒子胰腺内植入治疗进展期胰腺癌[J]. 山东大学学报(医学版), 2007, 45(4): 393-396.
[12]Sun Y, Gao JB, Zhou ZG, et al. CT guided implantation of I-125 particles combined with chemotherapy for advanced pancreatic cancer: a report of 25 cases[J]. Journal of Zhengzhou University (Medical Sciences), 2009, 44(6): 1273-1274. 孙勇, 高剑波, 周志刚, 等. CT引导下125I粒子植入联合化疗治疗晚期胰腺癌25例体会[J]. 郑州大学学报(医学版), 2009, 44(6): 1273-1274.
[13]Li K, Tao J, Wang CY, et al. Treatment of advanced unresectable pancreatic cancer by palliative operation combined with125I brachytherapy and chemotherapy [J]. Chin J Gen Surg, 2007, 22(2): 104-106. 李凯, 陶京, 王春友, 等. 姑息手术结合术中碘125粒子植入和术后化疗治疗晚期胰腺癌[J]. 中华普外科杂志, 2007, 22(2): 104-106.
[14]Shen JJ, Li HP, Huang YH, et al. Clinical study of transarterial chemotherapy in combined with iodine-125 seeds implantation in treating the advanced pancreatic carcinoma [J]. J Pract Radiol, 2010, 26(7): 1002-1005. 沈俊杰, 李鹤平, 黄勇慧, 等. 动脉灌注化疗联合CT引导下放射性I粒子植入术治疗中晚期胰腺癌的临床研究[J].实用放射学杂志, 2010, 26(7): 1002-1005.
[15]Peng XC, Liu YS, Dai WY, et al. Clinical research of CT guided percutaneous implantation of radioactive125I particles for the treatment of pancreatic cancer [J]. China Health Care & Nutrition, 2013, 23(6): 3402. 彭晓赤, 刘院生, 戴文燕, 等. CT引导下经皮穿刺植入放射性125I粒子治疗胰腺癌的临床研究[J]. 中国保健营养(上), 2013, 23 (6): 3402.
[16]Wu HQ, Wu HS, Yang ZY, et al. Efficacy of iodine-125 seed implantation in pancreatic carcinoma [J]. World Chinese Journal of Digestology, 2009, 17(28): 2951-2954. 吴汉青, 吴河水, 杨智勇, 等.125I粒子植入在胰腺恶性肿瘤治疗中的疗效分析[J]. 世界华人消化杂志, 2009, 17(28): 2951-2954.
[17]Yu YP, Yu Q, Guo JM, et al. (125)I particle implantation combined with chemoradiotherapy to treat advanced pancreatic cancer [J]. Br J Radiol, 2014, 87(1036): 20130641.
[18]Yang WK, Chen Y, Wang L, et al. CT-guided125I interstitial implantation combined with gemcitabine/cisplatin chemotherapy for treatment of locally advanced pancreatic carcinoma [J]. World Chinese Journal of Digestology, 2014, 22(10): 1455-1459. 杨文魁, 陈勇, 王磊, 等. CT引导下125I粒子植入联合GP方案治疗局部进展期胰腺癌[J]. 世界华人消化杂志, 2014, 22(10): 1455-1459.
[19]Li S, Zhou ZG, Gao JB, et al. Efficacy of CT-guided implantation of125I seeds combined with S-1 in treatment of pancreatic cancer in elderly patients [J]. Journal of Zhengzhou University (Medical Sciences), 2015, 52(2): 270-274. 李帅, 周志刚, 高剑波, 等. CT引导下组织间植入125I粒子联合替吉奥治疗老年胰腺癌疗效分析[J]. 郑州大学学报(医学版), 2015, 52(2): 270-274.
[20]Zhang J, Lu JD, Peng CH, et al. Controversy and consensus of the adjuvant therapy of pancreatic cancer [J].China Oncology, 2009, 19(8): 580-584. 张俊, 陆嘉德, 彭承宏, 等. 胰腺癌辅助治疗的争议和共识[J]. 中国癌症杂志, 2009, 19(8): 580-584.
[21]Wang SK, Zhang AY, Zhang WH, et al. Progress of radioactive seed implantation in the treatment of tumor [J]. BMU Journal, 2007, 30(2): 124-126. 王绍奎, 张爱云, 张维浩, 等. 放射性粒子植入治疗肿瘤的进展[J]. 滨州医学院院学报, 2007, 30(2): 124-126.
[22]Zhao YP. Introduction of NCC clinical guideline for pancreatic cancer(Chinese version) [J]. Chin J Surg, 2011, 49(9): 771-773. 赵玉沛. 2011年《NCCN胰腺癌临床实践指南》(中国版)解读[J]. 中华外科杂志, 2011, 49(9): 771-773.
[23]Xie DR, Liang HL, Yang Q, et al. Subgroup meta-analyses of survival rate of gemcitabine-based combinatione chemotherapy as fist-line therapy for advanced pancreatic cancer [J]. Journal of Sun Yat-Sen University (Medical Sciences), 2007, 28(5): 565-568. 谢德荣, 梁汉霖, 杨琼, 等. 吉西他滨联合化疗一线治疗晚期胰腺癌生存结果的亚组meta分析[J]. 中山大学学报(医学科学版), 2007, 28(5): 565-568.
[24]Yoshitomi H, Togawa A, Kimura F, et al. A randomized phase II trial of adjuvant chemotherapy with uracil/tegafur and gemcitabine versus gemcitabine alone in patients with resected pancreatic cancer [J]. Cancer, 2008, 113(9): 2448-2456.
[25]Jia L, Zheng JJ, Zhang SN, et al. Gemcitabine arterial infusion chemotherapy versus intravenous chemotherapy for patients with advanced pancreatic cancer:a comparative study [J]. Chin J Pancreatol, 2009, 9(1): 15-17. 贾林, 郑建军, 张世能, 等. 吉西他滨动脉灌注化疗与外周静脉化疗治疗中晚期胰腺癌的比较研究[J]. 中华胰腺病杂志, 2009, 9(1): 15-17.
(责任编辑:李 健)
Curative effect of I-125 particles implantation combined with chemotherapy and chemotherapy alone in pancreatic cancer: a Meta-analysis
NING Zheng1,2, LI Hongyu1,2, GUO Xiaozhong1,2, CUI Zhongmin1, QI Xingshun1, HOU Feifei1
1.Department of Gastroenterology, Shenyang Military General Hospital, Liaoning 110016; 2.Graduate School of Dalian Medical University, China
Objective To evaluate the curative effect of I-125 particles implantation combined with chemotherapy and chemotherapy alone in pancreatic cancer. Methods The relevant literatures were collected by searching the databases of WanFang, VIP, CNKI and PubMed. The effective rate, clinical benefit rate and survival rate of two methods were compared. Results A total of 14 literatures (859 patients) were included. They were divided into experimental group: I-125 particles implantation combined chemotherapy, and control group: chemotherapy alone. Compared with control group, the effective rate was improved by 24% in experimental group (95%CI: 0.16-0.32,P<0.00001), the clinical benefit rate were improved by 23% in experimental group (95%CI: 0.17-0.30,P<0.00001), the 6-month survival rate was improved by 22% in experimental group (95%CI: 0.10-0.34,P<0.00001), and the 12-month survival rate was improved by 27% in experimental group (95%CI: 0.15-0.39,P<0.00001). Conclusion Compared with chemotherapy alone, the I-125 particles implantation combined with chemotherapy can effectively improve effective rate, clinical benefit rate, and survival rate in the treatment of pancreatic cancer.
Pancreatic cancer; I-125 particles implantation; Chemotherapy; Effective rate; Clinical benefit rate; Survival rate
10.3969/j.issn.1006-5709.2016.03.024
宁峥,硕士研究生,研究方向:肝硬化。E-mail:ningzheng1988@126.com
李宏宇,博士研究生,副主任医师,研究方向:肝硬化。E-mail:13309887041@163.com
R735.9
A
1006-5709(2016)03-0320-06
2015-06-24

