山茱萸红色素稳定性的研究
吴海霞,马国刚
(运城学院生命科学系,山西运城 044000)
山茱萸红色素稳定性的研究
吴海霞,马国刚
(运城学院生命科学系,山西运城044000)
以A440 nm吸光度为指标,研究pH值、温度、光照、金属离子、氧化剂、还原剂及常用食品添加剂等对山茱萸红色素稳定性的影响。结果表明,山茱萸红色素在酸性条件下较为稳定,但随着酸性减弱,其颜色变浅;在一定的温度范围内(0~90℃)对热比较稳定;不同光照条件对其具有一定程度的降解作用;Na+,Ca2+,Mg2+,Al3+,Zn2+,K+,Cu2+等金属离子对色素影响不大,但Fe3+的存在会使色素变色而不稳定,而Ba2+会使色素溶液产生部分沉淀而浑浊;氧化剂H2O2和还原剂Na2SO3可使色素褪色;蔗糖、葡萄糖、抗坏血酸、苯甲酸钠等食品添加剂对色素稳定性影响不大,柠檬酸和食盐对色素具有一定的增色作用。
山茱萸;红色素;稳定性
色素是常用的食品添加剂,有合成色素和天然色素之分。与合成色素相比,天然色素作为生物体内原有的组成成分,其安全性较高,有的还具有增加消化液的分泌、促进食欲的功效[1]。但是,天然色素在着色性和稳定性方面还略逊于合成色素,同时由于其较高的原料价格及提取成本也使其在生产中的应用受到限制。山茱萸是一种传统中药材,其果实呈鲜艳红色,并含有丰富的营养成分和生理活性成分,目前的研究均侧重于对其中有效成分的研究利用[2-3],而对其色素的研究较少[4]。本试验在提取山茱萸红色素的基础上,对山茱萸红色素的稳定性进行研究分析,为新型天然色素的开发及山茱萸资源的深度利用提供思路。
1 材料与方法
1.1试验原料与主要试剂
山茱萸,采自山西临汾市浮山县。
甲醇、丙酮、抗坏血酸、苯甲酸钠、柠檬酸、过氧化氢、三氯化铝、邻苯二甲酸氢钾、三氯化铁等,均为分析纯。
1.2仪器设备
微型高速万能粉碎机,天津泰斯特仪器有限公司产品;101A-1E型思安热恒温鼓风干燥箱,上海实验仪器总厂产品;LXJ-II型离心沉淀机,上海医分仪器制造有限公司产品;WFZ UV-2100型紫外可见分光光度计,尤尼柯(上海)仪器有限公司产品;PHS-3C型精密酸度计,上海大普仪器有限公司产品。
1.3试验方法
1.3.1山茱萸红色素提取工艺流程
山茱萸粉→按料液比1∶20加入80%乙醇→超声波辅助提取(60℃,400 W,15 min)→离心(3 000 r/min,20 min)→取上清液→上清液即为色素溶液。
1.3.2最大吸收波长的确定
将提取所得色素溶液稀释后,用0.05 mol/L邻苯二甲酸氢钾-盐酸缓冲液将其pH值分别调至1.0,2.0,3.0,于400~500 nm下测其吸光度[5],确定其最适作用pH值及最大吸收波长。
1.3.3光照对色素稳定性影响
取山茱萸红色素样液,稀释1倍后调至pH值3.0,分别置于暗光、室内、L66强光下,每隔90 min取出,测定A440 nm。
1.3.4pH值对色素稳定性影响
取山茱萸红色素溶液,稀释1倍后分别用0.05mol/L的邻苯二甲酸氢钾-盐酸缓冲液、磷酸氢二钠-柠檬酸缓冲液及硼砂-氢氧化钠缓冲液,依次调溶液pH值至1.0~10.0,并测定A440 nm[6-8]。
1.3.5温度对色素稳定性影响
(1)温度和时间对色素稳定性影响。取5 mL色素溶液6份,稀释后调pH值至3.0,分别放入40,50,60,70,80,90℃的恒温水浴锅,每隔30 min测定A440 nm。
(2)温度和pH值对色素稳定性影响。取pH值1.0,2.0,3.0,4.0,5.0,6.0,7.0,8.0,9.0,10.0的色素溶液各1份,放入温度为40,50,60,70,80,90℃的恒温水浴锅内,30 min后测定A440 nm。
1.3.6金属离子对色素稳定性影响
分别配置含NaCl,CaCl2,MgCl2,AlCl3,ZnCl2,KCl,CuSO4,BaCl2(0.01,0.02,0.03 mol/L),FeCl3(0.001,0.002,0.003 mol/L) 的金属离子溶液,各取1 mL分别加入pH值3.0的色素溶液中,测定A440nm[6-8]。
1.3.7氧化剂对色素稳定性影响
配制含H2O2浓度为0,0.1%,0.5%的pH值3.0色素溶液,于室温暗置24 h,测其于400~500 nm波长范围内的吸光度[6-8]。
1.3.8还原剂对色素稳定性影响
配制含Na2SO3浓度为0,0.012,0.06 mg/mL的pH值3.0色素溶液,分别于室温暗置24 h,绘制于400~500 nm波长范围内吸光度,继续放置至7 d后,绘制吸光度[6-8]。
1.3.9食品添加剂对色素稳定性影响
分别配制含蔗糖(0,0.5%,5.0%,10.0%),葡萄糖(0,5%,10%,15%)以及柠檬酸(0,0.5%,1.0%,1.5%),抗坏血酸(0,0.5%,1.0%,1.5%),苯甲酸钠(0,0.01%,0.10%,0.50%),食盐(0,0.5%,1.0%,2.0%)的pH值3.0色素溶液,测定A440 nm[6-8]。
2 结果与分析
2.1山茱萸红色素最大波长的确定
最大吸收波长的确定见图1。
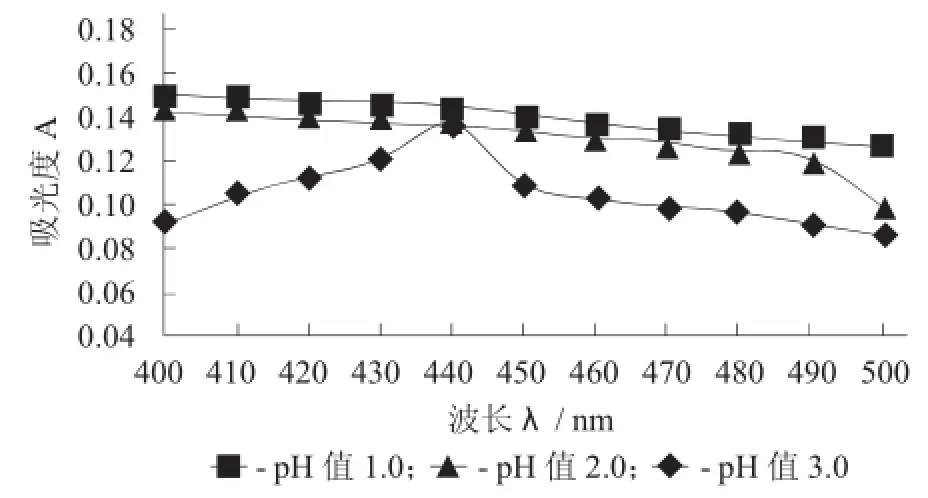
图1 最大吸收波长的确定
由图1可知,色素溶液在pH值3.0下,于400~ 500 nm间有1个最大吸收波峰,处于440 nm波长处。于400~440 nm范围内,随着波长的增大吸光度有所增大;当波长大于440 nm时,随着波长的增大吸光度反而有所降低。这是因为在不同的波长下,山茱萸红色素的选择性吸收所导致。因此,之后试验均将色素溶液pH值调至3.0,并且选择440 nm作为测定吸光度的最佳波长。
2.2光照对山茱萸红色素稳定性影响
光照对山茱萸红色素稳定性的影响见图2。
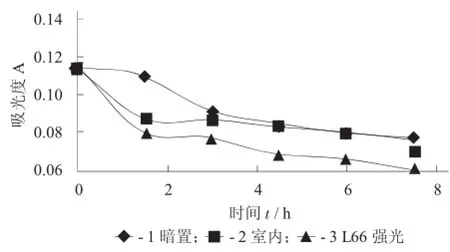
图2 光照对山茱萸红色素稳定性的影响
由图2可知,1.5 h内,暗光下放置的色素溶液随时间的延长吸光度下降不明显;在室内和L66强光下放置的色素溶液吸光度迅速下降,色素溶液颜色变淡。之后,暗置色素溶液的吸光度也开始迅速下降,3 h后3种溶液的吸光度趋于恒定,L66强光下溶液的颜色较其他2种放置条件下的稍淡。由此认为,山茱萸红色素对光照比较敏感,但在一定贮藏时间内,其稳定性较好。建议在对山茱萸红色素或其相关产品进行包装、储运、使用时,要注意光照对制品色泽的影响,建议采用深色包装或避光保存的方式进行贮藏。
2.3pH值对色素稳定性影响
pH值对色素稳定性的影响见表1。
溶液中不同浓度的H+和OH-会使色素的发色基团及化学结构发生变化,从而引起变色。由表1可知,山茱萸色素在pH值1.0~4.0的酸性溶液中比较稳定,呈鲜亮的红色;pH值5.0~6.0范围内,颜色略微变浅。在中性及碱性条件下,其颜色发生改变,逐渐由浅紫色变为紫色,pH值10.0时变为棕黄色。由于本色素在酸性条件下相对稳定,呈明亮鲜红色,故适宜应用于果汁、饮料等酸性食品中。

表1 pH值对色素稳定性的影响
2.4温度对色素稳定性影响
2.4.1温度与时间对色素稳定性的影响
温度与时间对色素稳定性影响见表2。

表2 温度与时间对色素稳定性影响
由表2可知,在相同温度下,色素溶液随着时间的延长其吸光度略有降低,但变化不明显;在不同的温度下放置相同的时间,色素溶液吸光度会随着温度的升高逐渐增大,但变化幅度也不大,溶液颜色变化不明显。说明山茱萸红色素对热的稳定性较好,并且可以较长时间放置,这与长时间光照下的变化一致。
2.4.2温度与pH值对色素稳定性影响
温度与pH值对色素稳定性影响见表3。
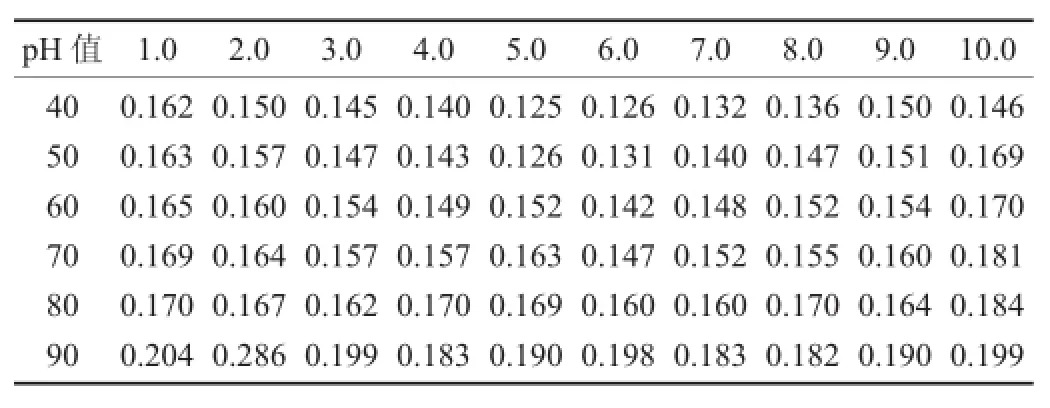
表3 温度与pH值对色素稳定性影响
由表3可知,在相同的pH值下,随着温度的升高,色素溶液的吸光度逐渐升高,但变化不明显;在任何温度下,不同pH值色素溶液颜色变化与2.3中的现象一致,均表现为随着溶液由酸到碱的变化,颜色会由红变紫。结果证明,该色素对热比较稳定,而pH值对其影响较大。
2.5金属离子对色素稳定性影响
金属离子对色素稳定性影响见表4。
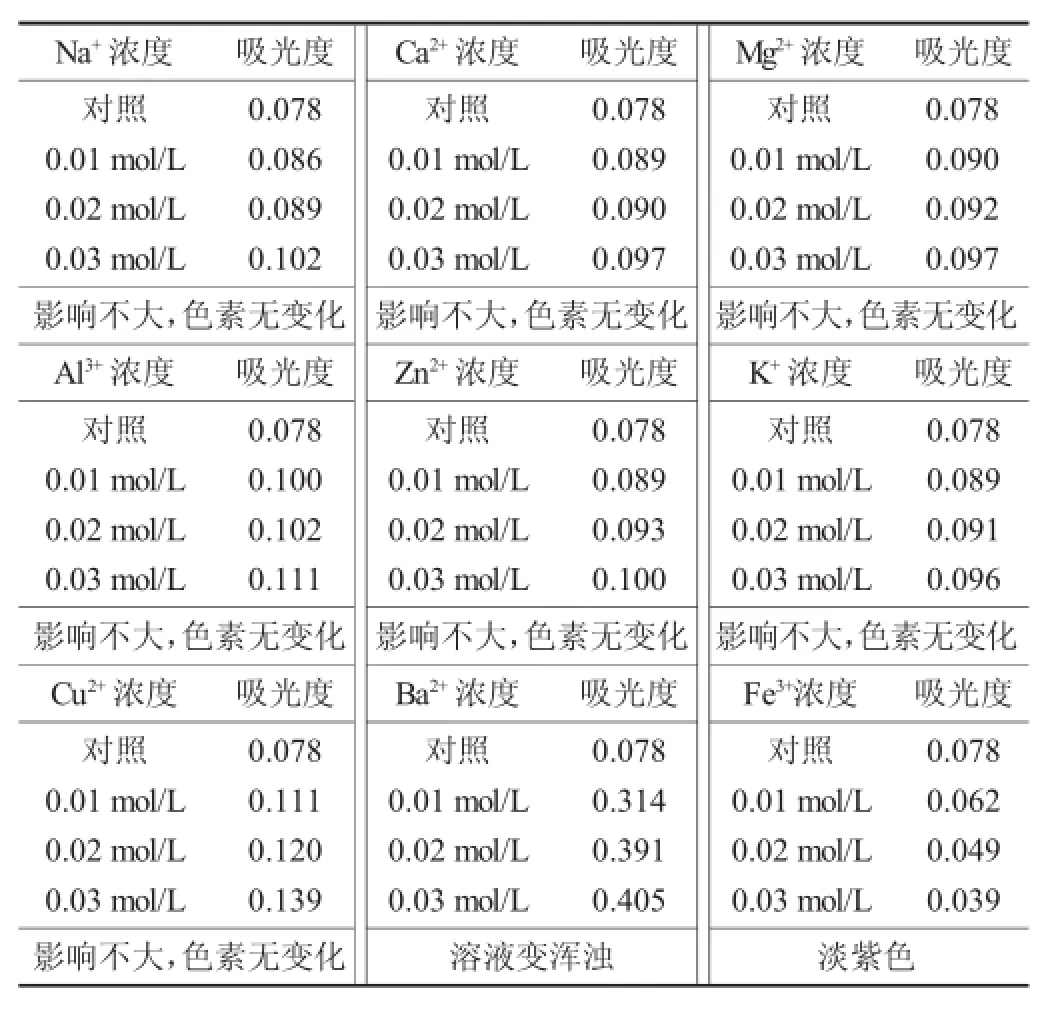
表4 金属离子对色素稳定性影响
由表4可知,含Na+,Ca2+,Mg2+,Al3+,Zn2+,K+,Cu2+的色素溶液与对照液相比,其吸光度均有不同程度的增加,但颜色变化不大;试验中观察到Fe3+会使色素溶液的颜色发生变色而变为淡紫色,说明该金属离子可能会与此色素中的某些基团反应而使其结构发生变化,或者通过影响溶液酸碱性而使色素结构改变,故在加工与储运中产品应避免与铁器接触;同时,不同浓度Ba2+的存在会使色素溶液变浑浊,这可能是由于Ba2+和山茱萸色素溶液中的某些成分反应生成沉淀的缘故。
2.6氧化剂对色素稳定性影响
H2O2对山茱萸红色素稳定性的影响见图3。
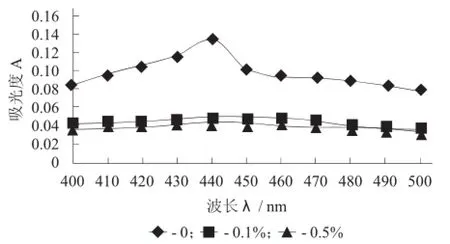
图3 H2O2对山茱萸红色素稳定性的影响
由图3可知,H2O2使色素溶液的吸收峰消失,紫外吸收特征的变化说明色素在氧化剂的作用下结构改变。同时,试验中观察到色素溶液的颜色随着H2O2浓度增大逐渐变浅,直至消失,可见色素对氧化剂极为敏感。
2.7还原剂对色素稳定性影响
Na2SO3对山茱萸红色素稳定性影响见图4。
由图4可知,加入Na2SO3暗置24 h的色素溶液,不同波长下的吸光度均明显降低,吸收峰也几近消失,同时色素溶液褪色,可见还原剂可以使色素发生还原反应而对其稳定性产生影响。继续暗置7 d后,色素溶液吸光度又有较大幅度回升,440 nm处又出现明显吸收峰,溶液的颜色也由淡红色逐渐又转变为红色。这可能是由于室温放置条件下SO2从溶液中溢出,使还原剂部分失效而引起。

图4 Na2SO3对山茱萸红色素稳定性影响
2.8食品添加剂对色素稳定性影响
食品添加剂对色素稳定性的影响见表5。
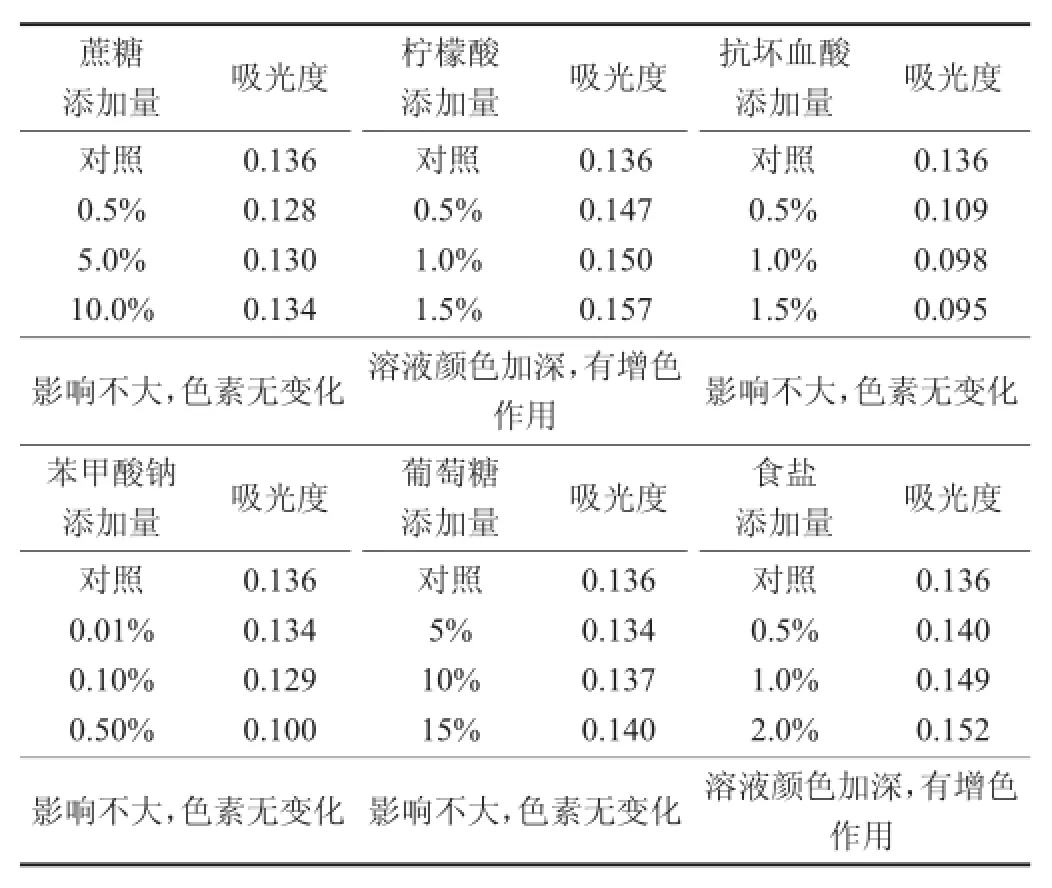
表5 食品添加剂对色素稳定性的影响
由表5可知,与对照相比,添加了不同浓度柠檬酸和食盐后,溶液的吸光度均较对照增大,溶液颜色也明显加深;添加了蔗糖、葡萄糖的色素溶液,其吸光度与对照差别不大,颜色基本没有变化;添加了抗坏血酸和苯甲酸钠的色素溶液,其吸光度均有降低,且浓度越高吸光值越小,但色素溶液的颜色变化不明显。因此,蔗糖、葡萄糖、抗坏血酸和苯甲酸钠对山茱萸红色素的稳定性影响不大,而柠檬酸和食盐对山茱萸红色素具有不同程度的增色作用。
3 结论
pH值3.0时,山茱萸红色素在可见光区440 nm处有最大吸收峰;山茱萸红色素在强酸性溶液(pH值1.0~4.0)中比较稳定,呈现鲜亮红色;0~90℃范围内山茱萸红色素对热比较稳定;山茱萸红色素对光不稳定,随光照强度增大,色素溶液颜色变浅;Na+,Ca2+,Mg2+,Al3+,Zn2+,K+,Cu2+对山茱萸红色素影响不大,Fe3+对该色素具有破坏作用,使色素颜色由红色变为淡紫色,而Ba2+可使色素溶液产生沉淀而浑浊;还原剂Na2SO3可使山茱萸红色素褪色,但脱硫后,色素颜色能基本复原;该色素对氧化剂极为敏感,不同浓度氧化剂均可使其褪色,甚至无色;常用食品添加剂蔗糖、葡萄糖、抗坏血酸、苯甲酸钠等对山茱萸红色素稳定性影响不大,柠檬酸和食盐则对该色素有一定的增色作用。
[1]乔华,张生万,李美萍,等.天然色素稳定性研究及其新的类型划分 [J].食品科学,2006,27(9):69-72.
[2]刘洪.山茱萸及其主要成分的药理学研究进展 [J].南京中医药大学学报,2003,19(4):254-255.
[3]李小平,陈锦屏.山茱萸果皮红色素稳定性的研究 [J].食品研究与开发,2002,23(4):25-28.
[4]皮文霞,蔡宝昌.HPLC法及UV法共同监控山茱萸制剂提取纯化工艺 [J].现代中药研究与实践,2003,17(4):58-59.
[5]徐固华,王欣,等.山楂红色素提取及稳定性研究 [J].安徽农业科学,2007,35(28):8 785-8 786.
[6]陈存社,董银卯,陆辛玫,等.食用天然色素的提取及其稳定性研究 [J].天然产物研究与开发,2001,13(6):39-41.
[7]谢程程,王勇,宫立晶.天然食用色素紫甘薯花青素的稳定性研究 [J].食品工业,2012(6):99-102.
[8]耿敬章.香樟籽色素的超声波辅助提取及其稳定性研究 [J].江西农业大学学报,2009,31(1):119-123.◇
Study on the Stability of the Red Pigment in Cornus officinalis
WU Haixia,MA Guogang
(Department of Life Science,Yuncheng University,Yuncheng,Shanxi 044000,China)
Taking absorbance at 400 nm as standard,the influences of some factors on the stability of the red pigment in Cornus officinalis are discussed.Such as pH value,temperature,light,metal ions,oxidant,reducer and some food additives.The results show that the red pigment is stable relatively for acid and heat,the color faded as the light intensity enhanced,metal ions of low thickness such as Na+,Ca2+,Mg2+,Al3+,Zn2+,K+,Cu2+had no influence on the pigment,but it is unstable if there are Fe3+and Ba2+in solutions.The oxidants and reducers had significant impact on its stability and common food additives had little influence,but citric acid and salt had hyperchromic effect on the pigment.
Cornus officinalis;red pigment;stability
TS202
A
10.16693/j.cnki.1671-9646(X).2016.06.030
1671-9646(2016)06b-0012-04
2016-05-19
运城学院博士启动基金(YQ-2014031)。
吴海霞(1980— ),女,博士,讲师,研究方向为生物活性成分。

