食品微生物DNA能力验证样品的均匀性和稳定性研究
侯大海,刘云国,张 亮,徐云峰,刘凌霄
(1.新疆大学生命科学与技术学院,新疆乌鲁木齐 830046;2.广东产品质量检验监督研究院,广东广州 510330;3.青州荣美尔生物科技有限公司,山东青州 262500;4.黄岛出入境检验检疫局,山东青岛 266000)
食品微生物DNA能力验证样品的均匀性和稳定性研究
侯大海1,2,*刘云国1,3,张亮3,徐云峰4,刘凌霄3
(1.新疆大学生命科学与技术学院,新疆乌鲁木齐830046;2.广东产品质量检验监督研究院,广东广州510330;3.青州荣美尔生物科技有限公司,山东青州262500;4.黄岛出入境检验检疫局,山东青岛266000)
食品微生物DNA能力验证,是利用DNA检测方法,通过实验室间微生物检测结果的比对来确定实验室检测能力的活动。以沙门氏菌(Salmonella)基因组DNA为测试目标,开展了实验室间食品微生物DNA检测能力验证样品的制备,研究了DNA检测能力验证中样品的均匀性和稳定性,以期为食品微生物DNA能力验证的运作提供指导。
食品微生物;DNA能力验证;均匀性;稳定性
实验室能力验证,是通过实验室间检测结果的比对来确定实验室能力的活动。通过持续地开展实验室能力验证活动,可以有效地提高实验室的品质控制能力和检测水平,并提高检测结果的可靠性和权威性[1]。同时,为科研工作以及政府管理工作提供科学、客观的信息。常规微生物能力验证,通常指寄送含或不含目标测试菌盲样时的验证能力。由于可能存在致病微生物,常规微生物能力验证方式在检测样品的运输、储存、检测时,存在较大的生物安全隐患。实验室能力验证活动中采用灭活的微生物,通过提取DNA进行检测的方法可消除这种危险。因而研究食源性致病微生物时,DNA检测能力验证的运作极其重要。能力验证计划中的样品制备不同于一般检测样品的制备,除保证样品具有代表性和可靠性外,还应考虑样品的均一性和稳定性[2]。基于以上能力验证规则的要求,本文研究了沙门氏菌(Salmonella)DNA样品能力验证中的均匀性和稳定性试验。
1 材料与方法
1.1沙门氏菌的培养和制备
沙门氏菌菌株,来源于美国典型微生物菌种保藏中心(ATCC)。沙门氏菌标准菌株(ATCC 49416)经活化后,挑取单菌落接种到含有200 mL的TSBYE三角瓶中大量培养,以转速10 000 r/min离心5 min收集沉淀,加入双蒸水重新悬浮,水浴灭活后,分装到Eppendorf管中冻干制样[3]。
1.2均匀性试验

若F<自由度为(v1,v2) 及给定显著性水平α(通常α=0.05)的临界值 Fα(v1,v2),则表明样品内和样品间无显著性差异,因而样品是均匀的。
1.3稳定性试验
采用室温条件下的储存温度(20℃),进行稳定性试验。样品制备完毕后间隔15 d,从沙门氏菌阳性样品中各随机抽取6份样品,进行荧光定量PCR检测。采用2个样本均数显著性检验-t检验进行统计分析。


自由度df=2(n-1)
若|t|<自由度为2(n-1)给定显著性水平α(α= 0.05)的临界值t0.05[2(n-1)],则表明2次检测结果无显著性差异,因而样品是稳定的。
2 结果与分析
2.1均匀性试验
(1)样品A为沙门氏菌阳性样品。随机选取A样品6个,进行荧光定量PCR检测,结果与已知本底结果相吻合,说明均为阳性。CT值的平均值为14.75。
(2)样品B为沙门氏菌阴性样品。经随机选取B样品6个,进行荧光定量PCR检测,结果与已知本底结果相吻合,说明结果均为阴性。
沙门氏菌阳性样品的均匀性试验结果(荧光定量PCR CT值)见表1,沙门氏菌样品均匀性试验方差分析结果见表2。

表1 沙门氏菌阳性样品的均匀性试验结果(荧光定量PCR CT值)

表2 沙门氏菌样品均匀性试验方差分析结果
F临界值F0.05(5,6)=4.387,计算的F值为0.106 4,该值<F临界值,无显著性差异,这表明样品中沙门氏菌含量均匀。
沙门氏菌均匀性试验荧光定量PCR扩增曲线见图1。

图1 沙门氏菌均匀性试验荧光定量PCR扩增曲线
2.2稳定性试验
沙门氏菌阳性样品稳定性试验结果(荧光定量PCR CT值)见表3。
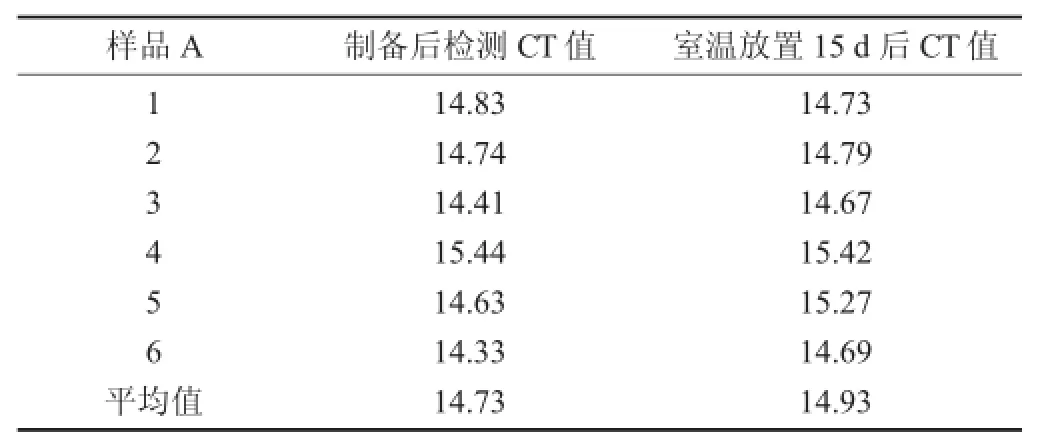
表3 沙门氏菌阳性样品稳定性试验结果(荧光定量PCR CT值)
由表3可知,沙门氏菌阳性样品第1次检测的平均值结果为14.73,室温条件下放置15 d后第2次检测的平均值结果为14.93。
沙门氏菌阳性样品稳定性试验结果见表4。

表4 沙门氏菌阳性样品稳定性试验结果
t临界值t0.05(10)=2.228,计算所得|t|值<t临界值,无显著性差异,这表明沙门氏菌样品的稳定性良好。
沙门氏菌稳定性试验荧光定量PCR扩增曲线见图2。

图2 沙门氏菌稳定性试验荧光定量PCR扩增曲线
3 结论与讨论
本次沙门氏菌DNA能力验证要求利用基于DNA技术的分子生物学手段进行检测,试验结果表明DNA样品符合均匀性和稳定性的要求。实验室间食源致病微生物DNA检测能力验证提供的沙门氏菌检测样品已经灭活,目的是消除能力验证活动中食源致病微生物在运输、储存、检测过程中的生物安全隐患。本次能力验证活动的样品在制备、保存、运输、安全性等技术指标上均能达到实验要求。本研究以CNAS-RL02∶2011能力验证规则、CNASPD21∶2011能力验证工作程序、CNAS-CL03∶2010能力验证计划提供者认可准则、ISO/IEC导则43-1∶1997利用实验室间比对的能力验证-能力验证计划的建立和运作、CNAS-CL04∶2010标准物质/标准样品生产者能力认可准则等规则为基础,结合食源致病微生物检测实验室的特点,通过对样品均匀性、稳定性等关键技术的研究,旨在建立一个与国际规范接轨、操作性强的食品微生物能力验证关键技术规范。
[1]中国实验室国家认可委员会.ISO/IEC 17025∶2005检测和校准实验室能力的通用要求 [S].北京:中国标准出版社,2005.
[2]中国合格评定国家认可委员会.CNAS-GL02∶2014能力验证结果的统计处理和能力评价指南 [S].北京:中国标准出版社,2014.
[3]中华人民共和国卫生部.GB 4789.4—2010食品安全国家标准食品微生物学检验沙门氏菌检验 [S].北京:中国标准出版社,2010.◇
Study on Uniformity and Stability of Food Micro-organism DNA Proficiency Testing
HOU Dahai1,2,*LIU Yunguo1,3,ZHANG Liang3,XU Yunfeng4,LIU Lingxiao3
(1.College of Life Science and Technology,Xinjiang University,Urumqi,Xinjiang 830046,China;2.Guangdong Testing Institute of Product Quality Supervision,Guangzhou,Guangdong 510330,China 3.Qingzhou Ronmer Biology Technology Co.,Ltd.,Qingzhou,Shandong 262500,China;4.Huangdao Entry-Exit Inspection and Quarantine Bureau,Qingdao,Shandong 266000,China)
Food micro-organism DNA proficiency testing is to determine the testing capacity by inter-laboratory testing results using DNA testing method.This study organized DNA proficiency testing of food micro-organism using genomic DNA of Salmonella as the test objective.The uniformity and stability of food micro-organism DNA samples are studied in order to provide guidance for the operation of DNA proficiency testing.
food micro-organism;DNA proficiency testing;uniformity;stability
R378
A
10.16693/j.cnki.1671-9646(X).2016.06.033
1671-9646(2016)06b-0022-03
2016-05-08
新疆大学自治区天山学者科研启动金资金项目(45030);新疆自治区高层次人才引进工程专项经费项目(45049)。
侯大海(1976— ),男,硕士,质量工程师,研究方向为食品加工。
*
刘云国(1977— ),男,博士,教授级高级工程师,硕士生导师,研究方向为食品生物技术。

