化学发光免疫法检测醛固酮和肾素浓度及对原发性醛固酮增多症诊断价值的评价
王芳,康金锁,邹玉宝,蒋雄京,丛祥凤,陈曦
化学发光免疫法检测醛固酮和肾素浓度及对原发性醛固酮增多症诊断价值的评价
王芳,康金锁,邹玉宝,蒋雄京,丛祥凤,陈曦
摘要
目的:对化学发光免疫法(CLIA)检测醛固酮和肾素浓度进行方法学评价,并通过和放射免疫法(RIA)比较评价其对原发性醛固酮增多症(原醛) 的诊断价值。
方法:依据美国临床实验室标准化协会的相关方案,对CLIA检测醛固酮和肾素浓度的精密度、准确性、线性范围及参考值范围进行评价和验证,同时对40例高血压原因待查患者分别用RIA和CLIA检测肾素活性或肾素浓度及醛固酮浓度,以临床诊断为金标准,比较两种方法测得的醛固酮浓度/肾素活性或浓度的比值(ARR或ADRR)用于原醛诊断的特异性和敏感性。
结果:CLIA检测醛固酮和肾素浓度的批内和批间精密度分别小于5%和10%;回收率分别为102%和95%;醛固酮浓度在3~74 ng/dl范围内、肾素浓度在0.99~330.00 µIU/ml范围内,线性关系良好;20例健康受试者除2例肾素浓度超过参考值范围,20例醛固酮浓度和ADRR均在厂商提供的正常人参考范围内。高血压原因待查患者的筛查试验结果显示CLIA和RIA的检测敏感性相同,为85.7%,特异性则分别为97.0%和94.0%。
结论:CLIA具有操作简单、重复性好、无放射性污染等优点,CLIA的检测结果符合临床要求,厂商提供的正常参考值范围可用于临床,本研究推荐用CLIA替代RIA。
关键词 醛固酮增多症;化学发光测定法;肾素;醛固酮
Objective: To evaluate chemiluminescence immunoassay (CLIA) for detecting blood levels of aldosterone and rennin with its diagnostic value of primary aldosteronism (PA) with comparison to radio immunoassay (RIA).
Methods: According to American protocols of CLSI, we conducted a verification study between RIA and CLIA for their precision, accuracy, linearity and reference ranges; meanwhile, taking clinical diagnosis as golden standard, examined renin activity or concentration and aldosterone concentration in 20 healthy volunteers and 40 hypertension patients by both RIA and CLIA, compared the ratios of ARR (aldosterone concentration/renin activity) or ADRR (aldosterone concentration/renin concentration) for the specificity and sensitivity of PA diagnosis.
Results: Within-lot and between-lot accuracies of CLIA for detecting aldosterone levels were below 5% and 10%, the recoveries were 102% and 95% respectively. There was a good linear correlation in the range of aldosterone at (3-74) ng/dl and renin at (0.99-330) µIU/ml. In healthy volunteers, renin level was higher in 2 subjects, while aldosterone level and ADRR ratio were within normal references in all subjects by the manufacturer. In hypertension patients, the sensitivity and specificity for aldosterone and rennin detections by CLIA were at 85.7% and 97.0%, by RIA were at 85.7% and 94.0%.
Conclusion: CLIA has the superiority of simple performance, repeatable and without radioactive contamination; it isrecommended for replacing RIA as necessity.
Key words Primary adlosteronism;Chemiluminescence immunoassay: Renin;Aldosterone
(Chinese Circulation Journal, 2016,31:606.)
原发性醛固酮增多症(原醛)是继发性高血压的常见原因之一,是由于肾上腺皮质腺瘤或增生,过量分泌醛固酮,导致水钠潴留,体液容量扩增继而引起血压升高、肾素-血管紧张素系统受抑制、钾分泌过多,严重者导致低钾血症。以往认为原醛的发病率占轻中度高血压患者的1%,但近些年的研究表明原醛在高血压患者中的比例超过10%[1-3],而且,相对于同年龄、同性别以及血压水平相当的原发性高血压患者,原醛患者的心血管疾病发生率和死亡率均更高[4,5],因此及早识别原醛对于早期治疗和改善预后尤为重要[6]。
近年来发展的全自动化学发光免疫法(CLIA)可直接测定血浆肾素浓度,具有操作简便、快速、无放射性污染的特点,已有研究表明醛固酮与肾素浓度的比值(ADRR)在鉴别原醛的效果上与RIA的醛固酮的浓度/肾素活性(ARR)相似[7,8],并且此方法已收入内分泌学会临床实践指南[9],但此方法目前并未在国内广泛开展,本研究对此方法进行了较为全面的检测方法学评价,以期为临床推广应用提供参考。
1 资料与方法
研究对象:选取2015-05至2015-08因高血压原因待查在阜外医院入院的患者40例,其中最终确诊原醛患者7例,原醛诊断以临床医生依据病史、体征、卧立位醛固酮、肾素和ARR、盐水负荷实验、肾上腺静脉采血等作出的综合判断为金标准。
入选北京地区健康受试者20例,年龄26~66岁,其中男性10例,女性10例,通过问卷调查方式将高血压、心脏病、肾脏疾病等除外。
肾素和醛固酮检测方法:CLIA采用意大利索灵公司全自动化学发光仪(Diasorin Liaison)检测,其原理是将一个能识别被测物的特异性单克隆抗体包被在磁微粒(固相)上,另一个被测物特有的单克隆抗体结合在发光底物上,只有被测物分子两侧都存在抗体的结合物被保留,在催化剂作用下产生光信号,发光强度与被测物浓度成正比。本文采用索灵公司醛固酮、肾素浓度检测试剂盒检测血浆醛固酮浓度(ng/dl)和肾素浓度(µIU/ml),并由此浓度值计算ADRR。
RIA采用北京北方生物技术研究所有限公司检测血浆肾素活性[ng/(ml·h)]和醛固酮浓度(ng/ ml),ARR=(醛固酮/肾素活性)×100。
标本采集和保存:由于临床上可依据患者由卧位到立位所产生的肾素和醛固酮的变化来协助判断原醛,因此本研究对每位受试者分别采集卧位和立位血进行检测。卧位标本于平卧过夜采集,立位标本站立2 h后静坐15 min后采集,收集于EDTA抗凝采血管,立即于室温离心(1760 g)10 min后收集血浆,分装保存于-80℃冰箱,检测时于37℃水浴迅速复融后用于测定。
检测性能评价:精密度验证:依据临床实验室标准化协会(CLSI) EP15-A文件(User Demonstration of Performance for Precision and Accuracy,2001年),将高低2个浓度水平血浆混合样本,分别重复检测20次,计算批内均值与变异系数;将高低2个浓度水平血浆混合样本分别每日检测2批次,每批次各检测2次,连续检测5天,计算批间均值与变异系数。
准确性验证:实验的准确性通过回收率来验证,将高浓度标本和低浓度标本按照1:2、1:4、1:8进行混合,各重复测定两次,取测定平均值与期望值计算回收率。
线 性 范 围 验 证:依 据CLSI EP6-A文 件(Evaluation of the Linearity of Quantitative Measurement Procedure,2003年),将接近线性范围上限的高值混合样本,用低值混合样本进行稀释制备出6个梯度样本,每份样本重复测定2次,计算平均值,以测定值为Y,理论值为X,使用统计软件拟合一次、二次、三次方程,评估是否线性。
参考值范围验证:依据CLSI C28-A2文件(How to Define and Determine Reference Intervals in the Clinical Laboratory,2000年),对生产厂家提供的参考值范围进行验证(醛固酮为3.0~35.3 ng/dl,肾素为4.4~46.1 µIU/ml,ADRR<3.7(ng/dl)/(µIU/ml),选取健康受试者20例,采血选择立位,对醛固酮和肾素浓度进行测定并计算ADRR值,应少于2人的测定值超过生产厂家提供的参考范围。
临床应用评价:高血压原因待查患者40例(包括原醛和非原醛高血压患者),进行筛查试验,即测定卧、立位血浆肾素和醛固酮水平,以临床诊断为金标准,评估CLIA区分原醛和非原醛患者的敏感性和特异性,并和RIA进行比较。CLIA原醛诊断标准:立位ADRR>3.7(ng/dl)/(µIU/ml);RIA原醛诊断标准:立位ARR>30(ng/ml)/[ng/(ml·h)]。
统计学方法:采用SPSS 17.0进行统计学分析。正态分布计量资料以±s表示,采用独立样本t检验;率的比较采用卡方检验。P<0.05为差异有统计学意义。
2 结果
CLIA法精密度验证(表1、2):醛固酮浓度的批内和批间变异系数分别小于5%和10%,肾素浓度的批内和批间变异系数均小于5%,均在可接受范围内。
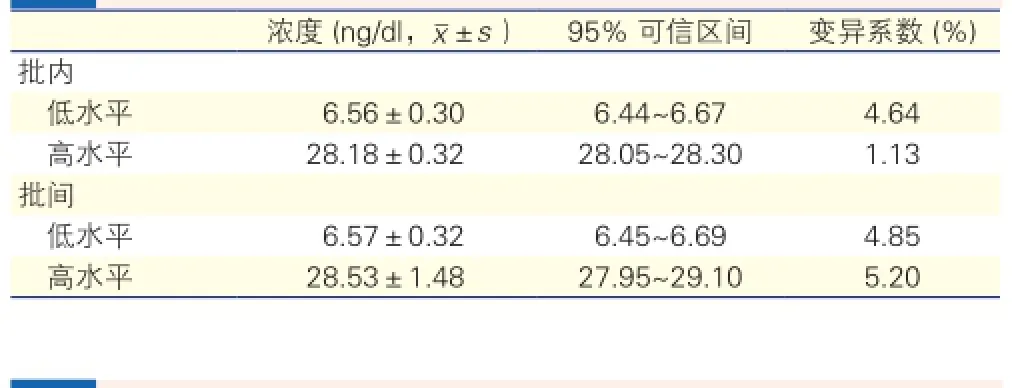
表1 化学发光免疫法醛固酮浓度精密度验证
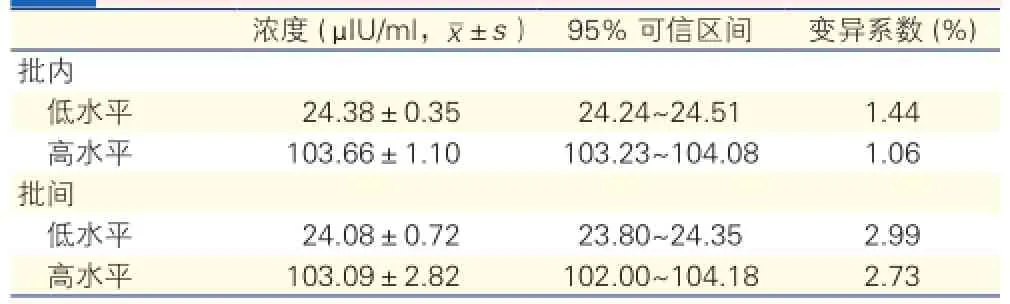
表2 化学发光免疫法肾素浓度精密度验证
CLIA法准确性验证(表3):醛固酮和肾素的平均回收率分别为102%和95%,在可接受范围内。
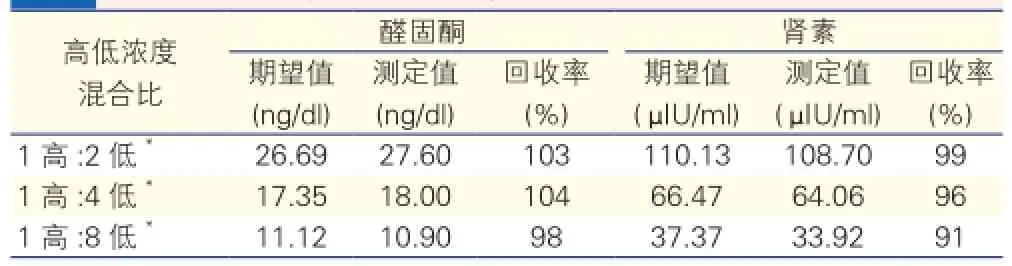
表3 醛固酮和肾素浓度的回收率
CLIA法线性范围验证:一次线性方程醛固 酮 为 y=0.9959x-0.0156,r2=0.9995;肾 素 为y=0.9945x+2.0761,r2=0.9999。两次多项式系数a的P>0.05;三次多项式系数a和b的P>0.05。显示二次、三次多项式系数与“0”无明显差异,说明醛固酮浓度在3~74 ng/dl范围内、肾素浓度在0.99~330.00 µIU/ml范围内呈线性。
CLIA法参考值范围验证:结果显示肾素浓度男女性各有1例超过参考值范围(4.4~46.1µIU/ml),分别为50.23 µIU/ml和50.97 µIU/ml,超出范围的百分数为10%,在可接受范围内。20例健康受试者醛固酮和ADRR值均在参考值范围内,表明可采用此参考值范围。
两种醛固酮和肾素检测方法诊断原醛的效能结果:CLIA的检测特异性和敏感性分别为97.0%和85.7%,RIA的检测特异性和敏感性分别为94.0% 和85.7% 。两种方法的检测敏感性相同,但CLIA的特异性略高于RIA。
3 讨论
本研究结果显示CLIA的精密度、准确性、线性范围均符合临床需要。对厂商提供的正常人参考范围进行的验证表明目前此参考值范围可用于临床。此外利用患者标本进行方法学比对,结果显示CLIA与RIA对原醛的诊断能力相当。
自1981年Hiramatsu等[10]首次提出检测肾素活性并计算ARR来筛查原醛后,此方法延用至今,目前临床上仍以RIA测定的醛固酮和肾素活性为主,其中肾素活性是通过测定血管紧张素原转换为血管紧张素Ⅰ的速率来间接测得,虽然这种方法在临床使用多年,但一直存在较明显的局限性:其一是检测周期长,出报告时间至少需要3天;其二是检测重复性差,检测受多种体内和体外因素影响,结果无可比性。因此,ARR在临床的使用面临了较大的挑战。2004年研究报道了全自动CLIA直接测定肾素浓度的方法[11],这种方法几乎克服了RIA测定肾素活性所有的不足,唯一的问题是肾素活性与肾素浓度的相关性以及利用肾素浓度计算所得的ADRR在筛查原醛的效果上是否与ARR相当,事实上,国外已经有许多研究表明这两种方法之间具有良好的相关性[7,8,12,13],甚至包括在卡托普利试验中的相关性[14],而在2008年的欧洲内分泌学会临床实践指南中也已纳入肾素浓度的检测方法[9]。但是国内则少有医院对此方法进行评价并投入临床使用,仅有中山大学附属第一医院赖凤华等[15]和重庆医科大学第一附属医院孙明芳等[16]分别报道了这两种方法的比对和在原醛诊断中的筛查价值。与国内外其他研究者的结果一致,我们的研究通过较为全面的方法学评价,表明了CLIA测定肾素浓度和醛固酮的可用性和基于肾素浓度的ADRR用于筛查诊断原醛的可行性。
ARR用于筛查原醛的诊断界值尚无定论。主要是因为肾素检测方法的不同而导致的诊断界值的差异,基于检测肾素活性的RIA通常采用的诊断界值是30 (ng/ml)/[ng/(ml·h)],而基于肾素浓度的CLIA的诊断界值则在不同的研究中提出不同的界值和单位,欧洲内分泌学会临床实践指南推荐的是立位ADRR大于3.7(ng/dl)/(μIU/ml)[9],而Glinicki等[8]的研究则为立位ADRR大于30(pg/ml)/(pg/ml),孙明芳等[16]的研究所确定的诊断界值则为立位ADRR大于43.45 (pg /ml) /(µIU/ml),造成差异的原因一是肾素浓度单位的差异,二是研究人群本身不同。本研究中厂家所采用的ADRR单位是(ng/dl)/(µIU/ml),其诊断界值为3.7(ng/dl)/(μIU/ml) ,因为本研究的主要目的是评价CLIA的检测性能,故本文并未建立本实验室的ADRR诊断界值,而是用给定的诊断界值判断检测结果并与临床诊断相比对,我们发现在筛查试验中RIA和CLIA的敏感性均为85.7%,而特异性则分别94.0%和97.0% ,这虽然证明了CLIA可替代RIA,但也提示了3.7(ng/dl)/ (μIU/ml) 可能并不是最佳诊断界值,因为作为筛查试验的敏感性略显不足,这也是为什么指南中RIA的诊断界值会是20~40(ng/dl)/[ng(ml·h)] 这样一个范围,而CLIA的最佳诊断界值则需要更多数据的积累。
本研究有其不足之处,一是对于正常参考值范围,我们仅是对厂商提供的参考范围进行了验证,但实际上应该针对中国人群建立我们实验室自己的参考值范围,不过这部分工作我们实验室已经在筹备进展中。另一个不足之处就是用于方法学比对的患者标本数量偏少,本研究是参照EP9-A2文件的最低样本量40例所开展,我们将进一步扩大标本量对两种方法进行更为完善的评价。
总之,本研究对CLIA检测醛固酮和肾素浓度诊断原醛进行了较为全面的方法学评价,我们认为与RIA相比,CLIA操作简单快速重复性好,没有放射性污染,对于原醛的诊断效果与RIA相似,可以替代RIA用于原醛的筛查试验。
参考文献
[1] Fardella CE, Mosso L, Gomez-Sanchez C, et al. Primary hyperaldosteronismin essential hypertensives: prevalence, biochemical profile, andmolecular biology. J Clin Endocrinol Metab, 2000, 85:1863-1867.
[2] Loh KC, Koay ES, Khaw MC, et al. Prevalenceof primary aldosteronism among Asian hypertensive patients in Singapore. J Clin Endocrinol Metab, 2000, 85: 2854-2859.
[3] Rossi GP, Bernini G, Caliumi C, et al. A prospective study of theprevalence of primary aldosteronism in 1, 125 hypertensive patients. J Am Coll Cardiol, 2006, 48: 2293-2300.
[4] Milliez P, Girerd X, Plouin PF, et al. Evidencefor an increased rate of cardiovascular events in patients with primary aldosteronism. J Am Coll Cardiol, 2005, 45: 1243-1248.
[5] Stowasser M, Sharman J, Leano R, et al. Evidence for abnormal left ventricular structure andfunction in normotensive individuals with familial hyperaldosteronismtypeI. J Clin Endocrinol Metab, 2005, 90:5070-5076.
[6] 龚艳春, 郭冀珍. 如何早期诊断原发性醛固酮增多症. 中国循环杂志, 2006, 21: 480-480.
[7] Wedatilake YN, Scanlon MJ, Bames SC, et al. The clinical utility of two renin mass methods to detect primaryhyperaldosteronism compared with renin activity. Ann Clin Biochem, 2011, 48: 256-262.
[8] Glinicki P, Jeske W, Bednarek-Papierska L, et al. The ratios of aldosterone / plasma reninactivity (ARR) versus aldosterone / directrenin concentration (ADRR). J Renin Angiotensin Aldosterone Syst, 2015, 16: 1298-1305.
[9] Funder JW, Carey RM, Fardella C, et al. Case detection, diagnosis and treatment of patients with primary aldosteronism: an Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab, 2008, 93: 3266-3281.
[10] Hiramatsu K, Yamada T, Yukimura Y, et al. A screening tothe identify aldosterone-producing adenoma by measuringplasma renin activity. Results in hypertensive patients. ArchIntern Med, 1981, 141: 1589-1593.
[11] Perschel FH, Schemer R, Seiler L, et al. Rapid screening test for primaryhyperaldosteronism: ratio of plasma aldosterone to renin concentrationdetermined by fully automated chemiluminescence immunoassays. Clin Chem, 2004, 50: 1650-1655.
[12] Rossi GP, Barisa M, Belfiore A, et al. The aldosterone-renin ratio based on the plasma renin activity andthe direct renin assay for diagnosingaldosterone-producing adenoma. J Hypertens, 2010, 28:1892-1599.
[13] Dorrian CA, Toole BJ, Alvarez-Madrazo S, et al. A screening procedure for primary aldosteronism based on the Diasorin Liaison automated chemiluminescentimmunoassay for direct renin. Ann Clin Biochem, 2010, 47: 195-199.
[14] Wu VC, Kuo CC, Chang HW, et al. Diagnosis of primary aldosteronism:comparison of post-captopril active renin concentration and plasma reninactivity. Clin Chim Acta, 2010, 411: 657-663.
[15] 赖凤华, 曹筱佩, 林慧美, 等. 两种血浆肾素、醛固酮检测方法对原发性醛固酮增多症筛查效率的评价. 中华高血压杂志, 2015, 23: 150-153.
[16] 孙明芳, 杨珊, 何小群, 等. 基于血浆醛固酮/肾素浓度比的联合策略在原发性醛固酮增多症中的筛查价值.军事医学, 2015, 39: 279-283.
(编辑:常文静)
Corresponding Author:CHEN Xi, Email:chenxifw@126.com
收稿日期:(2016-01-12)
作者单位:100037 北京市,中国医学科学院 北京协和医学院 国家心血管病中心 阜外医院 临床检验中心 (王芳、康金锁、丛祥凤、陈曦),心内科(邹玉宝、蒋雄京)
作者简介:王芳 助理研究员 博士 主要研究方向为心血管疾病生物标志物 Email:fray.163@163.com 通讯作者:陈曦 chenxifw@126.com
中图分类号:R54
文献标识码:A
文章编号:1000-3614(2016)06-0606-04
doi:10.3969/j.issn.1000-3614.2016.06.020
Evaluation of Chemiluminescence Immunoassay for Detecting Blood Levels of Aldosterone and Renin With its Diagnostic Value of Primary Aldosteronism
WANG Fang, KANG Jin-suo, ZOU Yu-bao, JIANG Xiong-jing, CONG Xiang-feng, CHEN Xi.
Department of Laboratory Medicine, Cardiovascular Institute and Fu Wai Hospital, CAMS and PUMC, Beijing (100037), China
Abstract

