某院576例药品不良反应病例回顾性分析
司福国,崔佳,王兆斌
·药物与临床·
某院576例药品不良反应病例回顾性分析
司福国,崔佳,王兆斌
[摘要]目的:分析某院2014年药品不良反应(ADR)监测情况,促进临床安全、合理用药。方法:采用回顾性分析研究方法,对某院2014年1月-12月上报的576例ADR进行统计、分析、评价。结果:576例ADR报告中,男285例,女291例;60岁以上患者较多,占37.33%,其次为0~10岁组,占17.36%;发生时间多数集中在24 h之内,占69.45%。静脉给药引起的ADR占81.77%,口服给药占16.32%。ADR报告中,抗感染药物占38.02%,抗肿瘤药占27.78%,中药制剂占12.33%。ADR最常见的表现为皮肤及附件与消化系统损害。结论:为减少ADR的发生,提高合理用药水平,应加强对患者用药期间的观察,加强药物尤其是抗感染药物以及抗肿瘤药、中药制剂的质量监测。
[关键词]药品不良反应; 合理用药; 回顾性分析
药物不良反应(adverse drug reactions,ADR)主要是指合格药品在正常用法用量下出现的与用药目的无关的或意外的有害反应[1]。药物不良反应监测是加强药品管理,提高用药质量和医疗水平的一种重要手段,开展ADR监测工作一方面可以保障用药安全,避免ADR的发生;另一方面又可以促进合理用药,提高临床用药水平。现对某院2014年576例ADR报告进行回顾性分析,旨在为临床合理用药提供参考。
1资料与方法
1.1资料利用“全国药品不良反应监测网络”数据库检索统计功能,收集到某院2014年呈报的院内不良反应576例。
1.2方法采用回顾性分析方法,对576例ADR分别从年龄、性别、发生时间、给药途径、涉及药品种类、临床表现等方面进行调查,并对上述结果进行分类统计、分析。
2结果
2.1ADR患者性别及年龄分布576例药物不良反应报告中,男285例,女291例,发生ADR患者性别比较,差异无统计学意义(P>0.05),患者年龄最小为3个月,最大为92岁。各年龄段分布,见表1。
2.2ADR发生时间及构成比发生ADR最短时间为用药即刻,最长时间为用药第82天,用药后0~24 h发生ADR最多,共计400例(69.45%)。见表2。

表1 发生ADR的患者性别与年龄分布

表2 ADR发生时间及构成比
2.3发生ADR的给药途径静脉给药引发的ADR为471例,占81.77%,而口服给药为94例,占16.32%,其他给药途径占3.82%。发生ADR的给药途径,见表3。
2.4ADR涉及药品种类576例ADR报告中,引发ADR的药品共计190种,其中抗感染药物引发的ADR最多,其次为抗肿瘤药与中药制剂。ADR涉及药品种类见表4。
2.5ADR涉及抗感染药物分类由抗感染药物引起的ADR报告共计219例,其中注射剂型为196例,口服剂型为23例。ADR涉及抗感染药物分类见表5。
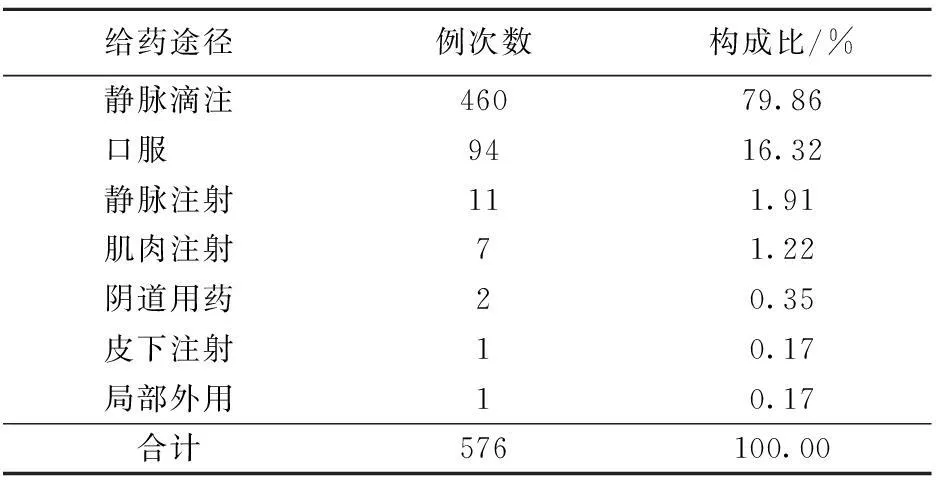
表3 发生ADR的给药途径分布

表4 引发ADR的药品种类分布

表5 ADR涉及抗感染药种类与构成
2.6ADR累及系统/器官及主要临床表现576例ADR报告中,累计器官最多的为皮肤及附件损害,其次为消化系统损害。ADR累及系统/器官及主要临床表现见表6。

表6 ADR累及系统/器官及主要临床表现构成
3讨论
3.1ADR与年龄的关系本报告中的ADR年龄分布显示,我院60岁以上老年患者和10岁以下儿童ADR发生率较高。原因除药物因素外,与其生理、病理特点也有关。随着年龄增长,老年人的组织器官生理机能减弱,各种酶的合成及活性均下降,肝肾对药物的处置能力减弱,对药物在体内的吸收、转化、代谢、排泄均有不同程度的影响,从而延长药物在体内的停留时间,使得ADR的发生率增加。有调查显示,多病共存也是老年人ADR发生的危险因素[2]。多病共存主要与老年人各种慢性病患病率高有关,多病共存的治疗必然存在多药合用,而药物-药物相互作用的概率可由同时应用两种药物的13%上升到7种药物的82%[3],可以导致ADR发生率升高。除此之外,老年人用药依从性差以及住院时间长,也与ADR的发生有着密切关系。国内有报道指出[4],儿童ADR的发生与机体功能状态密切相关。学龄前期器官的生理功能尚未发育成熟,神经、内分泌系统及肝肾功能发育还不完善,且个体差异较大,对药物的敏感性较高,耐受性差,药物清除力弱,导致药物毒性增加,同时儿童缺乏自主意识,当ADR发生时缺乏自我保护能力,因此更易发生ADR。结合以上特点,老年人需严格掌握适应征,需特别注意对肝肾损害较大的药物。儿童用药量必须严格按照换算公式计算,有时新生儿还需按日龄计算剂量,间隔时间也适当延长。
3.2ADR的发生时间576例ADR报告中用药0~24 h内出现ADR的有400例(69.45%),这可能与个体差异、联合用药、用药疗程等有关。由于新发现的ADR在药品说明书中未说明,个别严重的ADR鲜有发生,故存在不可预测性。因此临床应用药物时应密切观察,尤其在用药后的0.5h内,可以及早发现新的、严重的ADR。所以用药完毕后停留一定时间,注意可能发生的ADR[5],同时告知患者应用药物时可能会出现的不良反应,便于患者及时发现与医师沟通。
3.3给药途径与ADR的关系由表3所示,静脉给药引发的ADR比其他给药途径的发生率高,部分原因与我国医生及患者用药习惯有关[6]。静脉给药主要用于严重创伤脱水、不能口服补充液体、严重感染、病情严重无法口服药物4种情况,但患者因追求起效快而要求输液,部分医生认识不够或为满足患者要求而选择输液。据报道[7],静脉注射液的pH、渗透压、微粒、内毒素、低温输液、致过敏原等都可以是引发ADR的直接诱因,而输液质量不达标,不按规定储存运输,药物的配伍,添加药物质量不合格或剂量过大,药物稀释剂选择不当,输液的器具、操作、方式、滴速,以及环境变化和患者的个体情况都可以作为静脉给药引发ADR的人为因素。由此可见,静脉给药相对于其他给药方式更易引发ADR。要降低发生率,就必须加强对生产、流通、使用的各环节的监管力度;同时医生在给患者用药时应当首选口服给药。静脉给药前询问过敏史,要充分考虑患者年龄、体质、用药史、合理用药,尽量避免联合用药,注意控制滴注速度。
3.4药物与ADR的关系
3.4.1抗感染药物与ADR的关系综合表4与表5所示,抗感染药物引发的ADR所占比例最高,其前三名者依次为:青霉素类、头孢菌素类、喹诺酮类。产生这一现象的原因则与抗感染药物种类多、使用范围广、使用频率高及临床不合理使用甚至滥用有关,而医生作为治疗药物的使用决定者,其临床不合理使用抗感染药物则是导致ADR发生率升高的主要原因。主要表现为[8]:无指征的预防用药;不必要的联合用药或重复用药;用药剂量过大、用药间隔不当;用药时间不足或过长;无原则地使用新药与价格昂贵的药品等。因此,要加强对抗感染药物尤其是抗菌药物使用的监督管理,杜绝临床不合理使用。
3.4.2ADR与抗肿瘤药的关系有研究[9]表明:40岁以上患者抗肿瘤药致ADR发生率明显增加,发生率合计为88.26%,其中以50~59岁发生率最高,符合恶性肿瘤发病流行趋势。这是由于中老年患者的各脏器功能逐渐衰退,对药物的吸收、分布、代谢和排泄的功能逐渐减弱,尤其是对化疗药的耐受程度也进行性降低。576例ADR报告中,由抗肿瘤药引起的ADR报告共计219例,其中注射剂型为196例,口服剂型为23例。分析其原因[10]:静脉给药可使药物直接进人体循环,起效快、生物利用度高,因而被广泛应用于临床,尤其对于免疫力低下的肿瘤患者,静脉给药已经成为其常用给药途径;同时药物本身的PH值、渗透压、微粒、内毒素、及输液操作过程等都可能诱发ADR;而静脉给药通常在院内进行,医护人员对ADR的监测较严密,口服给药则大多在院外,无法进行ADR的监控,患者对ADR认识薄弱,报告例数可能会低于实际例数。
3.4.3ADR与中药制剂的关系ADR涉及的中药制剂中,注射剂56例,口服剂型15例。可见,中药注射剂同样也是诱发ADR的主要剂型。主要是因为[11]:(1)每味中药成分复杂多样,其活性成分稳定性差,制备过程中难以彻底除去中药材所含有的蛋白质、多肽、多糖、鞣质、色素等大分子物质,易导致过敏反应发生。(2)中药注射制备工艺低下,质量控制水平低,制备过程中加入的添加剂或包装材料及洁净度均可导致不良反应的发生。(3)调剂过程中所选择的溶媒、与其他药物的配伍、剂量、滴速、临床不遵循辨证论治,均可诱发ADR。
3.5ADR涉及的器官及其临床表现由表6可见,ADR累及的最多为皮肤及附件与消化系统,分别占35.59%和32.47%,可能由于这两个器官系统的不良反应症状较明显、强烈,如皮疹、瘙痒、恶心、呕吐等,短时间内便可表现,临床可以快速观察和诊断,与药物的相关性容易确认,同时不易与其他疾病相混淆;而且皮肤及附件的不良反应多为药疹,主要为变态反应所致,目前临床上常用的药物有的本身即为全抗原或半抗原,进入人体后较易引起变态反应[12]。
[参考文献]
[1]王南松,周学琴,王立军.459例药品不良反应报告分析[J].中国医院药学杂志,2009,29(13):1136.
[2]杨志伟,王琼,欧阳敏,等.老年患者药物不良反应危险因素[J].中国老年学杂志,2014,12(34):6769.
[3]Delafuente JC.Understanding and preventing drug interactions in elderly patients[J].Crit Rev Oncol Hematol,2003,48(2):133-143.
[4]黄艳,杜小换.我院241例儿童药品不良反应报告分析[J].中国药房,2011,22(14):1311.
[5]张维亚,刘小文,王娜,等.695例药品不良反应报告分析[J].中国医院药学杂志,2009,29(20):1805.
[6]马旭东,陈炜,杜光.滥用静脉输液的危害与防范[J].医药导报,2015,34(2):281.
[7]梁小岩,雷桂华,曾伟强,等.输液不良反应原因的系统分析与控制对策[J].中国医院药学杂志,2006,26(1):111-112.
[8]尤海生,董亚林,董卫华,等.676例药品不良反应报告分析[J].中国医院药学杂志,2009,29(24):2140.
[9]钱锦,张树,吴俊华,等.422例抗肿瘤药物不良反应分析[J].南京医科大学学报:自然科学版, 2013,33(7):915-920.
[10]李蓉,董志,路晓钦,等.重庆市818例抗肿瘤药不良反应报告分析[J].中国药房,2013,24(34):3225-3227.
[11]谭乐俊,王萌,朱彦.中药注射剂的不良反应研究进展[J].中国中药杂志,2014,39(20):3889-3897.
[12]张爱琴,白玉国,刘翎.我院2004年药品不良反应分析[J].中国医院药学杂志,2006,26(5):618.
[作者单位] 安徽省蚌埠市第三人民医院 药学部,233000 司福国(1984-),男,药师,大学。
DOI:10.14126/j.cnki.1008-7044.2016.04.045
[中图分类号]R 969.4
[文献标识码]A
[文章编号]1008-7044(2016)04-0469-04
(收稿日期:2016-01-12)

