PCOS患者促排卵过程中发生卵巢慢反应的影响因素分析
汤文娟,刘雨生,黄玲莉
(安徽医科大学附属省立医院生殖医学中心,合肥 230001)
PCOS患者促排卵过程中发生卵巢慢反应的影响因素分析
汤文娟,刘雨生*,黄玲莉
(安徽医科大学附属省立医院生殖医学中心,合肥230001)
【摘要】目的分析控制性超促排卵过程中多囊卵巢综合征(PCOS)不育症患者发生卵巢慢反应的临床指标,以指导其降调节及促性腺激素(Gn)启动剂量的调整。方法回顾性分析2011年1月至2015年4月,在我院生殖中心首次行体外受精-胚胎移植(IVF-ET)长方案助孕治疗的PCOS患者的临床资料,其中卵巢慢反应的57例患者为A组,114例卵巢反应正常的患者为B组。根据降调药物的不同将A组分为长效GnRH-a组(A1组)和短效GnRH-a组(A2组)。结果(1)A组的体重和体重指数(BMI)显著高于B组,A组的起始Gn剂量[(125.73±27.49)U]和起始每公斤体重Gn剂量[(1.99±0.43)U/kg]显著小于B组[分别为(135.41±29.42)U、(2.38±0.54)U/kg](P均<0.05);(2)多因素Logistic回归分析显示体重是PCOS卵巢慢反应的独立危险因素(P<0.01),起始每公斤体重Gn剂量是卵巢慢反应的独立保护因素(P<0.01)。(3)A1组和A2组相比启动日黄体生成素(LH)水平有降低趋势,但无显著性差异(P=0.073),A1组起始每公斤体重Gn剂量[(2.19±0.39)U/kg]显著高于A2组[(1.92±0.43)U/kg](P<0.05)。结论体重过大、低起始Gn剂量是PCOS患者发生卵巢慢反应的主要影响因素。长效GnRH-a可能较短效GnRH-a更容易导致PCOS患者发生卵巢慢反应。
【关键词】体外受精-胚胎移植;卵胞浆内单精子注射;多囊卵巢综合征;控制性超促排卵;卵巢慢反应
Objective: To investigate influencing factors of slow response in patients with polycystic ovary syndrome (PCOS) for guiding down-regulation protocol and adjusting starting dose of gonadotropin (Gn).
Methods: The data of the PCOS patients undergone IVF-ET with the long protocol in our hospital from January 2011 to April 2015 were retrospectively analyzed. The patients were divided to two groups:57 patients with slow response in group A and 114 patients with normal response in group B. According to the type of GnRH agonist (GnRH-a) used,group A was subdivided into long-acting GnRH-a group (group A1) and short-acting GnRH-a group (group A2).
Results: The body weight and BMI of the patients in group A were significantly higher than those in group B. The starting Gn dose [(125.73±27.49) vs. (135.41±29.42) U] and starting Gn dose per kilogram of body weight [(1.99±0.43) vs. (2.38±0.54) U/kg] were significantly lower than those in group B (P<0.05). Multivariate logistic regression analysis showed that body weight was an independent risk factor for PCOS slow response (P<0.01),and Gn starting dose per kilogram of body weight was an independent protective factor for PCOS slow response (P<0.01). LH levels on the starting day had a decreasing trend in group A1 but not significant (P=0.073),and starting Gn dose per kilogram of body weight [(2.19±0.39) vs. (1.92±0.43) U/kg] in group A1 was significantly higher than that in group A2 (P<0.05).
Conclusions: Overweight and low starting Gn dose are the major factors affecting the slow response of PCOS patients. Long-acting GnRH-a is more likely to lead to slower response than short-acting GnRH-a in PCOS patients.
Key words: IVF-ET;ICSI;Polycystic ovary syndrome;Controlled ovarian hyperstimulation;Slow response
(J Reprod Med 2016,25(5):395-400)
近年来,有研究认为在使用促性腺激素释放激素激动剂(GnRH-a)降调节长方案进行控制性超促排卵(COH)时,由于黄体生成素(LH)绝对或相对不足可能导致卵巢发生“慢反应”[1],表现为一定剂量的卵泡刺激素(FSH)治疗初期,卵泡募集及激素水平正常[10个卵泡直径≥6 mm并且雌二醇(E2)≥366 pmol/L],之后给予相同剂量的FSH,卵泡大小及血清雌二醇(E2)水平无明显增长,卵泡发育处于平台期,E2水平上升缓慢[2]。
多囊卵巢综合征(PCOS)患者被归类为对促性腺激素(Gn)高反应人群,因此,助孕治疗时常通过减小Gn启动剂量来防控卵巢过度刺激综合征(OHSS)的发生。然而,临床上发现,在超排卵中本应对Gn呈现高反应的PCOS患者中有一部分患者却发生了卵巢慢反应,少数甚至出现卵巢低反应而取消周期[3]。本研究回顾性分析于本院生殖中心接受体外受精/卵胞浆内单精子注射-胚胎移植(IVF/ICSI-ET)助孕治疗的PCOS患者的临床资料,以期为临床评估PCOS患者发生卵巢慢反应提供可能的指标和参考。
资料与方法
一、研究对象及分组
回顾性分析2011年1月至2015年4月,于我院生殖中心首次行IVF/ICSI-ET长方案助孕治疗的PCOS患者,共359例。纳入标准为:(1)符合2003年鹿特丹PCOS诊断标准[4];(2)年龄≤37岁,基础FSH<10 U/L;(3)18 kg/m2<体重指数(BMI)<28 kg/m2;(4)不育因素包括女方输卵管因素,轻、中度子宫内膜异位症,以及少、弱、畸精子症等;(5)第一次行IVF/ICSI-ET助孕治疗。排除标准为:合并有免疫性疾病、甲状腺功能异常、卵巢手术史(卵巢打孔术除外)、重度子宫内膜异位症的患者。
卵巢慢反应的判断标准[5-8]为:(1)促排卵第6~8日卵泡直径均<10 mm;(2)促排卵第6~8日E2<200 pg/ml(732 pmol/L);(3)卵泡生长缓慢,每3 d增大<2 mm;(4)增加Gn剂量后卵泡继续生长发育至HCG日。359例PCOS患者中存在卵巢慢反应的57例患者定为A组;对Gn呈正常反应的229例PCOS患者采用系统抽样法随机筛选出114例组成B组(对照组)。A组再根据降调药物的种类不同分为长效GnRH-a达菲林组(A1组)和短效GnRH-a达必佳组(A2组)。
超重的判断采用《中国成人超重和肥胖症预防控制指南》[9]推荐的标准:24 kg/m2≤BMI<28 kg/m2为超重。
二、研究方法
研究对象均采用长方案,于口服避孕药第17天时开始使用短效GnRH-a(达必佳,0.1 mg/支,辉凌,德国)0.1 mg/d,第14天评价垂体降调节指标,达标后GnRH-a改为0.05 mg/d,至人绒毛膜促性腺激素(HCG)注射日终止;或者一次注射减量的长效GnRH-a(达菲林,3.75 mg/支,博福-益普生,法国)1.5~1.88 mg,第14天评价垂体降调节指标,达到标准后开始超促排卵。
A组中50例使用重组卵泡刺激素(rFSH,75 U/支,默克雪兰诺,瑞士),起始剂量为75~225 U/d,其中41例发生卵巢慢反应后,添加人绝经期促性腺激素(HMG,上海丽珠,75 U/支),另外9例仅增加FSH剂量,待慢反应纠正后于卵泡晚期常规使用HMG;A组还有7例使用HMG或者rFSH+HMG启动,起始剂量为75~225 U/d,发生慢反应后增加Gn剂量。
B组均采用rFSH超促排卵,起始剂量为75~225 U/d,并于卵泡晚期常规使用HMG。
两组主导卵泡直径达到18 mm时注射HCG(艾泽,默克雪兰诺,瑞士)250 μg诱发卵母细胞成熟,注射HCG后34~36 h行阴道超声引导下取卵术,按本中心常规受精与胚胎培养,于取卵后72 h行ET及剩余胚胎冷冻或全胚冷冻。
三、观察指标
观察A、B两组的一般资料、COH天数、Gn用量(总Gn、起始Gn、起始每公斤体重Gn)、降调节幅度[(基础LH-Gn启动前LH)、(基础LH-Gn启动前LH)/基础LH]、获卵数、优质胚胎率和临床妊娠率等参数,以及A1、A2组的基础LH水平、启动日LH水平及起始用药情况。
四、统计学处理

结果
一、一般资料比较
两组患者的年龄、不育年限和基础性激素水平比较,无显著性差异(P>0.05)。A组57例患者中有30例超重,占52.63%。A组体重和BMI显著高于B组(P<0.01)(表1)。短效长方案周期比例在A、B两组分别为75.44%和85.96%,长效长方案周期比例在A、B两组分别为24.56%和14.04%,A组中长效长方案所占比例有略高于B组的趋势,但无显著性差异(P=0.087)。两组患者的基础生殖激素水平和Gn启动日生殖激素水平比较无显著性差异(P>0.05)(表1)。
二、两组患者HCG日相关指标和Gn使用情况比较
A组的起始Gn剂量和起始每公斤体重Gn剂量显著低于B组 (P<0.05)。A组的促排天数显著长于B组,总Gn用量显著高于B组,而HCG日E2水平显著低于B组(P<0.01)。值得注意的是,虽然A组HCG日≥14 mm的卵泡数显著低于B组(P<0.01),但HCG日≥10 mm的卵泡数A、B两组比较无显著性差异(P>0.05)(表2)。
三、两组患者促排卵情况及妊娠结局比较
两组获卵数和平均优质胚胎数比较无显著性差异(P>0.05),但A组的优质胚胎率(60.59%)显著低于B组(68.81%)(P<0.01)。两组因为出现OHSS倾向而取消鲜胚移植率比较无显著性差异(P>0.05)(表3)。
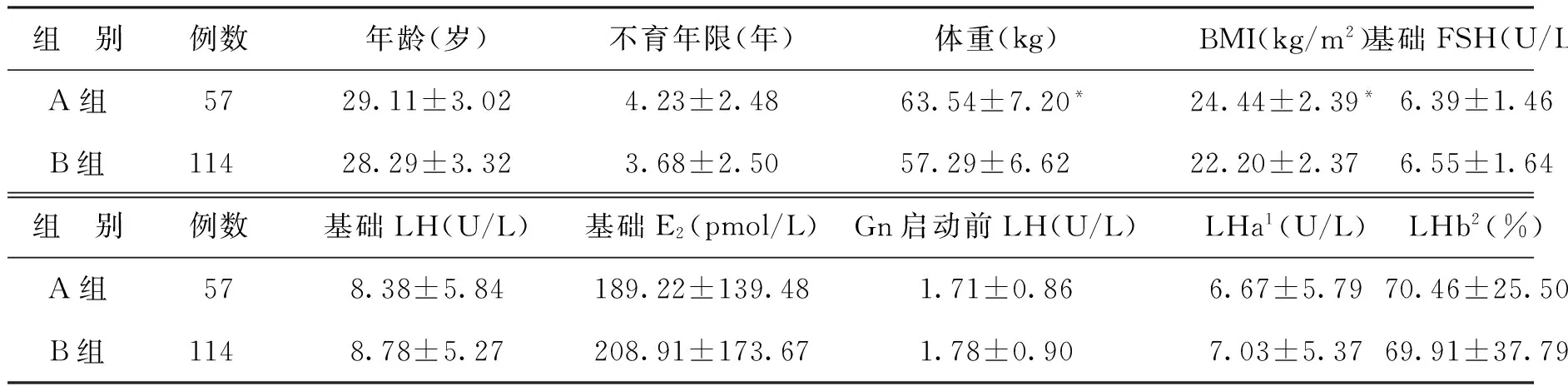
表1 两组患者一般资料比较(x-±s)
注:1LHa=基础LH-Gn启动前LH;2LHb=(基础LH-Gn启动前LH)/基础LH。与B组比较,*P<0.01
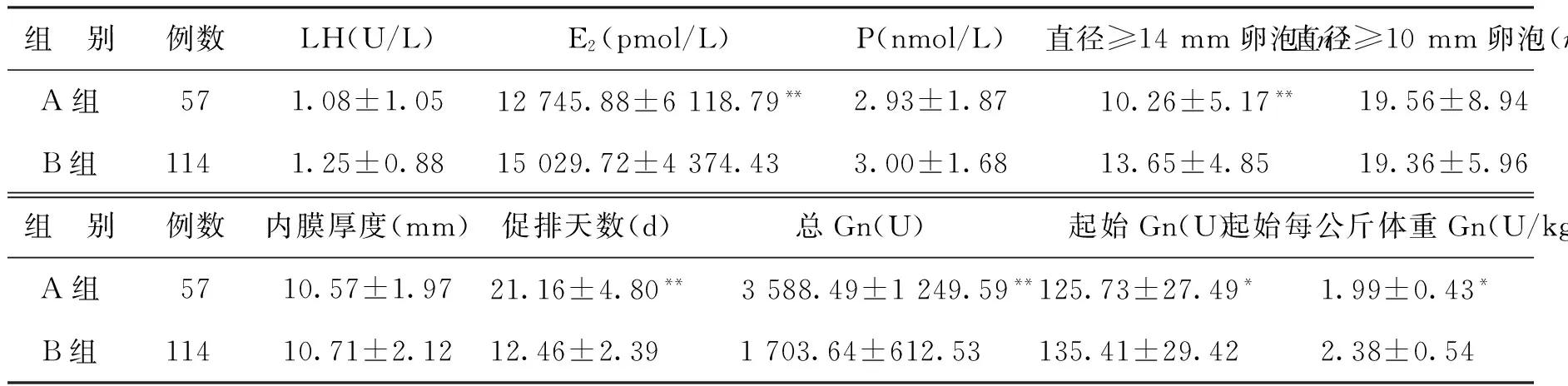
表2 两组HCG日相关指标和Gn使用情况比较 (x-±s)
注:与B组比较,*P<0.05,**P<0.01
四、卵巢慢反应的多因素Logistic回归分析
将差异有统计学意义的指标:体重、BMI、起始Gn、起始每公斤体重Gn纳入Logistic回归进一步分析,结果显示体重和起始每公斤体重Gn进入回归模型,体重是慢反应的独立风险因子,起始每公斤体重Gn是慢反应的独立保护因子(表4)。
五、A1、A2组LH水平及起始用药情况比较
A1组起始每公斤体重Gn显著高于A2组(P<0.05)。两组启动日LH水平比较,A1组较A2组有降低的趋势,但无显著性差异(P=0.073)(表5)。
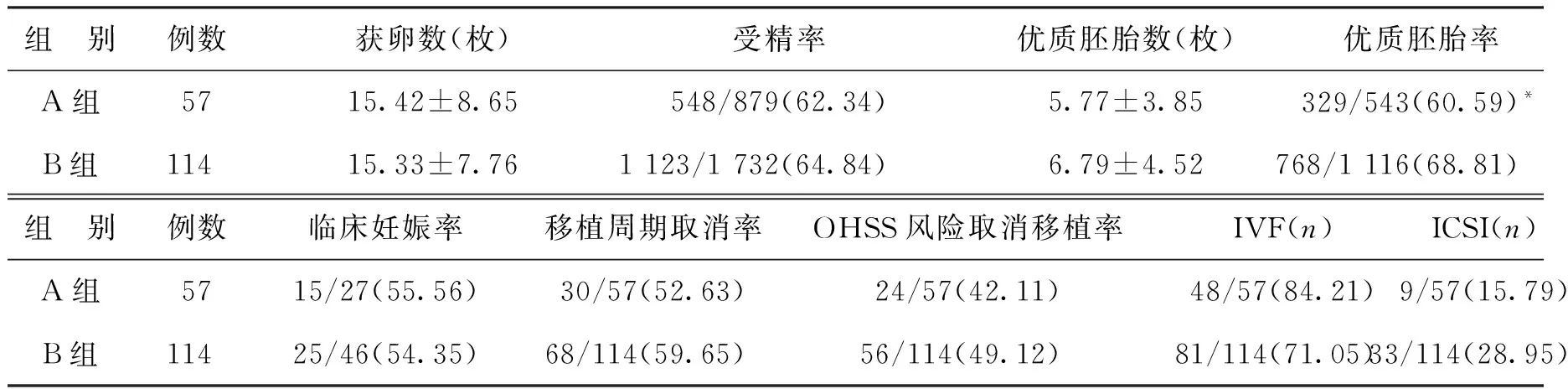
表3 两组促排卵情况及妊娠结局比较 [(x-±s),n(%)]
注:与B组比较,*P<0.01
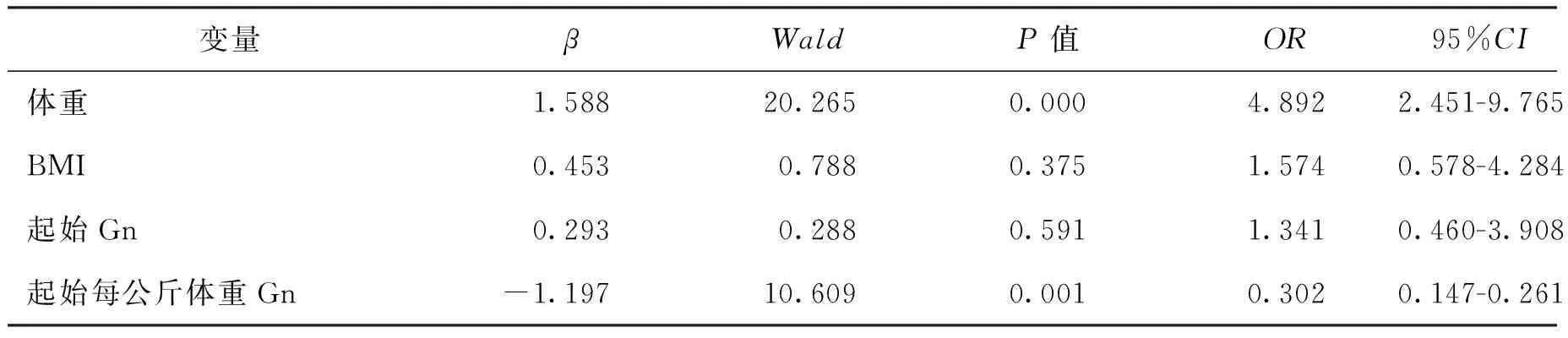
表4 PCOS卵巢慢反应相关因素Logistic回归分析
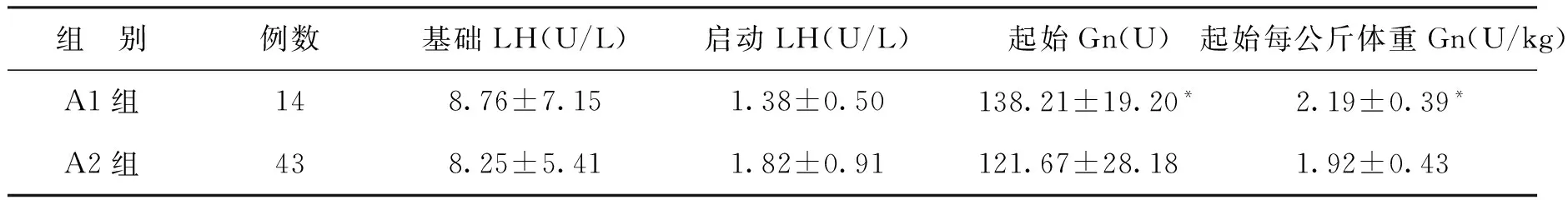
表5 A1、A2组LH水平及起始用药情况比较 (x-±s)
注:与A2组比较,*P<0.05
讨论
卵巢慢反应是超排卵中比较常见的异常情况。Ferraretti等[2]在排除PCOS患者后统计发现,对Gn反应正常的人群IVF助孕治疗中约70%的人对FSH卵巢反应性正常,15%出现反应低下,另外15%呈卵巢慢反应。而对于PCOS这类高反应人群,卵巢慢反应的发生率及其原因国内外报告均较少见。本研究对PCOS患者慢反应和正常反应的相关临床资料进行对比分析,研究结果显示PCOS患者行IVF助孕治疗过程中约16%(57/359)的患者发生卵巢慢反应,发生率与正常反应人群相近,其发生原因值得探讨。
一、PCOS患者发生慢反应后添加LH的有效性
正常反应人群行COH过程中发生卵巢慢反应被认为与LH缺乏有关。YazYlmaz等[10]对除外PCOS患者的137个IVF周期进行分析发现,在发生卵巢慢反应时补充重组黄体生成素(rLH)组,其种植率和临床妊娠率显著高于FSH组。帅振虹等[11]对COH过程中发生了卵巢慢反应的患者(排除PCOS患者)进行研究,发现补充HMG可减少COH天数及rFSH用量,降低了治疗费用;补充rLH 可提高HCG日E2水平,改善妊娠结局。李红真等[7]对60例发生卵巢慢反应、在COH过程中补充rLH的患者进行描述性统计分析,结果发现补充rLH可以改善卵巢的反应性,增加获卵数,改善妊娠结局,该入组标准中也除外了PCOS。
PCOS患者属于Gn高反应的人群,其卵巢慢反应的发生可能也与LH相对不足相关。本研究A组中有7例以rFSH+HMG启动超排卵,始终有LH的补充却依然发生了慢反应;另有9例以rFSH启动超排卵发生了慢反应后,仅增加rFSH制剂慢反应即得以纠正,之后于卵泡晚期常规使用HMG;另外41例在发现慢反应后即添加HMG以增加FSH和LH剂量慢反应得以纠正。本研究结果提示出现慢反应的PCOS患者需首先考虑增加FSH,在FSH剂量足够的基础上添加LH以纠正慢反应。另外,LH受体的多态性可能影响LH的有效性。Alviggi等[12]通过特殊的免疫学方法检测LH的多态性,发现IVF周期中rFSH的使用剂量超过3 500 U的患者中有31.8%的患者其血清检测到LH受体多态性,而rFSH使用剂量低于2 000 U的患者中没有检测到血清LH多态性的发生。
二、体重对慢反应发生的影响
有文献报道,中国女性BMI超过24 kg/m2时Gn用量增加,HCG日E2峰值减小,周期取消率增加,同时流产率增加[13]。在FSH刺激卵泡生长过程中需要血清FSH超过“门槛”才能启动多卵泡发育,肥胖患者这种“门槛”效应被削弱导致需要更多的FSH剂量刺激卵泡生长[14]。本研究慢反应组57个患者中30个超重或者肥胖,占52.63%,同时Logistic回归分析表明体重是慢反应的独立危险因素,说明肥胖会对IVF治疗造成一定的负面影响。
卵泡对外源性Gn的反应和持续生长取决于激素的浓度和给药模式。起始Gn低于FSH启动阈值,则不能驱动卵泡生长,后期增加Gn用量可能导致卵泡生长不一。Koundouros[15]对年轻的PCOS患者共225个周期进行研究,低剂量Gn递增方案组卵泡生长缓慢、不均一,周期取消率高于递减方案组,卵泡OHSS发生率低于递减方案组。本研究中慢反应组HCG日直径≥14 mm的卵泡数显著低于对照组(P<0.01),然而HCG日直径≥10 mm的卵泡数相仿,相应的优质胚胎率低于对照组,说明慢反应组较对照组卵泡发育更不均匀,与Koundouros[15]的结论相符。本研究将起始每公斤体重Gn纳入Logistic回归模型,得出起始每公斤体重Gn是慢反应的保护因素。
三、长短效GnRH-a制剂的使用对慢反应的影响
长短效GnRH-a制剂对降调的深度有影响,因此长效制剂可能加重慢反应的发生。本研究A组相比B组长效降调制剂所占比例有更高的趋势,但尚未达到统计学差异。将A组再分为长效组(A1组)和短效组(A2组)两个亚组进行统计分析,A1组启动LH水平较A2组有降低趋势,A1组在启动Gn剂量显著增高的情况下仍然发生了慢反应,提示长效GnRH-a制剂较短效制剂降调更容易导致慢反应的发生,但需要有更大的样本量来证实。
因本研究仅考虑了PCOS患者的体重、BMI、基础性激素水平等,未全面分析PCOS患者异常的内分泌环境,未对促排过程中FSH水平进行监测以指导Gn剂量的调整,并且纳入的样本量相对较小,因此存在一定的局限性。且亚组分析时主要侧重于长短效制剂应用的区别,仅对两个亚组基础LH和启动LH水平及起始用药情况进行了比较,未对两组的妊娠结局等进行分析,后期应该进一步完善相关参数的比较。
综上所述,体重过大、低起始Gn剂量是PCOS患者发生慢反应的主要影响因素。使用长效GnRH-a制剂可能较短效制剂更容易导致慢反应发生。
【参考文献】
[1]De Placido G,Mollo A,Alviggi C,et al. Rescue of IVF cycles by HMG in pituitary down-regulated normogonadotrophic young women characterized by a poor initial response to recombinant FSH[J]. Hum Reprod,2001,16:1875-1879.
[2]Ferraretti AP,Gianaroli L,Magli MC,et al. Exogenous luteinizing hormone in controlled ovarian hyperstimulation for assisted reproduction techniques[J]. Fertil Steril,2004,82:1521-1526.
[3]余蓉,赵军招,林金菊,等. 促性腺激素在多囊卵巢综合征患者体外受精-胚胎移植治疗中的应用探讨 [J]. 生殖医学杂志,2010,19:87-90.
[4]Rotterdam ESHRE/ASRM-Sponsored PCOS consensus workshop group. Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome (PCOS)[J]. Hum Reprod,2004,19:41-47.
[5]De Placido G,Alviggi C,Perino A,et al. Recombinant human LH supplementation versus recombinant human FSH (rFSH) step-up protocol during controlled ovarian stimulation in normogonadotrophic women with initial inadequate ovarian response to rFSH. A multicentre,prospective,randomized controlled trial[J]. Hum Reprod,2005,20:390-396.
[6]Wong PC,Qiao J,Ho C,et al. Current opinion on use of luteinizing hormone supplementation in assisted reproduction therapy:an Asian perspective[J/OL]. Reprod Biomed Online,2011,23:81-90.
[7]李红真,龚斐,蔡素芬,等. 卵巢刺激慢反应患者补充重组黄体生成素的疗效评价[J]. 生殖医学杂志,2013,22:92-96.
[8]De Placido G,Alviggi C,Mollo A,et al. Effects of recombinant LH (rLH) supplementation during controlled ovarian hyperstimulation (COH) in normogonadotrophic women with an initial inadequate response to recombinant FSH (rFSH) after pituitary downregulation[J]. Clin Endocrinol (Oxf),2004,60:637-643.
[9]陈春明,孔灵芝. 中国成人超重和肥胖症预防控制指南[M]. 北京:人民卫生出版社,2006:3.
[11]帅振虹,连方. 补充黄体生成素对控制性超促排卵过程中卵巢慢反应患者临床结局的影响[J]. 现代妇产科进展,2014,23:716-718.
[12]Alviggi C,Clarizia R,Pettersson K,et al. Suboptimal response to GnRHa long protocol is associated with a common LH polymorphism[J/OL]. Reprod Biomed Online,2011,22(Suppl 1):S67-S72.
[13]Li Y,Yang D,Zhang Q. Impact of overweight and underweight on IVF treatment in Chinese women[J]. Gynecol Endocrinol,2010,26:416-422.
[14]刘海鹏,贺平,陈艺,等. 体重指数对体外受精-胚胎移植治疗结局的影响分析[J]. 生殖医学杂志,2013,22:324-328.
[15]Koundouros SN. A comparison study of a novel stimulation protocol and the conventional low dose step-up and step-down regimens in patients with polycystic ovary syndrome undergoing in vitro fertilization[J]. Fertil Steril,2008,90:569-575.
[编辑:肖晓辉]
Influencing factors of slow response in women with polycystic ovary syndrome
TANG Wen-juan,LIU Yu-sheng*,HUANG Ling-li
Reproductive Medical Center,Anhui Provincial Hospital,Anhui Medical University,Hefei230001
【Abstract】
DOI:10.3969/j.issn.1004-3845.2016.05.002
【收稿日期】2015-10-15;【修回日期】2016-03-18
【基金项目】国家自然基金(No:81370757)
【作者简介】汤文娟,女,安徽人,硕士生,生殖医学专业.(*通讯作者,Email:shengzhizhongxin@126.com)

