无症状性颈动脉狭窄外科干预的循证医学证据
杨復唐 柏 骏 曲乐丰上海长征医院血管外科,上海 200003
无症状性颈动脉狭窄外科干预的循证医学证据
杨復唐 柏骏 曲乐丰*
上海长征医院血管外科,上海 200003
基金资助:国家自然科学基金项目(8157020854);上海市高校“东方学者”特聘教授基金*通信作者:曲乐丰,E-mail:qulefengsubmit@163.com
目前脑卒中是世界上最重要的致死性疾病之一,也是永久性神经性残疾的主要病因。以脑卒中为代表的脑血管疾病,已经成为当前国内居民的首要死因[1]。颅外段颈动脉狭窄是导致缺血性脑卒中的重要病因,根据美国卒中中心(www.strokecenter.org)的数据,约20%~30%脑卒中由颅外段颈动脉狭窄所致。根据临床症状区分,颈动脉狭窄可以分为症状性颈动脉狭窄和无症状性颈动脉狭窄。目前,症状性颈动脉狭窄的诊治已经趋于统一,本文旨在通过对现有相关循证医学证据进行归纳分析,为无症状性颈动脉狭窄的外科干预提供参考。
1 概念及流行病学调查
颈动脉狭窄是引发脑卒中的重要病因,其症状主要是脑部缺血的临床表现,例如视物模糊、头痛、记忆力减退等。无症状性颈动脉狭窄指患者在最近180 d内未发生过颈动脉狭窄侧的缺血性脑血管症状[2]。无症状性颈动脉狭窄斑块分为稳定性及不稳定性,均有斑块脱落导致栓塞脑梗的可能,例如狭窄进展,狭窄的程度增加,存在发生缺血性脑卒中的可能,亦存在在狭窄的基础上发生血栓形成、管腔狭窄,进而导致脑梗的可能。2004—2005年完成的全国第3次死因回顾性抽样调查报告显示[1],脑血管疾病已经跃升至国内疾病死因的首位。急性脑血管疾病(脑卒中)是单病种致残率最高的疾病,但是目前国内尚无针对脑卒中发病因素的大规模流行病学调查。根据英国卒中研究机构(www.stroke.org.uk)最近的流行病学调查显示,85%脑卒中病例是缺血性脑卒中,而在缺血性脑卒中病例中有20%(17/85)会影响到椎基底动脉供血区域,另有80%(68/85)会影响到颈动脉供血区域。在颈动脉受影响的病例中,约有50%病例(34/68)出现来源于颅外颈内动脉的栓塞。29%患者(20/68)颈内动脉狭窄<50%,21%栓塞病例 (14/68)为中重度颈内动脉狭窄(50%~99%)。而在狭窄程度较重的病例中21%患者(3/14)在发生脑卒中之前罹患警示性TIA。因此,在每100例脑卒中患者中约11例是由狭窄程度>50%无症状动脉狭窄导致。这意味着英国在每年新发的150 000例脑卒中患者中,约16 500例由无症状颈内动脉狭窄导致。这些病例(脑卒中总病例数的11%)构成了无症状性颈动脉狭窄外科治疗的研究目标,而关于这些患者的治疗方法选择,也成为目前学术界争论的议题。
2 主要治疗手段及外科干预指征
与症状性颈动脉狭窄相同,无症状性颈动脉狭窄的治疗方法分为保守治疗和外科治疗2类。前者包括高危因素控制、饮食习惯调整、适度地锻炼及抗血小板、他汀类药物治疗等综合治疗措施。外科治疗包括经典的颈动脉内膜斑块切术(CEA)[3]及在脑保护装置保护下颈动脉支架成形术(CAS)。在CEA术式选择上,常规采用外翻式CEA和补片式CEA,不推荐原位切开缝合的传统术式[4]。颈动脉支架成形术可以采用远端脑保护装置及近段脑保护装置(Moma)。而外科干预的指征,目前大多数医生仍然接受无症状性颈动脉狭窄,狭窄程度应该>70%[5]。有学者认为对狭窄程度<70%,明确的不稳定斑块及溃疡形成患者,亦适宜采用外科干预。
3 外科干预的争议
自1954年CEA作为治疗颈动脉狭窄,预防脑卒中的外科方案以来[6],无症状性颈动脉狭窄患者实施颈动脉手术的数量不断增加。许多著名的外科医生支持对无症状患者采用手术治疗[7],但是在20世纪80年代和90年代,对无症状性颈动脉狭窄患者是否应该进行手术的争议一直持续。直到有2篇划时代的随机对照试验,即无症状颈动脉粥样硬化研究(ACAS)和无症状颈动脉手术试验(ACST)分别于1995年和2004年发表[8-9],争议才告一段落。
ACAS和ACST的试验结果表明,CEA可以将5年内患者发生脑卒中的风险减少50%,即从12%减少至6%,同时ACST提示没有证据可以证明CEA能够使>75岁患者受益[9]。ACAS未发现行CEA可以使患者的5年致残性脑卒中发生风险减少,而ACST观察到行CEA 使5年致残性脑卒中发生风险相对减少了43%,从之前的6.1%减少至3.5%。ACST试验发表了10年间的数据并且证实急诊CEA与药物治疗方法相比,发生脑卒中风险的可能性减少了4.6%[10]。这相当于在每1000例CEA手术中46例可以预防脑卒中的发生。
随着CAS(颈动脉支架植入术)的普及和药物治疗方法的进步,目前争议主要在各种治疗方法分别适用何种情况的患者。在世界范围内对手术指征莫衷一是,美国倾向于进行积极的外科干预,在每年进行>120 000例CEA/ CAS手术[11]。在丹麦,无症状性颈动脉狭窄患者则不会实施任何外科干预。在英国、芬兰、瑞典和挪威,行CEA/ CAS的无症状性颈动脉狭窄患者的比例为15%~20%,澳大利亚为33%,匈牙利、瑞士为40%,意大利接近70%[12]。目前国内尚无权威的相关统计数据。积极外科干预的支持者与反对者的观点冲突可以参见表1[13]。
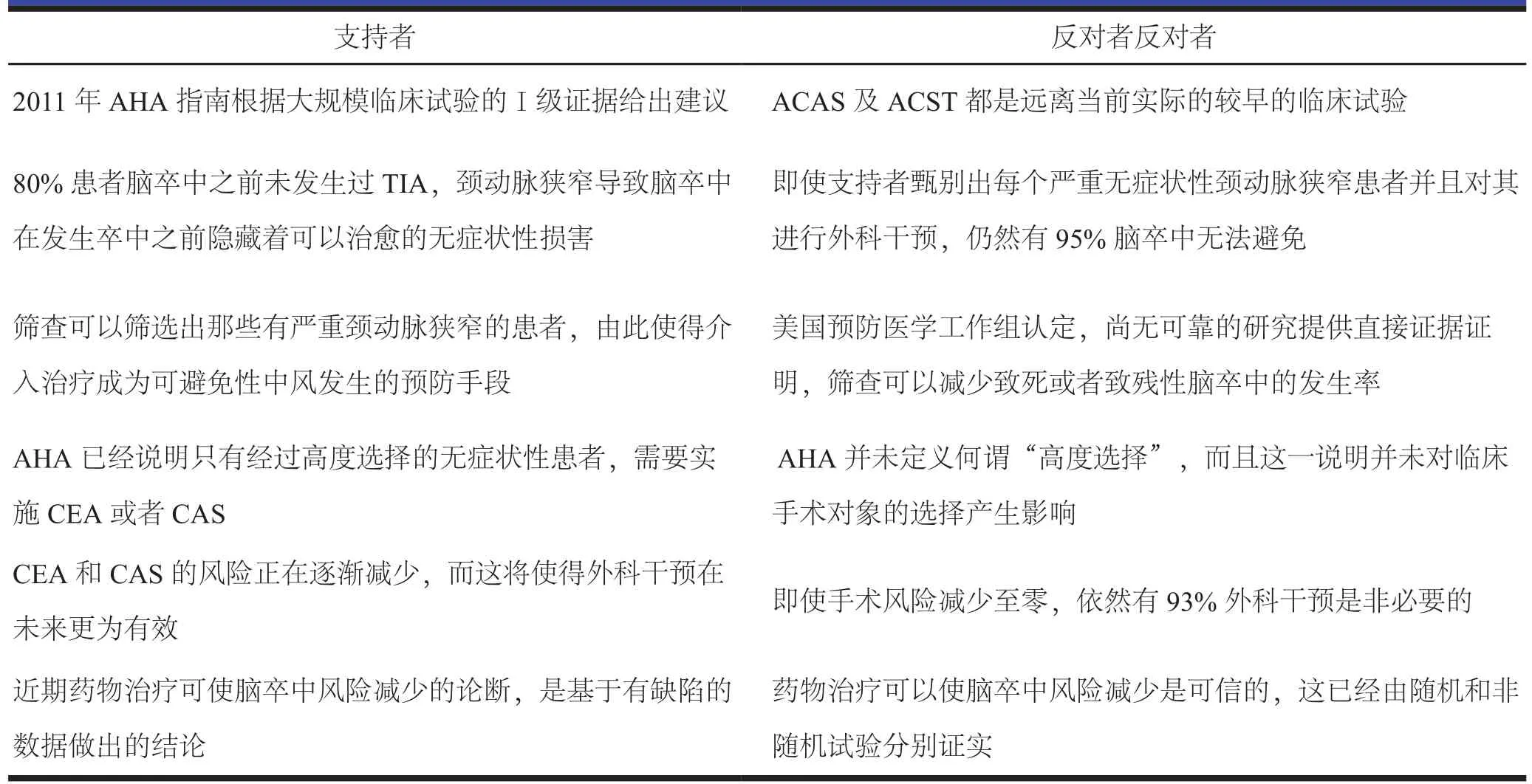
表1 积极外科干预的支持者与反对者的观点冲突
4 外科干预的相关指南
作为当前最权威的颈动脉相关疾病的治疗指南,2014年美国心脏病协会(AHA)对无症状性颈动脉狭窄患者行CEA和CAS的作用更新了指南[5]。他们建议应该筛查所有无症状性颈动脉狭窄患者是否有可治疗的危险因素,同时恰当地改变生活方式并且给予最优的药物治疗(BMT)(Ⅰ类,C层证据)。AHA建议,如果风险<3%,可以考虑对动脉狭窄程度达70%~99%高度选择患者行CEA(Ⅱa类,B层证据)。2011年AHA指南首次提出[14],对经高度选择的具有一般风险的患者,CAS可以作为CEA的替代治疗方法(Ⅱb类,B层证据)。目前AHA结论是针对行CEA术有高风险的患者,CAS(作为CEA的替代治疗方法)的效果尚不确切(Ⅱb类,B层证据)[5]。
尽管有Ⅰ等级证据支持CEA,各指南之间对治疗无症状性颈动脉狭窄的最佳方案未达成共识。十四协会联合指南[15]发表的建议与AHA建议十分相似。与之相对,澳大利亚和新西兰的指南建议对经过高度选择的普通风险的患者应该考虑只行CEA(Ⅰ类,A等级证据),不建议在任何情况下行CAS。他们还建议,对行CEA高风险患者,BMT(最佳药物治疗方法)是首选方案[16]。
英国国家健康研究院(NICE)建议,对经过高度选择的患者应该考虑行CEA,随机对照试验提示行CAS也合适。NICE没有针对行CEA术高风险的患者提供治疗指南。欧洲心脏病协会建议对经高度选择的70%~99%狭窄的患者行CEA(Ⅱa类,A等级证据),但是还认为在手术风险<3%的高水平治疗中心,给予CAS也是合理的(Ⅱb类,B等级证据)[17]。而美国血管外科学会建议,对存在一般风险的患者应该考虑只行CEA,同时对行CEA有高风险的无症状患者,药物治疗(而不是CAS)是首选的治疗方法[18]。
AHA和其它著名的指南制订机构建议,CEA应该对经过高度选择的患者实施。但是在实际操作中,“高度选择”是难以界定的概念。
最近,国际上将展开4项关于颈动脉狭窄治疗策略的大规模临床试验,其中2个随机对照试验(ACT-1 和ACST-2)目前正在收录患者但是未研究药物治疗方法[19]。另外2个旨在比较行CAS与CEA对无症状患者获益程度的多中心随机对照试验,SPACE-2试验[20]和CREST-2试验已经计划增加药物治疗方法选项来评估BMT作用,其采用的方法为“CEA+BMT vs BMT”或者“CAS+BMT vs BMT”。
5 诊疗建议
根据作者单位3000余例颈动脉狭窄手术治疗的多中心临床研究,对所有无症状性颈动脉狭窄的患者,建议予以高危因素控制,常规使用阿司匹林及他汀类药物。狭窄程度>50%的无症状患者,定期随访以评估疾病的变化,对有明确证据的不稳定性斑块或者溃疡形成患者,预计脑卒中发生的风险较高,无明显手术禁忌证患者,建议手术治疗。狭窄程度>70%的无症状患者,评估围手术期脑卒中、心肌梗塞及死亡等情况的风险较低(术后发生并发症的风险<3%)的患者建议手术治疗。关于手术方式的选择,作者科室会协同麻醉科,心内科等多学科共同进行评估,根据患者的情况:⑴ 全身情况,例如年龄、脏器功能、并存疾病和药物史等;⑵ 局部情况,例如颈部形态、有无外伤、手术和放疗史等;⑶ 病变情况,例如颈动脉狭窄程度、斑块性质,斑块的长度、范围、流入道和流出道,颅内Willis环状态等。结合患者的经济情况和个人意愿等综合因素,选择适合患者的最佳手术方式。但是无论采取何种方式均要遵守“4S+1A+1D”原则[4],即利用最简捷的手术操作(simple),尽量短的阻断和手术时间(short),充分保证手术和患者的安全(safe),同时尽可能节省移植物等其他材料的使用(save),通过以上措施达到最大程度避免手术及移植物相关并发症(avoidance),从而保持较高的中远期通畅率(durable)。
相信随着几项大型随机临床试验的陆续展开和对无症状性颈动脉狭窄相关研究的不断深入,对无症状性颈动脉狭窄的治疗方法及外科干预亦会逐渐达成共识。
参考文献
[1]陈竺. 全国第三次死因回顾抽样调查报告· 北京. 中国协和医科大学出版社,2008:1-9.
[2]Solomon, Caren G.; Grotta, James C. (19 September 2013). "Carotid Stenosis". New England Journal of Medicine 369 (12): 1143–1150.
[3]曲乐丰,柏骏. 关于“颈动脉内膜切除术”手术名称的商榷[J]. 中国血管外科杂志(电子版),2015(2):76-77.
[4]曲乐丰,柏骏,Raithel D,等. 颈动脉内膜切除手术技巧及围手术期处理:多中心临床经验总结[J]. 中华神经外科杂志,2014,30(11):1104-1107.
[5]Meschia JF, Bushnell C, Boden-Albala B, et al. Guidelines for the Primary Prevention of Stroke A Statement for Healthcare Professionals From the American Heart Association/American Stroke Association[J]. Stroke, 2014, 45(12): 3754-3832.
[6]Eastcott HH, Pickering GW, Rob CG. Reconstruction of internal carotid artery in a patient with intermittent attacks of hemiplegia. Lancet, 1954, 267:994-996.
[7]Thompson JE, Patman RD, Talkington CM. Asymptomatic carotid bruit: long term outcome of patients having endarterectomy compared with unoperated controls. Ann Surg, 1978, 188: 308-316.
[8]Executive Committee for the Asymptomatic Carotid Atherosclerosis Study. Endarterectomy for asymptomatic carotid artery stenosis. JAMA, 1995, 273:1421-1428.
[9]Asymptomatic Carotid Surgery Trial Collaborators. The MRC Asymptomatic Carotid Surgery Trial (ACST): carotid endarterectomy prevents disabling and fatal carotid territory strokes. Lancet, 2004, 363: 1491-1502.
[10] Halliday AH, Harrison M, Hayter E, et al. 10-year stroke prevention after successful carotid endarterectomy for asymptomatic stenosis (ACST-1): a multicentre randomised trial. Lancet, 2010, 376: 1074-1084.
[11] McPhee JT, Schanzer A, Messina LM, et al. Carotid artery stenting has increased rates of post-procedure stroke, death and resource utilization than does carotid endarterectomy in the United States, 2005. J Vasc Surg, 2008, 48: 1442-1450.
[12] Vikatmaa P, Mitchell D, Jensen LP, et al. Variation in clinical practice in carotid surgery in nine countries 2005e2010: lessons from VASCUNET and recommendations for the future of national clinical audit. Eur J Vasc Endovasc Surg, 2012, 44: 11-17.
[13] Naylor AR. Why is the management of asymptomatic carotid disease so controversial?[J]. Surgeon, 2015, 13(1): 34-43.
[14] Goldstein LB, Bushnell CD, Adams RJ, et al. Guidelines for the primary prevention of stroke. Guideline for healthcare professionals from AHA/ASA.Stroke, 2011, 42: 517-584.
[15] Brott TG, Halperin JL, Abbara S,et al. ASA/ACCF/AHA/ AANN/AANS/ACR/ASNR/CNS/SAIP/SCAI/SIR/SNIS/ SVM/SVS. Guideline on management of patients with extracranial carotid and vertebral arterydisease. Circulation, 2011, 124: e54-e130.
[16] Bladin C, Chambers B, Crimmins D, et al. Guidelines for patient selection and performance of carotid-artery-stenting: Inter-Collegiate Committee of the RACP/RACS/RANZCR. Intern Med J, 2011, 41: 344-347.
[17]Tendera M, Aboyans V, Bartelink I, et al. ESC guidelines
on the diagnosis and treatment of peripheral artery diseases: document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteries: the Task Force on the Diagnosis and Treatment of Peripheral Artery Diseases of the European Society of Cardiology. Eur Heart J, 2011, 32: 2851-2906.
[18] Ricotta JJ, AbuRahma A, Ascher E, et al. Updated Society for Vascular Surgery guidelines for management of extracranial carotid disease: executive summary. J Vasc Surg, 2011, 54: 832-836.
[19] Naylor AR, Ricco JB. The story of anybody, somebody, nobody and everybody. Eur J Vasc Endovasc Surg, 2013, 46: 506-507.
[20]Reiff T, Amiri H, Ringleb PA, et al. Treatment of asymptomatic carotid artery stenosis: Improvement of evidence with new SPACE-2 design necessary. Nervenarzt, 2013, 84: 1504-1507.
文章编号:2096-0646.2016.02.01.14

