葛根素凝胶膏剂的制备工艺
勾怡娜, 张 宁, 陈贤金, 刘建利, 房敏峰, 刘竹兰
(西北大学生命科学学院,西部资源生物与现代生物技术教育部重点实验室,陕西西安710069)
葛根素凝胶膏剂的制备工艺
勾怡娜, 张 宁*, 陈贤金, 刘建利, 房敏峰, 刘竹兰
(西北大学生命科学学院,西部资源生物与现代生物技术教育部重点实验室,陕西西安710069)
摘要:目的 筛选葛根素凝胶膏剂的最优处方。方法 采用单因素考察及正交试验,以感官指标、初黏力、持黏力为评价指标,进行直观分析和方差分析,优选出葛根素凝胶膏剂的最佳基质配方。然后,利用Franz扩散池法考察其体外经皮渗透性,优选最佳透皮吸收促进剂。结果 葛根素凝胶膏剂的最优处方为CMC-Na-明胶-聚丙烯酸钠-甘油-葛根素-氮酮为0.02∶4∶0.75∶3∶0.25∶0.25。不同透皮吸收促进剂的促渗效果依次为氮酮>二甲基亚砜>冰片,故氮酮为最佳透皮促进剂,透皮速率为56.246 μg/(cm2·h)。结论 以最优处方制得的葛根素凝胶膏剂具有良好的黏附性及皮肤渗透性。
关键词:葛根素;凝胶膏剂;透皮吸收;单因素试验;正交试验;Franz扩散池
dol:10.3969/j.issn.1001-1528.2016.02.012
KEY W 0RDS: Puerarin;cataP1asm;transderma1 absorPtion;sing1e factor exPeriment;orthogona1 exPeriment;Franz diffusion ce11
葛根素(Puerarin)是中药葛根的主要有效成分,具有提高免疫、增强心肌收缩力、降血压、扩张冠脉及脑血管、改善微循环、降低心肌耗氧指数、保护缺血心肌、抗血小板聚集等作用,临床应用广泛[1],但由于其自身化学结构的特点,水溶性和脂溶性都较差。药代动力学研究表明,葛根素口服自胃肠道吸收较快,但吸收程度差,生物利用度低[2]。因此,临床多以静脉注射给药,但注射剂又存在使用不便,体内消除快,需长期大剂量给药,具有血管内溶血的不良反应等问题,严重制约了其应用[3]。
现代药剂学研究表明,经皮给药可以改善药物口服生物利用度低、注射给药不便及不良反应多等问题[4]。凝胶膏剂作为经皮给药制剂,与传统膏剂相比,具有透气性好、贴敷舒适、可反复黏贴、载药量大、用药方便、能缓控释等优点[5]。因此,本实验拟将葛根素制成凝胶膏剂,以期为葛根素经皮给药研究提供依据。
1 材料
1.1试药 葛根素原料药(西安华萃生物技术有限公司,纯度99.8%);葛根素对照品(中国食品药品检定研究院,批号110752 -200209)。明胶(天津市化学制剂批发公司);CMC-Na为化学纯(天津市凯通制剂有限公司);聚丙烯酸钠为分析纯(天津市科密欧化学制剂有限公司);甘油为分析纯(天津市标准科技有限公司)。甲醇为色谱纯(天津市科密欧化学试剂有限公司);其他试剂均为分析纯。
1.2 仪器 DZF-6050真空干燥箱(上海精宏实验设备有限公司);HH-2电热恒温水浴锅(北京科伟永兴仪器有限公司);涂布器(自制);CZY-G初粘性测试仪、CZY-2S持粘性测试仪(济南兰光机电技术有限公司);TT-6(B)透皮吸收试验仪(天津市正通科技有限公司);BP221s电子天平(德国赛多利斯公司)。LC-10AT高效液相色谱仪,配有Shimadzu LC–10A二元泵、Shimadzu SPD–M10A DAD检测器、Shimadzu CTO-10AS柱温箱;Shimadzu色谱工作站、Shimadzu shim-Pack C18色谱分析柱(250 mm× 4.6 mm,5 μm)、Shimadzu C18保护柱(12.5 mm× 4.6 mm,5 μm)(日本岛津公司)。
1.3 动物 SD大鼠(西安交通大学实验动物中心),雄性,体质量(250±10)g。
2 方法与结果
2.1 初步筛选葛根素凝胶膏剂基质处方
2.1.1 黏合剂的选择 取以明胶为代表的动植物胶类、以CMC-Na、PVP及卡波姆为代表的高分子材料类,考察其作为黏合剂对凝胶膏剂黏性和外观的影响,从而选出最佳黏合剂。
凝胶膏剂的制备:将适量的CMC-Na、PVP、卡波姆及明胶分别加入适量水中,溶胀过夜,于第2天放置在50℃水浴锅中加热,搅拌使其成为均一胶体,作为Ⅰ相;将聚丙烯酸钠加入甘油中搅拌均匀,作为Ⅱ相。将Ⅱ相加入Ⅰ相中,搅拌均匀,最后加入葛根素0.25 g,边加边搅拌至基质均匀,涂布,即得。观察黏性和感官性状,结果见表1。由表可知,以CMC-Na和明胶作为黏合剂时,所得凝胶膏剂的黏性及外观均较好。
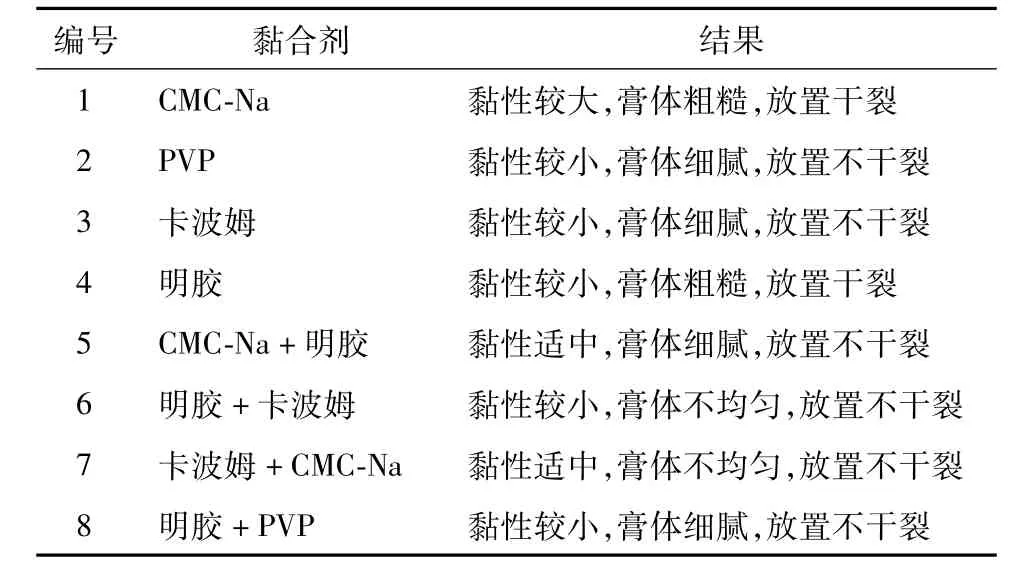
表1 黏合剂对凝胶膏剂黏性及感官的影响Tab.1 Effects of adheslves on the stlck lness and sensory perceptlon of cataplasm
2.1.2 保湿剂的选择 选取甘油、山梨醇、丙二醇及甘油+丙二醇作为保湿剂,以明胶和CMC-Na为黏合剂,按“2.1.1”项下方法制备凝胶膏剂,考察以甘油、山梨醇、丙二醇及甘油+丙二醇为保湿剂时,对凝胶膏剂保湿性能的影响。然后,将所制凝胶膏剂置于37℃恒温箱中15 d以上,计算累计失水率,评价保湿性能[6],结果见表2。
累计失水率=[(m1-m2)/m1]×100%,其中m1为凝胶膏剂原质量,m2为失水后质量。

表2 保湿剂对凝胶膏剂保湿性能的影响Tab.2 Effects of hum ectants on the m olsture retentlon of cataplasm
由表可知,以丙二醇、山梨醇为保湿剂时,在第1天的累计失水率就已较高,而在15 d后达40%左右;以甘油及甘油+丙二醇为保湿剂时,凝胶膏剂随着时间的改变,累计失水率变化均不大,但甘油保湿剂在15 d后的失水率为23.7%,稍好于甘油+丙二醇。综上所述,选择甘油作为保湿剂。
2.1.3 含水量的确定 以明胶和CMC-Na为黏合剂,以甘油为保湿剂,按“2.1.1”项下方法,制备含水量分别为20%、40%、60%的葛根素凝胶膏剂,观察黏性和感官性状,结果见表3。

表3 含水量对凝胶膏剂黏性及感官的影响Tab.3 Effects of molsture on the stlck lness and sensory perceptlon of catap lasm
由表可知,当凝胶膏剂含水量为40%时,其各项感官指标均基本符合要求,膏体性状较佳。因此,控制本品含水量为40%。
2.2 正交试验优选葛根素凝胶膏剂基质配比
2.2.1 指标选择与评分标准 根据《中国药典》2010年版一部贴膏剂项下黏附力测定方法[7],参照文献[8-10],确定本实验中凝胶膏剂的考察指标为初黏力、持黏力及感官指标。
2.2.1.1 初黏力测定 取供试品3片,置于倾斜板中央,膏面向上,斜面上部10 cm及下部15 cm用薄膜覆盖,中间留出5 cm膏面,将不同质量的钢球自斜面顶端自由滚下,根据供试品能够黏住的钢球质量,评价其初黏力的大小。本实验以黏住大于13号钢球为满分20分;11号钢球为15分;9号钢球为10分;7号钢球为5分;5号钢球为0分。
2.2.1.2 持黏力测定 采用持黏力测试仪测试,将供试品纵向黏贴在紧挨着的实验板和加载板中部,用压辊在供试品上来回滚压3次,放置2 h,加1 000 g砝码后固定于实验架,记录测试起始的时间,30 min后卸去重物,测量供试品位移值。移动距离越小,表明持黏力越好,0 cm为满分20分;>10 cm为不合格,0分;0~10 cm按距离在20~0分间评分。
2.2.1.3 感官指标检测方法(1)膏体是否均匀、细腻水润、无颗粒、拉丝、气泡,是否涂展性好、易涂布、不透过背衬;(2)膏体膏面平整、光洁、色泽均匀;(3)膜残留性,即将成型凝胶膏剂180°剥离后,残留在聚乙烯薄膜上的量;(4)皮肤追随性,借鉴日本评价凝胶膏剂的方法,将成型凝胶膏剂贴于手腕背部,用力甩10下是否脱落。其中,各项满分均为15分,每项据膏体的实际性状在0~15分之间评分。
2.2.2 凝胶膏剂的制备 分别称取处方量的明胶、CMC-Na、聚丙烯酸钠、甘油及葛根素原料药,按照“2.1.1”项下方法制备葛根素凝胶膏剂,将药膏涂布于无纺布上,厚度约为1 mm,面积为6 cm×10 cm,盖上聚乙烯薄膜,室温放置。
2.2.3 正交试验设计及结果 根据预试验及单因素试验结果,在固定加水量5 mL,加药量0.25 g的基础上,以CMC-Na(A)、明胶(B)、聚丙烯酸钠(C)、甘油(D)为因素,采用L9(34)表进行正交试验。因素水平见表4,试验设计方案及结果见表5~6。

表4 因素水平Tab.4 Factors and levels
由表5直观分析R可知,基质对凝胶膏剂初黏力、持黏力及感官性状的影响为C>B>D>A,即聚丙烯酸钠的影响最大。由表6方差分析可知,明胶、聚丙烯酸钠对实验结果有显著性影响。综上所述,葛根素凝胶膏剂最佳基质配比为A1B1C3D1,即CMC-Na-明胶-聚丙烯酸钠-甘油为0.02∶4∶0.75∶3。
2.2.4 验证试验 用优选的基质处方配比制备3批葛根素凝胶膏剂样品,测试初黏力、持黏力及进行感官评价,结果见表7。由表可知,制得的凝胶膏剂膏体细腻均匀,无拉丝、气泡、颗粒,涂展性好、易涂布、不透过背衬,膏面平整、光洁、色泽均匀,膜或皮肤上无残留,黏性较好、可反复揭贴。初黏力、持黏力、感官各项指标均较好,而且重复性理想,说明该制备工艺稳定可行,质量可靠。

表5 正交试验结果Tab.5 Results of orthogonal experlm ent
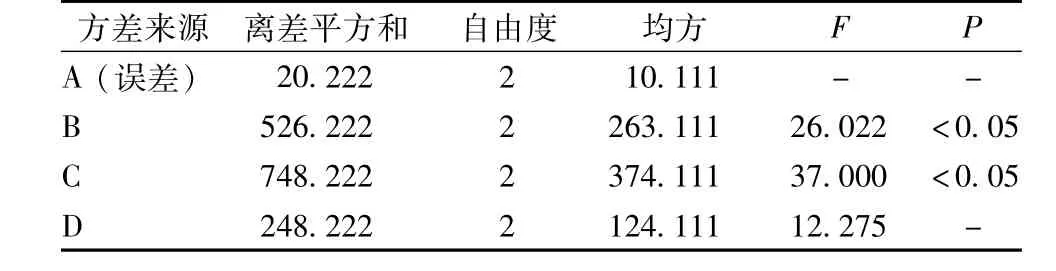
表6 方差分析结果Tab.6 Results of analysls of varlance

表7 验证试验结果Tab.7 Results of verlflcatlon test
2.3 葛根素凝胶膏剂透皮吸收促进剂的选择
2.3.1 透皮吸收促进剂的选择及样品制备 选择氮酮、冰片、二甲基亚砜各0.25 g作为透皮吸收促进剂,制备时将不同促进剂分别加入到甘油中,搅拌混合均匀,再加入聚丙烯酸钠,继续搅拌均匀制成Ⅱ相,其他步骤同“2.1.1”项下方法。分别制备5种凝胶膏剂样品,即空白基质、不含促进剂的葛根素凝胶膏剂和含透皮吸收促进剂氮酮、冰片、二甲基亚砜各0.25 g的葛根素凝胶膏剂。
2.3.2 体外鼠皮的制备 取健康大鼠,小心脱去腹部细毛,用生理盐水反复冲洗干净,一周后断颈处死,取腹部皮肤,剥离皮下脂肪及组织,用0.9%氯化钠溶液反复冲洗干净,置于-20℃冰箱中冷藏备用,实验时取出,室温下自然解冻。
2.3.3 透皮吸收实验 采用Franz扩散池,取处理好的鼠皮,用滤纸吸干多余水分,剪成大小适宜的5块,外侧皮肤面朝上,将5种凝胶膏剂分别贴于鼠皮上,固定在5套透皮吸收实验装置的扩散室与接收室之间(背衬层朝向扩散室)。在接收室中注入预温37℃的0.9%氯化钠溶液,排除气泡,使接受液与皮肤紧密接触,直至加到接收室的刻度线处。在(37±1)℃,100 r/min下恒速搅拌,分别于2、4、6、8、10、12、24、36、48 h时取出接受液2 mL,同时补加同体积预温37℃的0.9%氯化钠溶液,并排尽气泡。HPLC法测定葛根素浓度,计算累计透过量。
2.3.4 葛根素定量测定方法
2.3.4.1 溶液的制备 标准溶液的制备:精密称取葛根素标准品适量,置于10 mL量瓶中,加25%乙醇溶解并稀释至刻度,制成1 mg/mL标准贮备液。精密吸取1 mL,置于10 mL量瓶中,加25%乙醇稀释至刻度,制成0.1 mg/mL的标准溶液。
供试品溶液的制备:将各时间点的接收液水浴蒸干,25%乙醇溶解残渣,定容于10 mL量瓶中,0.45 μm微孔滤膜过滤,取续滤液,即得。
阴性对照溶液的制备:取24 h不含葛根素的凝胶膏剂经皮渗透接受液,按供试品溶液制备方法制备,即得。
2.3.4.2 色谱条件[7]Shimadzu shim-Pack C18分析柱(250 mm×4.6 mm,5 μm)、Shimadzu C18保护柱(12.5 mm×4.6 mm,5 μm);流动相为甲醇-水(25∶75);体积流量0.8 mL/min;柱温30℃;检测波长250 nm;进样量10 μL。在上述条件下,葛根素与其他组分色谱峰均达到基线分离,阴性对照溶液无干扰,测得葛根素色谱峰的保留时间在14 min左右。理论塔板数按葛根素峰计算,不低于4 000,其与相邻峰的分离度大于1.5,符合要求。
2.3.4.3 方法学验证 线性关系:分别精密吸取标准溶液0.1、0.5、1.0、1.5、2 mL,置于10 mL量瓶中,25%乙醇稀释至刻度,制得质量浓度分别为1、5、10、15、20 μg/mL的葛根素标准系列溶液。在“2.3.4.2”项下条件测定,以葛根素质量浓度为横坐标(X),峰面积为纵坐标(Y)建立标准曲线,计算回归方程及相关系数。结果,葛根素在1~20 μg/mL范围内线性关系良好,回归方程为Y=63 905X-21 609,r2=0.999 2(n =5)。
精密度试验:取低、中、高3种质量浓度(5、10、15 μg/mL)的溶液,于1 d内重复进样5次,计算日内精密度RSD分别为0.52%、0.46%、0.75%(n =5);每天进样1次,连续进样5 d,计算日间精密度RSD为1.23%、1.65%、1.54% (n =5),表明仪器精密度良好。
稳定性试验:取供试品溶液适量,分别在0、4、8、12、24、48 h进样测定,记录峰面积。结果,RSD为1.73%(n =6),表明该方法稳定性良好。
重复性试验:取同一批样品,按“2.3.4.1”项下方法平行制备供试品溶液6份,在“2.3.4.2”项色谱条件下分别进样测定,记录峰面积。结果,RSD为0.84%(n =6),表明该方法重复性良好。
加样回收率试验:在24 h空白凝胶膏剂皮肤渗透液中加入葛根素对照品适量,制成5、10、15 μg/mL的系列浓度溶液,在“2.3.4.2”项色谱条件下进样,测定峰面积。结果,平均回收率为98.97%,RSD为1.15%(n =6)。
2.3.5 体外透皮实验结果 按下式计算葛根素单位面积累计透过量[11-12]: Q=(CnV+n
i∑=-11CiV1)/A。其中,Q为第n个时间点的单位面积累积透过量(μg/cm2),Cn为第n次取样点实测药物质量浓度(μg/mL),V为接收室体积(5 mL),V1为取出的接受液体积(2 mL),A为渗透面积(0.636 cm2)。
以时间为横坐标(X),葛根素单位面积累计透过量为纵坐标(Y),作出4种含不同促进剂的葛根素凝胶膏剂经皮渗透曲线,见图1。然后,将曲线部分0~24 h的数据进行零级、一级、Higuchi、Hixson-Crowe11、Ritger-PePPas方程拟合[12-13],发现这4种葛根素凝胶膏剂的体外透皮吸收均符合零级方程,见表8。

图1 不同促进剂对凝胶膏剂中葛根素经皮渗透的影响Flg.1 Effects of d lfferent penetratlon enhancers on the transdermal permeatlon of puerarln cataplasm

表8 4种凝胶膏剂中葛根素透皮吸收参数Tab.8 Parameters for the transdermal absorptlon of puerarln ln four k lnds of cataplasms
由图、表可知,葛根素凝胶膏剂中葛根素可以经皮渗透,而且透过量随时间的延长而增加。同时,促进剂氮酮、二甲基亚砜、冰片均有促渗作用,其促渗效果为氮酮>二甲基亚砜>冰片,其中氮酮的透皮速率为56.246 μg/(cm2·h)。因此,本实验选择氮酮作为葛根素凝胶膏剂的促进剂。
3 讨论
依据中医“内病外治”传统理论,外用膏剂不仅可以应用于消炎镇痛、活血化瘀等外伤和骨科疾病的治疗,也可在许多内科疾病,如心脑血管疾病[8]、痛经[14]、胃肠道疾病[15]等的治疗中发挥作用。由此,本实验制备了葛根素凝胶膏剂,旨在改善葛根素口服生物利用度低、注射不良反应多等问题,为其发挥“内病外治”的作用提供依据。
在葛根素凝胶膏剂的基质研究中,本实验采用单因素考察及正交试验,以感官指标、初黏力、持黏力为评价指标,得到葛根素凝胶膏剂的最佳基质配方为CMC-Na-明胶-聚丙烯酸钠-甘油-葛根素-氮酮的质量比为0.02∶4∶0.75∶3∶0.25∶0.25。实验过程中发现,含水量是影响凝胶膏剂成型和质量的重要指标,含水量在40%时,基质的性状较佳。同时,搅拌速度、搅拌时间,涂布时间、涂布温度及基质的加入顺序对凝胶膏剂的性状也有影响,如搅拌速度过快,会产生大量气泡,导致膏体涂布不均匀、出现膜残留;搅拌时间过长,由于破坏了基质中的高分子材料而致使黏性下降;涂布过晚,则基质交联,导致延展性下降,出现涂布不均匀的现象。因此,通过大量研究,确定本凝胶膏剂的基质成型工艺条件为搅拌时间30 min,搅拌速度400 r/min,膏体温度50℃,将促进剂氮酮溶于甘油中,混匀后加入聚丙烯酸钠,再将该油相加入到CMC-Na和明胶的混合溶液中,最后加入葛根素。结果表明,该工艺稳定可行,所得葛根素凝胶膏剂的初黏力、持黏力、感官等各项指标均符合要求。
在体外透皮研究中,本实验考察了氮酮、二甲基亚砜、冰片对葛根素透皮吸收的影响。结果表明,不同促进剂对葛根素的累积透过量均有提高,尤以氮酮的促渗效果最好,24 h累计透过量为不含促进剂的7.045倍,透皮速率Js为56.246 μg/(cm2·h),故确定以氮酮为葛根素凝胶膏剂的促进剂。体外透皮参数显示,葛根素的透皮过程符合零级动力学方程,说明所得葛根素凝胶膏剂可以恒定速率给药,为皮控型的给药系统[16-17]。另外,氮酮能增加脂质的流动性,改变其双分子层的致密性,增加皮肤角质层含水量,使该层细胞膨胀,药物在该层形成储备库,从而促进了药物的透皮吸收[18]。但是,在该凝胶膏剂的透皮研究中只考察了单一促进剂作用,对同一促进剂不同浓度、多促进剂配伍的作用有待进一步考察。
参考文献:
[1] 李伟平,张喜平.葛根素制剂的药理和临床应用及存在问题分析[J].医学研究杂志,2012,41(1): 16-18.
[2] 陈晓兰,杜守颖,陆 洋,等.葛根提取物不同途径给药后葛根素在大鼠体内药代动力学研究[J].中华中医药杂志,2011,26(10): 2408-2411.
[3] 徐 杰.葛根素新型给药途径的研究进展[J].中国医院药学杂志,2013,33(14): 1184-1187.
[4] 何爱明.中药透皮给药系统的研究进展[J].中西医结合研究,2014,6(1): 46-51.
[5] 董 礼,徐希明,余江南.中药凝胶膏剂研究概述[J].中国药师,2011,14(1): 129-131.
[6] 王文忠,王玉翠,郑平.紫草巴布剂基质处方的优化[J].中成药,2013,35(4): 861-864.
[7] 国家药典委员会.中华人民共和国药典: 2010年版一部[S].北京:中国医药科技出版社,2010.
[8] 鹿 静,魏希颖,张 琼,等.灯盏花素巴布剂的处方优选[J].中成药,2013,35(3): 74-78.
[9] 严国鸿,潘旭东,李 煌,等.均匀设计法优选双藤痹痛凝胶膏剂的基质处方[J].中国实验方剂学杂志,2014,20 (15): 11-14.
[10] 李 旸,陈 晨,李银科,等.复方积雪草苷凝胶贴膏的制备工艺研究[J].中国药师,2014,17(10): 1672-1674.
[11] 白 洁,陆 洋,杜守颖,等.川芎贴膏制备工艺及其体内外评价研究[J].中华中医药杂志,2013,28(5): 1259-1266.
[12] 刘聪敏,白 洁,杜守颖,等.止痛凝胶膏剂体外透皮行为研究[J].中国中药杂志,2013,38(16): 2609-2613.
[13] 方 睿,张海鸣,王成芳,等.不同透皮吸收促进剂对灯盏花素凝胶剂透皮吸收的影响[J].中成药,2012,34(6): 1174-1176.
[14] 李 周,王利胜,陈辉清,等.温经止痛凝胶膏剂的促渗剂优选[J].中国实验方剂学杂志,2015,21(3): 18-20.
[15] 刘慧敏,刘 莉,刘 强,等.小儿腹泻外敷凝胶膏剂的制备及质量控制[J].中国实验方剂学杂志,2013,19(13): 42-44.
[16] 夏裕发,李 煌,张 勋,等.双藤痹痛凝胶膏剂的体外释放及其透皮吸收[J].中国医院药学杂志,2013,33(12): 925-928.
[17] 宋立华,杜茂波,刘淑芝,等.止痛凝胶膏剂的体外释放和经皮渗透性研究[J].中国中药杂志,2013,38(14): 2306-2308.
[18] 杨大凯,刘志辉,刘汉清.消炎镇痛巴布膏剂的体外透皮吸收研究[J].中草药,2011,42(5): 881-885.
Preparatlon of puerarln cataplasm
GOU Yi-na, ZHANG Ning*, CHEN Xian-jin, LIU Jian-1i, FANG Min-feng, LIU Zhu-1an
(School of Life Science,Northwest University;Ministry of Education Key Laboratory for Resources Biology and Biotechnology in Western China,Xi'an 710069,China)
ABSTRACT:AIM To screen the best formu1ation of Puerarin cataP1asm.METH0DS The bestmatrix formu-1ation of Puerarin cataP1asm was determined through sensory PercePtion,its initia1bonding strength and endurance bonding strength eva1uation,by sing1e factor and orthogona1exPeriment.Franz diffusion ce11method was aPP1ied to the study of Percutaneous Penetration to verify the best Penetration enhancer.RESULTS The oPtima1matrix formu1ation of Puerarin cataP1asm was 0.02(CMC-Na)∶4(g1utin)∶0.75(sodium Po1yacry1ate)∶3(g1ycero1)∶0.25(Puerarin)∶0.25(azone).With regard to the three different enhancers' Performance in Penetration(azone>dimethy1su1foxide>borneo1),azonewas seen as the best Penetration enhancer,which gave abook=289,ebook=67steady-state infi1tration rate of 56.246 μg/(cm2·h).C0NCLUSI0N The Puerarin cataP1asm Processed according to the oPtima1 formu1ation shows good adhesive ProPerty and skin Permeabi1ity.
*通信作者:张 宁(1979—),女,博士,副教授,从事中药化学成分与制剂工艺研究。Te1:(029)88302013,E-mai1: zhangning@ nwu.edu.cn
作者简介:勾怡娜(1991—),女,硕士,研究方向为中药化学成分与制剂工艺。Te1:(029)88302013,E-mai1: ZL_ 313173104@163. com
基金项目:国家自然科学基金资助项目(20872118,30070905);陕西省自然科学基金资助项目(2014JM4125);陕西省中医管理局课题资助项目(13-JC012);陕西省教育厅专项资助项目(14JK1737);陕西省春笋计划课题研究项目(201481)
收稿日期:2015-04-20
中图分类号:R944
文献标志码:A
文章编号:1001-1528(2016)02-0288-06

