基于纳米金/聚对氨基苯酚/多壁碳纳米管纳米复合材料修饰电极对尿酸的灵敏检测
王存,王益平,彭莉,张毅
(1.重庆第二师范学院生物与化学工程系,重庆 400067) (2.重庆市食品药品检测检验研究院、重庆市医药过程和质量控制研究中心,重庆 401121)
基于纳米金/聚对氨基苯酚/多壁碳纳米管纳米复合材料修饰电极对尿酸的灵敏检测
王存1*,王益平2,彭莉1,张毅1
(1.重庆第二师范学院生物与化学工程系,重庆 400067) (2.重庆市食品药品检测检验研究院、重庆市医药过程和质量控制研究中心,重庆 401121)
该文首先将多壁碳纳米管(MWCNTs)滴涂在玻碳电极(GCE)的表面;然后用循环伏安法和电沉积的方法依次沉积对氨基苯酚(AP)和纳米金(Au),最后制成金/聚对氨基苯酚/多壁碳纳米管纳米复合材料修饰电极(Au/p-AP/MWCNT/GCE)。采用循环伏安法和示差脉冲伏安法等电化学技术研究了尿酸(UA)在该修饰电极上的电化学行为。结果表明该修饰电极对UA具有较好的电催化活性,在pH6.0磷酸盐缓冲溶液中,其检测下限为3.3 μmol/L,线性范围分别为15~510 μmol/L。干扰实验表明,共存物质抗坏血酸(AA)和多巴胺(DA)对UA的检测没有干扰。同时该修饰电极用于实际样品(尿液和血清)中UA的测定也得到较好的效果。该研究为UA的快速检测提供了一种新方法。
多壁碳纳米管;纳米金;聚对氨基苯酚;尿酸;玻碳电极
0 引言
尿酸(UA)又名2,6,8-三羟基嘌呤,是核酸组成单位中嘌呤核苷酸分解代谢的产物[1]。UA在人体中含量的变化,可充分反映出人体内代谢、免疫等机能的状况,UA的生成和排泄不平衡时,会引起血液中UA含量的异常,诱发多种疾病,如痛风、白血病、肾功能衰竭、高尿酸血症等,对人体产生严重危害[2-4]。因此,对人体体液中UA的定量分析无论是在药物控制方面还是在临床诊断方面都具有重要意义。目前检测UA的方法主要有光谱法[5-6]、高效液相色谱法[7]、酶分析法[8]、电化学发光法[9]和电泳法[10]等,但是这些方法大都存在样品预处理过程多且繁琐,仪器昂贵,操作麻烦,成本高和操作条件受一定限制等缺点。而电化学方法[11-12]因具有操作简单、灵敏度高、成本低、样品不需要复杂前处理等优点受到广泛的关注,是目前测定UA切实可行的方法之一。
多壁碳纳米管(MWCNTs)具有良好的导电性和高度稳定性等优点,将其用作电极修饰材料可以促进电活性物质的电子传递。基于MWCNTs修饰电极在快速定量检测UA已经得到广泛的研究,已在测定方法多样性、测量精确度、稳定性和抗干扰能力等方面得到了很大的提高。如Ronald J.Mascarenhas工作团队将铁纳米粒子(Fe)修饰到MWCNTs表面制成了Fe/MWCNTs碳糊电极,使用循环伏安法(CV)研究了UA在修饰电极上的电化学特性,建立一种电化学检测UA的新方法。该方法具有电极制备简便、稳定性好、使用寿命长、检出限低等特点。该方法已经成功应用于实际样品(人的血清和尿液)中UA的含量检测,结果满意[13]。张卉通过静电相互作用在十二烷基苯磺酸钠处理过的单臂碳纳米管表面固定硫堇和尿酸酶制成修饰电极并用于尿酸的检测,该电极具有稳定性好,抗干扰能力强,快速检测等优点[14]。另一方面,金纳米颗粒(Au)作为纳米材料中的一员,具有米颗粒尺寸小,比表面积大和导电性好等优点,应用于传感器具有很高的化学催化活性。基于此,该文通过利用纳米材料的纳米尺寸和电催化效应,为达到增强电化学响应信号的目的,制备了金/聚对氨基苯酚/多壁碳纳米管纳米复合材料(Au/p-AP/MWCNT),并用于玻碳电极修饰。实验表明该修饰电极可用于UA的灵敏检测,为UA的测定提供了一个快速、可靠的方法。该方法重现性好,灵敏度高,不需经过任何预处理步骤,已经用于人的尿液和血清中UA的测定,测定结果令人满意。
1 实验部分
1.1 试剂与仪器
尿酸(UA)和对氨基苯酚(AP)(分析纯,aladdin试剂公司);氯金酸(HAuCl4,>99.9%)、多壁碳纳米管(MWCNTs)(sigma公司)。磷酸盐缓冲溶液(PBS)由K2HPO4-KH2PO4配制,支持电解质为0.1 mol/L KCl。其他试剂均为分析纯试剂,整个实验过程用水均为二次蒸馏水。
电子天平(FA2004B,上海恒平科技有限公司),KQ5200型超声仪(昆山市超声仪器有限公司)。CHI-660E型电化学工作站(上海辰华仪器有限公司),实验采用常规的三电极系统:表面修饰的玻碳电极为工作电极,铂丝为对电极,饱和甘汞电极作为参比电极。以循环伏安法(CV)和示差脉冲伏安法(DPV)考察电极表面不同修饰状态的电化学特性。
1.2 修饰电极的制备
首先,将玻碳电极(GCE,直径3 mm)在金相砂纸上依次用1.0,0.3和0.05 μm的氧化铝粉进行抛光,分别在无水乙醇、超纯水中各超声5 min,室温下干燥备用。其次,将2 mg多壁碳纳米管(MWCNTs)超声分散于2 mL水中,得到l g/L的多壁碳纳米管分散液。取20 μL溶液滴加在玻碳电极表面,室温下晾干,得到多壁碳纳米管修饰电极(MWCNTs/GCE)。然后,将MWCNTs/GCE放入聚合液中电沉积对氨基苯酚(AP),沉积聚合液由1 mmol/L AP和0.5 mol/L H2SO4组成,采用CV方法,在-0.2~1.0 V之间以扫速为50 mV/s循环扫描20圈,沉积结束后用蒸馏水洗净电极,然后在0.1 mol/L PBS(pH6.0)缓冲溶液中扫至稳定的循环伏安曲线,室温晾干,得到聚对氨基酚/多壁碳纳米管修饰电极(p-AP/MWCNTs/GCE)。最后沉积纳米金(Au),将聚合后的电极于1 mmol/L HAuCl4和0.5 mol/L H2SO4混合溶液中,-0.2 V电位沉积80 s,蒸馏水冲洗后得到Au/p-AP/MWCNTs/GCE。室温下晾干,使用前先用蒸馏水轻微冲洗并用滤纸将余留水分吸干。
2 结果与讨论
2.1 对氨基苯酚在电极上的电化学聚合
图l为以MWCNTs/GCE为基础电极,以50 mV/s的扫速沉积聚对氨基苯酚膜(p-AP)时的循环伏安(CV)图。由图可见,在+0.50和+0.56 V左右分别出现两对较强的氧化还原峰,在+0.22和+0.74 V左右分别出现两对较弱的氧化还原峰。随着扫描次数的增加,电流逐渐增大,说明对氨基苯酚(AP)已经通过电化学的方法聚合在电极表面。循环扫描一定圈数后,电流增加的幅度减小,证明随着聚合反应的进行,电极表面的聚合物薄膜趋于完整,聚合沉积速率减缓,修饰过程完成。
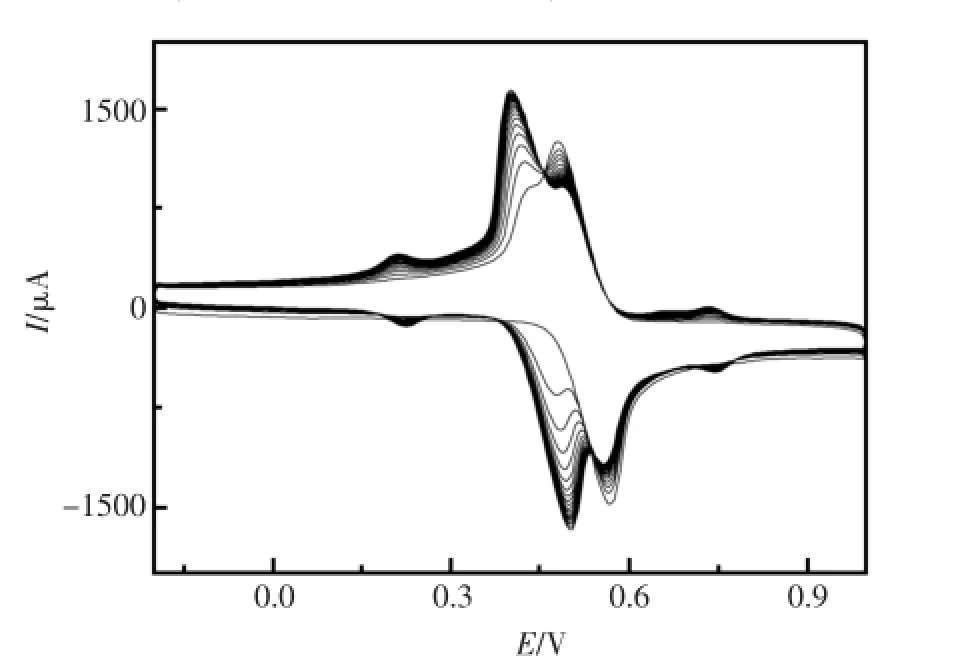
图1 对氨基苯酚聚合过程的循环伏安曲线Fig.1Cyclic voltammograms of p-aminopenol in the polymerization process
2.2 电极修饰过程的电化学表征
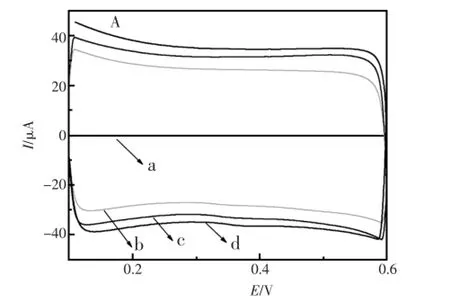
图2 在0.1 mol/L PBS(pH6.0)溶液中不同修饰电极循环伏安图形,(a)裸玻碳电极,(b)多壁碳纳米管修饰玻碳电极,(c)对氨基苯酚/多壁碳纳米管修饰玻碳电极,(d)金/对氨基苯酚/多壁碳纳米管修饰玻碳电极。扫速:0.05 V/sFig.2cyclic voltammograms of(a)bare GCE,(b)MWCNTs/ GCE,(c)p-AP/MWCNTs/GCE,(d)Au/p-AP/MWCNTs/GCE in 0.1 mol/L PBS(pH6.0).Scan rate:0.05 V/s
用循环伏安法研究了电极组装过程中的电化学特性。图2为不同修饰电极在0.1 mol/L PBS (pH6.0)溶液中的循环伏安图谱。从图中可以看出,MWCNTs/GCE(图2b)的背景电流远远大于裸的玻碳电极(图2a)背景电流,这可能是由于碳纳米管的比表面积大,增加了电极表面电荷所致[15]。当沉积了AP到电极表面时,p-AP/ MWCNTs/GCE(图2c)背景电流相对MWCNTs/ GCE背景电流稍微增大,表明p-AP具有良好的导电性。由于纳米金(Au)具有大的比表面积和良好的导电性,Au/p-AP/MWCNTs/GCE(图2d)背景电流相对p-AP/MWCNTs/GCE背景电流增大。以上过程表明,目标电极制备成功。图3为Au/p-AP/MWCNTs修饰电极的制备过程图。
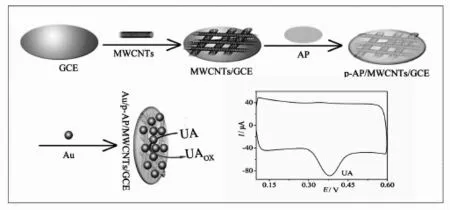
图3 Au/p-AP/MWCNTs修饰电极的制备过程Fig.3The preparation process of Au/p-AP/MWCNTs modified electrode
2.3 UA在复合修饰电极上的伏安特性
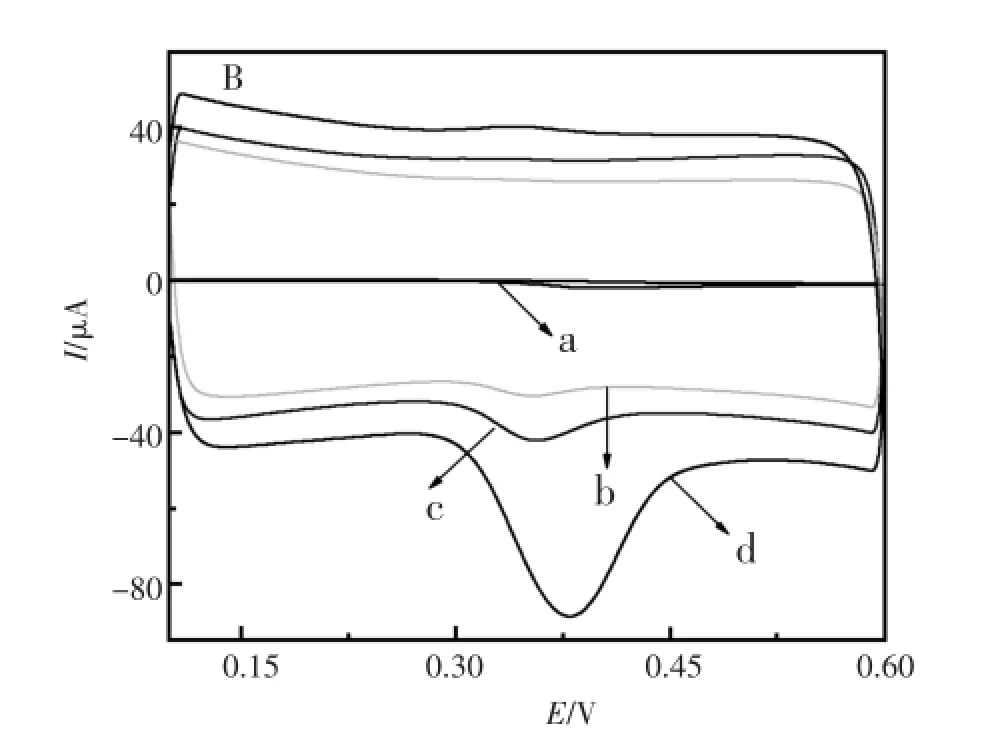
图4 在含有50 μmol/L UA的0.1 mol/L PBS(pH6.0)缓冲溶液中不同修饰电极循环伏安图形,(a)裸玻碳电极,(b)多壁碳纳米管修饰玻碳电极,(c)对氨基苯酚/多壁碳纳米管修饰玻碳电极,(d)金/对氨基苯酚/多壁碳纳米管修饰玻碳电极。扫速:0.05 V/sFig.4cyclic voltammograms at(a)bare GCE,(b) MWCNTs/GCE,(c)p-AP/MWCNTs/GCE,(d)Au/p-AP/ MWCNTs/GCE in 0.1 mol/L PBS(pH6.0)containing 50 μmol/L UA.Scan rate:0.05 V/s
图4为bare GCE,MWCNTs/GCE,p-AP/ MWCNTs/GCE和Au/p-AP/MWCNTs/GCE在含有50 μmol/L UA的0.1 mol/L PBS(pH6.0)中的循环伏安曲线。由图可见,UA在bare GCE(图4a)上基本没有响应。在MWCNTs/GCE(图4b)和p-AP/ MWCNTs/GCE(图4c)上的峰电流响应比较弱。值得注意的是,UA在Au/p-AP/MWCNTs/GCE(图4d)的响应电流非常大,相较于bare GCE约增大87倍左右,相较于MWCNTs/GCE和p-AP/ MWCNTs/GCE峰电流约增大了2.9和2.1倍左右。目标电极对UA有较大响应,原因大致可以归纳为以下几个方面:1)Au具有大的比表面积和高的电子传递速率[16];2)MWCNTs的边缘缺陷或边缘石墨性质可以加速对UA的催化氧化[17];3)Au、p-AP和MWCNTs三者形成的复合材料中三者协同作用使得该种复合材料修饰的电极对UA有明显的催化作用所致。总之,实验结果表明,目标电极可用于UA检测。
2.4 pH缓冲液尿酸的电化学行为影响
在其他条件一定的情况下,研究了磷酸缓冲溶液pH值在3.0~8.0范围内对UA的峰电流影响。具体表现如图5。图5A为UA峰电流与pH之间关系图,由图可知,UA在pH3.0处有较大峰电流,但是UA的峰电流在pH4.0~pH8.0范围内先增加后减小,在pH6.0处取得最大值。图5B为UA峰电位与pH之间关系图,由图可知,UA峰电位则随着pH值的增大而降低,表明UA是等电子等质子参加的反应[18]。综合考虑,选择pH6.0作为Au/p-AP/MWCNTs修饰电极对UA选择性测定的底液。
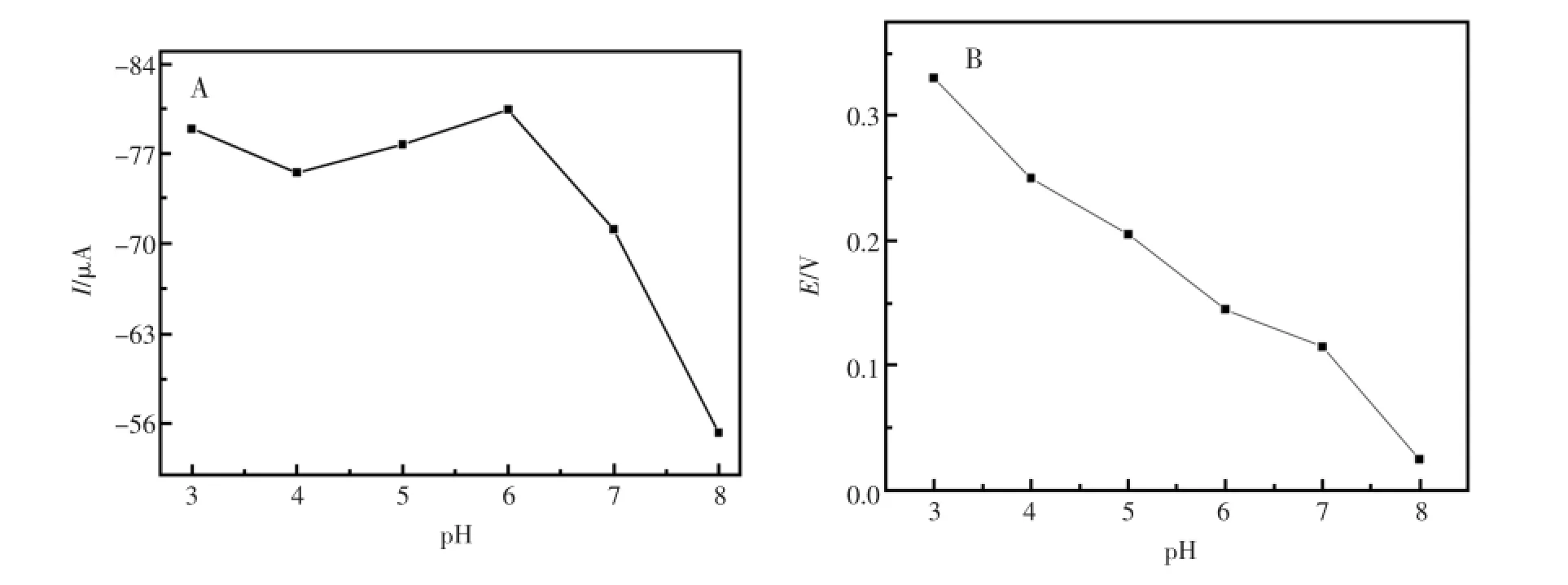
图5 (A)pH对UA峰电流的影响和(B)pH对UA峰电位的影响Fig.5(A)Dependence of UA peak current on pH and(B)Dependence of UA peak potential on pH
2.5 示差脉冲伏安法测定UA
由于示差脉冲伏安法(DPV)比CV具有更好的分辨率和更高的灵敏度,常被用于UA含量测定研究。因此,该实验采用DPV法对不同浓度的UA进行测定,结果如图6所示。图中UA浓度从上往下依次增大,分别为15、25、50、60、140、165、195、205、270、300和510 μmol/L。由图可见,UA峰电流随其浓度的增加而线性增加,并在15~510μmol/L范围内与其浓度呈良好的线性关系,其线性方程为:I(μA)=-227.043-0.04203cUA(μmol/L),检出限(S/N=3)为3.3 μmol/L。
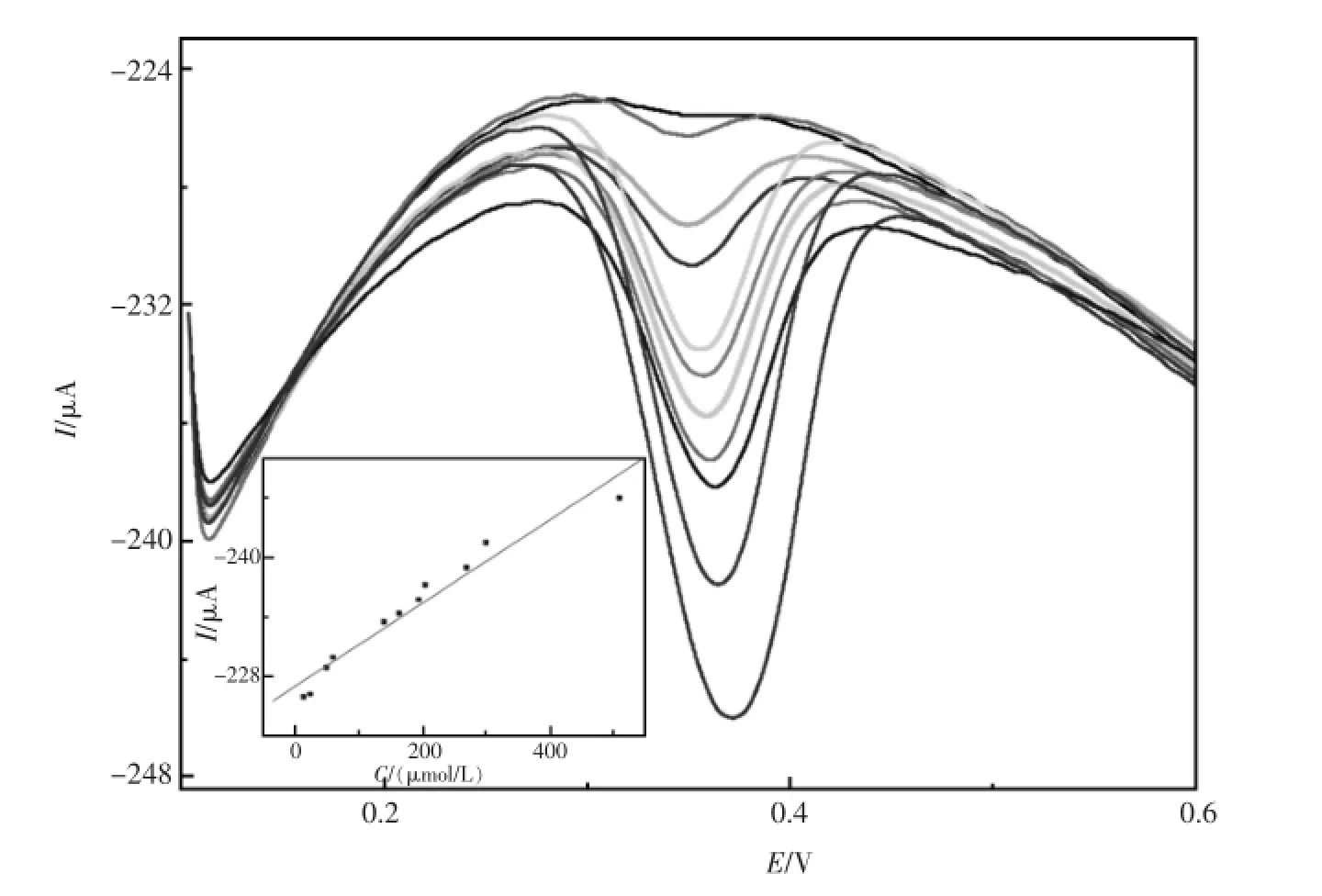
图6 Au/p-AP/MWCNTs/GCE对不同浓度UA响应的DPV曲线。UA浓度从上往下依次增大,分别为15、25、50、60、140、165、195、205、270、300和510 μmol/L。插图为响应电流与相应UA浓度的线性关系曲线Fig.6DPV curves of Au/p-AP/MWCNTs/GCE responding to different concentrations of UA.The concentrations of UA(from inner to outer)are:15、25、50、60、140、165、195、205、270、300 and 510 μmol/L.The inset shows a linear plot of response current vs.concentration
2.6 干扰实验和稳定性
在最佳实验条件下,在含有50 μmol/L UA的0.1 mol/L PBS(pH6.0)中,考察了与UA电位相近物质及常见的金属离子、阴离子对UA测定的影响。结果表明,抗坏血酸、多巴胺、葡萄糖、L-半胱氨酸、K+、Fe3+、Na+、Ca2+、SO42-、NO2-、NO3-、Mg2+、Zn2+等基本不干扰UA的测定,说明该修饰电极具有较好的抗干扰能力。当该传感器不用时,室温保存。10 d后,该传感器对UA响应电流下降约2.3%。20 d后,该传感器电流响应下降约6.7%。说明此电极具有良好的稳定性。
2.7 实样分析
采用加标回收的方法,考察了Au/p-AP/ MWCNTs修饰电极对人血清和尿液样品中UA含量的测定。血清和尿液样品直接使用没有进行预处理,测定时分别将血清样品与尿液样品用0.1 mol/L PBS(pH6.0)缓冲溶液稀释100倍,检测结果见表1,该方法对UA测定的回收率为98.5%~101.0%,说明该方法可以满足实际样品中UA的定量分析。
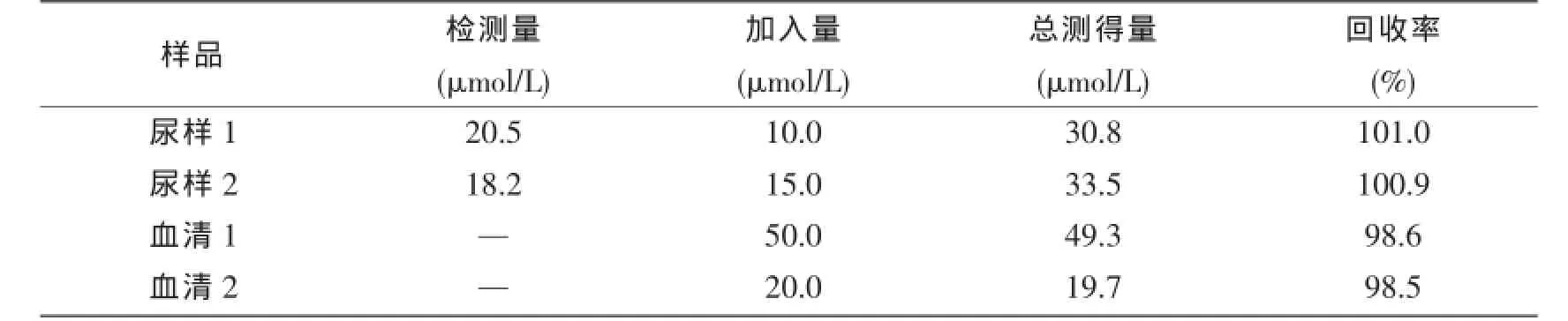
表1 人的尿液和血清样品中尿酸的测定及回收率Tab.1Determination of uric acid in human serum and urine samples and corresponding recovery
3 结论
该实验成功制备出Au/p-AP/MWCNTs纳米复合材料,并用于玻碳电极修饰,研究了该修饰电极对UA的电化学行为,建立了UA含量测定的新方法。通过Au、p-AP和MWCNTs协同作用,提高了该传感器对UA检测的灵敏度和线性范围。结果表明,该方法相对简单,且具有较高的灵敏度、较宽的线性范围、较高稳定性和较强抗干扰能力,已经成功应用于实际样品(人的血清和尿液)中UA的含量检测。因此,该方法在实际样品或临床医学样品检测UA具有一定的研究意义和参考价值。
[1]Yu Y Y,Chen Z G,Zhang B B,et al.Selective and sensitive determination of uric acid in the presence of ascorbic acid and dopamine by PDDA functionalized graphene/ graphite composite electrode[J].Talanta,2013,112: 31-36.
[2]Xue Y,Zhao H,Wu Z J,et al.The comparison of different gold nanoparticles/graphene nanosheets hybrid nanocomposites in electrochemical performance and the construction of a sensitive uric acid electrochemical sensor with novel hybrid nanocomposites[J].Biosens.Bioelectron., 2011,29:102-108.
[3]Niu X L,Yang W,Guo H,et al.A novel and simple strategy for simultaneous determination of dopamine,uric acid and ascorbic acid based on the stacked graphene platelet nanofibers/ionic liquids/chitosan modified electrode[J].Talanta,2012,99:984-988.
[4]Li H X,Wang Y,Ye D X,et al.An electrochemical sensor for simultaneous determination of ascorbic acid, dopamine,uric acid and tryptophan based on MWNTs bridged mesocellular graphene foam nanocomposite[J]. Talanta,2014,127:255-261.
[5]董文举,李晶,郭敬红.聚邻氨基对酚磺酸修饰电极测定尿酸[J].化学研究与应用,2008,20(9):1235-1238.
[6]Tullia M C C,Cozzi F,Carpita N C.Measurement of uronic acids without interference from neutral sugars[J]. Anal Biochem.,1991,197:157-162.
[7]张春梅,戴新华,杨屹,等.高效液相色谱法准确测定血清中的尿酸[J].分析试验室,2008,27(5):84-87.
[8]Hoshi T,Saiki H,Anzai J.Amperometric uric acid sensors besed on polyelectrolyte multilayer films[J].talana, 2013,61:363-368.
[9]Ballesta C J,Rodríguez G R,Capitán V L F.Disposable biosensor based on cathodic electrochemiluminescence of tris(2,2-bipyridine)ruthenium(II)for uric acid determination[J].Anal.Chim.Acta,2013,770:153-160.
[10]Chen S,Zheng H,Wang J,et al.Carbon Nanodots As a Matrix for the Analysis of Low-Molecular-Weight Molecules in Both Positive-and Negative-Ion Matrix-Assisted Laser Desorption/Ionization Time-of-Flight Mass Spectrometry and Quantification of Glucose and Uric Acid in Real Samples[J].Anal.Chem.,2013,85: 6646-6652.
[11]Zhou S H,Shi H Y,Feng X,et al.Design of templated nanoporous carbon electrode materials with substantial high specific surface area for simultaneous determination of biomolecules[J].Biosens.Bioelectron.,2013,42: 163-169.
[12]Wang C Q,Du J,Wang H W,et al.A facile electrochemical sensor based on reduced graphene oxide andAu nanoplates modified glassy carbon electrode for simultaneousdetection of ascorbic acid,dopamine and uric acid [J].Sens.Actuators B,2014,204:302-309.
[13]Bhakta A K,Mascarenhas R J,Souza O J,et al.Iron nanoparticles decorated multi-wall carbon nanotubes modified carbon paste electrode as an electrochemical sensor for the simultaneous determination of uric acid in the presence of ascorbic acid,dopamine and l-tyrosine [J].Mater.Sci.Eng.,2015,57:32-337.
[14]张卉,陈冬晓,蔡称心.基于硫堇碳纳米管修饰电极对过氧化氢的催化还原低电位检测尿酸[J].分析化学,2009,37(A03):348-348.
[15]王晓丽,张芬芬,陈燕,等.碳纳米管修饰的尿酸传感器的研制及应用[J].化学传感器,2003,23(3):55-61.
[16]Huo Z H,Zhou Y L,Liu Q,et al.Sensitive simultaneous determination of catechol and hydroquinone using a gold electrode modified with carbon nanofibers and gold nanoparticles[J].Microchim.Acta,2011,173:119-125.
[17]Zhang Y,Yuan R,Chai Y Q,et al.Simultaneous voltammetric determination for DA,AA and NO2-based on graphene/poly-cyclodextrin/MWCNTsnanocomposite platform[J].Biosens.Bioelectron.,2011,26:3977-3980.
[18]Lian Q W,He Z F,He Q,et al.Simultaneous determination of ascorbic acid,dopamine and uric acid based on tryptophan functionalized graphene[J].Anal.Chim., Acta,2014,823:32-39.
Au/poly(p-aminopheno)/multi-walledcarbon nanotubes nanocomposite materials modified electrode for the sensitive determination of uric acid
Wang Cun1*,Wang Yi-ping2,Peng Li1,Zhang Yi1
(1.Department of Biological&Chemical Engineering,Chongqing University of Education,Chongqing 400067, China)
(2.Chongqing food and drug inspection and Testing Research Institute,Chongqing Engineering Research Center for Pharmaceutical Process and Quality Control,Chongqing 401121,China)
In this paper,firstly,the multi-walled carbon nanotubes(MWCNTs)were coated on the surface of glassy carbon electrode(GCE);then,p-aminopheno(AP)and gold nanoparticles(Au)were deposited by cyclic voltammetry and electrodeposition;finally,an Au/poly(p-aminopheno)/multi-walledcarbon nanotubes(Au/p-AP/MWCNTs) nano-composite materials modified electrode was fabricated.The electrochemical behavior of UA was investigated by cyclic voltammogram and differential pulse voltammetry,indicating that the modified electrode possessed an enhanced electrocatalytic activity to the UA.In 0.1 mol/L PBS(pH6.0),the modified electrode showed good response to UA,the linear calibrations for UA were obtained over ranges of 15 to 510 μmol/L with detection limits of 3.3 μmol/L.The interference test showed that the coexisted ascorbic acid(AA)and dopamine(DA)had no electrochemical interference toward UA.In addition,the modified electrode was successfully applied for the determination of analytes in real sample(urine and serum)with satisfactory results.This study provides a new method for the rapid detection of UA.
multi-walled carbon nanotubes;gold nanoparticles;poly(p-aminopheno);uric acid;glassy carbon electrode
重庆市教委科学技术研究项目(KJ1501404)、重庆市工程技术研究中心建设项目(cstc2015yfpt-gcjsyjzx0027)资助
*通信联系人,Tel:15696106894,E-mail:wangcun5224@126.com

