怡康片指纹图谱研究和两个指标成分定量测定*
张海弢,徐振秋,付 娟,王振中,萧 伟**
(1.江苏康缘药业股份有限公司 连云港 222001;2.中药制药过程新技术国家重点实验室 连云港 222001)
怡康片指纹图谱研究和两个指标成分定量测定*
张海弢1,2,徐振秋1,2,付 娟1,2,王振中1,2,萧 伟1,2**
(1.江苏康缘药业股份有限公司 连云港 222001;2.中药制药过程新技术国家重点实验室 连云港 222001)
目的:建立怡康片的指纹图谱,进行两个指标成分的定量分析,为评价怡康片提供依据。方法:采用Kromasil C18柱(4.6 mm×250 mm,5 μm),以甲醇-水梯度洗脱,流速1.0 mL·min-1,柱温30℃,检测波长为250 nm。结果:得到分离度、重现性均较好的怡康片指纹图谱,标示出19个共有峰,各批次样品相似度在0.96以上;通过对照品比对,确定了两个成分,分别为葛根素和姜黄素,并对其进行定量分析。结论:本实验同时对怡康片指纹图谱和两个指标成分进行分析,快速、简便、准确,可作为全面评价该制剂质量的有效方法之一。
怡康片 指纹图谱 葛根素 姜黄素 高效液相色谱法
怡康片由葛根、灵芝、红景天、甘草、积雪草等中药组成,经过传统工艺提取、浓缩、干燥、粉碎后,加入姜黄提取物和适量辅料,经过总混、制粒、压片、包衣等制剂工序制成具有对化学性肝损伤起辅助保护功能的保健食品。葛根黄酮是中药葛根的主要成分,大量的实验证明葛根黄酮具有抗氧化、降低血压、解酒保肝和提高免疫功能等功效[1,2],葛根黄酮类化合物越来越广泛地被应用于药物和保健食品[3-5]。姜黄素是姜黄的活性成分,是一种多酚类物质,具有较强的抗氧化等药理作用。近年来,中药姜黄的研究越来越多,其中,对姜黄素抗肝损伤作用的研究已陆续展开,其机理主要表现在抑制肝脏炎症反应、去除自由基等方面[6]。肝病疾病是现今威胁人类健康的主要疾病之一,其预防和治疗受到了广泛的关注,它是医学界的重要任务,也是食品行业所面临的巨大挑战。由此说明,饮食对人体生命、健康、肝病预防有着重要的意义[7]。
怡康片是具有对化学性肝损伤起辅助保护功能的保健食品,标志性成分为葛根素、粗多糖、总黄酮成分[8]。为了更好地对怡康片保健食品的质量进行控制,确保其功能,需建立一个较为全面的评价制剂质量的方法[9,10]。该方中药味多,都是可以用于制作保健食品的原料,但是其成分复杂[11-13],处方经合提后,可以最大程度地提取出有效成分。然而,单味药或者几味药所提取到的单一活性成分或两个活性成分,并不能客观地反映出中药处方可以达到的整体效果。指纹图谱的特点是可以解决成分复杂、有效成分不明确的植物药质量检测等问题,因此,可以利用指纹图谱技术手段对怡康片处方进行宏观分析[14-18]。怡康片两个指标成分分别为葛根素和姜黄素,实验采用高效液相色谱(High Performance Liquid Chromatography,HPLC)法同时对怡康片进行指纹图谱研究和两个指标成分的定量测定,可作为一个有效的方法来全面控制保健食品怡康片的质量。
1 仪器和材料
Ultimate 3000 HPLC,DAD紫 外 检 测 器(美国赛默飞世尔科技公司);Centrifuge 5415D高速离心机(德国艾本德公司);KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司);Milli-Q Academic纯水机(美国密理博公司);FA1004电子天平(上海舜宇恒平科学仪器有限公司);Mettler AE240电子分析天平(瑞士梅特勒公司)。
怡康片(江苏康缘药业股份有限公司生产,批号:140601、140602、140603、140701、140801、140901、141001、141002、141003和141201);对照品均购自中国食品药品检定研究院,姜黄素(批号:110823-201404,质量分数以98.8%计),葛根素(批号:110752-201313,质量分数以95.5%计);超纯水(实验室自制),色谱甲醇(美国天地公司),其它试剂均为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱采用Kromasil C18(柱长为250 mm,内径为4.6 mm,粒径为5 μm);甲醇-水为流动相,梯度洗脱,洗脱程序为0-40 min,5%-56%甲醇,40-55 min,56%-95%甲醇;流速为1.0 mL·min-1;检测波长为250 nm;柱温为30℃;进样量为10 μL;姜黄素峰计算理论板数不低于3 000。详见色谱图1。
2.2 溶液的制备
2.2.1 对照品溶液的制备
取姜黄素、葛根素对照品适量,分析天平精密称定,置于100 mL棕色容量瓶中,加甲醇制成含姜黄素35.32 μg·mL-1、葛根素116.86 μg·mL-1的混合对照品储备液。
2.2.2 供试品溶液的制备
取本品约1 g,研钵研细,分析天平精密称定,置150 mL磨口具塞锥形瓶中,精密加入现配的50%甲醇50 mL,称定重量,置于超声波清洗器内(功率250 W,40 kHz)提取30 min,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀,滤过,取续滤液过0.22 μm滤膜,即得。
2.3 精密度试验
精密吸取“2.2.2”项下制备的供测试样品(批号:140701)10 μL,按照“2.1”项下色谱条件,连续进样6针,以峰面积计算各指标成分相对标准偏差(Relative Standard Division,RSD)值,结果显示,姜黄素为0.96%、葛根素为0.47%。以葛根素为参照峰,计算各个共有峰相对保留时间RSD值均小于1.76%,19个共有峰相对峰面积RSD值均小于2.55%。
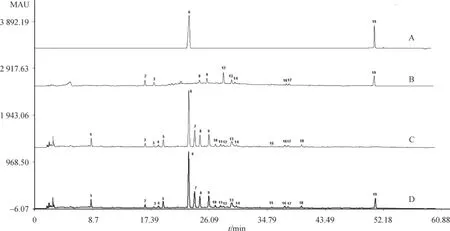
图1 HPLC色谱图
2.4 线性关系的考察
精密称取姜黄素、葛根素适量,加甲醇制成含姜黄素191.65 μg·mL-1、葛根素584.15 μg·mL-1的混合对照品储备液,将此储备液作为母液用甲醇等比稀释,按照“2.1”项下色谱条件,精密吸取10 μL进样,注入Ultimate 3000液相色谱仪,测定,以浓度为横坐标(X)、峰面积为纵坐标(Y)进行线性拟合,得姜黄素、葛根素线性回归方程分别为Y=0.553 7X-1.541 1,r=1.000 0;Y=0.521 9X-1.466 3,r=1.000 0。姜黄素、葛根素在线性范围内呈良好的线性关系,线性范围分别为5.99-191.65、18.25-584.15 μg·mL-1。
2.5 稳定性试验
取同一对照品溶液,按照“2.1”项下色谱条件,精密吸取10 μL进样,分别在0、3、6、10、16、20、24 h注入Ultimate 3000高效液相色谱仪,以峰面积为指标计算各成分RSD值,结果显示,姜黄素为0.55%、葛根素为0.63%。
取同一供试品约1 g(批号:140701),研钵研细,分析天平精密称定,按上述“2.2.2”项下供试品溶液的制备方法制备供试品溶液,精密吸取10 μL,分别于0、3、6、10、16、20、24 h注入Ultimate 3000液相色谱仪,以峰面积为指标计算各成分RSD值,姜黄素为1.10%、葛根素为0.61%。以葛根素为参照峰,计算各个共有峰相对保留时间RSD均小于1.51%,19个共有峰相对峰面积RSD值均小于1.96%。结果表明,本品24 h内稳定性良好。
2.6 重复性试验
取同一供试品约1 g(批号:140701),研钵研细,分析天平精密称定,按上述“2.2.2”项下供试品溶液制备方法制备供试品溶液,平行制备6份供试品溶液,按照“2.1”项下色谱条件进行测定。结果显示,姜黄素、葛根素的含量分别为1.29、4.54 mg·g-1,RSD值分别为1.15%、0.72%。以葛根素为参照峰,计算各个共有峰相对保留时间RSD值均小于1.27%,19个共有峰相对峰面积RSD值均小于2.03%。结果表明,本方法重复性良好,符合指纹图谱要求。
2.7 回收率试验
精密称定9份同一供试品约0.5 g(批号:140701),研钵研细,置具塞锥形瓶中,每3份为一组,9份样品分别精密加入(含姜黄素0.650 mg·mL-1、葛根素2.253 mg·mL-1)0.8、1.0、1.2 mL的混合对照品溶液,再精密加入现配的50%甲醇至50 mL,置于超声波清洗器内(功率250 W,40 kHz)提取30 min,放冷,滤过,取续滤液过0.22 μm滤膜,按照“2.1”项下色谱条件,注入Ultimate 3000高效液相色谱仪,计算回收率。结果显示,姜黄素、葛根素的平均回收率分别为100.12%、99.91%,RSD值分别为0.24%、0.15%。
2.8 样品测定结果
取10批怡康片,精密称定,按“2.2.2”项下供试品溶液制备的方法处理,按“2.1”项下色谱条件进行进样分析,测定其峰面积,分别计算姜黄素、葛根素两个指标性成分的含量。根据表1可以得出,10批怡康片中姜黄素、葛根素两个指标性成分的含有量差异较小。
2.9 指纹图谱的建立与分析
采用国家药典颁布的《中药色谱指纹图谱相似度评价系统A版》进行分析,经过数据匹配,标定19个共有峰,建立了10批怡康片样品的指纹图谱,具体指纹图谱见图2。怡康片10批次所测供试品色谱图与对照指纹图谱相似度都在0.96以上,具体批次结果分别为:0.983、0.990、0.964、0.973、0.978、0.984、0.970、0.989、0.981和0.992。
2.10 指纹图谱中共有峰的归属
在“2.1”项下色谱条件下,将中药葛根、灵芝、积雪草、红景天、甘草、姜黄药材分别取样后,按“2.2.2”项下方法制备供试品溶液,测定上述供试品溶液,通过保留时间和DAD扫描结果进行比较分析,结果显示,指纹图谱中标定的19个共有峰分别来自葛根、红景天、甘草、姜黄药材,其中1、4、5、6、7、10、11、15、18号峰来源于葛根,3、13号峰来源于红景天,2、8、9、12、14号峰来源于葛根和红景天,14号峰来源于甘草、葛根和红景天,16号峰来源于甘草和葛根,17号峰来源于甘草,19号峰来源于姜黄,结果见色谱图3。
3 讨论
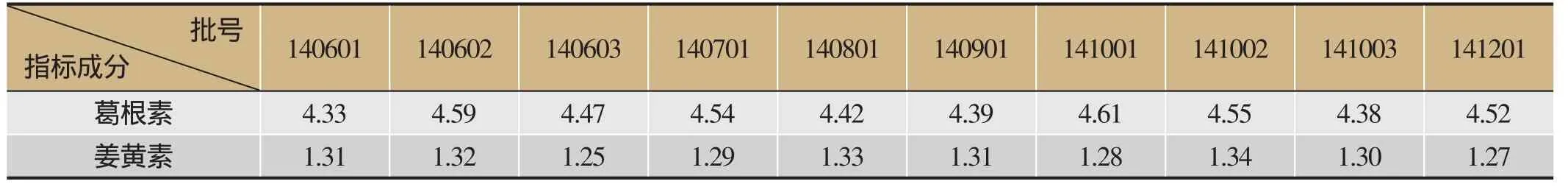
表1 10批怡康片两个指标成分测定结果(n=2,mg·g-1)
对190-400 nm范围扫描的各波长下的色谱图进行比较分析,结果显示,250 nm波长下记录的色谱图基线平稳,各色谱峰分离较好,此波长下反映出的信息全面,而且葛根素在250 nm波长下有较强吸收,所以选择250 nm波长作为怡康片指纹图谱的检测波长。
通过考察怡康片供试品的提取方法、提取时间、提取溶剂及其提取溶剂用量,最终确定了怡康片采用50%甲醇超声提取30 min效果较好,适用于指纹图谱分析;通过比较流动相甲醇-0.01%磷酸、乙腈-水、甲醇-水系统对指纹图谱的影响,结果显示,甲醇-水流动相系统所得指纹图谱中各色谱峰的分离情况和峰形优于另外两种系统;比较了使用色谱柱Waters XBridge C18(4.6×250 mm,5 μm)、Kromasil C18(4.6×250 mm,5 μm) 和 Thermo syncronis C18(4.6×250 mm,5 μm)3种色谱柱对指纹图谱的影响,结果显示,使用色谱柱Kromasil C18(4.6×250 mm,5 μm)时指纹图谱中各色谱峰分离较好,用3支该类型的色谱柱进行试验,重复性较好,因此选择该类型色谱柱来测定怡康片指纹图谱;比较了柱温为25、30、35℃所得图谱,结果显示,柱温为30℃时所得指纹图谱中各色谱峰分离较好;比较了流动相流速为0.8、1.0和1.2 mL·min-1所得图谱,结果显示,流速为1.0 mL·min-1时所得指纹图谱中各色谱峰分离较好。方法学验证试验结果表明,本试验所采用的检测方法耐用性良好。
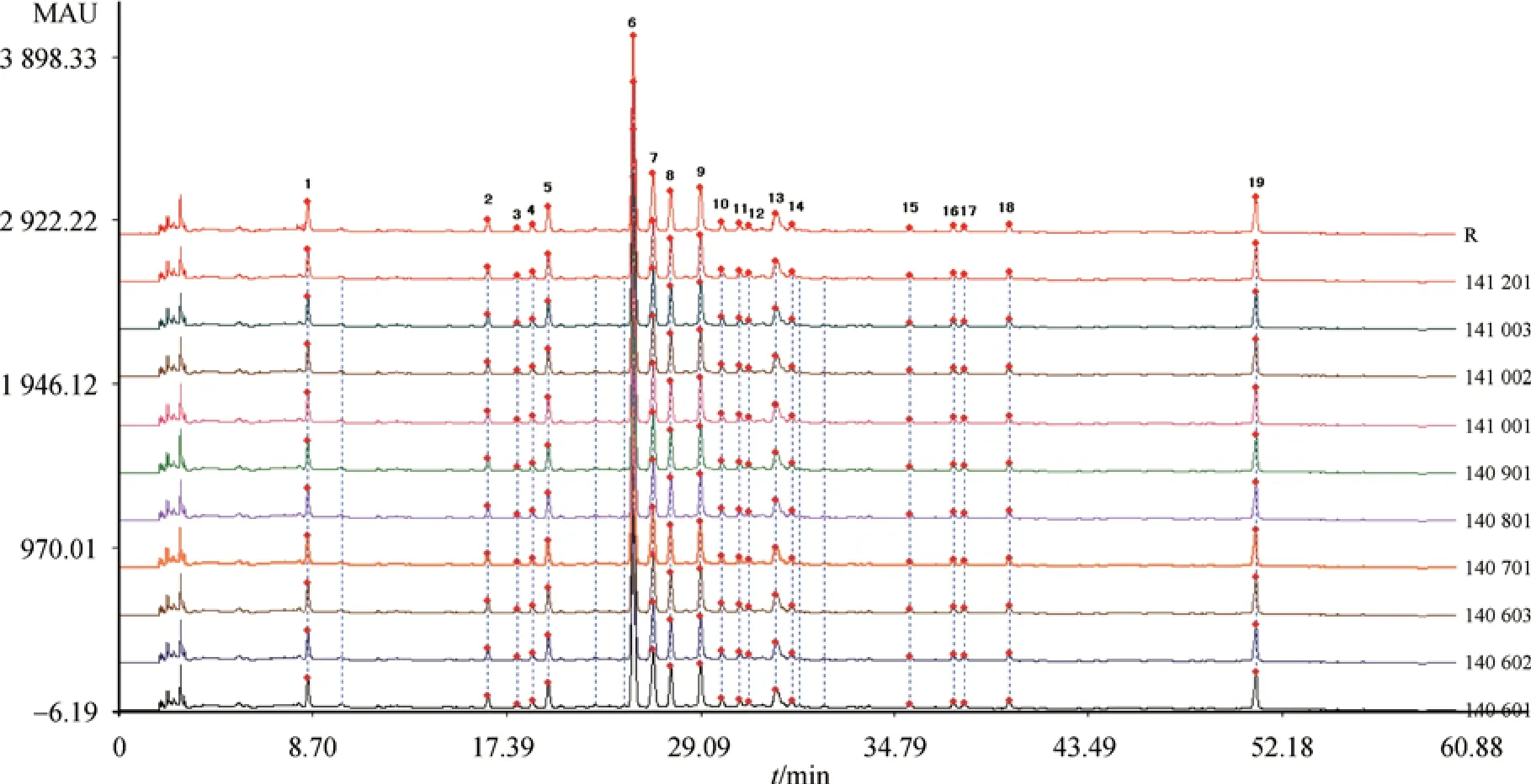
图2 10批怡康片指纹图谱
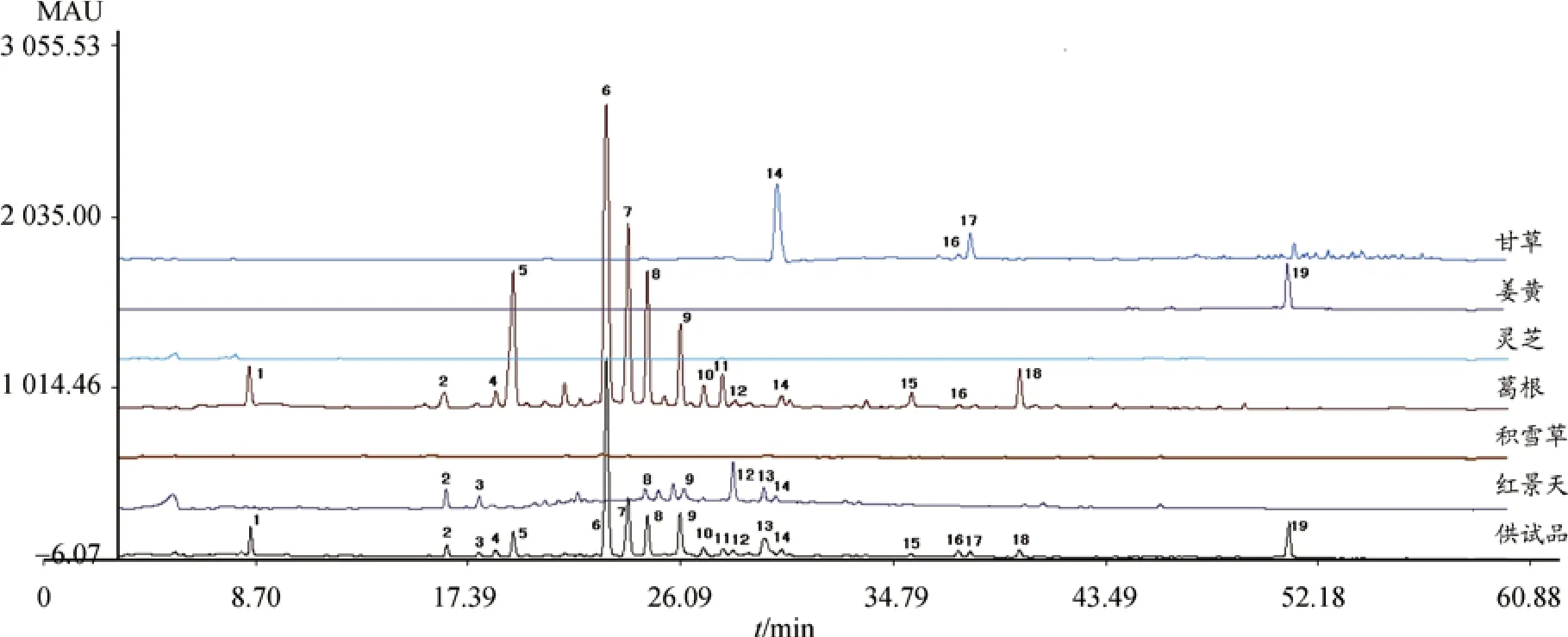
图3 怡康片指纹图谱中各共有峰归属色谱图
本试验的含量测定结果和指纹图谱显示,10批怡康片(140601、140602、140603、140701、140801、140901、141001、141002、141003和141201批)中姜黄素、葛根素两个指标性成分的含有量差异较小,且两个指标成分质量较稳定。根据怡康片中葛根、灵芝、红景天、甘草、积雪草等中药材特性,建立了指纹图谱及姜黄素、葛根素两个指标成分的质量控制方法,为全面控制怡康片的质量提供了依据,本试验可作为全面评价该制剂质量的有效方法之一。
1 吕鹏,黄晓舞,吕秋军.黄酮类化合物吸收、分布和代谢的研究进展.中国中药杂志, 2007, 32(19): 1961-1964.
2 郭喆,吕秋军,郭建平,等.葛根黄酮的辐射防护及其机制的研究.中华放射医学与防护杂志, 2006, 26(6): 579-582.
3 李国辉,张庆文,王一涛.葛根的化学成分研究.中国中药杂志, 2010, 35(23): 3156-3160.
4 王苏静,赵新杰.葛根素的药理作用研究进展.内蒙古中医药, 2010, 29(2): 107-108.
5 张鹏斐,吴卫国.葛根黄酮类化合物的研究进展.农产品加工(学刊), 2012(3): 113-116, 139.
6 彭景华,胡义扬.姜黄素抗肝损伤研究进展.国外医学(消化系疾病分册), 2005, 25(6): 373-375.
7 陆艳芹,王婧,徐振秋,等. HPLC法同时测定清葛片中葛根素、没食子酸及姜黄素的含量.世界科学技术-中医药现代化, 2015, 17(1): 230-233.
8 任亚东,朱艳林.不同产地葛根中总黄酮和葛根素的含量测定.辽宁中医药大学学报, 2008, 10(5): 160-161.
9 孙永成,窦霞,尚强,等.桂枝茯苓胶囊(精制)多成分指纹图谱的研究.世界科学技术-中医药现代化, 2010, 12(2): 294-297.
10 秦建平,吴建雄,李家春,等.散结镇痛胶囊中皂苷类成分的指纹图谱研究和多指标成分定量测定.世界科学技术-中医药现代化, 2013, 15(9): 1980-1984.
11 Mao Y, Li Y, Yao N. Simultaneous determination of salidroside and tyrosol in extracts of Rhodiola L. by microwave assisted extraction and high-performance liquid chromatography. J Pharm Biomed Anal, 2007, 45(3): 510-515.
12 Mun S C, Mun G S. Dynamics of phytoestrogen, isoflavonoids, and its isolation from stems of Pueraria lobata (Willd.) Ohwi growing in Democratic People's Republic of Korea. J Food Drug Anal, 2015: 1-7. 13 Long Y L, Zhang W P, Wang F, et al. Simultaneous determination of three Curcuminoids in Curcuma longa L. by high performance liquid chromatography coupled with electrochemical detection. J Pharm Anal, 2014, 4(5): 325-330.
14 杨东风,梁宗锁.中药指纹图谱研究进展.中国药房, 2007, 18(6):467-470.
15 宋坤,毛颐晴.指纹图谱在中药复方研究中的应用.时珍国医国药, 2002, 13(11): 699-700.
16 王睿,徐伟,方翼.中药指纹图谱研究进展.中国药师, 2004, 7(10): 764-767.
17 黄晟,谷莉,黄河舟,等.中药色谱指纹图谱研究进展.药学实践杂志, 2003, 21(6): 326-329.
18 秦昆明,方前波,蔡宝昌.指纹图谱技术在方剂现代研究中的应用现状.世界科学技术-中医药现代化, 2009, 11(2): 287-293.
Fingerprint and Two-component Quantitative Determination of Yi-Kang Tablet
Zhang Haitao1,2, Xu Zhenqiu1,2, Fu Juan1,2, Wang Zhenzhong1,2, Xiao Wei1,2
(1. Jiangsu Kanion Pharmaceutical Co. Ltd., Lianyungang 222001, China; 2. State Key Laboratory of Pharmaceutical Process New-tech for Chinese Medicine, Lianyungang 222001, China)
This study was aimed to establish a HPLC fingerprint and quantitative determination on two components of Yi-Kang (YK) tablet in order to provide evidences for its evaluation. The Kromasil C18column (4.6 mm× 250 mm, 5 μm) was used with a mobile phase of methanol-water gradient elution. The flow rate was 1.0 mL ·min-1. The column temperature was 30℃. And the detection wavelength was 250 nm. The results showed that the degree of separation and reappearance of YK tablet fingerprint was relatively good. There were 19 mutual peaks. The similarity among different batches was more than 0.96. Compared with the controls, two components, which were puerarin and curcumin, were identified. The quantitative analysis was given on these two components. It was concluded that the experiment simultaneously analyzed the fingerprint and two components. This method was rapid, simple and accurate, which can be used as one of the effective methods in the comprehensive quality evaluation of this preparation.
Yi-Kang tablet, fingerprint, puerarin, curcumin, HPLC
10.11842/wst.2016.01.017
R284.1
A
(责任编辑:刘馨雨 张志华,责任译审:王 晶)
2015-06-24
修回日期:2015-10-13
* 科学技术部国家重大新药创制项目(2013ZX09402203):现代中药创新集群与数字制药技术平台,负责人:王振中。
** 通讯作者:萧伟,本刊编委,研究员级高级工程师,博士,主要研究方向:中药新药的研究与开发。

