酰胺类氮氧自由基的合成及辐射防护性能研究
田 敏,张 改
(西安工业大学 材料与化工学院,西安 710021)
酰胺类氮氧自由基的合成及辐射防护性能研究
田 敏,张 改
(西安工业大学 材料与化工学院,西安 710021)
针对氮氧自由基类化合物清除体内有害自由基,有效防护辐射损伤,文中将4-醛基苯甲酸酰氯化,与手性试剂S-1-甲基苯乙胺缩合、最后与双羟胺缩合、氧化,合成了一种酰胺类手性氮氧自由基S-1,经EA、IR和MS确证产物结构.选择健康雄性昆明鼠作为研究对象,以阳性对照药WR2721为参比测定了化合物抗辐射性能.研究结果表明:中间体S-11合成的最佳反应条件为室温搅拌8 h后回流2 h,S-1-甲基苯乙胺:4-醛基苯甲酰氯最佳配比为1∶2;目标产物S-1合成的最佳反应条件为回流24 h,NaIO4作为氧化剂;抗辐射性能结果显示在6.0 Gyγ、6.5 Gyγ和7.0 Gyγ三种不同辐照剂量新型酰胺类氮氧自由基S-1的抗辐射作用均优于阳性对照药WR2721.
4-醛基苯甲酸;酰胺类氮氧自由基;抗辐射;化学合成
氮氧自由基是一类包含氮氧自旋单电子的稳定有机化合物.作为研究对象,它曾活跃在生物学[1]、磁学[2]和光学[3]等领域,比如作为自旋示踪剂用于描述细胞膜结构及其功能[4].近年来,它再次引起科学家的关注,是由于其在抗辐射领域药物的贡献[5].
氮氧自由基抗辐射的原因在于从根本上消除了产生辐射致伤的关键因子—高密度的有害自由基[6],它可以通过模拟体内超氧化物歧化酶(Superoxide Dismutase,SOD)的作用[7]、防止脂质体过氧化作用[8]和阻止活性HO·自由基的生成[9]这三种途径降低过氧化物引发的有害自由基对机体的损伤,使自由基和有害自由基之间再结合,从而抑制了芬顿效应的产生,对辐射损伤进行防护[10].
基于氮氧自由基的抗辐射作用,本文拟合成一种酰胺类自由基S-1,并研究了三个不同浓度的新型氮氧自由基在三种不同辐照剂量下在小鼠体内的抗辐射作用效果,为研发新型的抗辐射药物提供实验依据.
1 实验材料与方法
1.1 试剂和仪器
核磁数据所有产品均选择以DCCl3为溶剂,TMS为内标,由Bruker AV-300 NMR spectrometer (400 MHz)型核磁共振仪测定;红外数据由BRUKER TENSOR27型红外光谱仪测定;所有固体试剂熔点采用XRC-1型数字显微熔点仪(温度计未校正)测定;元素分析数据由Perkin-Elemer 240型元素分析仪测定;质谱数据由Varian 7.0T ESI-FTICR-MS型质谱仪测定;选择用V(氯仿):V(石油醚)=1∶1的混合溶剂为展开剂,Alugramsilica gel/uv 254薄层板,薄层色谱法(Thin-Layer Chromatography,TLC)法监测反应进程;柱分离用粒径为∅0.074~0.049 mm硅胶.双羟胺自制,醛酸等试剂纯度均为化学纯.
1.2 实验过程
图1列出S-1的合成过程.
1.2.1 中间体S-10的制备
在250 mL的单口瓶中 加入4-醛基苯甲酸6.00 g(30 mmol),随后加入新蒸的80 mL的SOCl2,搅拌待溶解后,室温再搅拌0.5 h,然后逐渐升温至回流,薄层板监测反应,反应完毕后,多余SOCl2溶剂被减压蒸除,得到淡褐色液体,称重5.33 g,产率为79%.
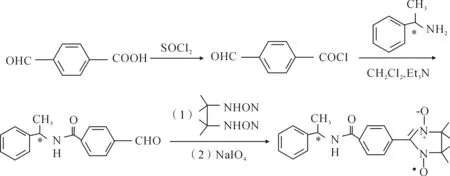
图1 S-1的合成路线
1.2.2中间体S-11的制备
3.60 g(30 mmol)S-1-甲基苯乙胺加入到250 mL的三颈瓶中,加入150 mL处理过的四氢呋喃,搅拌溶解,再加入6.4 mL三乙胺,冰浴下滴加溶有5.06 g(30 mmol)4-醛基苯甲酰氯(上述1.2.1制得)的100 mL THF溶液.滴加完毕后,室温下搅拌8 h继续回流2 h.用(3×50 mL)乙酸乙酯萃取,(2×50 mL)饱和碳酸氢钠依次洗涤.合并有机相,用无水MgSO4干燥、旋蒸溶剂后得白色针状固体,用乙醚重结晶,得产物6.23 g.
1.2.3 自由基S-1的制备
将上述1.2.2产物2.79 g(11.04 mmol)置于100 mL单口瓶中,加入2,3-二羟胺-2,3-二甲基丁烷1.62 g(11.04 mmol),70 mL 甲醇,搅拌溶解,回流反应24 h,蒸除溶剂,在残渣中加入100 mL CH2Cl2,冰浴搅拌0.5h,滴加溶有NaIO42.13 g(10.05 m·mol-1)的50 mL水溶液,冰浴搅拌2h,反应结束后静置分层,收集有机相,并用无水Na2SO4干燥,过柱子分离得纯品2.19 g.
1.3 酰胺类自由基的抗辐射效果研究
选用雄性健康昆明小鼠作为研究对象,随机将其按每组20只分为四组:照射对照组、正常对照组、受试药物组阳性和药物对照组.照射对照组照前一次给予0.5~1.0 mL的生理盐水.受试药物分成3种剂量给药,照射前30 min给药组小鼠一次性腹腔或灌胃给药,每组给药体积0.5~1.0 mL(5%二甲基亚砜溶解),照射对照组、受试药物组阳性和药物对照组动物接受一次性全身性照射.以十天为一个阶段,每天观察在记录表上记录受辐照小鼠的状况、死亡时间和死亡数,记录三阶段.从而研究受试药物对急性放射病小鼠存活率的抗辐射作用影响.
2 结果与讨论
2.1 化合物的表征结果
S-11为白色晶体,产率为87.5%.选用CH2Cl2为溶剂,浓度为1.1 g·cm-3,计算出比旋光度[a]D20=+67.2; 产物1H NMR以CDCl3为溶剂测出化学位移δ9.90单峰为 -CHO上的氢,δ8.43双峰为苯环上的氢,δ8.28单峰为苯环上的氢,δ8.12双峰为苯环上的氢;δ8.08双峰为苯环上的氢;δ7.45-7.18多重峰为苯环上的峰;δ4.24双峰为次甲基上的氢;δ1.36双峰为次甲基上的氢;IR以KBr压片:3 400 cm-1为仲酰胺N-H伸缩振动峰,2 880 cm-1和2 828 cm-1为醛基C-H伸缩振动峰,1 788 cm-1为醛基C=O伸缩振动峰,1 623 cm-1为酰胺Ⅰ带C=O伸缩振动峰,1 533 cm-1为酰胺Ⅱ带N-H面外震动和C-H伸缩振动偶合峰,1 351 cm-1为酰胺Ⅲ带N-H面外震动和C-H伸缩振动偶合峰,855 cm-1苯环上两个邻接氢的=CH面外变形震动峰,700 cm-1苯环上五个邻接氢的=CH面外变形震动峰; 元素分析(C16H15NO2)显示C(75.84%)、H(5.96%)和N(5.51%),与计算值C(75.86%)、H(5.97%)和N(5.53%)相符.
S-1为蓝色晶体,产率52%.MS显示分子离子峰m/z为380.92[M+H]+; IR以KBr压片:1 625 cm-1为酰胺Ⅰ带C=O伸缩振动峰,1 566 cm-1为酰胺Ⅱ带N-H面外震动和C-H伸缩振动偶合峰,1 339 cm-1为酰胺Ⅲ带N-H面外震动和C-H伸缩振动偶合峰,853 cm-1苯环上两个邻接氢的=CH面外变形震动峰,698 cm-1苯环上五个
邻接氢的=CH面外变形震动峰; 元素分析(C22H26N3O3):C(69.11%)、H(7.36%)、 N(11.01%),与计算值C(69.09%)、 H(7.38%)、N(10.99%)相符.
2.2 中间体S-11合成的影响因素分析
2.2.1 时间对产物反应产率的影响
实验发现,在合成过程中,反应时间对产物中间体S-11产率的影响非常明显,回流使得反应速率得到很大提升,但回流时间不需要太长,时间过长反应速率增加不明显.由表1可知,室温搅拌8 h后回流2 h的产率最高,即为S-11合成的最佳反应时间.
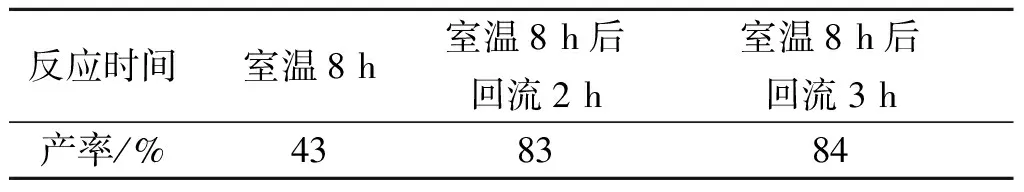
表1 反应时间对产率的影响
2.2.2 反应物配比对反应的影响
实验发现不同的反应配比对产物影响很大,考察了反应物S-1-甲基苯乙胺与4-醛基苯甲酰氯不同配比对产物产率的影响.如图2所示.
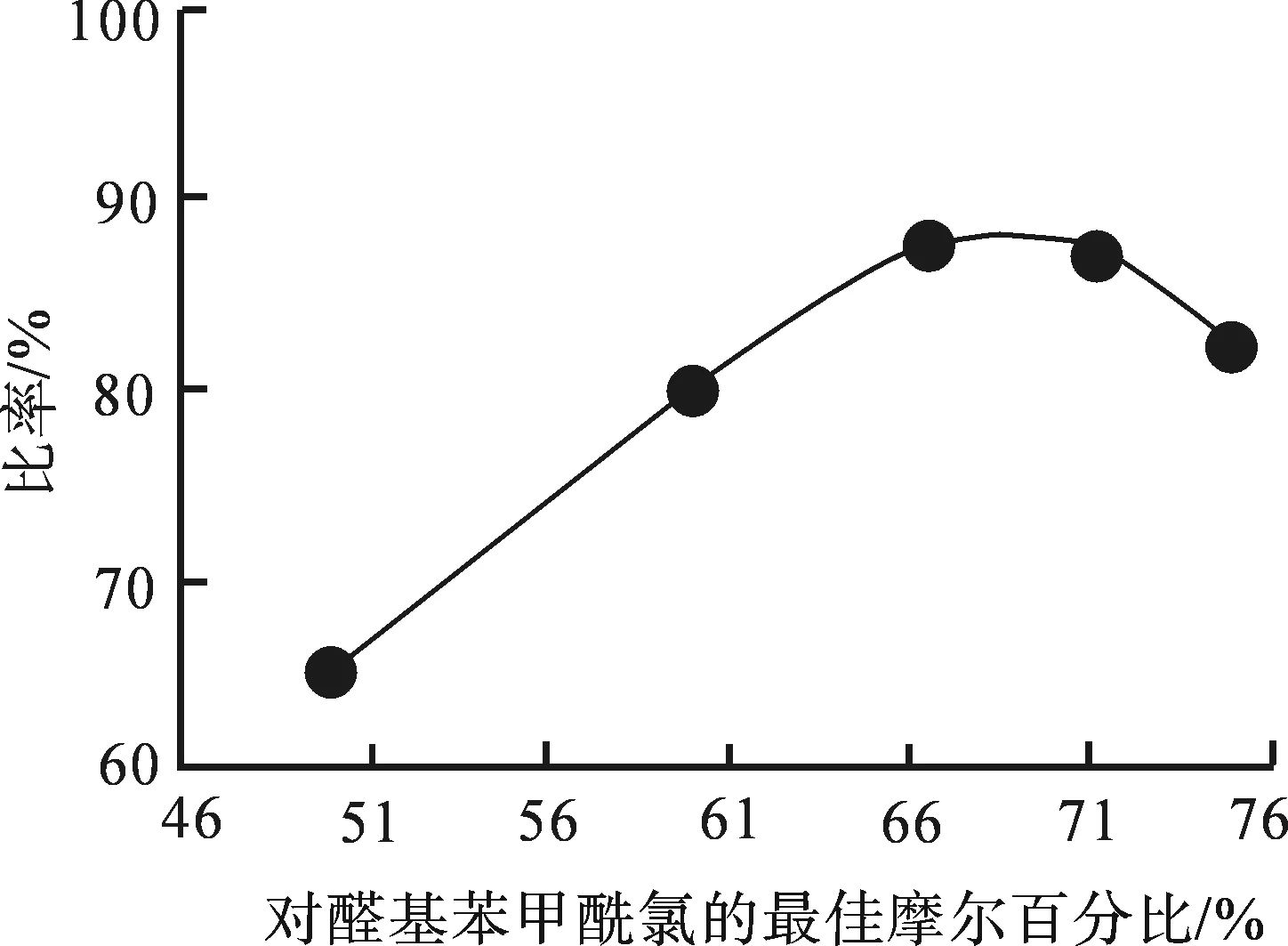
图2 反应配比对产率的影响
由图2可知,当比值低于1∶2时,因原料浓度过低,反应缓慢,随着4-4-醛基苯甲酰氯的用量的增大, S-11的产率增大幅度较大.当4-醛基苯甲酰氯的摩尔百分比等于66.7%,即S-1-甲基苯乙胺∶4-醛基苯甲酰氯等于1∶2时产率达到最大.当配比超过1∶2之后在薄层板上二取代产物点明显增加,产率增加不明显,由图2可知,4-醛基苯甲酰氯的最佳摩尔百分比为66.7%,即S-1-甲基苯乙胺∶4-醛基苯甲酰氯为1∶2,配比最佳.
2.3 目标产物S-1合成的影响因素分析
2.3.1 时间对产率的影响
实验发现反应时间对产物S-1产率影响很大,以甲醇做溶剂回流反应6 h后反应瓶中有白色沉淀的产生,24 h后白色沉淀不再增加,可知最佳反应时间为24 h.
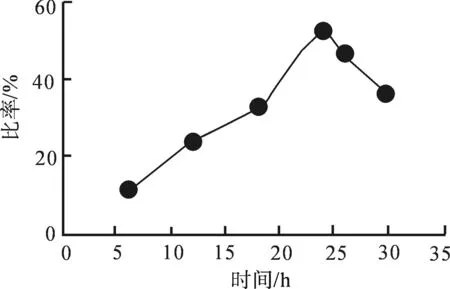
图3 反应时间对S-1产率的影响
2.3.2 氧化体系对产率的影响
二羟基咪唑的氧化文献中通常选用的氧化剂是PhO2和NaIO4.二氧化铅体系氧化剂用量较大、反应时间相对较长,反应过程因二氧化铅本身为褐色而难以观察反应进程,薄层板监测反应,产物点浓度很低,副产物较多,后处理麻烦.而NaIO4作为氧化剂时,通过控制反应温度和监测反应进程,可以较高产率得到目标产物.
2.4 目标化合物抗辐射活性
将生理盐水组、受试药物组(三个浓度剂量0.1 mmol·kg-1、0.25 mmol·kg-1、0.5 mmol·kg-1)阳性对照药(0.5 mmol·kg-1)接受6.0 Gyγ射线照射见表2.由表2可知随着各个阶段天数的增加,未受药物保护的正常小鼠由于受到辐射损伤,小鼠的存活率逐渐减少,因辐射剂量较小,服用阳性对照药的小鼠和服用三种不同浓度的受试药物基本均未受到辐射损伤,结果显示出S-1的初步药效.表3中辐射剂量提升至6.5 Gy,受γ射线照射的小鼠存活率受到影响,均有不同程度明显的下降,而接受S-1药物的小鼠降低幅度明显比阳性对照药WR2721降低的幅度小,显示出了优于阳性药物的抗辐射作用效果.为了观察受试药的进一步药效,我们把剂量提升至7.0 Gy(见表4)时,小鼠存活率减少幅度都增大,S-1降低幅度仍然小于WR2721阳性对照药.以上结果显示S-1的抗辐射作用比阳性对照药WR2721作用更好.

表2 在6.0 Gyγ射线下不同浓度的S-1对雄性昆明小鼠生存率影响
注:每组20只小鼠,#是指与正常组比较,P<0.05,*是指与生理盐水组比较,P<0.05.
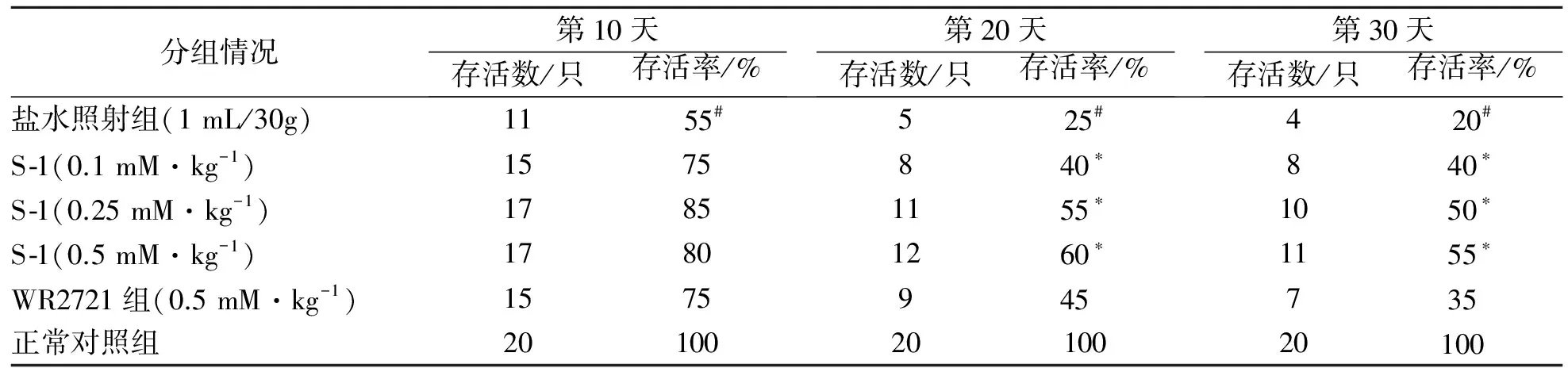
表3 在6.5 Gyγ射线下不同浓度的S-1对雄性昆明小鼠生存率影响
注:每组20只小鼠,#是指与正常组比较,P<0.05,*是指与生理盐水组比较,P<0.05.

表4 在7.0 Gyγ射线下不同浓度的S-1对雄性昆明小鼠生存率影响
注:每组20只小鼠,#是指与正常组比较,P<0.05,*是指与生理盐水组比较,P<0.05.
3 结 论
1) 通过四步合成了一种酰胺类氮氧自由基S-1,并通过IR,1HNMR,质谱等对其结构进行表征.每组选择20只健康雄性昆明鼠做为研究对象,与阳性对照药物WR2721进行了比较,在6.0 Gyγ、6.5Gyγ和7.0 Gyγ三个不同辐射强度下对其存活率进行了研究.
2)通过分析中间体S-11合成时间对产率的影响,得到最佳反应时间室温搅拌8 h后回流2 h.通过分析中间体S-11合成中S-1-甲基苯乙胺和4-醛基苯甲酰氯不同配比对产率的影响,得到最佳配比S-1-甲基苯乙胺:4-醛基苯甲酰氯为1∶2.
3) 通过分析目标产物S-1合成时间对产率的影响,得到最佳反应时间24 h.通过分析目标产物S-1合成中不同氧化剂对产率的影响,选择NaIO4作为氧化剂.
4) 综合三组生物体外活性实验,结果显示:S-1有较好的抗辐射作用,比阳性对照药WR2721抗辐射作用好,可以作为新型的抗辐射药物来研究.
[1] LIKHTENSHTEIN G I,YAMAUCHI J,NAKATSUJI S,et al.Nitroxides:Applications in Chemistry,Biomedicine,and Materials Science[J].Wiley-VCH Verlag GmbH & Co.KGaA,2008(2): 438.
[2] WANG L Y,WANG X Q,JIANG K,et al.Syntheses,Crystal Structures and Magnetic Properties of a New Nitronyl Nitroxide NIT2-Bithph and its Manganese(II) Compound[Mn(hfac)2(IMHBithph)]2·(NIT2-bithph) (C6H14)[J].Journal of Molecular Structure,2007,840(1/3):14.
[3] WANG H M,ZHANG D Q,GUO X F,et al.Tuning the Fluorescence of 1-imino Nitroxide Pyrene with Two Chemical Inputs:Mimicking the Performance of an “AND” Gate[J].Chemical Communications,2004(6):670.
[4] HARBOUR J R,BOLTON J R.Superoxide Formation in Spinach Chloroplasts:Electron Spin Resonance Detection by Spin Trapping[J].Biochemical and Biophysical Research Communications,1975,64(3):803.
[5] WANG H B,JIA Y J,GAO P,et al.Synthesis,Radioprotective Activity and Pharmacokinetics Characteristic of a New Stable Nitronyl Nitroxyl Radical-NIT2011[J].Biochimie,2013,95(8):1574.
[6] RAYMOND Z,CHRISTOPHE S,HENRIKE H,et al.Previous Article Next Article Table of Contents Strong Exchange Interactions Between Two Radicals Attached to Nonaromatic Spacers Deduced from Magnetic,EPR,NMR,and Electron Density Measurements[J].Journal of the American Chemical Society,2004,126(39) :12604.
[7] ROBERT A F,RICHARD D K,CHULHEE C,et al.Nitrones as Therapeutics[J].Free Radical Biology & Medicine,2008,45(10):1361.
[8] DAMIANI E,CASTAGNA R,GRECI L.The Effects of Derivatives of the Nitroxide Tempol on UVA-mediated in Vitro Lipid and Protein Oxidation[J].Free Radical Biology & Medicine,2002,33(1):128.
[9] SOULE B P,HYODO F,MATSUMOTO K,et al.The Chemistry and Biology of Nitroxide Compounds[J].Free Radical Biology & Medicine,2007,42(11):1632.
[10] KOCHERGINSKY N,SWARTZ H M.Nitroxide Spin Labels:Reactions in Biology and Chemistry[J].CRC Press,1995,32:1143.
(责任编辑、校对 潘秋岑)
Synthesis of a New Amide Nitroxide and Its Radioprotective Effect
TIANMin,ZHANGGai
(School of Materials and Chemical Engineering,Xi’an Technological University,Xi’an 710021,China)
Based on scavenging harmful free radicals in vivo of nitrogen oxygen free radicals,a new amide free radical was synthesized by the acetylation of the aldehyde acid and the condensation of S-1-phenylethylamine and double hydroxylamine.The product was characterized by the techniques of EA,IR and MS.The optimum conditions for synthetic reaction are as follows.For intermediates S-11,the optimum condition is stirring at room temperature for 8hs and refluxing for 2hs,with the mass ratio of S-1-methyl phenethylamine to 4 aldehyde benzoyl chloride being 1∶2.For S-1,the optimum condition is stirring and refluxing for 24 hs ,with NaIO4as an oxidant.The effect of the radiation protection in vivo was studied through the experiment on healthy male Kunming mice.The result shows that the anti-radiation activity of the new amide free radical is better than that of WR2721.
the aldehyde acid;chiral nitroxides;anti-radiation activity;chemical synthesis
10.16185/j.jxatu.edu.cn.2016.11.001
2016-05-19 基金资助:国家自然科学青年基金(21501139 ),西安工业大学材料与化工学院科研项目培育基金
田 敏(1978-),女,西安工业大学讲师,主要研究方向为有机化合物的合成及性能研究.E-mail:tiannminn@163.com.
O626.23
A
1673-9965(2016)11-0861-05

