HIV/AIDS患者一线治疗失败的发生率及相关因素分析
种雪静,戴国瑞,汪 笛,徐 玲,郝 禹,赵红心
HIV/AIDS患者一线治疗失败的发生率及相关因素分析
种雪静,戴国瑞,汪 笛,徐 玲,郝 禹,赵红心
目的研究HIV/AIDS患者一线治疗失败的发生率并分析其危险因素,从而对预警治疗失败的发生和提高抗病毒治疗的效果提供依据。方法以2005—2015年在北京地坛医院接受免费抗病毒治疗且发生一线治疗失败的HIV/AIDS患者为研究对象,回顾性分析患者的基本信息、基线特征以及一线治疗失败的发生率,并通过logistic回归分析治疗失败的相关危险因素。结果一线治疗失败率为3.39%。血液传播(OR=3.713)、基线CD4+T淋巴细胞<200个/μl(OR=2.167)、病毒载量(viral load, VL)≥5log copies/ml(OR=2.137)、合并机会性感染(opportunistic infectiion, OI)(OR=3.476)是发生一线治疗失败的危险因素。一线治疗失败与性别、年龄、基线是否合并HBV/HCV感染以及从确诊到治疗的间隔长短无关。结论一线治疗失败的发生与血液传播、低基线CD4+T淋巴细胞计数、基线OI和高基线VL有关。今后应该对具有危险因素的患者给予充分重视,必要时优化治疗方案,注意药物间相互作用。
艾滋病;高效抗逆转录病毒治疗;一线治疗失败;影响因素
自国家免费抗病毒项目(National Free Antiretroviral Treatment Program, NFATP)开展以来,HIV/AIDS患者的病死率明显下降[1-2]。有报道显示,我国约20.8% HIV/AIDS患者经过高效抗逆转录病毒治疗(highly active antiretroviral therapy, HAART)后发生治疗失败[3],而更换二线药物的患者有36%会再次发生治疗失败,且其死亡风险增加[4-5],因此保证一线方案的成功是使患者维持治疗和长期存活的关键。本文以2005—2015年在北京地坛医院接受免费抗病毒治疗的患者为研究对象,回顾性分析一线治疗失败患者的基本信息和基线特征,并评估影响因素,从而预警治疗失败的发生,减少二线方案的更换,为提高抗病毒治疗的效果提供依据。
1 对象与方法
1.1 对象 2005年1月—2015年11月在本院启动抗病毒治疗的3835例HIV/AIDS患者,其中130例发生治疗失败(治疗失败组),3705例取得持续病毒抑制(持续病毒抑制组)。纳入标准:①根据《中华医学会修订的AIDS诊疗指南(第三版)》进行AIDS的诊断和治疗,且经北京市疾病控制中心确诊抗HIV阳性。②于本院启动抗病毒治疗。排除标准:①失访、死亡以及转出前未发生治疗失败。②转入患者。治疗失败的诊断标准:一线治疗6个月以上,病毒载量(viral load, VL)持续≥1000 copies/ml,或者基因型检测存在耐药。
1.2 方法 采集患者人口学特征、CD4+T淋巴细胞、VL、合并HBV/HCV感染、机会性感染(opportunistic infectiion, OI)发生情况以及传播途径等基线资料,并进行回顾性研究,对比分析治疗失败组与持续病毒抑制组的临床资料的差异,探讨患者发生一线治疗失败的相关因素。
1.3 统计学处理 采用SPSS 22.0进行统计分析。计量资料用中位数并四分位数[Q2(Q1, Q3)]描述;计数资料用频数和构成比进行描述。通过二分类logistic回归分析HIV/AIDS患者发生一线治疗失败的相关危险因素。P<0.05表示差异有统计学意义。
2 结 果
2.1 基本信息与基线特征 2005年1月—2015年11月,在地坛医院进行抗病毒治疗的3835例HIV/AIDS患者中,一线治疗失败患者有130例(其中死亡前发生治疗失败的1例,失访前发生治疗失败的2例,转出前发生治疗失败的3例),累积失败率为3.39%。130例患者发生一线治疗失败的时间中位数为12.5(7.3,122.2)个月。基线CD4+T淋巴细胞计数为105(22,242)个/μl,VL为5.08(4.75,5.51)log copies/ml。
2.2 一线治疗失败因素分析
2.2.1 单因素分析 治疗失败组血液传播、基线CD4+T淋巴细胞<200个/μl、VL≥5log copies/ml、基线合并OI的比例高于持续病毒抑制组(P<0.05)。见表1。
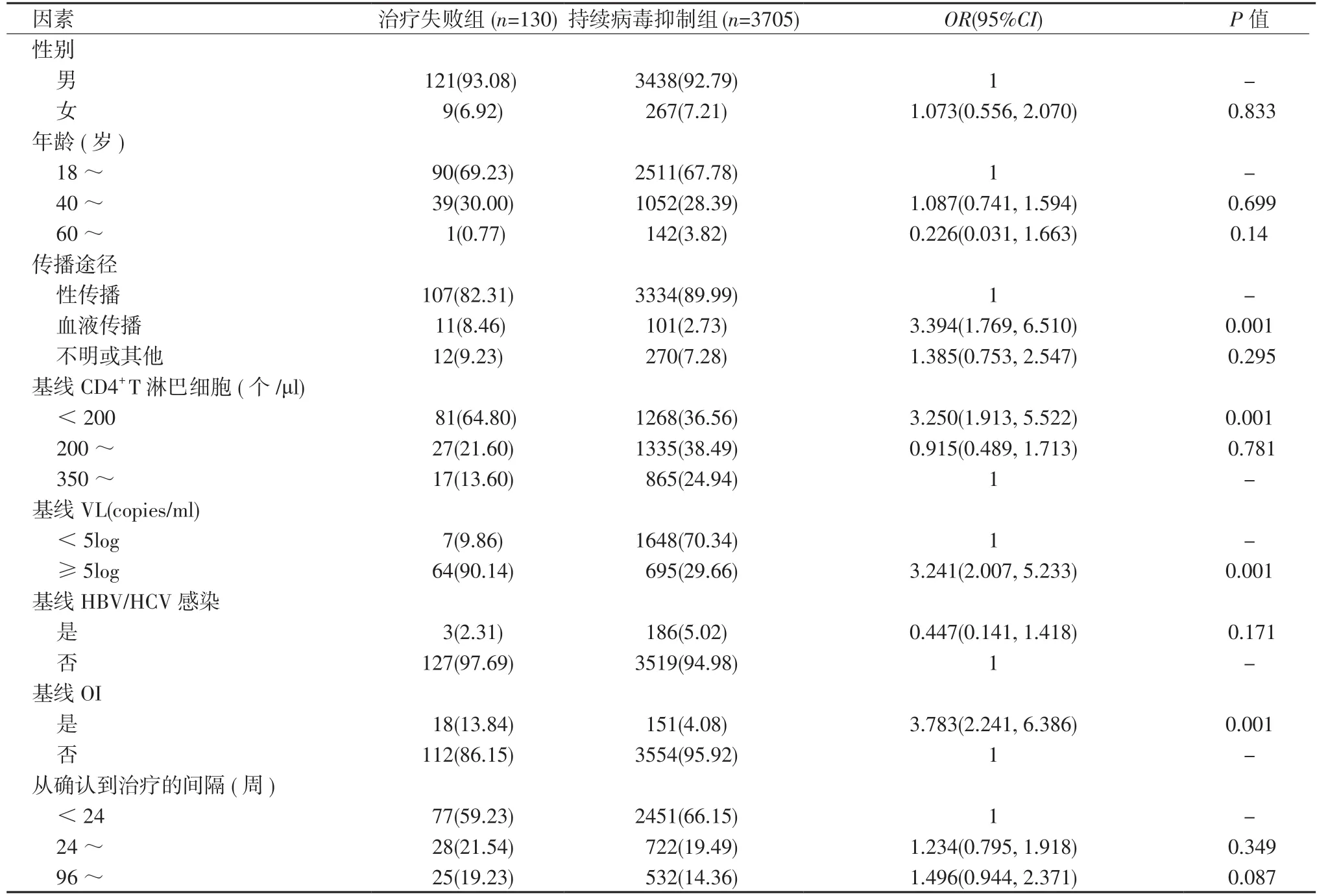
表1 HIV/AIDS患者一线治疗失败的单因素分析[例(%)]Table 1 Univariate analysis of first-line treatment failure among HIV/AIDS patients[cases(%)]
2.2.2 多因素分析 患者一线治疗失败的可能因素赋值情况见表2。采用二分类logistic回归分析强迫法将所有因变量都引入回归方程,得出血液传播(P=0.012)、基线CD4+T淋巴细胞<200个/μl(P=0.029)、VL≥5log copies/ml、OI是发生一线治疗失败的危险因素。其他因素不变的情况下,血液传播的患者一线治疗失败的发生率是其他传播途径患者的3.713倍,低基线CD4+T淋巴细胞组一线治疗失败的发生率是高基线CD4+T淋巴细胞组的2.167倍,高基线VL组一线治疗失败的发生率是低基线VL患者的2.137倍,基线合并OI组一线治疗失败的发生率是无OI组的3.476倍。见表3。
3 讨 论
HAART的广泛应用显著降低了HIV/AIDS患者的病死率[1-2],同时减少了HIV在人群中的传播[6]。但HAART是一个长期的过程,抗病毒药物潜在的药物毒性及耐药都可能增加治疗失败的风险。随着NFATP的开展和治疗时机的不断更新,接受抗病毒治疗的患者逐渐增多,出现治疗失败的患者也越来越多[7]。目前我国抗病毒治疗药物选择十分有限,一旦发生治疗失败,可更换代替的药物很少,了解一线治疗失败的发生率和评估治疗失败的影响因素就显得尤为重要。

表2 HIV/AIDS 患者一线治疗失败的相关因素与赋值Table 2 Related factors and assignment of first-line treatment failure among HIV/AIDS patients

表3 HIV/AIDS患者一线治疗失败的多因素分析Table 3 Multivariate regression analysis of first-line treatment failure among HIV/AIDS patients
中国疾病预防控制中心曾报道我国一线治疗失败发生率为20.80%[3],接受HAART治疗6~11个月、 12~23个月以及超过24个月的治疗失败发生率分别为10.00%、14.00%、18.00%[8]。地坛医院诊治HIV/AIDS患者一线治疗失败率仅3.39%,明显低于全国发生率,可能与及时的实验室指标监测和强化的依从性训练有关。即便如此,也应该对治疗失败的影响因素进行分析,将失败的风险降到最低。
很多因素可以导致HIV/AIDS患者的抗病毒治疗失败。既往研究认为,地域因素,临床工作者的医疗水平,患者是否漏服药物,HAART方案和持续时间都是治疗失败的影响因素[8]。美国卫生与人类服务部最新修订的青年和成人HIV-1抗病毒指南指出:高基线VL,低基线CD4+T淋巴细胞水平,伴随疾病,HIV耐药株的存在,依从性差,药物毒副反应,药代动力学不良,药物效能下降以及药物负担等都可以导致治疗失败[9]。目前依从性并没有一个严格的判断标准,往往通过患者自我报告、问卷调查等方式来评价[5,10]。因此,本研究主要从患者自身因素和疾病状态方面,探讨影响一线治疗失败的因素。国外研究并没有传播途径影响病毒学应答的相关报道,但多因素分析提示血液传播是HIV/AIDS患者发生治疗失败的一个危险因素,这与我国疾病预防控制中心之前的报道相符[11]。“四免一关怀”政策实施早期,非法采供血活动造成了HIV在中国部分地区农村卖血人群中的流行。2007年以前,血液传播是我国HIV/ AIDS患者的主要传播方式[12]。这部分患者起始治疗较早,HAART持续时间长。有研究报道,治疗时间每增加1年,出现依从性欠佳的风险为原来的1.43倍[13]。既往报道认为,基线CD4+T淋巴细胞水平和VL会影响病毒学应答[14-15],而我们的研究也证实基线低CD4+T淋巴细胞水平、高VL的患者更容易发生治疗失败。绝大多数OI发生在CD4+T淋巴细胞<200 个/μl的患者,同时CD4+T淋巴细胞<200 个/μl也是患者服用复方新诺明预防肺孢子菌肺炎的指征[16-18],加重的服药负担会影响患者依从性[19]。同时,服用的抗逆转录病毒药物(antiretroviral, ARV)和复方新诺明均有一定的毒副作用。国外的一项报道指出,患者无法耐受的毒副反应会使其生活质量和依从性下降,进而发生耐药和治疗失败[20]。基线合并OI也会受到高药物负荷和毒副反应的影响。此外,不同OI的治疗药物对AVR的影响不同,例如,利福平可以使依非韦伦的血药浓度下降25%,与利福布丁合用时奈韦拉平血药浓度降低16%等[21]。多种药物负荷、合并严重的OI、药物间相互作用和毒副反应,都会影响到患者的依从性。而随着HIV/AIDS患者依从性下降,耐药风险加大,治疗失败发生率显著提高[22]。还有研究表明,相比起始治疗时低VL的患者,高VL的患者治疗后不容易取得病毒学抑制,且容易出现病毒反弹的情况[23-24]。高基线VL的患者的病毒株存在多样性,可能包含更多的耐药株,且在药物选择压力下更容易变异产生耐药株,国外研究报道基线VL≥105copies/ml的患者耐药发生率较基线VL<105copies/ml的患者高[25]。针对这部分患者,应选用广谱强效抗病毒药物,否则容易发生治疗失败。因此,美国卫生与人类服务部将高基线VL水平列为治疗失败的诱因,并指出阿巴卡韦和利匹韦林禁用于基线VL≥105copies/ml的患者[9]。
综上,血液传播、基线CD4+T淋巴细胞<200个/μl、合并OI、VL≥5log copies/ml是一线治疗失败的危险因素。一线抗病毒治疗失败人群中有相当大比例是依从性差造成的,本研究因采用回顾性研究,无法根据自我评价、问卷调查等评估患者的依从性,故没有具体分析,且对患者的分析仅选取地坛医院就诊的患者会造成一定的选择偏倚。即便如此,本研究仍具有一定的参考价值。临床工作者应对HIV/AIDS患者基线情况给予充分重视,尤其是具有危险因素的患者,必要时优化治疗方案,注意药物间相互作用。
[1]Huang P, Tan J, Ma W, et al. Long-term effectiveness of antiretroviral therapy in China: an observational cohort study from 2003-2014[J]. Int J Environ Res Public Health, 2015, 12(8):8762-8772.
[2]Zhang F, Dou Z, Ma Y, et al. Five-year outcomes of the China National Free Antiretroviral Treatment Program[J]. Ann Intern Med, 2009, 151(4):241-251, W-52.
[3] Leng X, Liang S, Ma Y, et al. HIV virological failure and drug resistance among injecting drug users receiving first-line ART in China[J]. BMJ Open, 2014, 4(10):e005886.
[4]Jespersen S, Honge BL, Medina C, et al. Lack of awareness of treatment failure among HIV-1-infected patients in Guinea-Bissau - a retrospective cohort study[J]. J Int AIDS Soc, 2015, 18(1):20243.
[5]Ochieng W, Kitawi RC, Nzomo TJ, et al. Implementation and operational research: correlates of adherence and treatment failure among kenyan patients on long-term highly active antiretroviral therapy[J]. J Acquir Immune Defic Syndr, 2015, 69(2):e49-e56.
[6]Jia Z, Mao Y, Zhang F, et al. Antiretroviral therapy to prevent HIV transmission in serodiscordant couples in China (2003-11): a national observational cohort study[J]. Lancet, 2013, 382(9899): 1195-1203.
[7]Zhang M, Shang M, Yang W, et al. Treatment effect and drugresistant mutations in Chinese AIDS patients switching to secondline antiretroviral therapy[J]. PLoS One, 2014, 9(10):e110259.
[8]Ma Y, Zhao D, Yu L, et al. Predictors of virologic failure in HIV-1-infected adults receiving first-line antiretroviral therapy in 8 provinces in China[J]. Clin Infect Dis, 2010, 50(2):264-271.
[9]Department of Health and Human Services. Guidelines for the use of antiretroviral agents in HIV-1-infected adults and adolescents[R]. Ochieng: Department of Health and Human Services, 2015.
[10]Mghamba FW, Minzi OM, Massawe A, et al. Adherence to antiretroviral therapy among HIV infected children measured by caretaker report, medication return, and drug level in Dar Es Salaam, Tanzania[J/OL]. BMC Pediatr, 2013, 13:95[2016-10-10]. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3691638. DOI: 10.1186/1471-2431-13-95.
[11]Hui X, Yuhua R, Jingyun L, et al. HIV drug resistance and its impact on antiretroviral therapy in Chinese HIV-infected patients[J]. PLoS One, 2013, 8(2):e54917.
[12]郝阳,崔岩,孙新华,等. “四免一关怀”政策实施十年来中国艾滋病疫情变化及特征分析[J]. 中华疾病控制杂志,2014,18(5):369-374.
[13]Jordan MR, Obeng-Aduasare Y, Sheehan H, et al. Correlates of non-adherence to antiretroviral therapy in a cohort of HIV-positive drug users receiving antiretroviral therapy in Hanoi[J]. Int J STD AIDS, 2014 , 25(9):662-668.
[14]WHO. Antiretroviral therapy for HIV infection in adults and adolescents[R]. Geneva: World Health Organization, 2010.
[15]Mellors JW, Muñoz A, Giorgi JV, et al. Plasma viral load and CD4+lymphocytes as prognostic markers of HIV-1 infection[J]. Ann Intern Med, 1997, 126(12):946-954.
[16]Masur H, Brooks JT, Benson CA, et al. Prevention and treatment of opportunistic infections in HIV-infected adults and adolescents: updated guidelines from the centers for disease control and prevention, national institutes of health, and HIV medicine association of the infectious diseases society of america[J]. Clin Infect Dis, 2014, 58(9):1308-1311.
[17]WHO. Consolidated guidelines on the use of antiretroviral drugs for treating and preventing HIV infection: recommendations for a public health approach[R]. Geneva: Switzerland WHO, 2013.
[18]张钰,田云飞,肖江,等.有效的高效抗反转录病毒治疗后低CD4/CD8比值HIV/AIDS患者免疫学特征分析[J]. 传染病信息,2015,28(6):357-361.
[19]Juday T, Gupta S, Grimm K, et al. factors associated with complete adherence to HIV combination antiretroviral therapy[J]. Hiv Clinical Trials, 2011, 12(2):71-78.
[20]Sivadasan A, Abraham OC, Rupali P, et al. High rates of regimen change due to drug toxicity among a cohort of South Indian adults with HIV infection initiated on generic, first-line antiretroviral treatment[J]. J Assoc Physicians India, 2009, 57:384-388.
[21]《国家免费艾滋病抗病毒药物治疗手册》编写组. 国家免费艾滋病抗病毒药物治疗手册[M]. 北京,人民卫生出版社,2007,12:61-64.
[22] Ekstrand ML, Shet A, Chandy S, et al. Suboptimal adherence associated with virological failure and resistance mutations to firstline highly active antiretroviral therapy (HAART) in Bangalore India[J]. Int Health, 2011, 3(1):27-34.
[23]Ledergerber B, Egger M, Opravil M, et al. Clinical progression and virological failure on highly active antiretroviral therapy in HIV-1 patients: a prospective cohort study. Swiss HIV Cohort Study[J]. Lancet, 1999, 353(9156):863-868.
[24]Mocroft A, Miller V, Chiesi A, et al. Virological failure among patients on HAART from across Europe: results from the EuroSIDA study[J]. Antivir Ther, 2000, 5(2):107-112.
[25]TenoRes Study Group. Global epidemiology of drug resistance after failure of WHO recommended first-line regimens for adult HIV-1 infection: a multicentre retrospective cohort study[J]. Lancet Infect Dis, 2016, 16(5):565-575.
(2016-11-10收稿 2016-11-25修回)
(责任编委 王永怡 本文编辑 胡 玫)
Analysis on incidence and risk factors of first-line treatment failure among HIV/AIDS patients
CHONG Xue-jing, DAI Guo-rui, WANG Di, XU Ling, HAO Yu, ZHAO Hong-Xin*
Peking University Ditan Teaching Hospital, Beijing 100015, China
ObjectiveTo analyze the incidence and risk factors of first-line treatment failure among HIV/AIDS patients who received first-line highly active antiretroviral treatment (HAART). The outcomes of the study aim to provide early warnings to treatment failure and improve the HIV treatment efficacy.MethodsThe evaluation of basic demographic information, baseline characteristics, incidence, and risk factors of treatment failure was conducted retrospectively in HIV/AIDS patients who received free first-line HAART in Beijing Ditan Hospital from 2005 to 2015.ResultsOverall incidence of first-line was 3.39% in our cohort. Blood transmission (OR=3.713), baseline CD4 counts<200 cells/μl(OR=2.167), baseline VL≥5log copies/ml(OR=2.137), combined with the opportunistic infections(OR=3.476) were risk factors of first regimen failure. Treatment failure was not associated with gender, age, baseline HBV/ HCV co-infection and the interval from the confirmation to initial treatment.ConclusionsFirst-line failure was associated with blood transmission, lower baseline CD4 counts, baseline opportunistic infection and higher baseline VL. Adequate attention involving better treatment regimen options and notice of drug interaction is needed to ensure optimal treatment outcomes among HIV/AIDS patients, especially ones with these risk factors.
HIV/AIDS; HAART; first regimen failure; risk factors
R512.91
A
1007-8134(2016)06-0340-05
10.3969/j.issn.1007-8134.2016.06.006
国家自然科学基金(81371804);2014年首都卫生发展科研专项项目(2014-2-2173) ;感染病科国家临床重点专科建设项目
100015,北京大学地坛医院教学医院(种雪静、汪笛、赵红心);首都医科大学附属北京地坛医院感染一科 北京市中西医结合感染性疾病研究所(种雪静、戴国瑞、汪笛、徐玲、郝禹、赵红心)
赵红心,E-mail: 13911022130@163.com
*Corresponding author, E-mail: 13911022130@163.com

