同时测定银黄胶囊中绿原酸、木犀草苷和黄芩苷的含量
徐 玫,张忠泉,王璟奕
(1.河南大学 药学院 河南 开封 475004;2.河南大学 教育科学学院,河南 开封475004)
同时测定银黄胶囊中绿原酸、木犀草苷和黄芩苷的含量
徐玫1,张忠泉1,王璟奕2
(1.河南大学 药学院 河南 开封 475004;2.河南大学 教育科学学院,河南 开封475004)
摘要:目的建立同时测定银黄胶囊中绿原酸、木犀草苷和黄芩苷含量的方法。方法HPLC等度洗脱法。C18色谱柱;流动相为甲醇∶水∶磷酸(53∶47∶0.1);流速1.0 mL/min;检测波长328 nm;柱温30℃。结果绿原酸在2.200~44.00 μg/mL范围内(r2=0.999 9)、木犀草苷在0.080~22.00 μg/mL范围内(r2=0.999 5)、黄芩苷在24.20~242.0 μg/mL范围内(r2=0.999 2)线性关系均良好;其平均回收率分别为99.6%、99.3%和99.7%。结论该方法操作简便,成本低,工作效率高,可作为银黄胶囊质量的控制方法。
关键词:HPLC法;银黄胶囊;绿原酸;木犀草苷;黄芩苷;同时测定
中图分类号:R927.2
文献标识码:识码: A
文章编号:章编号: 1672-7606(2015)01-0029-03
收稿日期:2014-10-1
基金项目:河南大学大学生创新性实验计划项目(10NB028)。
作者简介:徐玫(1968-),女,河南开封人,副教授,从事药物质量控制工作。
Abstract:ObjectiveTo establish a method for determination of chlorogenic acid, galuteolin and baicalin in Yinhuang Capsule. MethodsHPLC method Isocratic elution. column:C18column; mobile phase: methanol-water-phosphoric acid (53∶47∶0.1); flow rate:1.0 mL/min; detection wavelength:328 nm; column temperature:30 ℃. ResultsChlorogenic acid in within the range of 2.200~44.00 μg/mL peak area as well linear relationship (r2=0.9999), the average recovery was 99.6%; galuteolin in within the range of 0.080~22.00 μg/mL peak area as well linear relationship (r2=0.9995), the average recovery was 99.3%; baicalin in within the range of 24.20~242.0 μg/mL peak area as well linear relationship (r2=0.9992), the average recovery was 99.7%. Conclusion The method is simple and increases efficiency, can be used as a method of the determination of silver yellow capsule.
Simultaneous determination chlorogenic acid, galuteolin and baicalin of Yinhuang Capsule
XU Mei1, ZHANG Zhongquan1, WANG Jingyi2
(1.HenanUniversityCollegeofPharmacyDepartment,Kaifeng,Henan475004,China; 2.HenanUniversityCollegeofEducationScience,Kaifeng,Henan475004,China)
Key words: HPLC method; Yinhuang Capsule; chlorogenic acid; galuteolin; baicalin; simultaneous determination
银黄制剂主要是由金银花和黄芩药材经提取精致而成,金银花其活性成分主要为有机酸类(绿原酸、异绿原酸等)、黄酮类(木犀草苷等);黄芩中的主要成分为黄芩苷。该类制剂具有清热解毒、消炎等功效,应用于临床多达十几种剂型[1]。但现行版的《中国药典》收载的剂型只有银黄口服液和银黄颗粒冲剂,均采用反相高效液相色谱法对其中的有效成分黄芩苷和绿原酸分别进行测定[2]。目前国内文献[3-8]报道的对银黄制剂分别测定及同时测定的目标性物质,也均是绿原酸和黄芩苷两种有效成分。为更有效地控制银黄制剂的质量,提高工作效率、降低成本,对金银花中另一主要活性成分木犀草苷[9-11]同时进行测定很有必要。
1仪器、试剂与试药
1.1 仪器
LC2010A高效液相色谱仪、二极管阵列检测器(日本岛津公司); AS3120超声仪(奥特赛恩斯仪器有限公司);BP211D电子天平(Sartorius公司)。
1.2 药品和试剂
银黄胶囊(通化久铭药业有限公司,批号:090801、090802、090803);黄芩苷对照品(批号:110715-200914)和绿原酸对照品(批号:110753-200913),木犀草苷对照品(批号:1117202200604)(中国药品生物制品检定所);甲醇(色谱纯,天津赛孚世纪科技发展有限公司);磷酸(分析纯,济南金恒益化工有限公司);乐百氏饮用纯净水(乐百氏(广东)食品饮料有限公司)。
2方法与结果
2.1 色谱条件
色谱柱:C18柱(5 μm 250 mm×4.6 μm);流动相为甲醇∶水∶磷酸(53∶47∶0.1);柱温:30 ℃;检测波长:328 nm;流速:1.0 mL/min;进样量20 μL。
2.2 对照品溶液的制备
精密称取绿原酸对照品0.220 0 mg、木犀草苷对照品0.110 0 mg和黄芩苷对照品1.210 0 mg,分置3个5 mL棕色量瓶中;各加体积分数60%甲醇适量,超声溶解并稀释至刻度,摇匀,即得44.00 μg/mL绿原酸对照液、22.00 μg/mL木犀草苷对照液及242.0 μg/mL黄芩苷对照液,在上述色谱条件下分别进样20 μL测定,混合对照品色谱图见图1。
2.3 供试品溶液的制备
取同批次银黄胶囊20粒,去除囊壳,称取内容物5份,每份约0.1 g,精密称定,置50 mL棕色量瓶中,加体积分数60%的甲醇溶剂约40 mL,超声提取50 min,加体积分数60%的甲醇溶剂至刻度,摇匀,过滤。精密量取1 mL滤液至25 mL棕色量瓶中,加体积分数60%的甲醇溶剂至刻度,摇匀,0.45 μm微孔滤膜滤过,即得,供试品色谱图见图2。
2.4 线性关系的考察
分别精密量取黄芩苷对照液、绿原酸对照液和木犀草苷对照液各适量,分别加体积分数60%的甲醇溶剂稀释制成不同梯度浓度的溶液。按上述色谱条件,分别精密吸取各系列对照液20 μL进样,以质量浓度(x,μg/mL)为横坐标,峰面积(y)为纵坐标进行线性回归,黄芩苷回归方程:y=34.728x-158.73,r2=0.999 2;绿原酸回归方程:y=51.161x+0.785 6,r2=0.999 9;木犀草苷回归方程:y=2 537.98x+269.08,r2=0.999 5。
2.5 精密度实验
精密吸取同一黄芩苷、绿原酸和木犀草苷对照品混合溶液20 μL,在上述色谱条件下连续进样6次,测得三者峰面积的RSD分别为1.7%、1.8%和2.0%。
2.6 稳定性实验
精密量取供试品溶液20 μL,依上述色谱条件分别于0,2,4,8,16,24 h进样,黄芩苷、绿原酸和木犀草苷峰面积的RSD分别为1.9%、1.7%和2.3%,表明供试品在24 h内稳定性良好。
2.7 回收率实验
精密称取同批次样品9份(约半粒内容物的量)于10 mL棕色量瓶中;按以下要求分别加入依“2.2”法制备的黄芩苷、绿原酸和木犀草苷对照液。在1~3号样品中加入3.0 mL对照液;4~6号样品中加入4.0 mL对照液;7~9号样品中加入5.0 mL对照液。加体积分数60%甲醇溶剂适量,超声提取50 min,定容,过滤,按上述色谱条件依次进样测定,计算出回收率,结果见表1。
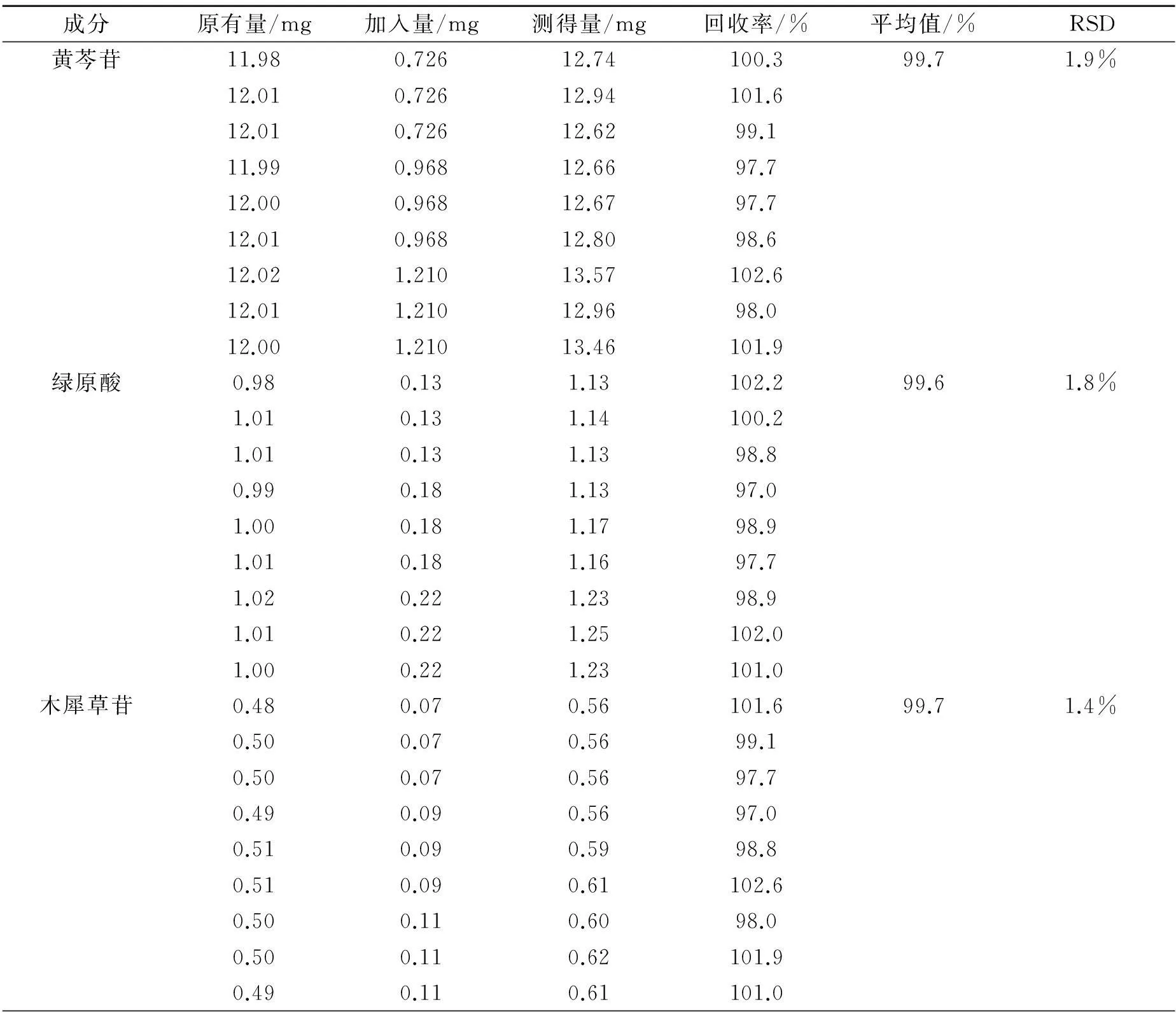
表1 黄芩苷、绿原酸和木犀草苷的回收率实验(n=9)
2.8 样品含量测定
分别取3批次银黄胶囊,按“2.3”法制备供试品溶液,分别进样测定,按回归方程计算,每批次平行测定3次,结果见表2。
3讨论
用二极管阵列检测器对绿原酸、木犀草苷和黄芩苷的对照品色谱峰进行紫外扫描:绿原酸次强吸收分别在218 nm和318 nm,最强吸收在328 nm;黄芩苷次强吸收在328 nm,最强吸收在278 nm;木犀草苷最强吸收在220 nm,但此处溶剂峰会产生干扰,次强吸收分别在255 nm和350 nm处。由于银黄胶囊中木犀草苷的含量低于绿原酸且两者含量均远远低于黄芩苷,若以最低含量的木犀草苷的次强吸收255 nm和350 nm为检测波长,绿原酸、黄芩苷的吸收均较弱(吸收处于峰谷或峰末尾处);而在绿原酸的最强吸收328 nm处,黄芩苷有次强吸收,木犀草苷也有较强吸收。因此,为减小测量误差,以三者吸收均较强的328 nm作为检测波长。
参考文献:
[1] 江苏新医学院.中药大辞典下册[S].上海:上海科学技术出版社,1986:2 017.
[2] 中华人民共和国药典委员会.中华人民共和国药典2010版(一部)[M].北京:化学工业出版社,2010:1 084.
[3] 郑敏霞,诸葛周,戴德雄,等.HPLC法测定银黄滴丸中绿原酸和黄芩苷[J].中草药,2011,42(6):1 138-1 140.
[4] 秦三海,刘华钢.复方银黄微型灌肠剂家兔体内药代动力学研究[J].中国中药杂志,2006,31(1):54-56.
[5] 李新圃.高效液相色谱在银黄制剂分析研究中的应用[J].兰州大学学报:医学版2007,33(1):55-59.
[6] 陈雄泉,李来生,杨汉荣,等.HPLC法同时测定银黄制剂中绿原酸和黄芩苷的含量[J].药物分析杂志,2007,27(1):52-55.
[7] 刘永利,李冬梅,冯丽,等. RP-HPLC法同时测定银黄胶囊中绿原酸和黄芩苷的含量[J].中成药,2006,28(8):1 142-1 144.
[8] 张婷,美尔哈巴·热西提,林潇,等.HPLC-MS/MS法测定银黄颗粒中绿原酸和黄芩苷[J].中草药,2012,43(4):711-713.
[9] 时军波,徐娜,刘长安,等.金银花不同部位中绿原酸和木犀草苷含量的测定[J].化学分析计量,2010,19(6):45-47.
[10] 王珂,王艳艳,赵东宝,等.HPLC法测定金银花不同部位中木犀草苷素及其苷的含量[J].河南大学学报:自然科学版,2011,41(1):39-43.
[11] 张元元,李进,陈涛,等.高效液相色谱法同时测定金银花中绿原酸和木犀草苷的含量[J].天津中医药大学学报,2011,30(2):107-109.
[责任编辑李武营]

