纳米级二氧化锡的清洁制备
马敬环,赵宝军,吴绍斌,刘 莹,康雪婧,胡道友
(1.天津工业大学环境与化学工程学院,天津300387;2.天津滨瀚环保科技发展有限公司,天津300451)
纳米级二氧化锡的清洁制备
马敬环1,2,赵宝军1,吴绍斌1,刘 莹1,2,康雪婧1,胡道友1
(1.天津工业大学环境与化学工程学院,天津300387;2.天津滨瀚环保科技发展有限公司,天津300451)
以结晶氯化锡为原料,采用水热法制备纳米级二氧化锡,过程中不添加沉降剂和分散剂,避免在晶体洗涤过程中产生酸液及有机废液,实现了纳米二氧化锡的清洁制备.采用X射线衍射仪(XRD)、热重分析仪、傅里叶红外光谱(FT-IR)、粒度分析仪、扫描电子显微镜(SEM)对制备的纳米级二氧化锡进行晶体结构及性能表征.结果表明:所制备纳米二氧化锡具有良好的结晶性、热稳定性和较高的相纯度;粒径分布均匀,粒径范围在40~60 nm之间.
纳米级二氧化锡;清洁制备;晶体结构
纳米二氧化锡具有独特的光学、电学性能、表面特性和吸附特性,其在化工催化、气体传感器、涂料、压敏材料、电池电极材料以及有机废水处理等众多领域都具有广泛的应用[1].但其性能对颗粒尺寸有较强的依赖性,要得到性能优异的二氧化锡纳米材料,就必须制备出粒径小、粒度分布均匀、分散性好的二氧化锡纳米粉体[2].纳米二氧化锡材料的研究非常活跃,在过去20年中,纳米结构的二氧化锡成为最受关注的氧化物纳米材料[3].
现阶段制备二氧化锡的方法有很多,如水热法[4]、机械化学法[5]、溶胶凝胶法[6]、化学沉淀法[7]、电沉积法[8]等.其中水热法工艺和设备简单,易于控制,无需高温灼烧处理,且产物结晶和分散良好,已成为当今纳米材料重要的制备方法.目前,在水热法制备过程中大都通过添加强酸或碱液作为沉降剂以方便进一步沉降分离,这就使得在沉淀洗涤的过程中造成了大量废酸液和有机废液,不仅难以回收处理,而且不当的排放会造成水体污染.鉴于此,本文亦采用该法制备纳米级二氧化锡,但不同以往的是在制备过程中不添加硝酸[9]等作为沉降剂,也不加入正丁醇[4]等有机试剂作为分散剂,仅以结晶四氯化锡为原料,采用适当的水热处理条件制备粒径适当、粒度分布均匀的二氧化锡纳米粉体,并研究了不同的水热温度对二氧化锡粒子粒径和晶型的影响及该法所制备的粉体的热稳定性.
1 实验部分
1.1 实验药品及仪器
所用药品包括:五水结晶四氯化锡,分析纯,350.6 g/mol,天津市科密欧化学试剂有限公司产品;硝酸银,分析纯,169.87 g/mol,天津市赢大稀贵化学试剂厂产品.
所用仪器包括:FA2004N型精密电子天平,上海箐海仪器有限公司产品;TD5A-WS型高速离心机,湘仪仪器有限公司产品;WO-5L型智能数显恒温油水浴锅,天津科诺仪器设备有限公司产品;KSW-6-12型马弗炉,北京市永光明医疗仪器厂产品;NICOLET 6700 FT-IR型傅里叶红外光谱仪,TA Thermo-fisher公司产品;S-4800型场发射扫描电子显微镜,日本日立仪器有限公司产品;Zetasizer nano ZS90型纳米粒径电位分析仪,英国马尔文仪器有限公司产品;Dmax2500型X射线衍射仪,日本理学公司产品;SDT Q600型热重(TG)分析仪,美国TA公司产品.
1.2 纳米级粒子的制备
(1)回流:称取17.53 g五水结晶四氯化锡溶于1 000 mL去离子水中,室温下磁力搅拌30 min使其充分溶解.然后将该水溶液在95℃条件下搅拌回流2 h,待溶液自然降温至室温后离心分离得到沉淀,采用去离子水洗涤沉淀直至洗涤液中不能检测出氯离子(硝酸银滴定法).最后通过冷冻干燥机冷冻干燥24 h获得干燥粉末.
(2)水热处理:将所得粉体分为3份,其中1份作为对比样品即不进行水热处理(HTT);另外2份分别取部分样品置入各自反应釜中,然后加入适量去离子水,将2份样品分别在100℃和150℃下水热处理24 h.
(3)焙烧:将未经水热处理和经100℃、150℃水热处理的样品分别置于马弗炉中,分别进行400℃和600℃高温焙烧,持续5 h,以验证本文区别于传统水热法所制备的二氧化锡粉体的热稳定性.
1.3 性能表征
采用X射线衍射仪(XRD)表征粉体的晶体结构;采用热重分析仪(TG)对所制备粉体的热稳定性进行测定;采用傅里叶红外光谱仪(FT-IR)对其进行相纯度表征;采用纳米粒径电位分析仪测定粉体的粒径及其分布范围;采用场发射扫描电子显微镜(SEM)确定其表面形貌.
2 结果与讨论
2.1 粒子物象及晶型表征
图1所示为制得粉体的X射线衍射(XRD)谱图.
由图1可以看出,在2θ分别为26.6°(110晶面)、33.9°(101晶面)、51.8°(211晶面)出现了衍射峰,在水热处理温度大于100℃时在38°(200晶面)附近出现了另一个峰,经400和600℃焙烧后在62°(310晶面)以及65°(112晶面、301晶面)附近出现衍射峰,这些峰的峰位与JCPDS标准衍射图(卡片号:41-1445)吻合,说明本试验所制备的粉体为四方晶系金红石型二氧化锡.
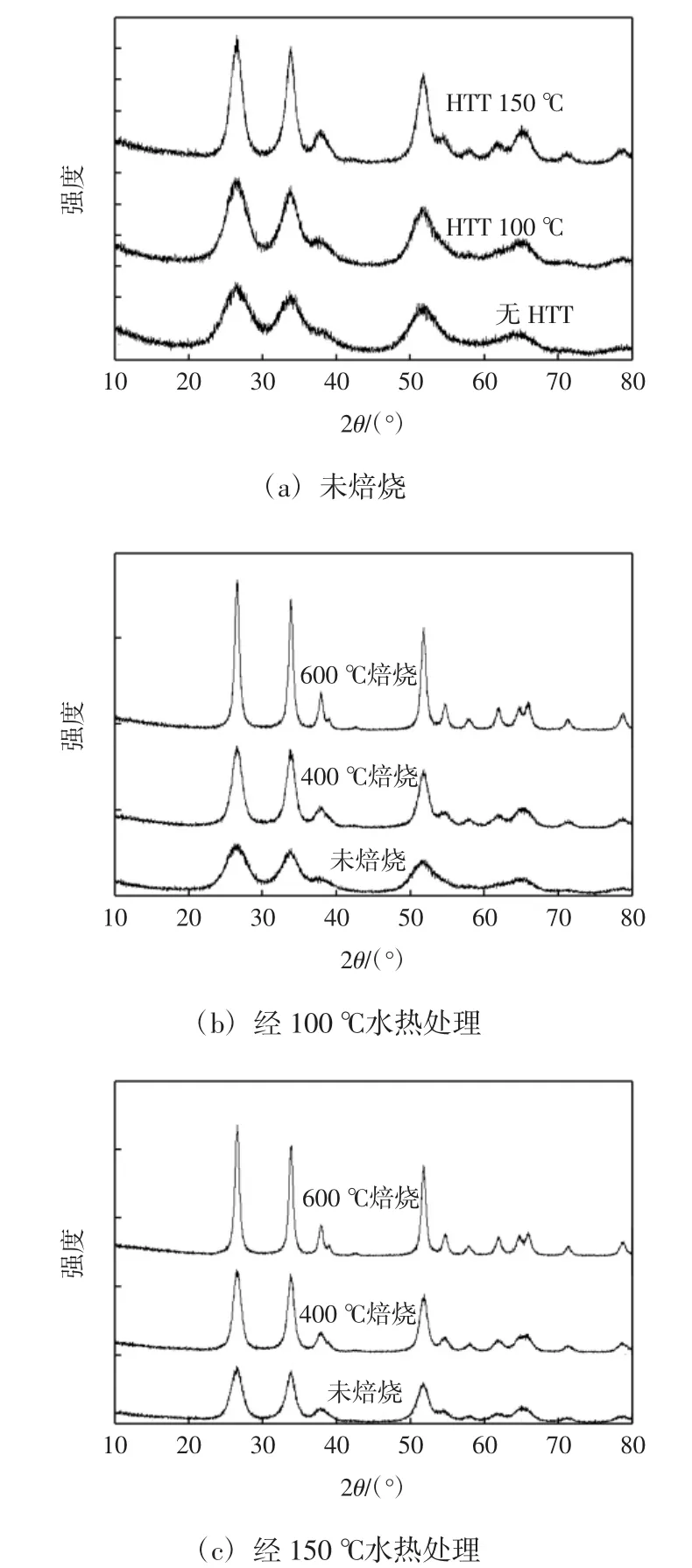
图1 二氧化锡粒子XRD谱图Fig.1 XRD patterns of SnO2particles
由图1(a)可以看出,随着水热温度的增加衍射峰逐渐趋于尖窄,表明粒子逐渐长大,结晶性越来越好.随着温度的升高,粒子内部发生接触重结晶,由无定型向结晶型的转变更为充分[10].
由图1(b)和(c)可以看出:在100℃或150℃水热处理后,与未经高温焙烧的粒子的谱图相比,经400℃或600℃焙烧后粒子的衍射峰位置并没有发生变化,而且衍射峰更加尖窄.表明通过100℃和150℃水热处理所制得的二氧化锡粒子具有较好的热稳定性,且随着焙烧温度的升高粒子的结晶性越好.这可以解释为水热处理使得纳米二氧化锡微晶中不规则排布的原子或离子趋于规则化、均一化,从而使得所制备的粒子具有较好的热稳定性.而经400℃或600℃焙烧后在60°至70°之间又出现了晶面310、112及301[11-12],这是由于高温焙烧的情况下晶粒出现生长,其生长方式有表面扩散和晶界位移,而在600℃后出现衍射峰裂分亦是由于高温焙烧使得晶胞发生收缩或膨胀,从而晶面间距发生变化所致[13].
2.2 粉体热稳定性表征
图2所示为在100℃和150℃情况下,水热法所制备二氧化锡的热重曲线图.

图2 水热法制备的二氧化锡纳米粒子的热重(TG)曲线Fig.2 TG plots of hydrothermally treated SnO2particles
由图2可知,在100℃附近出现失重峰,这是由于样品中物理吸附水的脱除引起的,对于100℃或者150℃水热法所制得的二氧化锡纳米粒子在这一点上基本一致.图中失重过程一直持续到约450℃,这是由于样品的结合水在这一过程中缓慢脱除,此后曲线趋于平滑[14].相较于图2(a),图2(b)中失重曲线稍早达到了恒重,这可能是由于采用150℃作为水热温度时粒子的结晶化程度较高,从而使得样品中含有较少的结合水所致.
2.3 粉体相纯度的表征
图3所示为水热法所制备的二氧化锡样品以及在400℃和600℃焙烧时的傅里叶红外光谱图.
由图3可知,位于3 430和1 630 cm-1处的吸收谱带是由二氧化锡表面水所引起的;位于2 350 cm-1处的峰是空气中少量CO2的吸收峰;而在850至1 350 cm-1之间出现的弱峰是二氧化锡表面不同类型的羟基造成的;在600 cm-1处的强峰则是Sn-O-Sn的对称和非对称振动引起的.
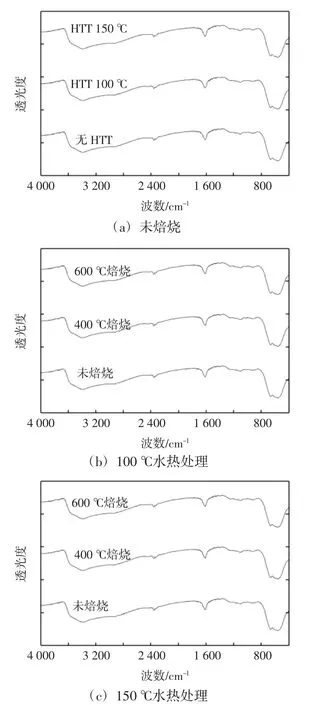
图3 二氧化锡粒子红外光谱谱图Fig.3 FT-IR spectra of SnO2particles
图3(a)为未进行水热处理(HTT)、经100℃和150℃水热处理(HTT)24 h样品的傅里叶红外光谱图,可以看出,3份样品各吸收峰位置高度一致,由此可知,回流及水热处理过程中并未引入其他杂质,试验制得的二氧化锡粉体相纯度高.图3(b)为经100℃水热处理后未经焙烧和分别在400℃和600℃焙烧.图3(c)为经150℃水热处理后未经焙烧和分别在400℃和600℃焙烧,可以看出水热法制备所得的二氧化锡粒子在400℃和600℃焙烧后依然保持较高的相纯度.
2.4 纳米级粒子的粒径及其分布
图4所示为100℃水热法制得的二氧化锡粒子的粒径分布图.
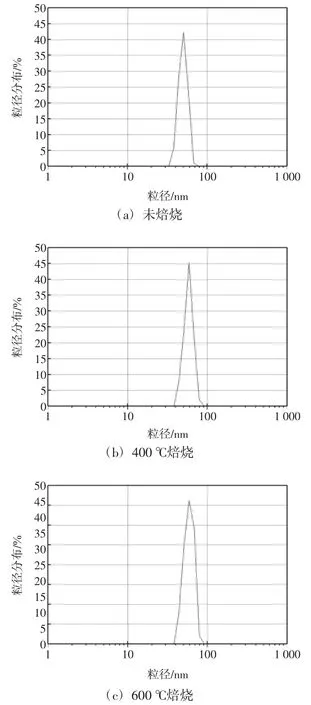
图4 100℃水热处理所制备二氧化锡粒子的粒径分布图Fig.4 Size distribution of SnO2particles hydrothermally treated at 100℃
由图4可以看出,100℃水热处理条件下所制得的二氧化锡粒子其粒径基本处于40~60 nm之间,经过400℃和600℃焙烧后其粒径范围基本位于50~70 nm之间.这是由于高温焙烧使得粒子出现了生长,这一结果正好与图1所示XRD谱图结果相吻合,但从图中发现其粒径增长幅度较小.
图5所示为150℃水热法制得的二氧化锡粒子的粒径分布图.
由图5可以看出,在150℃水热处理条件下所制得的二氧化锡粒子其粒径也基本处于40~60 nm之间,经过400℃和600℃焙烧后其粒径范围基本位于50~70 nm之间,可以判断采用100℃和150℃水热处理所制备的纳米级二氧化锡粒子其粒径基本一致,而且高温煅烧对其粒子粒径的影响并不明显.
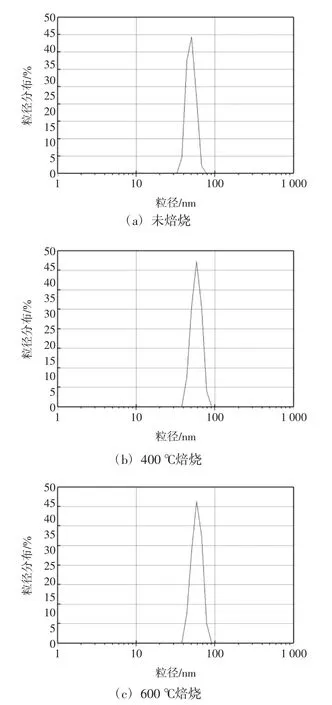
图5 150℃水热处理所制备二氧化锡粒子的粒径分布图Fig.5 Size distribution of SnO2particles hydrothermally treated at 150℃
2.5 粒子的微观形貌表征
图6所示为经100℃水热处理后二氧化锡粒子的扫描电镜图.
由图6可以看出,在水热温度为100℃时所制备的二氧化锡粒子粒径均位于40~60 nm之间,且粒子粒径分布较为均匀;随着焙烧温度的增加,粒子逐渐长大,结晶性越来越好,但是粒径增长幅度并不大.
图7所示为经150℃水热处理后二氧化锡粒子的扫描电镜图.
综合图6与图7可以看出,水热法所制备的二氧化锡粒子粒径均位于40~60 nm之间,且粒子粒径分布较为均匀,但是仔细观察还是能发现后者中粒子的表观粒径稍大于前者中粒子的粒径,这一结果与图1XRD谱图相契合;随着水热处理温度由100℃增至150℃衍射峰变尖窄,粒子在这一过程中出现生长,从而导致粒子粒径有少许增加.而图7(b)和图7(c)亦再次验证了图5中所示粒径分布图的结果.

图6 100℃水热处理所制备二氧化锡粒子的扫描电镜图Fig.6 SEM images of SnO2particles hydrothermally treated at 100℃

图7 150℃水热处理所制备二氧化锡粒子的扫描电镜图Fig.7 SEM images of SnO2particles hydrothermally treated at 150℃
3 结论
区别于传统水热法,在制备过程中不加入任何沉降剂(硝酸或氨水等)和有机试剂,避免了在结晶洗涤过程中产生难以回收处理的酸液和有机废液,实现了纳米级二氧化锡的清洁制备.实验结果表明:
(1)所制备的纳米级二氧化锡粉体粒径位于40~60 nm之间,粒度适中且分布均匀.
(2)在100℃或者150℃水热处理温度下,制得的纳米级二氧化锡粉体具有较好的热稳定性.在400℃和600℃条件下焙烧5 h,均对粒子的粒径和形貌无较大影响,仅是粒子出现少许生长.
(3)水热处理温度从100℃增加至150℃,使得粒子具有更好的结晶性,粒子有少许生长,但均具有较好的热稳定性.
[1]周存,郑帼,程博闻.掺锑氧化锡纳米粉体的表面改性[J].天津工业大学学报,2008,27(4):34-38.
[2]庞承新,张丽霞,谭健,等.溶胶-凝胶法制备纳米二氧化锡的研究[J].广西师范学院学报:自然科学版,2006,23(3):26-29,40.
[3]韩卫清,周刚,王连军,等.阳极氧化制备二氧化锡纳米孔[J].无机材料学报,2007,22(3):395-399.
[4]杨幼平,张平民,张永龙,等.水热法制备超细均匀二氧化锡粉体[J].铜业工程,2004(4):23-25.
[5]敖伟琴,李均钦,杨华明.机械化学法合成二氧化锡纳米晶[J].深圳大学学报:理工版,2007,24(1):24-28.
[6]王迪,田均庆,张书涛,等.溶胶凝胶法制备二氧化锡纳米晶体[J].哈尔滨商业大学学报:自然科学版,2014,30(2):224-228.
[7]张晓顺,邱竹贤,翟秀静,等.超声波-化学沉淀法制备纳米二氧化锡[J].东北大学学报,2005,26(4):265-267.
[8]李超,魏伟,方少明,等.SnO2的电沉积法制备及电化学性能[J].郑州轻工业学院学报:自然科学版,2008,23(5):1-4,20.
[9]刘冬,施哲,朱云.凝胶水热法制备纳米二氧化锡[J].云南冶金,2003,32(1):26-29.
[10]张义华,张景新,王学勤,等.二氧化锡纳米粒子的制备及表征[J].大连理工大学学报,2000,40(1):64-66.
[11]于桂霞,祝洪良,姚奎鸿.二氧化锡(SnO2)纳米颗粒的水热合成及表征[J].浙江理工大学学报,2006,23(2):166-168.
[12]BILLIK P,CAPLOVICOVA M.Synthesis of nanocrystalline SnO2powder from SnCl4by mechanochemical processing[J]. Powder Technology,2009,191(3):235-239.
[13]CHETRI Pawan,CHOUDHURY Amarjyoti.Investigation of optical properties of SnO2nanoparticles[J].Physica E,2013(47):257-263.
[14]KRISHNAKUMAR T,JAYAPRAKASH R.Microwave-assisted synthesis and investigation of SnO2nanoparticles[J].Materials Letters,2009,63(11):896-898.
Pollution free preparation of SnO2nanoparticles
MA Jing-huan1,2,ZHAO Bao-jun1,WU Shao-bin1,LIU Ying1,2,KANG Xue-jing1,HU Dao-you1
(1.School of Environmental and Chemical Engineering,Tianjin Polytechnic University,Tianjin 300387,China;2.BIN HAN Eco-Technologies Co Ltd,Tianjin 300451,China)
Tin oxide nanoparticles were made from Stannic chloride pentahydrate by applying pollution free methods,in which precipitant and dispersant were not added firstly in comparing with the traditional routes for avoiding wastewater includes acid and organic substance which were hard to be reused during cleaning of the crystal.The crystal structure and characters of tin oxide nanoparticles were identified by X-ray diffraction(XRD)analysis,Thermal Gravity Analysis,Fourier transform infrared(FT-IR)spectroscopy,size instrument Zetasizer nano and scanning electronic microscope(SEM).The results show that the tin oxide nanoparticles have good crystallization,excellent thermal stability,high phase purity and uniform size distribution which is between 40-60 nm.
tin oxide nanoparticles;pollution free preparation;crystal structure
TQ134.3.2
A
1671-024X(2015)06-0041-05
10.3969/j.issn.1671-024x.2015.06.009
2015-09-25基金项目:天津市科技计划项目(14ZCZDSF00013);国家自然科学基金资助项目(51308390)
马敬环(1964—),女,博士,教授,博士生导师,主要研究方向为海水淡化与水资源综合利用.E-mail:13920893096@163.com

