HPLC–ICP–MS法测定地表水体中砷的形态*
杨正标,陆喜红,任兰,杨丽莉
(南京市环境监测中心站,南京 210013)
砷是一种自然界中广泛存在的元素,目前砷污染已成为严重的环境问题之一。不同形态砷其生物毒性差异很大,亚砷酸根[As(Ⅲ)]和砷酸根[As(Ⅴ)]等无机砷的毒性较大,而一甲基砷(MMA)、二甲基砷(DMA)和砷甜菜碱(AsB)等有机砷毒性较小。因此仅仅测定砷总量已经不能充分反映砷的环境健康效应,砷形态分析对于研究各种砷形态的迁移转化及其毒性毒理具有重要意义[1–5]。
目前砷的形态分离方法主要有高效液相色谱法、毛细管电泳法和离子色谱法。砷的检测技术主要有原子吸收法、电感耦合等离子体发射光谱法、原子荧光法和电感耦合等离子体质谱法。高效液相色谱法分离效果好,应用广泛;电感耦合等离子体质谱法抗干扰能力强,灵敏度高,线性范围宽,因此高效液相色谱–电感耦合等离子体质谱法(HPLC–ICP–MS)已成为砷形态分析最具应用前景的技术之一[6–13]。笔者通过优化实验条件,建立了HPLC–ICP–MS测定环境水体中砷形态的方法,方法检出限低,精密度高,回收率稳定。
1 实验部分
1.1 主要仪器与试剂
高效液相色谱仪:1260型,配有在线真空脱气机、梯度四元泵、自动进样器,美国安捷伦科技公司;
ICP–MS分析仪:7700x型,美国安捷伦科技公司;
亚砷酸根标准溶液:(75.7±1.2)μg/g,编号为GBW 08666,国家标准物质研究中心;
砷酸根标准溶液:编号为GBW08667,(17.5±0.4)μg/g,国家标准物质研究中心;
一甲基砷标准溶液:编号为GBW08668,(25.1±0.8)μg/g,国家标准物质研究中心;
二甲基砷标准溶液:编号为GBW08669,(52.9±1.8)μg/g,国家标准物质研究中心;
砷甜菜碱标准溶液:编号为GBW08670,(38.8±1.1)μg/g,国家标准物质研究中心;
磷酸二氢铵:HPLC缓冲溶液添加剂,德国CNW科技公司;
碳酸氢铵:HPLC缓冲溶液添加剂,德国CNW科技公司;
硫酸铵:ACS级,德国CNW科技公司;
氨水:ACS级,美国Sigma-Aldrich公司;
实验用水为二次去离子水。
1.2 仪器工作条件
1.2.1 HPLC条件
色谱柱:Dionex IonPac AS19阴离子分析柱(250 mm×4 mm,赛默飞世尔科技公司);流动相:2.0 mmol/L 磷酸二氢铵–2.0 mmol/L 碳酸氢铵–2.0 mmol/L 硫酸铵,用氨水调节pH值为10.3,流速为1.0 mL/min;进样体积:50 μL。
1.2.2 ICP–MS条件
RF功率:1 550 W;采样深度:7.5 mm;载气流量:0.92L/min;补偿气流量:0.23 L/min;玻璃同心雾化器;石英雾化室和矩管;雾化室温度:2℃;镍采样锥和截取锥;同位素75As;积分时间:0.5 s。
1.3 样品处理
采集地表水体样品后,用0.45 μm微孔纤维滤膜对水样进行过滤。过滤后的水样可直接进入色谱系统用于砷形态测定,或者用于ICP–MS分析直接测定总砷。
2 结果与讨论
2.1 流动相pH值
选择磷酸二氢铵、碳酸氢铵、硫酸铵为流动相,对色谱分离条件进行优化。结果表明,流动相的pH值对砷形态的分离影响较大,特别是对DMA与As(Ⅲ)的分离影响很大。随着流动相pH值的增大,DMA与As(Ⅲ)逐渐分离,当pH值大于9.5时,DMA与As(Ⅲ)达到基线分离;当pH为10.3时,5种砷形态在15 min内能够完全分离;最终选择流动相pH值为10.3。
2.2 流动相缓冲液浓度
选用IonPac AS19阴离子分析色谱柱,在流动相pH值为10.3时,对磷酸二氢铵、碳酸氢铵、硫酸铵浓度进行试验。结果表明,流动相浓度对砷形态保留时间影响较大,随着流动相浓度的增大,5种砷形态的保留时间均减小;同时流动相缓冲液中的盐类会在ICP–MS锥口产生积碳,影响仪器的稳定性。因此最终选择流动相磷酸二氢铵、碳酸氢铵、硫酸铵的浓度均为2.0 mmol/L。不同流动相浓度时砷形态色谱图见图1。
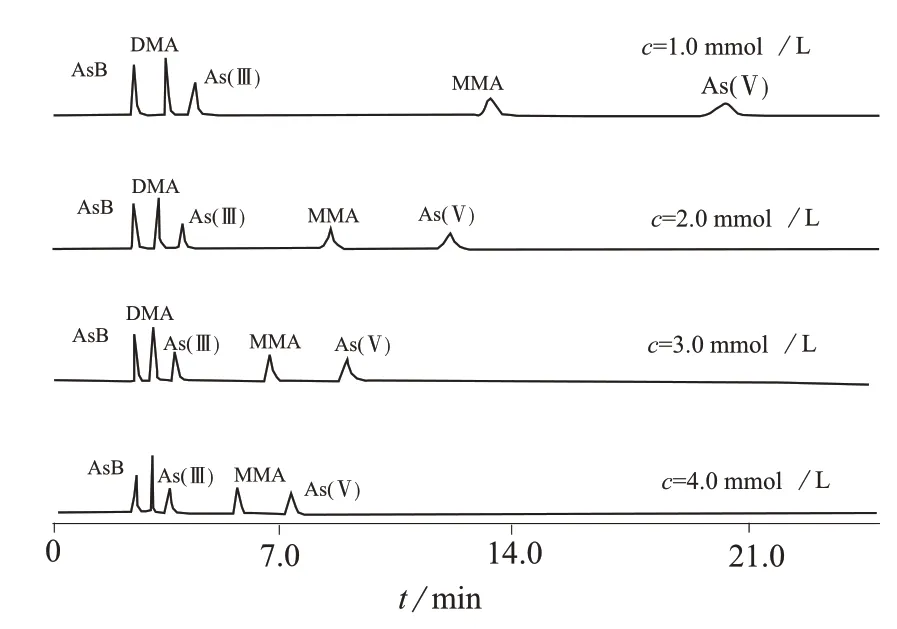
图1 不同流动相浓度时砷形态色谱图
2.3 氯离子干扰消除
在ICP–MS测定时,等离子体中的Ar易与样品基质中大量的Cl结合形成75ArCl分子离子。如果样品中氯离子的含量过高,可能会严重干扰75As的测定。在上述液相色谱条件下,氯离子的出峰时间在5~6 之间,与5种砷形态的出峰时间能完全错开,因此不会干扰砷形态的定量,5种砷形态和氯离子的色谱图见图2。
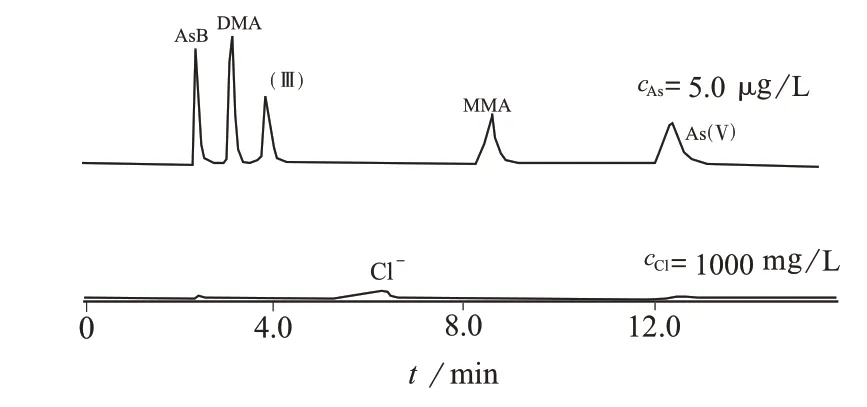
图2 5种砷形态和氯离子的色谱图
2.4 ICP–MS条件优化
ICP–MS调谐模式使用no gas模式,联机前用ICP–MS专用调谐液(1 μg/L Ce,Co,Li,Mg,Tl,Y)进行调谐,以确保仪器的最佳状态和稳定性。RF功率采用1 550W,以提高砷的电离效率;同时调节采样深度、载气和补偿气流速、矩管位置和透镜电压;提高89Y检测灵敏度并降低氧化物和双电荷的比率,满足CeO/Ce<2%,Ce2+/Ce+<3%。最终选择的ICP–MS工作条件见1.2.2。
2.5 标准曲线与检出限
配制0.0,2.5,5.0,10.0,20.0,30.0 μg/L的系列砷化合物混合标准溶液,在优化实验条件下进行分析。以砷化合物的响应值(Y)为纵坐标、对应的砷质量浓度(X,μg/L)为横坐标进行线性回归。5种砷化合物的工作曲线方程、相关系数见表1。

表1 5种砷形态的标准曲线方程与方法检出限
平行配制7份含5种砷化合物均为0.5 μg/L的空白加标溶液进行测定,计算标准偏差s,根据MDL=s×t(n-1,0.99)计算5种砷化合物的检出限(n=7时,t=3.143),结果列于表1。
2.6 样品分析
选取长江、玄武湖和秦淮河3类地表水体,在1.2条件下,用HPLC–ICP–MS进行砷形态分析,同时分析水样中总砷的含量,结果见表2。由表2可知,地表水体中的砷化合物主要以五价无机砷为主要存在形态,其它形态的砷含量较低,色谱回收率在90%左右。
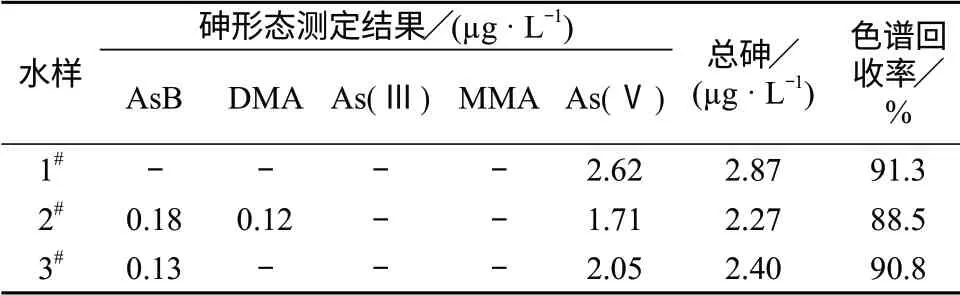
表2 实际样品中5种砷形态的测定结果
2.7 方法精密度和准确度
在长江、玄武湖和秦淮河3类地表水体样品中中分别加入2.0,5.0,15.0 μg/L砷化合物混合标准溶液,进行6次平行测定,结果见表3。由表3可知,3个加标水平下测定结果的相对标准偏差为1.5%~4.6%,加标回收率为91.6%~104.5%,说明该方法得到的数据准确可靠。
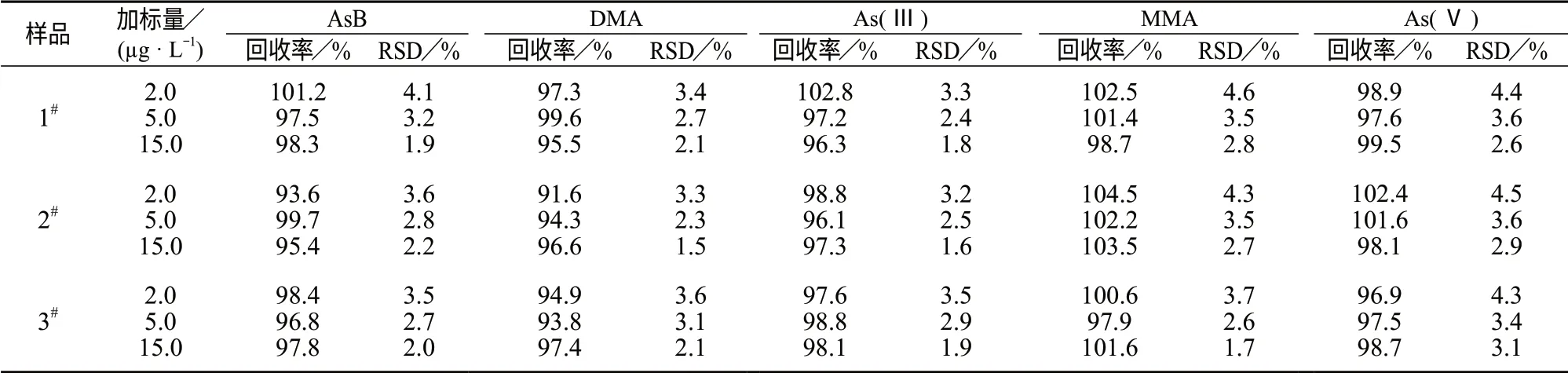
表3 精密度及加标回收试验结果(n=6)
3 结语
建立了HPLC–ICP–MS联用技术测定地表水体中AsB,DMA,As(Ⅲ),MMA,As(Ⅴ)5种砷形态的方法,HPLC与ICP–MS连接简单,方法检出限低、精密度高、回收率稳定。该方法对于研究水体中各种砷形态的迁移转化及其毒性毒理具有重要价值。
[1]Castillo A,Boix C,Fabregat N,et al. Rapid screening of arsenic species in urine from exposed human by inductively coupled plasma mass spectrometry with germanium as internal standard[J]. Anal at Spectrom,2012,27: 354–358.
[2]田靖,陈昌云.砷形态分析技术研究进展[J].化学分析计量,2011,20(5): 92–95.
[3]肖亚兵,阎华,陈其勇. HPLC–ICP–MS连用技术在有机砷形态分析中的应用[J].食品研究与开发,2011,32(9): 227–230,250.
[4]张金玲,钟耀广,孙晓红,等.砷及砷的形态检测方法的研究现状[J].食品工业科技,2012,33(23): 408–413.
[5]徐晶晶,刘淑娟,罗明标,等.环境样品中砷的形态分析[J].环境监测管理与技术,2009,21(5): 8–11,16.
[6]顾海东,陈邵鹏,秦宏兵.高效液相色谱–原子荧光光谱联用分析土壤中形态砷[J].环境监测管理与技术,2012,24(1): 38–42.
[7]刘锋,石志芳,姜霞,等. HPLC–ICP–MS法分析太湖沉积物中砷的形态及分布特征[J].质谱学报,2011,32(3): 170–175.
[8]林立,陈光,陈玉红,等.液相色谱–电感耦合等离子体质谱法联用测定白酒中的无机砷[J].环境化学,2008,27(6): 853–855.
[9]方军,舒永红,腾久委,等. HPLC–ICP–MS测定中药中砷的形态[J].分析试验室,2006,25(12): 95–98.
[10]倪张林,汤富彬,曲明华,等.高效液相色谱–电感耦合等离子体质谱联用技术测定花茶中砷形态[J].分析科学学报,2013,29(4): 506–510.
[11]吕超,刘丽萍,董慧茹,等.高效液相色谱–电感耦合等离子体质谱联用技术测定水产类膳食中5种砷形态的方法研究[J].分析测试学报,2010,29(5): 465–468.
[12]杨丽君,宋晓华,陈丽娟,等.高效液相色谱–电感耦合等离子体质谱法同时测定果蔬中6种砷形态[J].分析试验室,2011,30(7): 62–65.
[13]余晶晶,曹煊,崔维刚,等.高效液相色谱–电感耦合等离子体质谱测定浒苔中砷及砷化学形态[J].食品科学,2009,30(16): 223–227.

