干法脱硫剂脱除SO2的机理及动力学研究进展
李从,张婷,李俊青,叶萌
(兰州理工大学 石油化工学院,甘肃 兰州 730050)
干法脱硫技术相比于湿法脱硫技术,具有占地面积小、副产品少等特点,是现今脱硫技术研究的重要方向。
常用的干法脱硫剂有钙基脱硫剂、吸附型脱硫剂、金属氧化物脱硫剂和负载型金属氧化物脱硫剂等。石灰/石灰石法是目前火电厂采用最多的脱硫方法,此法原料易得、设备投资费用低、运转费用低。活性炭、活性炭纤维、沸石、活性氧化铝等吸附剂因具有较高的比表面积,在不添加任何助剂和选择载体的情况下,均有较好的脱硫效果。金属氧化物脱硫剂大体可分为单一金属氧化物脱硫剂和复合金属氧化物脱硫剂2 种。单一氧化物脱硫剂主要有氧化铁、氧化锌、氧化钙、氧化铜、氧化锰、氧化锡和稀土金属氧化物等,复合金属氧化物脱硫剂主要有钛酸锌、铁酸锌等[1]。负载型金属氧化物烟气干法脱硫其原理是以金属氧化物作吸收剂,以有活性的Al2O3、TiO2、活性炭和硅胶等为载体制备成的脱硫剂。以活性氧化铝为载体负载金属氧化物的脱硫剂(CuO/γ-Al2O3)已得到广泛的研究[2-5];本课题组采用凹凸棒石复合活性氧化铝为载体并负载金属氧化物四氧化三钴,制得的负载型复合脱硫剂Co3O4-γ-Al2O3/ATP 也具有较好的脱硫效果[6]。
各种脱硫剂脱硫机理各自有着多种论述,但各种论述之间存在着很大的差异,下文将提及的干法脱硫剂脱硫机理均是较为公认的机理学说。通过明确这几类脱硫剂的脱硫机理可以揭示脱硫剂的结构与脱硫反应能力的关系,了解物质变化的内部原因。
关于动力学的研究方面,现今研究的重点在于活性炭和负载型金属氧化物脱硫剂的动力学研究,通过对脱硫剂动力学的研究可以更好地控制和调节脱硫反应速率,有助于人们选择加快脱硫反应的速率,降低或抑制副反应的发生;通过对脱硫机理及动力学的研究可以研制出脱硫反应温度更低、硫容量更大、脱硫速率更高、机械性能更为优异的脱硫剂,这对于干法脱硫技术的发展具有现实的指导作用。
1 各种干法脱硫剂的脱硫机理研究现状
1.1 钙基脱硫剂的脱硫剂机理
将石灰石直接喷射进锅炉,停留时间很短,迅速进行硫氧化物脱除过程的锻烧、吸附和氧化反应[7]:

从上述反应可以看出,石灰/石灰石法的原理就是以碱性的CaO 吸收酸性的SO2,并在有氧气存在的情况下,将中和产物CaSO3氧化成CaSO4的过程。
石灰/石灰石法是目前火电厂采用最多的脱硫方法,此法原料易得、设备投资费用低、运转费用低。但脱硫效率较低、设备易结垢,这是因为钙基脱硫剂在脱硫反应过程中,生成的CaSO4的摩尔体积是CaO 的3 倍多,且CaO 颗粒内气孔分布纤细而密集,在脱硫反应中CaO 颗粒内气孔很快就被CaSO4堵塞,从而阻止了SO2向其内部的扩散,从而使得脱硫效率降低,脱硫剂的利用率也很低[8-10]。且气流中未反应的石灰会使静电除尘器的效率降低,增加除尘设备的负荷。
1.2 吸附型脱硫剂吸附脱硫机理
吸附型脱硫剂的种类较多,近年来,以活性炭(焦)、活性炭纤维、沸石、活性氧化铝为脱硫剂和变压吸附法烟气脱硫研究取得了较快的进展。下面以活性炭脱硫剂为例来说明吸附型脱硫剂的脱硫机理。
活性炭材料是一种低温脱硫剂,其孔结构良好、比表面积大、表面基团丰富,具有高效的吸附能力,适用于高空速的操作,现今应用最为广泛。
活性炭对烟气中SO2的吸附过程中既有物理吸附又有化学反应,当烟气中不存在氧气和水蒸气时,仅有物理吸附时,吸附量较小。当烟气中存在着氧气和水蒸气时,化学反应非常明显。活性炭的脱硫过程为催化氧化过程,其表面对SO2与O2的反应有催化作用,反应结果生成SO3。SO3易溶于水而生成硫酸,此为化学反应,从而使吸附量比单纯物理吸附时大了许多。人们将反应的总过程用以下化学方程式描述[11]:

但由于活性炭质材料表面性质复杂,脱除烟气SO2反应的组分多,活性炭吸附SO2过程十分复杂,因此直至现在还没有一种确切的机理能用来明确活性炭质材料脱除烟气SO2过程中吸附与反应过程。以下为较为公认的由Tamura[12]等提出的脱硫机理:
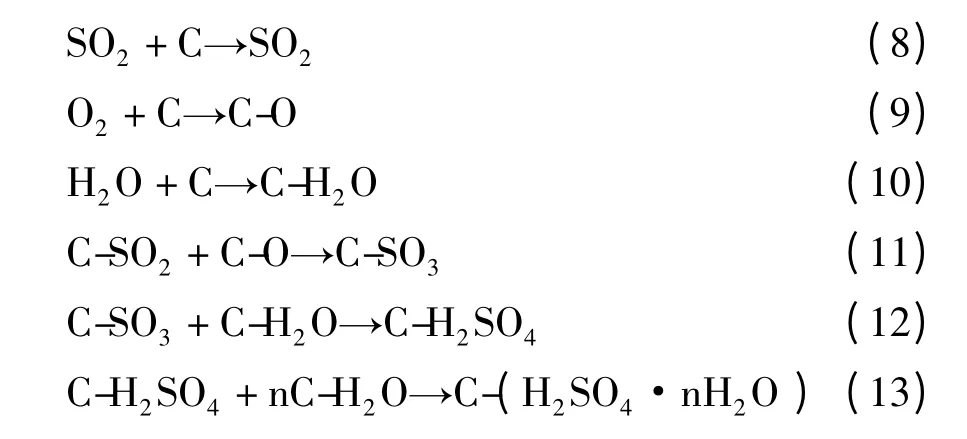
(C 表示活性炭表面的活性位,-表示吸附作用,下同)
上述SO2的吸附氧化反应中,反应控制步骤是反应(5),即将吸附态SO2氧化为吸附态SO3。Tamura[12]认为SO2、O2和H2O 全部被吸附在活性炭表面上,且此三个吸附态分子之间只要保持足够近的距离和适当的空间构型,彼此之间就能反应并生成H2SO4。
Mochida 等[13]则认为SO2与O2分子存在竞争活性位的现象,只有气态的O2才能和吸附态的SO2进行。在可能存在的3 种氧化反应中,只有反应(8)可以顺利进行。
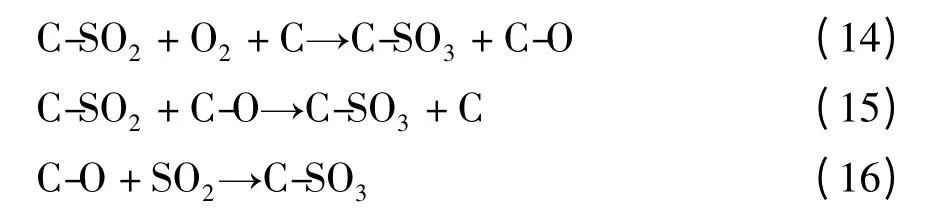
Zawadzki 等[14]认为在有水的环境下,活性炭表面的吡喃酮官能团和离域π 电子均会与H2O 分子反应生成H2O2,这是一种强氧化剂,可将SO2溶于水后形成的H2SO3氧化为H2SO4。
1.3 金属氧化物脱硫机理

铁、锌、锰、铜及其相应金属氧化物广泛应用于各种气体的精脱硫,这些金属氧化物都极易与SO2发生反应,都能够催化氧化SO2为SO3,且吸附SO2为硫酸盐,从而达到脱硫的目的,其脱硫机理及还原再生机理如下:郭汉贤[15]认为金属氧化物脱硫具有3 个重要的特征:①脱硫并不是金属氧化物的表面物理吸附过程,而是硫离子向固体晶粒内不断渗入的体相吸收过程;②脱硫并非可逆的物理吸附或毛孔冷凝,而是不可逆的化学反应;③金属氧化物的脱硫过程同时受到孔扩散及粒子扩散的阻碍,比较容易进行,因其反应的本征活化能较低。
实际生产过程中,在良好的吸收设备和适宜的操作条件下,金属氧化物脱硫剂脱硫吸收效率很高,适用于精脱硫环节。对其脱硫产物实施氧化可以金属硫酸盐形式回收硫和金属资源;而过滤后采取热分解工艺又可以回收高浓度SO2,并产出金属氧化物进行循环脱硫;采用酸分解工艺则可回收高浓度SO2和金属硫酸盐。
1.3.1 氧化锌脱硫剂 氧化锌脱硫剂是一种重要的中温脱硫剂,在低温时硫容较低,脱硫精度高,用于中温脱硫时,其硫容较高,但脱硫精度低。目前,提高氧化锌的低温硫容一直是脱硫技术研究的重点。
氧化锌法用于气体精细脱硫可以脱除SO2,过程主要反应为[5]:
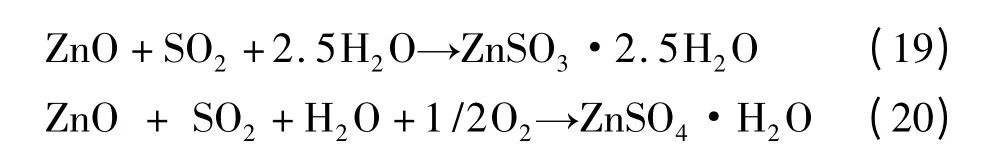
上述反应可在50 ℃下进行。
Ebrahim 等[16]研究ZnO 等金属氧化物对SO2的吸附模型,在考察了ZnO 的孔结构和O2在SO2转变成SO42-过程中的作用,在ZnO 去除SO2的过程中,SO2是以SO42-的形式直接被固定在吸附剂上的。部分未被氧化的SO2分子以不稳定的SO32-形式附在金属氧化物表面,待脱硫过程达到平衡后,这部分未被氧化的SO2分子逐渐被空气中的O2氧化
成SO42-。
1.3.2 氧化铁脱硫剂 氧化铁脱硫剂是一种低温脱硫剂,硫容量较大,脱硫精度较低。大量的数据表明,氧化铁既可用于高浓度硫化氢的粗脱,也可以用于低浓度的硫化氢的精脱。因氧化铁是按化学机理脱硫,因此在有氧或无氧的条件下均可使用,但空速不高,耐水性也稍差。
在脱硫过程中,脱硫剂Fe2O3与SO2主要进行的非催化气固反应为:

Anatolii 等[17]利用FTIR 光谱发现α-Fe2O3在脱硫过程中,α-Fe2O3脱硫剂脱硫机理为H2S 分子扩散到氧化铁水合物表面,透过脱硫剂的微孔向内部扩散;在颗粒表面的水膜中离解为HS-、S2-并与α-Fe2O3·H2O 中的氧(OH-、O2-)进行置换,从而生成Fe2S3·H2O。
1.4 负载型脱硫剂的脱硫机理
负载型脱硫剂干法脱硫的关键是制备性能优良的脱硫剂,普通的金属氧化物脱硫剂虽然得到广泛应用,但普遍存在脱硫精差、强度低、遇水易粉化的缺点。因此新型的脱硫剂往往采用加入少量的碱金属氧化物来提高脱硫剂的空隙率,使其变得膨松、有利于SOx扩散到脱硫剂内部,提高固硫率,并添加助剂压片成型制得,具有成本低、硫容高、脱硫精度高、机械强度高的特点。
铝基氧化铜脱硫剂(CuO/γ-Al2O3)是一种应用广泛的高温脱硫剂,脱硫精度高、硫容量大。CuO/γ-Al2O3脱硫剂具有较好的脱硫性能,但其有载体成本高、起始活性温度高等缺点,限制了其工业应用;而活性炭等具有孔结构发达,比表面积大的特点,以活性炭为载体制备的脱硫剂在常温时硫容较高,但活性炭不易成型,因此通过对碱金属,活性炭或其他载体如凹凸棒土的改性来制备出性质更为优良的负载型脱硫剂已经成为目前脱硫工艺中的研究重点之一。
1.4.1 CuO/γ-Al2O3脱硫剂 此方法是以CuO 作吸收剂,以有活性的Al2O3为载体制备成的脱硫剂。具体做法是将活性氧化铝于铜盐溶液中浸渍、焙烧制得脱硫吸附剂。由于活性氧化铝具有多孔结构,高比表面积且处于不稳定的过渡态,因而具有较大的活性。多孔的活性氧化铝还具有吸附特性,本身对SO2有吸附作用;在负载了金属氧化物之后,金属氧化物又可以与SO2反应[3-5]:

Centi 等[2]建立了脱硫微观动力学模型用以研究铝基氧化铜脱硫剂脱硫的机理。他们认为在有氧的高温(300 ~450 ℃)环境下,SO2分子首先化学吸附在CuO/Al2O3的表面的晶格氧上,后与邻近的氧化态铜位催化氧化为SO3,进而在CuO/Al2O3表面主要生成CuSO4并同时通过表面转移到相邻的游离Al 位点上在此表面上生成Al2(SO4)3,而体相Al2O3则不会发生变化。
Lin 等[18]认为,以溶胶-凝胶法制备的CuO/γ-Al2O3比表面积大、抗冲击强度高、硫化性能良好,与活性炭、沸石及硅胶等吸附载体相比是更加有效的吸附脱硫剂。
1.4.2 Co3O4-γ-Al2O3/ATP 脱硫剂 本课题组以甘肃产凹凸棒石(ATP)为基体,辅以活性氧化铝、成型剂等成分,经造粒后附载过渡金属氧化物Co3O4,制得了一种新型复合吸附脱硫剂Co3O4-γ-Al2O3/ATP[6]。
经适当条件制备的Co3O4-γ-Al2O3/ATP 吸附脱硫剂,具有吸附二氧化硫和催化脱除二氧化硫的能力。样品表面固有的原子结构和活化处理产生的表面电荷不平衡现象而形成了吸附中心,当烟气通过吸附脱硫剂时,SO2被活性位吸附,与邻位吸附态的O2反应生成SO3,然后与吸附态的H2O 反应生成硫酸,储存于吸附脱硫剂的微孔或中孔中。反应方程式如下:

(注:上述各反应中“* ”表示吸附态)
其中(23)、(24)、(25)为物理吸附过程,(26)、(27)、(28)为化学吸附过程。总反应式可表示成:
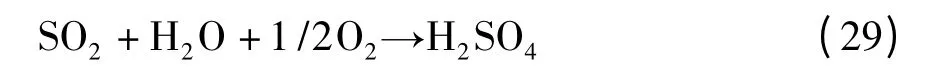
在上述反应中,活性氧化铝和ATTP 既是载体,又作为催化剂促进了该反应的进行。除上述反应外,还有如下的化学反应过程:

2 脱硫动力学研究现状
2.1 活性炭脱硫剂脱硫吸附动力学的研究现状
黄祥等[19]采用以农业废弃物核桃壳为原料,天然软锰矿为添加剂共混制成的新型柱状活性炭进行了不同水蒸气含量下的烟气脱硫实验。以Bangham模型和Elovich 模型两种模型进行动力学模拟后发现Elovich 模型具有更高的精度。高继贤等[20-21]通过动态吸附烟气脱硫实验,考察了烟气中在SO2体积分数不同的条件下对炭基吸附剂脱硫行为的影响,使用Bangham 模型、Elovich 模型、准二级动力学模型、Lagergren 准一级动力学模型、粒内扩散模型等多种动力学模型进行研究总结后发现Bangham模型模拟效果最优,SO2的催化氧化反应对化学吸附有重要影响。马双忱等[22]利用微波的诱导催化作用结合了活性炭的吸附还原能力进行脱硫实验。其研究结果表明微波不仅以其热效应促进了脱除反应的进行,更发挥了它的诱导催化效应。程振民等[23]在不存在水蒸气的情况下,采用Langmuir-Hinshelwood 方法研究了SO2在活性炭上的催化氧化反应动力学。其实验结果表明吸附速率常数并不符合简单的Arrhenius 关系,而是多种因素共同作用的结果。张立强等[24]认为不同种类活性炭的脱硫性能差别较大,活性炭的表面化学特性对其脱硫性能产生重要影响。在进行动力学模拟分析后发现Bangham 模型的模拟值与实验值吻合,适于描述流化床内粉状活性炭吸附烟气中SO2的过程。楚英豪等[25]认为混合烟气流量>400 mL/min 时可消除外扩散的影响,在此消除了内外扩散的条件下对SO2-O2-N2-H2O 体系,使用脱硫专用活性炭纤维脱除烟气中SO2的过程进行了本征动力学研究,其得到的脱 硫动力学方程为:rD= kCSO20.4936CO20.7381CH2O0.7021,其反应活化能为8.85 kJ/mol。陈军辉[26]进行了活性炭纤维催化脱硫颗粒级宏观动力学实验,在与本征动力学实验相同的实验条件下得出消除内外扩散影响的活性炭脱硫反应速率方程,归纳得到了颗粒级宏观动力学方程:R = 0.001 63exp(-E/RT)CSO21.173CO20.1023,其反应活化能为3.9 kJ/mol。
2.2 金属氧化物脱硫剂脱硫吸附动力学的研究现状
刘世斌等[27-28]利用热重实验装置考察了SO2、O2浓度及反应温度对复合金属氧化物脱硫剂脱硫反应的本征及宏观反应速率的影响,根据流固相非催化反应理论,采用Marquart 非线性回归法由实验数据求得动力学参数,经检验表明,以幂函数表达本征动力学是合理的,随机孔模型可很好地模拟宏观动力学规律。另外考察了CO2、H2O 对复合金属氧化物脱硫剂脱除SO2反应的影响。实验表明,CO2对脱硫反应的速率及转化率影响很小,可视作惰性气体;H2O 对脱硫反应的影响有区间性,在H2O <7%时,随着水浓度增加脱硫反应速率明显提高,H2O >7%时,H2O 浓度影响很小,可忽略其影响。魏国等[29]对钙铝复合脱硫的机理和效果进行了研究,在CaO 基脱硫剂中加入铝对应时刻脱硫率均优于基准对照组;在一定的范围内,铝添加量越大,效果越好。郭汉贤等[30]认为氧化锌中温脱除二氧化硫存在补偿效应,在反应过程中先后在动力学控制区和粒子扩散控制区进行,指出晶粒表面及内部缺陷等的随机指数分布是出现该效应的主要原因。
2.3 负载型金属氧化物脱硫剂脱硫吸附动力学的研究现状
郁 青 春 等[31-32]对CuO/γ-Al2O3及CeO2/γ-Al2O3脱硫剂脱除烟气中SO2的反应动力学进行了研究,研究表明Langmuir 反应动力学模型可以很好地描述CuO/γ-Al2O3脱硫剂为0.12 g/g 时硫化过程中CuO 与SO2的反应,对SO2的反应级数为1级,其反应活化能为19.98 kJ/mol;而通过热重法研究的CeO2/γ-Al2O3脱硫剂脱硫的本征动力学结果表明,对SO2的反应级数为1 级,其反应活化能为12.54 kJ/mol。贾哲华等[33]建立了CuO/Al2O3脱硫剂的固定床反应模型并探讨了床层的动态脱硫行为,给出了固定床内硫分布曲线的数学表达式。其实验结果表明固相硫及气相硫沿床层位置的变化规律相同,床层利用率量随反应气体浓度及流量的增大而降低,而与床层高度无关。
3 结束语
经过多年的发展,干法脱硫技术在实际应用方面已经有了长足的进步,各类脱硫剂的硫容量提升较高,脱硫反应温度逐步降低,反应速率提升较快,工业化应用也已逐步展开,但国内外的干法脱硫制剂的制备仍有各种问题存在,例如氧化锌等脱硫剂低温时硫容小,工业化的脱硫反应仍处在一个较高的温度下才能进行,需要耗费相当的能源;吸收功能较为单一,吸收有机硫的硫容较小等。
国内外关于活性炭脱硫剂或碱金属脱硫剂的脱硫机理及其动力学的理论研究方面还有许多相关问题有待进一步研究解决。迄今为止,关于干法脱硫剂的脱硫机理的研究,各类动力学的研究仍是在较为简单、单一的条件下研究而成,实验条件的设定仍是静态的、外生的而不是结构的、内在的、动态的;当条件发生偏移,整体的实验结果也会出现大的偏差。由此可以看出未来的脱硫剂脱硫机理及动力学的研究仍有很大的空间。
[1] 张密林,张红霞,陈野.ZnO 型复合脱硫剂的制备研究[J].应用科技,2004,31(12):58-60.
[2] Centi G,Passarini N,Perathoner S,et al. Combined De-SO2/De-NO reaction on a copper on alumina sorbent-catalyst 1. mechanism of SO2oxidation-adsorption[J]. Ind Eng Chem Res,1992,31(8):1947-1955.
[3] 苏胜,向军,马新灵,等. 铝基氧化铜干法烟气脱硫及再生研究[J].燃料化学学报,2004,32(4):407-412.
[4] 马新灵,王亚立,邓德兵,等.CuO/Al2O3干法烟气脱硫研究[J]. 华中科技大学学报:自然科学版,2002,30(12):95-97.
[5] 王雁,张超,郑瑛,等.CuO/γ-Al2O3干法烟气脱硫[J].燃烧科学与技术,2004,10(6):535-538.
[6] 张婷,俞树荣,冯辉霞,等. 钴负载凹凸棒石基复合吸附脱硫剂脱除SO2的实验研究[J]. 矿物岩石,2008,28(3):24-28.
[7] 卞兆双.低浓度二氧化硫烟气脱硫治理方案研究[J].江汉石油学院学报,2004,26(2):171-172.
[8] 陈兵,张学学. 干法脱硫中单颗粒数学模型研究进展[J].工业锅炉,2003,77(1):16-19.
[9] 陈兵,金浩,张学学.干法脱硫非均匀初始孔隙率数学模型[J].环境污染与防治,2004,26(1):46-47.
[10]颜岩,贾力,彭晓峰,等. 干法烟气脱硫反应的实验研究[J].环境工程,2002,20(3):38-41,24.
[11]彭万旺,王乃计,戢绪国,等. 气流床烟气干法脱硫技术的初步试验研究[J]. 洁净煤技术,1999,5(4):22-26.
[12] Tamura H,Okazaki M. Influence of acidic surface oxides of activated carbon on gas adsorption characters carbon[J].Carbon,1997,35:1361-1366.
[13]Mochida I,Kuroda K,Kawano S.Kinetic study of the continuous removal of SOxusing polyacrylonitrile-based activated carbon fibresⅡKinetic Model[J].Fuel,1997(6):537-541.
[14]Zawadzki J.Infrared studies of SO2on carbon I interaction of SO2with carbon films[J].Carbon,1987,28 (3):431-436.
[15]王恩过,郭汉贤. 金属氧化物固定床脱硫的动力学行为[J].化工学报,1997,48(1):94-101.
[16]Ebrahim H A. Application of random. pore model to SO2capture by lime[J]. Ind Eng Chem,2010,49(1):117-122.
[17]Anatolii Davydov,Karl T Chuang,Alan R Sanger.Mechanism of H2S oxidation by ferric oxide and hydroxide surfaces[J].Phys Chem B,1998,102:4745-4752.
[18]Lin Y S,Deng S G. Removal of trace sulfur dioxide from gas stream by regenerative sorption processes[J].Separation and Purification Technology,1998,13(1):65-77.
[19]黄祥,杨志山,陈杰,等. 新型柱状核桃壳活性炭脱硫动力学[J].环境工程学报,2013,7(6):2273-2277.
[20]高继贤,王铁峰,王光润,等. 不同烟气水蒸气体积分数时ZL50 活性炭吸附SO2的动力学[J].清华大学学报:自然科学版,2010,50(3):434-437.
[21]高继贤,王铁峰,王金福.SO2体积分数对ZL50 活性炭吸附脱硫行为的影响和动力学分析[J]. 环境科学,2010,31(5):1152-1159.
[22]马双忱,姚娟娟,金鑫,等. 微波辐照活性炭床脱硫脱硝动力学研究[J].中国科学:技术科学,2011,41(9):1234-1239.
[23]程振民,蒋正兴,袁渭康.活性炭脱硫研究(I):SO2-N2-O2体系中SO2的氧化反应动力学[J].环境科学学报,1997,17(3):268-272.
[24]张立强,蒋海涛,李兵,等.粉状活性炭流化床吸附SO2的实验研究及吸附动力学分析[J]. 煤炭学报,2012,37(6):1046-1049.
[25]楚英豪,尹华强,刘中正.活性炭纤维(ACF)脱硫动力学研究[J].四川环境,2001,20(2):8-11.
[26]陈军辉.新型炭法烟气脱硫过程动力学研究[D]. 成都:四川大学,2004.
[27]刘世斌,李存儒. 复合金属氧化物脱硫剂脱除SO2动力学[J].燃料化学学报,1998,26(1):83-88.
[28]刘世斌,刘祖愉. 复合金属氧化物脱除SO2的气氛效应及动力学[J].燃料化学学报,2001,29(6):524-527.
[29]魏国,孙瑜,何奕波,等. 铁水钙铝复合脱硫的机理分析及研究[J]. 东北大学学报,2012,33(12):1737-1740.
[30]郭汉贤,樊惠玲,李彦旭. 金属氧化物脱硫/固硫反应动力学中的补偿效应[J]. 化学学报,2002,60(10):1806-1810.
[31]郁青春,张世超,王新东,等.CuO/γ-Al2O3脱硫动力学研究[J].环境工程,2007,25(5):48-51.
[32] 郁青春,张世超,王新东,等. CeO2/γ-Al2O3脱硫动力学研究[J].洁净煤技术,2007,13(3):74-77.
[33]贾哲华,刘振宇,赵有华.CuO/Al2O3脱除SO2的固定床模型研究[J]. 化学反应工程与工艺,2007,23(3):200-206.

