HPLC法快速测定乳粉中VC棕榈酸酯的含量
杜淑霞,徐丽,廖延智,司徒满泉,李文清
(1.广东轻工职业技术学院,广东广州510300;2.暨南大学,广东广州510632)
HPLC法快速测定乳粉中VC棕榈酸酯的含量
杜淑霞1,徐丽1,廖延智1,司徒满泉1,李文清2
(1.广东轻工职业技术学院,广东广州510300;2.暨南大学,广东广州510632)
建立了利用高效液相色谱仪快速测定乳粉中Vc棕榈酸酯含量的方法。以含0.1%草酸的乙醇溶液为提取剂,以甲醇和0.15%草酸(体积比为90∶10)为流动相,经Inertsil ODS-SP色谱柱分离,采用二极管阵列检测器,在245 nm波长下进行测定。VC棕榈酸酯的质量浓度在0.5 μg/mL~100 μg/mL浓度范围内与峰面积呈良好的线性关系。以3倍基线噪声所对应的浓度计算VC棕榈酸酯的检出限为2 μg/g。加标回收率在92.01%~105.84%之间,相对标准偏差(n=6)在1.02%~2.70%之间。
VC棕榈酸酯;高效液相色谱法(HPLC);乳粉
VC棕榈酸酯又称抗坏血酸棕榈酸酯(简称AP),分子式为C22H38O7,结构式为

由棕榈酸与L-抗坏血酸酯化而得。它是氧的清除剂、金属螯合剂,同时保留了抗坏血酸的生理活性,被世界卫生组织(WHO)食品添加剂委员会(FIO)定为具有营养性、无毒、高效,使用安全的抗氧剂,同时被美国药典收载[1],也是我国食品添加剂使用标准中规定许可的用于乳粉中的抗氧化剂[2],起到抗氧化、护色、营养强化等功效,同时可以提高产品的货架期[3]。VC棕榈酸酯的应用越来越广泛,有必要建立简单、快速的方法准确地测定其含量,指导VC棕榈酸酯的合理使用。目前,关于纯的食品添加剂VC棕榈酸酯的检测方法主要有碘滴定法[4],而2,6-二氯酚靛酚法[5]、薄层扫描法[6]和液相色谱法[7],主要用于食用油脂、焙烤食品和方便米面食品中抗坏血酸棕榈酸酯含量的测定。而关于乳粉中抗坏血酸棕榈酸酯的检测方法尚未见报道。本文用0.1%草酸的乙醇溶液提取试样中的VC棕榈酸酯,以甲醇和0.15%草酸为流动相进行洗脱,使用高效液相色谱法可以快速地测定乳粉中抗坏血酸棕榈酸酯的含量。
1 材料与方法
1.1材料与仪器
VC棕榈酸酯:东莞广益食品添加剂有限公司提供;甲醇和乙腈为色谱纯:迪马公司;乙醇、草酸、柠檬酸、三氯乙酸为国产分析纯试剂。
岛津LC-20A高效液相色谱仪,配有LC-20AT溶液传输单元(泵)和SPD-M20A二极管阵列(PDA)检测器:日本岛津公司;色谱柱(Inertsil ODS-SP,5 μm,4.6 mm×250 mm)、BS210S电子天平:北京赛多利斯天平有限公司;HS6150D超声波清洗器、MixPlus旋涡混合器:合肥艾本森科学仪器有限公司。
1.2方法
1.2.1色谱条件
色谱柱:Inertsil ODS-SP,5 μm,4.6 mm×250 mm;检测器:二极管阵列(PDA)检测器;柱温:30℃;流速:1 mL/min;进样量:20 μL;检测波长:245 nm;流动相:甲醇:0.15%草酸溶液=90∶10(体积比)。
1.2.2VC棕榈酸酯的稳定性
准确称取0.100 0 g VC棕榈酸酯分别用乙醇、0.1%草酸的乙醇溶液、0.1%柠檬酸的乙醇溶液、0.1%三氯乙酸的乙醇溶液溶解并定容至100 mL,移取其中5 mL于4个100 mL容量瓶中,分别用上述4种溶液定容至100 mL,得50 μg/mL的VC棕榈酸酯溶液,用0.45 μm有机相滤膜过滤后按1.2.1色谱条件每隔一定时间进样一次,根据峰面积的变化判断VC棕榈酸酯在上述溶液中的稳定性。
1.2.3标准曲线的绘制
准确称取0.100 0 g VC棕榈酸酯用0.1%草酸的乙醇溶液溶解并定容至100 mL,得1 mg/mL的VC棕榈酸酯溶液,用0.1%草酸的乙醇溶液稀释成0.5、1、5、10、50、100 μg/mL标准系列,用0.45 μm有机相滤膜过滤后在1.2.1色谱条件下依次注入液相色谱,以浓度为横坐标,峰面积为纵坐标绘制标准曲线。
1.2.4样品的测定
称取3 g~5 g试样于50 mL离心管中,加入95%乙醇(其中含有0.1%的草酸)至25 mL,混匀,涡旋中速振荡,离心,取上清液用0.45 μm有机相滤膜过滤后上机测定。根据保留时间定性,外标标准曲线定量。
2 结果与讨论
2.1测定波长的选择
所用溶剂或流动相的不同可能影响化合物的最大吸收波长,本文将VC棕榈酸酯标准溶液在200 nm~400 nm范围利用二极管阵列检测器进行紫外扫描,发现在波长为245 nm处的吸光度最大,故测定波长选为245 nm。
2.2流动相的选择
固定流动相流速为1 mL/min,本文考察了流动相体积比为甲醇:0.15%草酸=95∶5、90∶10、85∶15、80∶20时的出峰情况,发现流动相配比为95∶5时,VC棕榈酸酯在4.5 min时出峰,周围杂峰多,与试样中组分分离效果差;当流动相中甲醇低于85%时,VC棕榈酸酯在10min之后出峰,延长了分析时间且峰型质量差,当流动相体积比为甲醇:0.15%草酸=90∶10时,分离效果最好。
2.3VC棕榈酸酯的稳定性
不同溶剂中VC棕榈酸酯稳定性见表1。

表1 不同溶剂中VC棕榈酸酯的稳定性Table 1 Effect of different solvent on stability of ascorbyl palmitate
VC棕榈酸酯结构上含有烯二醇式结构,温度、光线、金属离子及碱性环境等因素都可能促进VC棕榈酸酯的氧化。本文探讨了不同的酸性条件下VC棕榈酸酯的稳定性,由表1可以看出在0.1%草酸乙醇溶液中VC棕榈酸酯最稳定,常温下放置20 h,残留量仍然在95%以上,而在0.1%三氯乙酸乙醇溶液中,常温下放置5 h时仅残留10%。
2.4提取剂的选择
实验发现,VC棕榈酸酯在乙醇中的溶解性远远优于甲醇、乙腈等其他有机溶剂,且95%乙醇溶液作为提取剂可以达到良好的提取效果[8],但VC棕榈酸酯在乙醇溶液中稳定性欠佳,为了避免VC棕榈酸酯的损失,本文用含0.1%草酸的95%乙醇浸泡试样,涡旋中速振荡8 min,4 000 r/min离心5 min,能较完全地提取试样中的待测组分。
2.5线性范围和检出限
按实验方法测得的VC棕榈酸酯各浓度标准系列对应的吸光度结果见表2,峰面积-浓度标准曲线见图1。

表2 各浓度VC棕榈酸酯对应的峰面积Table 2Peak area of different concentrations of ascorbyl palmitate
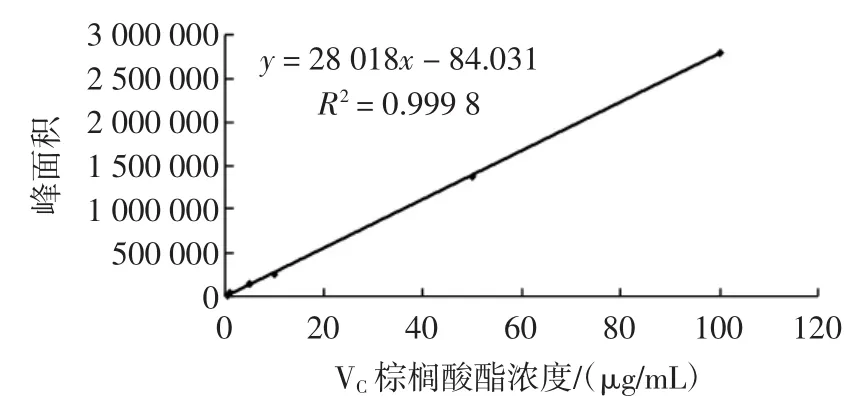
图1 VC棕榈酸酯标准曲线Fig.1Standard curve of ascorbyl palmitate
由图1可知,VC棕榈酸酯在0.5 μg/mL~100 μg/mL浓度范围内,峰面积与浓度呈现良好的线性关系。以3倍基线噪声所对应的浓度计算本方法的检出限,VC棕榈酸酯的检出限为2 μg/g。
2.6方法的精密度和准确度试验
称取未检出VC棕榈酸酯的乳粉试样,加入不同量的VC棕榈酸酯标准溶液,做高、中、低3个浓度的加标回收。按方法进行样品处理和测定,每个浓度各测6次,空白试样的色谱图和加标样品的色谱图见图2和图3。根据峰面积和线性回归方程计算VC棕榈酸酯的含量,以测定值计算回收率和精密度,结果见表3。

图2 空白试样的色谱图Fig.2Chromatogram of blank sample
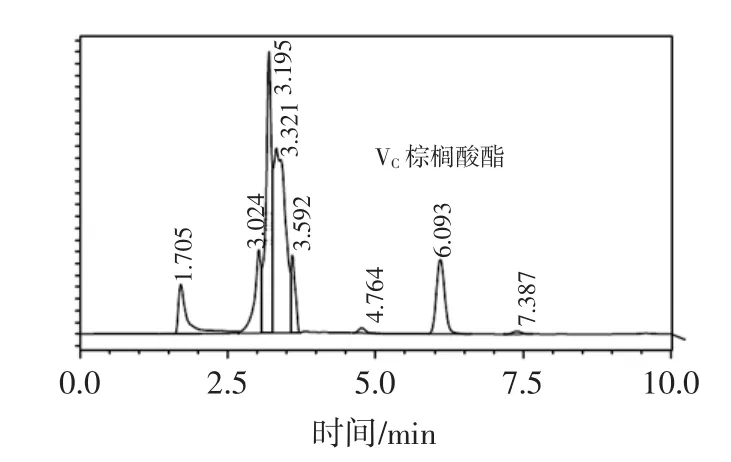
图3 加标样品的色谱图Fig.3Chromatogram of sample with ascorbyl palmitate addition

表3 回收率和精密度试验结果(n=6)Table 3Results of recovery and precision test(n=6)
2.7样品分析
目前市场上乳粉品牌和种类很多,本文随机采集了8份乳粉按上述方法进行检测,其中有3份产品含有VC棕榈酸酯,含量最高的为0.071 g/kg。
3 结论
本文建立了高效液相色谱法快速测定乳粉中VC棕榈酸酯含量的方法。该方法样品处理方法简单,分析速度快,回收率为92.01%~105.84%,相对标准偏差(n=6)为1.02%~2.70%,说明方法回收率高,精密度好,结果可靠,可应用于Vc棕榈酸酯的快速检测及质量控制。
[1]高荫榆,雷占兰,谢何融,等.L-抗坏血酸棕榈酸酯的抗氧化效果研究[J].食品科学,2007,28(11):60-62
[2]中华人民共和国卫生部.GB 2760-2011食品安全国家标准食品添加剂使用标准[S].北京:中国标准出版社,2011:40
[3]林富强,陈永恒,何松.L-抗坏血酸棕榈酸酯在配方乳品中的应用[J].现代食品科技,2010,26(10):1114-1116
[4]国家技术监督局.GB 16314-1996中华人民共和国国家标准食品添加剂L-抗坏血酸棕榈酸酯[S].北京:中国标准出版社,1996:3-4
[5]黄少强,刘志同.食用油中L-抗坏血酸棕榈酸酯含量测定方法研究[J].中国粮油学报,2006,21(2):121-123
[6]汤鲁宏,孙云飞,张浩.薄层扫描法测定L-抗坏血酸棕榈酸酯[J].食品工业科技,1999(5):57-58
[7]陆志芸,张辉,赵敏,等.高效液相色谱法测定食品中抗坏血酸棕榈酸酯[J].理化检验-化学分册,2010,46(8):869-871
[8]胡波年,谢华林,胡汉祥,等.化妆品中L-抗坏血酸棕榈酸酯的薄层色谱分析[J].武汉理工大学学报,2004,26(11):39-41
Rapid Determination of Content of Ascorbyl Palmitate in Milk Powder by HPLC
DU Shu-xia1,XU Li1,LIAO Yan-zhi1,SUTU Man-quan1,LI Wen-qing2
(1.Guangdong Industry Technical College,Guangzhou 510300,Guangdong,China;2.Jinan University,Guangzhou 510632,Guangdong,China)
The method for rapid determination of the content of ascorbyl palmitate in milk powder by high performance liquid chromatograph(HPLC)was established.It was separated through Inertsil ODS-SP chromatographic column with ethanol containing 0.1%oxalic acid as extraction agent and with methanol and 0.15%oxalic acid(vol/vol=90∶10)as mobile phase,and then was measured under 245 nm wavelength with a diode array detector.There was a good linear relationship between mass concentration of ascorbyl palmitate and peak area when the mass concentration was from 0.5 μg/mL to 100 μg/mL.Detection limit of ascorbyl palmitate was calculated as 2 μg/g by the concentration which corresponded to 3 times baseline noise.Standard addition recovery was 92.01%-105.84%,and relative standard deviation(n=6)was 1.02%-2.70%.
ascorbyl palmitate;high performance liquid chromatograph(HPLC);milk powder
10.3969/j.issn.1005-6521.2015.13.024
2013-09-17
广东省科技计划项目“安全、高效食品添加剂的开发”(2010A080403001);广东省产学研基地滚动项目“酶法合成L-抗坏血酸棕榈酸酯的中试研究”(2013CXZDC006)
杜淑霞(1969—),女(汉),教授,硕士,研究方向:食品分析。

