柠檬酸荧光碳点的合成及其在Fe(Ⅲ)检测和细胞成像中的应用
唐 荣, 李 琛, 叶志强, 张德蒙, 马小军, 谭明乾*, 袁景利
(1.大连理工大学精细化工重点实验室,辽宁大连 116023; 2.中科院大连化学物理研究所生物技术部,辽宁大连 116023; 3.长春市疾病预防控制中心,吉林长春 130033)
荧光碳点作为碳纳米材料家族的新成员,因具有突出的性能,例如:良好的水溶性和光稳定性、无光眨眼、抗光漂白、低的细胞毒性,以及良好的生物相容性等,受到越来越多的关注[1 - 4]。荧光碳点的显著特性在于其激发光谱较宽,且发射光谱随着激发波长的变大而发生红移,可发出不同颜色的荧光[5]。荧光碳点的合成方法已有很多文献报道,主要有激光消融法[6]、电化学法[7]、化学氧化法[8]、水热法[9]以及微波法[10]等。这些合成方法大多是通过一步合成形成荧光碳点,操作简单。另外,可以用来合成荧光碳点的原料来源广泛,例如草木灰[11]、有机小分子[12]、糖类[13,14]以及面包食品[15]等均可以用来制备荧光碳点。合成荧光碳点的原料来源广泛和合成方法简单为其应用奠定了基础。
荧光碳点良好的生物相容性和较低的细胞毒性,使其在生物成像领域[5,16,17]得到广泛的应用。随着研究的进展,荧光碳点的应用已经不再局限于生物成像,研究者们利用荧光碳点的光稳定性好、无光闪烁等优点,将其用于光催化[18]和LED灯[19]中。由于合成荧光碳点的原料大部分为含碳的有机物质,因此在反应的过程中表面会形成大量的官能团,如-NH2、-COOH等,可以直接或间接地用于金属离子的检测[20,21]。因此,荧光碳点的这些优良性能及广谱的应用性使其有望成为一种新型的、有潜力的荧光纳米材料。
本研究基于荧光碳点的这些优良的性能,选择柠檬酸为碳源,以水热法合成了表面带有羧基和羟基的荧光碳点。利用羧基和羟基与Fe(Ⅲ)络合导致碳点的荧光猝灭的特性,建立了检测Fe(Ⅲ)的新方法,该方法具有良好的选择性和较宽的线性范围,并被成功用于自来水中Fe(Ⅲ)的检测。同时还对柠檬酸荧光碳点进行了细胞荧光成像评价。结果表明,柠檬酸荧光碳点在金属离子检测和细胞成像方面有潜在的应用价值。
1 实验部分
1.1 仪器与试剂
LS55荧光分光光度计(美国,PerkinElmer公司);Burker Vector 22 傅里叶红外光谱仪 (德国,BRUKER公司);UV-2550 紫外分光光度计(日本,岛津公司);FV 1000共聚焦显微镜(日本,奥林巴斯公司);Bruker DRX400核磁共振谱仪(瑞士,Bruker公司);JEM-2000透射电子显微镜(日本,JEOL公司);动态光散射纳米粒径分析仪(英国,Malvern Instruments公司)。
HEPES(百灵威),葡聚糖G -25凝胶(上海叶源生物有限公司),硫酸奎宁(阿拉丁),氢氧化钠(中国天津大陆化学试剂有限公司),磷酸(中国天津恒兴化学试剂有限公司),硼酸(中国天津保地化学试剂有限公司),盐酸(北京化工厂),柠檬酸(天津市大茂化学试剂厂),三氯化铁(沈阳市试剂五厂),氯化钠、氯化钾(天津石英钟厂霸州市化工分厂),氯化钙(阿拉丁),氯化钡(天津市光复科技发展有限公司),无水硫酸镁(沈阳新兴试剂厂),氯化铜(天津市天大化学试剂厂)。所有试剂为分析纯。实验用水为去离子水。
1.2 实验方法
1.2.1碳点的制备以柠檬酸为原料,采用水热法合成荧光碳点。称取1.15 g柠檬酸,将其溶于20 mL去离子水中,超声使其充分溶解。将配好的溶液转入30 mL含有聚四氟乙烯内衬的水热反应釜中,于马弗炉中200 ℃反应4 h。待反应结束后,将反应体系自然冷却到室温,移出上清液,依次过0.45、0.22 μm的水系滤膜,最终得到淡黄色的碳点溶液。
1.2.2碳点的表征荧光发射光谱和紫外吸收光谱分别使用LS55荧光分光光度计和UV-2550 紫外分光光度计,所有的荧光光谱检测的狭缝宽度均为10 nm,扫描速度为500 nm/min。荧光猝灭曲线使用FV 1000共聚焦显微镜,样品浓度为19 mg/mL,使用405 nm激光器作为激发源,功率为13.0%,HV值为700,Gain值为2.00,Offset值为0,扫描速度为2.0 s/Pixel。
时间分辨荧光使用Horiba Jobin Yvon FluoroMax-4荧光分光光度计,用376 nm激光器作为激发光源,发射波长范围为390~620 nm,狭缝宽度为6.0 nm,扫描速度为500 nm/min,记录最大发射波长447 nm处的荧光寿命。采用Horiba公司提供的商业软件进行数据分析。
透射电镜(TEM)使用功率为200 kV的JEM-2000透射电子显微镜观察。
Zeta电位使用动态光散射纳米粒度仪(Zetasizer Nano ZS90,英国Malvern Instruments公司)记录,样品浓度为19 mg/mL。
红外(IR)光谱表征使用Burker Vector 22 傅里叶红外光谱仪,将样品与溴化钾混合研磨制片,记录500~4 000 cm-1范围内的数据。
1.2.3量子产率的计算将硫酸喹啉溶于0.1 mol/L的H2SO4中作为标准物,其在360 nm处的标准荧光量子产率值为0.54,用荧光分光光度计记录其在360 nm激发下的发射光谱,同时测量其在360 nm处的吸光度值。所合成的柠檬酸碳点测量其在310 nm处的吸光度和荧光发射光谱。以上所测得的所有荧光发射光谱都用Origin软件求得峰面积。荧光碳点的量子产率根据如下公式计算:Фx=ФR×(Ix/IR)×(AR/Ax)×(nx/nR)2。式中,I指代荧光发射曲线的峰面积,A指代吸光光度值,Ф指代荧光量子产率值,n代表溶剂的折射率,下标x代表待测物,下标R代表标准物。
1.2.4Fe(Ⅲ)的检测在5 mL离心管中依次加入2.3 mL 10 mmol/L HEPES缓冲溶液(pH=7.0),100 mL 34.3 mg/mL的荧光碳点,100 mL不同浓度的Fe(Ⅲ)溶液,空白加入100 mL去离子水,所有的样品平行配制三份。荧光光谱的激发波长皆为310 nm,发射波长范围为330~580 nm,狭缝宽度为10 nm,扫描速度为500 nm/min。以415 nm处的荧光强度I对Fe(Ⅲ)的浓度绘制曲线。
1.3 细胞标记与共聚焦显微镜成像
在24孔板中,加入500 mL小鼠黑色素瘤细胞(B16-F10,6×104cells/mL)悬浮液,使用含10% 胎牛血清及青霉素、链霉素各100 U/mL的RPMI1640作为培养液,在37 ℃、5% CO2细胞培养箱中培养24 h。而后将培养液换成含5 mg/mL荧光碳点的RPMI1640,孵育12 h。移去培养液并用PBS溶液洗涤2~3次以除去细胞外围的荧光碳点。对照试验组仅加入不含荧光碳点的培养基,其它操作与试验组完全一致。最后利用FV 1000共聚焦显微镜,分别选用405 nm与488 nm激光作为激发光源,在425~475 nm,500~600 nm范围采集发射光信号进行体外细胞成像。激光器功率为10%,HV值为700,Gain值为2.00,Offset值为0,扫描速度为2.0 s/Pixel,扫描分辨率800成像。
2 结果与讨论
2.1 荧光碳点的物化性质
采用水热法,以柠檬酸为原料合成的荧光碳点,仅仅需要一种原料,无需强酸碱等苛刻反应条件就可以一步制备荧光碳点。从表1中可以看出,所合成的荧光碳点的最大激发波长为310 nm,最大发射波长为415 nm。以硫酸喹啉作为参照物,计算得出所合成的荧光碳点在310 nm处的量子产率(QY)为5.3%。Zeta电位为-35 mV,说明其表面带有负电荷,推测可能含有羧基和羟基。荧光碳点的荧光寿命为5.3 ns。

表1 荧光碳点的物化性质
2.2 荧光碳点的透射电镜表征
图1为所合成的荧光碳点的透射电镜(TEM)图,从图中可以看出所合成的荧光碳点呈比较规则的球形,且分布均匀,通过统计120个纳米粒得到粒径分布柱形图,其粒径主要分布在1.4~5.0 nm范围内,平均粒径为2.9 nm。柠檬酸碳点在紫外灯下发出肉眼可见的明亮蓝色荧光(λex=312 nm)。

图1 荧光碳点的透射电子显微镜(TEM)图(a)及粒径统计分布图(b);插图是荧光碳点在紫外灯下的照片Fig.1 TEM image (a) and particle size histograms (b) of fluorescent carbon dots;Inset is the fluorescence picture under irradiation of ultraviolet lamp
2.3 荧光碳点的紫外-可见吸收和荧光发射光谱
图2为荧光碳点的紫外-可见吸收光谱和荧光发射光谱。从图中可以看到,用柠檬酸合成的荧光碳点在可见光区域内没有显著的吸收峰,但是在200~300 nm之间有明显吸收。其发射光谱随着激发波长红移而向长波方向移动,且荧光强度呈现先上升后下降的趋势,这与之前文献所报道[18]的相一致。其发射带较宽,从405 nm一直延伸到520 nm,说明柠檬酸荧光碳点可以发出多色的荧光。
2.4 荧光碳点的红外光谱
为了考察柠檬酸以及用其合成的荧光碳点官能团的变化,我们做了红外(IR)光谱表征。如图3所示,图中3 295 cm-1为O-H的伸缩振动吸收峰,而形成荧光碳点之后,O-H伸缩振动吸收峰由3 295 cm-1处的尖峰变成3 082 cm-1处的宽峰,这可能是由于所合成的荧光碳点更容易形成氢键的原因。1 757 cm-1和1 690 cm-1为C=O的伸缩振动吸收峰,因为柠檬酸分子本身含有两种类型的羧基,所以才会在红外光谱中出现两种类型的羰基伸缩振动吸收峰。1 402 cm-1为C-H的变形振动峰,1 217 cm-1为C-O的伸缩振动吸收峰,947 cm-1为二聚体O-H的变形振动吸收峰。红外光谱表征结果表明,合成的荧光碳点所含有的官能团与柠檬酸本身相似,表面含有羧基和羟基,这与我们之前所测得的Zeta电位为负值相符。

图2 荧光碳点的紫外-可见吸收和荧光发射光谱Fig.2 UV-Vis absorption and fluorescence emission spectra of fluorescent carbon dots
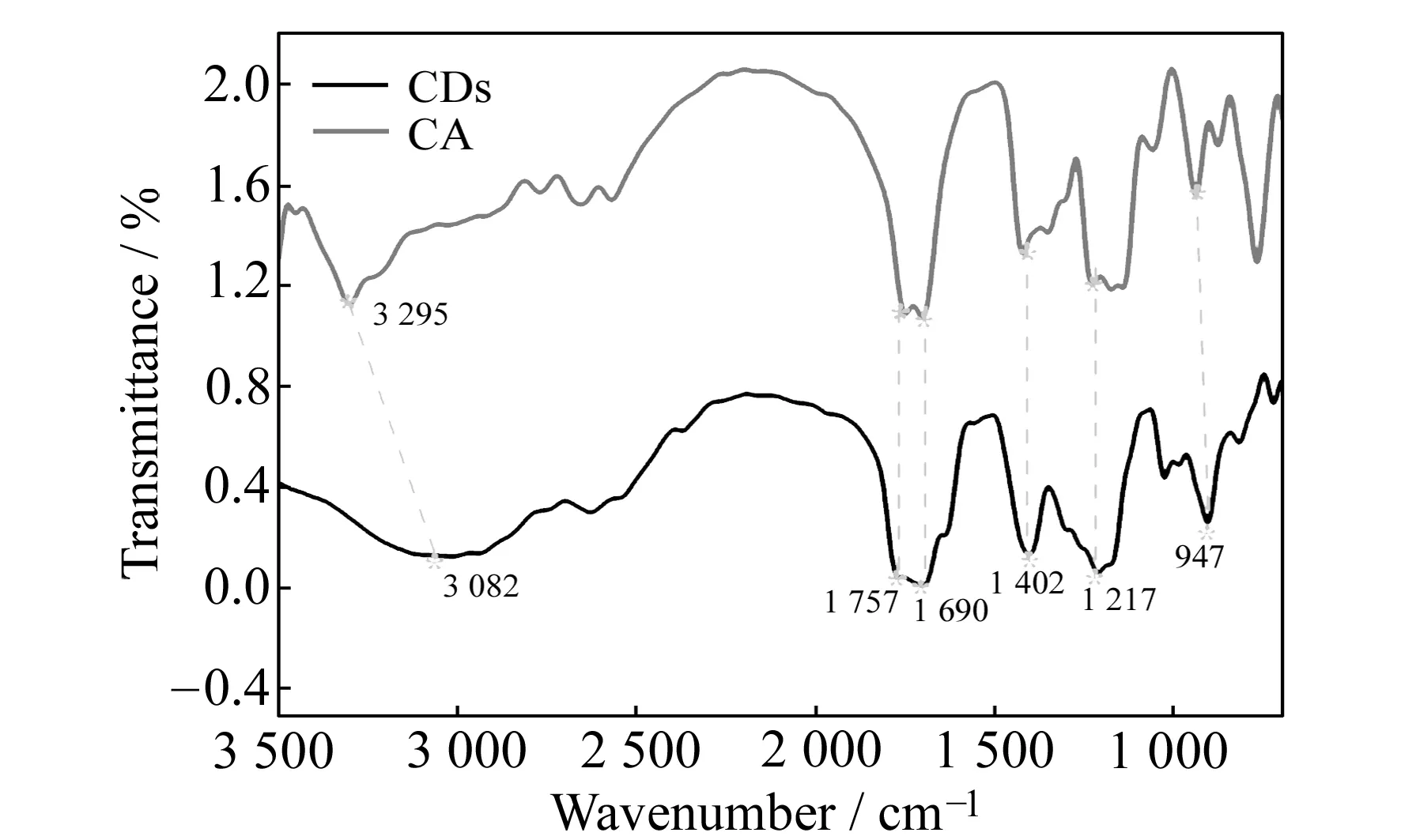
图3 荧光碳点和柠檬酸(CA)的红外光谱Fig.3 Infrared spectra of carbon dots and citric acid(CA)
2.5 荧光碳点的光稳定性
光稳定性是评价荧光材料的一项重要指标。图4为荧光碳点的光稳定性图,从图中可以看出,在405 nm光源激发,激发光源激光功率为13%,HV值为700的条件下,经过1 000 s照射后,荧光素的荧光强度猝灭为30%,而所合成荧光碳点的荧光强度猝灭仅为7%,说明柠檬酸荧光碳点具有较好的光稳定性。该结果与已经报道的草木灰[11]和天然糖类[22]制备的碳点的光稳定结果相一致。
2.6 荧光碳点的pH稳定性
图5是pH值对荧光碳点的影响。与利用活性炭合成的荧光碳点不同[23],从图5可以看出,所合成的荧光碳点在pH=2~11范围内具有良好的pH稳定性。这种性质与利用草木灰合成的荧光碳点相似[11],揭示出柠檬酸荧光碳点的激发辐射复合过程不受pH值变化的显著影响,预示该种荧光碳点可能在较宽泛的pH范围内具有很好的应用前景。

图4 荧光碳点的光稳定性Fig.4 Photostability of carbon dots
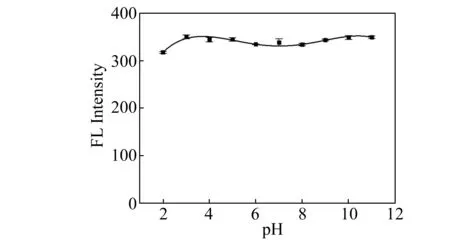
图5 pH对荧光碳点的影响Fig.5 The effect of pH to carbon dots(CDs) B-R buffer(pH=2-11).cCDs=1.73 mg/mL.λex=310 nm,λem=415 nm.

图6 荧光碳点对Fe(Ⅲ)(700 μmol/L)的选择性Fig.6 Selectivity of carbon dots towards Fe(Ⅲ)(700 μmol/L)
2.7 荧光碳点对Fe(Ⅲ)的选择性
图6是不同金属离子对荧光碳点荧光强度的影响。结果表明,除了Cu(Ⅱ)和Fe(Ⅱ)会对碳点的荧光强度产生一定的影响以外,其他的金属离子几乎都不会使荧光碳点的荧光发生改变,而向荧光碳点中加入700 μmol/L Fe(Ⅲ) 后,荧光碳点的荧光强度几乎完全被猝灭(荧光强度衰减80%),说明我们所合成的柠檬酸荧光碳点对Fe(Ⅲ) 具有较好的选择性。荧光碳点荧光猝灭的原因,根据文献的报道[24],可能是因为Fe(Ⅲ)可以与荧光碳点表面的羟基和羧基发生络合反应,从而产生非特异性相互作用,猝灭了荧光碳点的荧光所致。
2.8 线性范围与检出限
考察了不同浓度的Fe(Ⅲ)对柠檬酸荧光碳点荧光强度的影响。图7(A)是荧光滴定曲线,图7(B)是相对应的415 nm处的荧光强度与Fe(Ⅲ)浓度的关系。结果表明:随着F(Ⅲ)浓度的增加,荧光碳点的荧光强度逐渐降低,在100~500 μmol/L范围内,荧光碳点的荧光强度与Fe(Ⅲ)的浓度呈现良好的线性关系,线性相关系数为0.99,线性方程为:I=-0.20cFe(Ⅲ)+177.93。其中,cFe(Ⅲ)为Fe(Ⅲ)的浓度(μmol/L),I为荧光碳点在415 nm处的荧光强度, 计算得到检出限(3S0/k)为112.5 nmol/L。
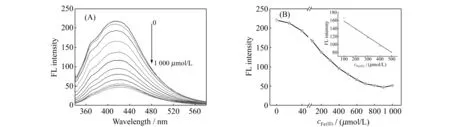
图7 (A) 加入不同浓度的Fe(Ⅲ)后荧光碳点的荧光光谱;(B) I415与Fe(Ⅲ)浓度的关系,插图为标准曲线Fig.7 (A) Fluorescence spectra of carbon dots with different concentrations of Fe(Ⅲ);(B) The correlation of Fe(Ⅲ) concentration and fluorescence intensity at 415 nm(I415),inset shows the standard curve
2.9 回收率测定
为了进一步证明荧光碳点可以用来检测Fe(Ⅲ),进行了自来水和去离子水样品的加入回收试验。选取250和300 μmol/L两个浓度点,结果如表2所示。从表中可以看出,无论在自来水还是去离子水中,所合成的荧光碳点对Fe(Ⅲ)的检测都有较好回收率,且相对标准偏差(RSD)都较小,说明这种方法具有较高的准确度和精确度。
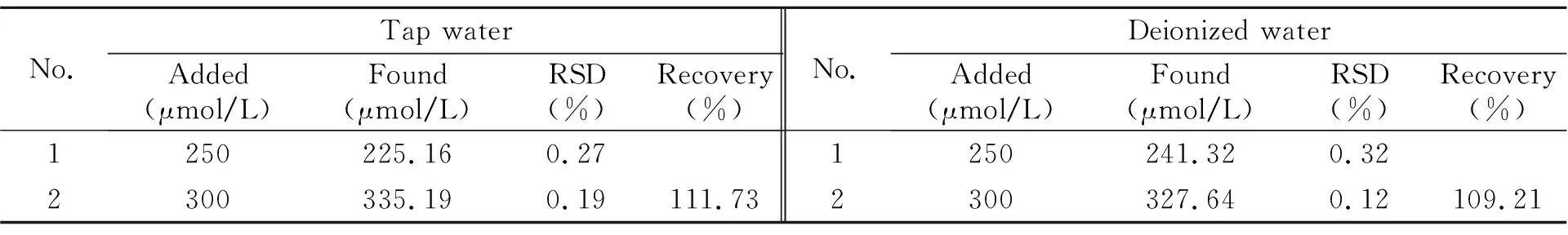
表2 自来水和去离子水中Fe(Ⅲ)的回收率试验结果(n=3)

图8 柠檬酸荧光碳点(CA-CDs)及对照组的B16-F10细胞成像图。最右列是明场(Bright-field)和蓝色激光(Ex=405 nm)及绿色激光(Ex=488 nm)激发下的叠加图。标尺为100 μmFig.8 Confocal fluorescence imaging of B16-F10 cells incubated with CA-CDs and medium(control).Right column is the overlay of bright-field and fluorescence image excited with 405 nm laser and 488 nm laser.Scale bar is 100 μm
2.10 细胞成像
荧光碳点因其优良的理化性质已经被应用于活细胞成像。如图8所示,将柠檬酸荧光碳点应用于小鼠黑色素瘤细胞的荧光成像。从图中可以看出柠檬酸荧光碳点跟B16-F10细胞共孵育12 h后,在405 nm和488 nm激发光下,细胞呈现明亮的蓝色或绿色荧光,而荧光信号主要分布在细胞质和细胞核内。相比较而言,未加入荧光碳点的对照组细胞在相同的拍摄条件下却没有发出任何荧光信号。说明所合成的柠檬酸荧光碳点成功地进入到了细胞内,且有部分荧光碳点进入到了细胞核内,同时可以发出多色荧光,实现了细胞的多色成像。
3 结论
本文以柠檬酸为原料,通过水热法合成了水溶性的荧光碳点,并用来检测水样中的Fe(Ⅲ)及细胞成像。实验结果表明,所合成的柠檬酸荧光碳点在310 nm处的量子产率为5.3%,粒径主要分布在1.4~5.0 nm范围内,平均粒径为2.9 nm。红外光谱和Zeta电位表明,在荧光碳点表面分布着-COOH和-OH等带负电荷的基团。由于表面的-COOH和-OH可以与Fe(Ⅲ)络合,使得碳点的荧光猝灭,从而可以用于Fe(Ⅲ)的检测。Fe(Ⅲ)浓度在100~500 μmol/L范围内,荧光碳点的荧光强度I与Fe(Ⅲ)浓度呈现良好的线性关系,检出限为112.5 nmol/L。该方法操作简单,选择性好,灵敏度高,而且有望用于实际水样中Fe(Ⅲ)的检测。细胞成像结果显示,所合成的柠檬酸荧光碳点可以同时进入到细胞质及细胞核内,并在不同的激发光源下发出多色的荧光,说明柠檬酸荧光碳点可以作为荧光探针用于细胞标记。

