丹皮酚在十二烷基苯磺酸钠现场自组装膜与离子液体复合修饰碳糊电极上的电化学性质及电分析方法
冯 芸, 张 瑞, 张 龙, 犹 卫, 彭 娟, 高作宁*
(宁夏大学化学化工学院,宁夏银川 750021)
丹皮酚(Paeonol,PN),化学名称为2-羟基-4甲氧基苯乙酮,是中药牡丹皮和徐长卿的主要活性成分,其药理活性广泛,具有解热、镇痛、镇静、抗炎、抗菌、抗过敏、催眠、降压、止血、免疫调节等作用[1]。目前PN的测定方法主要有反相高效液相色谱法[2]、气相色谱法[3]、近红外光谱法[4]、荧光光谱法[5]和电化学方法[6 - 10]等。其中,电化学方法中主要有毛细管电泳电化学检测[6]、超微铂电极[7]、Nafion/MWNTs复合修饰玻碳电极[8]、乙炔黑修饰玻碳电极[9]和金盘电极[10]等。而采用十二烷基苯磺酸钠(SDBS)现场自组装膜与离子液体N-丁基吡啶六氟磷酸盐([Bupy]PF6)复合修饰碳糊电极(SDBS-[Bupy]PF6/CPE),研究PN的电化学性质及电分析方法尚未见文献报道。
本文在前期工作[11 - 15]基础上,制备了SDBS-[Bupy]PF6/CPE,研究了PN在该修饰电极上的电化学性质,测定了PN在此电极上的电极过程动力学参数,据此建立了PN的电化学定量测定新方法。
1 实验部分
1.1 仪器与试剂
CHI660A电化学工作站(美国,CHI仪器公司),三电极体系:以CPE、[Bupy]PF6/CPE、SDBS/CPE和SDBS-[Bupy]PF6/CPE为工作电极,饱和甘汞电极(SCE)为参比电极,CHI115铂丝为辅助电极。
PN原料药(纯度99%,上海希匹吉生物有限公司);[Bupy]PF6(纯度99%,上海成捷化学有限公司);所用其它试剂均为分析纯。实验用水均为二次蒸馏水。
本文所涉及的电位均为相对于饱和甘汞电极(SCE)的电极电位。在电化学测试前于电解池中通入高纯氮除氧5 min。所有电化学测试均在室温下进行。
1.2 电极制作
裸碳糊电极(CPE)的制作参照文献方法[15]。将0.4 g [Bupy]PF6溶于0.4 mL N,N-二甲基甲酰胺(DMF)中,与1.2 g石墨粉混合均匀,研磨直至DMF完全挥发。按照与制作CPE相同的质量比例加入液体石蜡,研磨均匀,压入聚四氟乙烯管内,压实,在聚四氟乙烯管的另一端插入一根铜丝作导线,即制得离子液体修饰碳糊电极([Bupy]PF6/CPE)。将制得的电极在称量纸上抛光后,待用。
将所制得的CPE和[Bupy]PF6/CPE分别浸入含有1.0×10-4mol/L SDBS的0.10 mol/L磷酸盐缓冲液(PBS)中,搅拌80 s后静置10 s,即分别制得SDBS/CPE和SDBS-[Bupy]PF6/CPE。测试之前推出部分碳糊抛光后,按上述方法重新修饰。
2 结果与讨论
2.1 电极的电化学阻抗谱表征
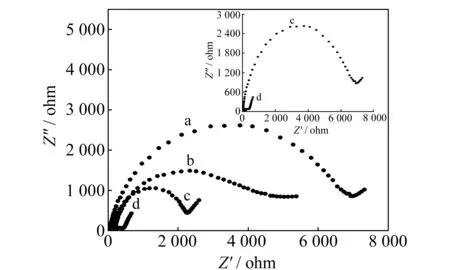
图1 不同电极的电化学阻抗谱图Fig.1 Electrochemical impedance spectroscopy of CPE(a),[Bupy]PF6/CPE(b),SDBS/CPE(c) and SDBS-[Bupy]PF6/CPE(d) in 5.0×10-3 mol/L mol/L KCl;Insert:electrochemical impedance spectrum of SDBS/CPE(c) and SDBS -[Bupy]PF6/CPE(d)
电化学阻抗反映了电极表面修饰过程中电极表面电阻变化信息[16]。图1分别为CPE、[Bupy]PF6/CPE、SDBS/CPE 和SDBS-[Bupy]PF6/CPE在5.0×10-3mol/L[Fe(CN)6]3-/4-+1.0 mol/L KCl溶液中的电化学交流阻抗谱图。结果表明,CPE(曲线a)在高频部分出现明显的半圆弧(半圆弧直径代表电极表面电荷转移电阻[17]),这是由于不导电液体石蜡的存在而降低了CPE导电能力,因此表现出较大的电阻。与曲线a相比,[Bupy]PF6/CPE(曲线b)和SDBS/CPE(曲线c)上的半圆弧直径明显小于曲线a,即二者电阻均小于CPE电阻,这可能是由于SDBS/CPE和[Bupy]PF6/CPE加速了 PN在电极与自组装膜之间的电子传递速率,从而促进了PN的电化学氧化还原反应,加快了电子传递速率。SDBS-[Bupy]PF6/CPE(曲线d)的半圆弧直径远远小于曲线a、b和c,该结果表明SDBS-[Bupy]PF6/CPE的表面电阻最小,这可能是由于表面活性剂SDBS和离子液体[Bupy]PF6二者的同时存在使SDBS-[Bupy]PF6/CPE具有更好的导电性,从而极大地提高了修饰电极的导电效率。
2.2 PN的伏安行为
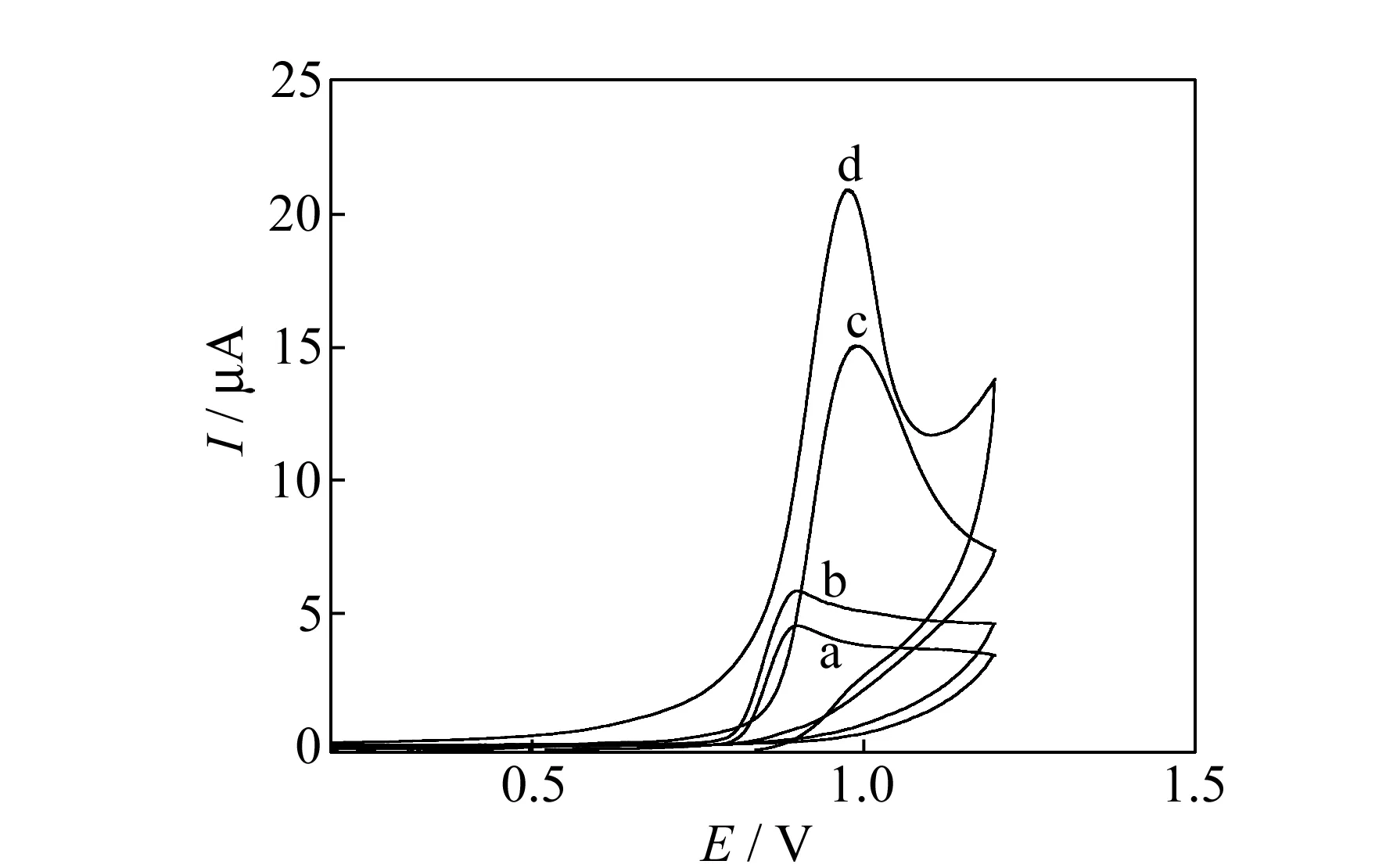
图2 3.0×10-4 mol/L PN在不同电极上的循环伏安(CV)曲线Fig.2 The CV curves of 3.0×10-4 mol/L PN in 0.10 mol/L PBS at CPE(a),[Bupy]PF6/CPE(b),SDBS/CPE(c) and SDBS-[Bupy]PF6/CPE(d)Scan rate:50 mV/s.
在电位窗口0.0~1.2 V及0.10 mol/L PBS中以50 mV/s的扫描速度得到3.0×10-4mol/L PN在CPE、[Bupy]PF6/CPE、SDBS/CPE和SDBS-[Bupy]PF6/CPE上的循环伏安(CV)曲线(图2)。图中曲线a表明PN在CPE上的电极反应是一不可逆电化学氧化过程。实验结果表明,与CPE相比,PN在[Bupy]PF6/CPE上的氧化峰电位略有负移,在SDBS/CPE上的氧化峰电位略有正移,氧化峰电流都明显增大。而与曲线a、b、c相比,PN在SDBS-[Bupy]PF6/CPE上PN氧化峰电位Ep略有正移,氧化峰电流Ip明显增大(曲线d)。表明SDBS-[Bupy]PF6/CPE对PN电化学氧化具有良好的促进作用。该促进作用可能基于以下原因:其一是SDBS作为一种阴离子表面活性剂,在电极表面易形成膜结构,使PN在电极表面的浓度增加,提高了其电极响应[18],并且它可以有效地吸附在碳糊电极表面,与碳糊中的液体石蜡通过表面相互作用,进而改变溶液与电极界面的结构,促进PN在电极表面电荷的传递;其二是[Bupy]PF6具有良好的导电性,能够有效地提高修饰电极的导电效率[19]。因此是二者的协同作用使SDBS-[Bupy]PF6/CPE对PN具有良好的促进作用。
在10~1 000 mV/s扫描速度范围内,运用CV法研究了扫速对PN伏安行为的影响。实验结果表明,PN在SDBS-[Bupy]PF6/CPE上的氧化峰电流Ip与扫描速度平方根v1/2呈良好线性关系,表明PN在SDBS-[Bupy]PF6/CPE上电化学氧化反应是一受扩散控制的不可逆电极反应过程。
2.3 实验条件的影响
考察了SDBS浓度对PN在SDBS -[Bupy]PF6/CPE上氧化峰电流的影响。实验结果表明,当SDBS浓度由1.0×10-5mol/L增至1.0×10-4mol/L时氧化峰电流Ip达到最大值,且峰形较好,再增加SDBS浓度,Ip基本保持不变,所以选择SDBS浓度为1.0×10-4mol/L。
考察了自组装时间对PN在SDBS-[Bupy]PF6/CPE上的氧化峰电流影响,当自组装时间t=80 s时氧化峰电流达到最大值,再增加自组装时间,Ip基本保持不变,因此选择自组装时间为80 s后静止10 s。
在电位窗口0.0~1.2 V,以50 mV/s扫速,分别以0.10 mol/L NaAc、Na2SO4、NaClO4、Na2HPO4、NaH2PO4、PBS(Na2HPO4-NaH2PO4)和B-R(Britton-Robinson)缓冲溶液为支持电解质进行CV测试。结果表明,PN在PBS中具有良好的电化学行为,因此选用pH=6.0的PBS为支持电解质。在pH=2.0~11.0范围内考察了介质pH对PN伏安行为的影响。结果表明,在pH=2.0~11.0范围内,PN氧化峰电位Ep随pH增加而减小,且氧化峰电位Ep与pH呈良好线性关系,其线性方程为:Ep(mV)=1205-51/pH,R=0.9950,斜率为51 mV/pH。依据能斯特方程:Ep=E-59(m/n)pH,得到m/n≈1,表明参与PN氧化过程的质子数与电子数相等。在pH=2.0~4.0范围内,PN氧化峰电流Ip随pH增加而减小,在pH=4.0~5.5范围内,氧化峰电流Ip基本保持不变,在pH=5.5~11.0范围内,氧化峰电流Ip随着pH增加逐渐降低。
在电位窗口0.0~1.2 V,及扫描速度10~1 000 mV/s范围内对PN在SDBS-[Bupy]PF6/CPE上进行CV测试。结果表明PN氧化峰电位Ep与logv呈良好线性关系,其线性方程为:Ep(mV)=822+100logv(v,mV/s),R=0.9890。
对于完全不可逆电极反应过程,电化学氧化峰电位与扫描速度关系符合下述方程[20]:
(1)
其中,Eo′为标准电极电位,ko为标准反应速率常数,DR为扩散系数,α为电荷转移系数,F为法拉第常数96485(C/mol)。
通常对于完全不可逆电极过程α假定为0.5[21],由线性方程和式(1)可得0.5×2.303(RT/αnF)=0.1,由此计算得到电子转移数n≈1。由pH与氧化峰电位的关系可知PN氧化过程的电子数和质子数相等,可以得到PN在SDBS-[Bupy]PF6/CPE上电化学氧化过程是1个电子和1个质子参与的不可逆电化学氧化过程。
平板电极上可逆电化学反应的电流响应遵循如下关系式[22]:
(2)
2.4 电分析方法应用

图3 3.0×10-4 mol/L PN不同电极上的方波伏安曲线Fig.3 SWV curves of 3.0×10-4 mol/L PN at CPE(a),[Bupy]PF6/CPE(b),SDBS/CPE(c) and SDBS -[Bupy]PF6/CPE(d)
2.4.1PN的方波伏安行为在优化的实验条件(振幅10 mV,电势增量6 mV,频率60 Hz)下,在0.0~1.2 V电位窗口及0.10 mol/L PBS中采用方波伏安法(SWV),考察了3.0×10-4mol/L PN在CPE、[Bupy]PF6/CPE、SDBS/CPE和SDBS-[Bupy]PF6/CPE上的方波伏安行为(图3)。结果表明,与CPE相比,PN在[Bupy]PF6/CPE氧化峰电位略有负移,PN在SDBS/CPE氧化峰电位略有正移,而氧化峰电流都增大。与曲线a、b相比,PN在SDBS-[Bupy]PF6/CPE上PN氧化峰电位Ep略有正移,氧化峰电流Ip显著增大(曲线d)。而与曲线c相比,PN在SDBS-[Bupy]PF6/CPE上PN氧化峰电位Ep基本不变,氧化峰电流Ip明显增大。
在上述优化实验条件下,用SWV法对PN进行直接测定。结果表明,PN在SDBS -[Bupy]PF6/CPE上氧化峰电流(Ip)与其浓度在5.0×10-5~3.8×10-4mol/L范围内呈良好线性关系,线性方程为:Ip(A)=-5.715+189.394c(10-3mol/L),R=0.9980,检测限(S/N=3)为2.0×10-6mol/L。
2.4.3电极重现性与稳定性用同一支修饰电极对3.0×10-4mol/L PN平行测定10次,相对标准偏差(RSD)为2.9%,将电极在4 ℃下保存四周后进行测定,其RSD为3.0%,表明SDBS-[Bupy]PF6/CPE具有良好的重现性和稳定性。
2.4.4样品测定准确称取一定量PN原料药,用二次蒸馏水溶解后定容至100 mL,运用SWV法进行电化学定量测定,然后加入已知量PN标准品进行回收率测定,测定结果见表1。
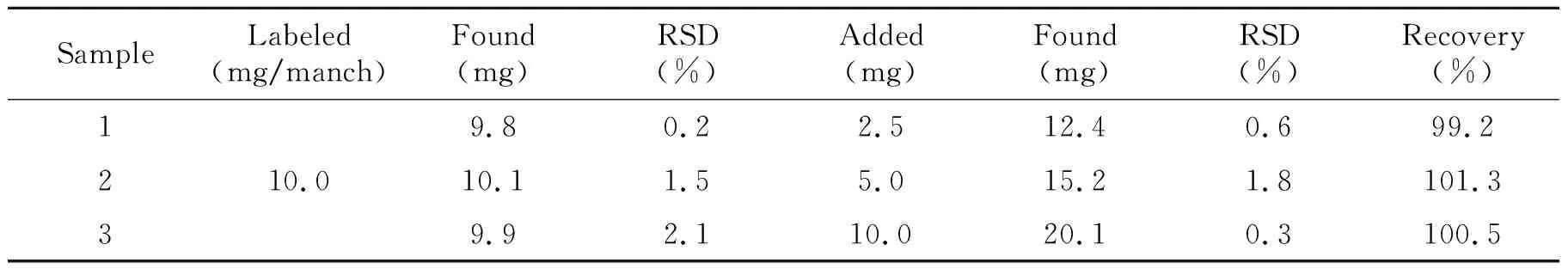
表1 样品测定结果(n=6)
由表1样品测定结果可看出,样品测定结果的RSD在0.2%~2.1%之间,加标回收率在99.2%~101.3%范围。说明本方法的精密度和准确度符合定量测定要求。
3 结论
用CV、CA和SWV等方法研究了PN在CPE、[Bupy]PF6/CPE、SDBS/CPE和SDBS-[Bupy]PF6/CPE上的电化学行为。实验结果表明,PN在SDBS-[Bupy]PF6/CPE上出现了一敏锐的不可逆氧化峰,与CPE相比氧化峰电位基本不变,氧化峰电流显著增大,表明SDBS-[Bupy]PF6/CPE对PN电化学氧化具有良好的促进作用。同时用CA法分别测定了PN在CPE、[Bupy]PF6/CPE、SDBS/CPE和SDBS-[Bupy]PF6/CPE上的电极过程动力学参数,并据此建立了样品丹皮酚片中PN含量的电化学定量测定新方法。

