HPLC测定果汁饮料中两种邻苯二甲酸酯
李巧玲,魏冠棉,2,李劭彤,刘峰
(1.河北科技大学生物科学与工程学院,河北石家庄050018;2.江南大学食品学院,江苏无锡214122)
HPLC测定果汁饮料中两种邻苯二甲酸酯
李巧玲1,魏冠棉1,2,李劭彤1,刘峰1
(1.河北科技大学生物科学与工程学院,河北石家庄050018;2.江南大学食品学院,江苏无锡214122)
建立了高效液相色谱(HPLC)对果汁饮料中邻苯二甲酸二乙酯(DEP)和邻苯二甲酸二丁酯(DBP)进行定性和定量分析的方法。果汁饮料样品经正己烷溶解、超声波辅助提取、高速离心、过SPE小柱等预处理后,用HPLC进行定性和定量分析。结果表明:DEP和DBP在1.0 mg/L~40 mg/L浓度范围内线性关系良好,线性相关系数(R2)均大于0.999,3个水平的样品添加回收率为88.3%~99.9%,相对标准偏差在0.94%~1.95%之间,2种目标化合物的检出限分别为0.1 mg/L和0.05 mg/L。
高效液相色谱;邻苯二甲酸二乙酯;邻苯二甲酸二丁酯;果汁饮料
近两年,随着塑化剂在一些饮料、酒中的不断检出,塑化剂对食品的污染引起了人们强烈关注。塑化剂是一种能够提高材料柔软性的添加剂,它通过削弱聚合物分子之间的范德华力,增加了聚合物分子链的移动性,降低了聚合物分子链的结晶性,从而增加了聚合物的塑性[1]。塑化剂对食物的污染主要来自2个方面:一方面是由于食品包装材料(例如聚氯乙烯)中添加了塑化剂,在同食物进行接触的过程中,包装材料中的塑化剂迁移进入食物中[2];另一方面是非法添加入食品中,例如,代替起云剂。
塑化剂种类繁多,使用最普遍的是邻苯二甲酸酯类(phthalie acid esters,PAEs)化合物。邻苯二甲酸酯类化合物是可用于食品包装材料的增塑剂。《食品容器、包装材料用添加剂使用卫生标准》(GB9685-2008)中严格规定了该类塑化剂在食品及食品添加剂中的最大残留量,其中邻苯二甲酸二(2-乙基己)酯(DEHP)、邻苯二甲酸异壬酯(DINP)和邻苯二甲酸二丁酯(DBP)最大残留量分别为1.5、9.0 mg/kg和0.3 mg/kg[3]。邻苯二甲酸酯类塑化剂都具有类雌激素作用[4]。研究表明,邻苯二甲酸酯类进入人体后与相应激素受体结合,影响生物体内激素的正常分泌,使得人体生殖功能产生障碍、发育迟缓,甚至引发恶性肿瘤,产生致畸、致癌和致突变性以及免疫抑制性[5-10]。
《食品中邻苯二甲酸酯的测定》(GB/T 21911-2008)中规定了气相色谱-质谱联用法为食品中邻苯二甲酸酯类化合物的检测方法。尽管用高效液相色谱法测定塑化剂成分已有研究[11-17],但是对于饮料中塑化剂含量的测定报导较少。本文拟采用超声波辅助正己烷提取、SPE小柱净化、富集,高效液相色谱检测的方法测定果汁饮料中DEP和DBP的含量,以期了解饮料中受PAEs污染的程度,找到一种检测成本低,适用于各基层单位的PAEs塑化剂的检测方法,从而完善饮料中塑化剂的检测手段。
1 材料与方法
1.1 材料、试剂与仪器
塑料瓶装安梨汁饮料600 mL,购买于超市。
实验用水为超纯水;甲醇(色谱纯),正己烷、丙酮、无水硫酸钠:均为分析纯,天津康科德科技有限公司;邻苯二甲酸二乙酯和邻苯二甲酸二丁酯标品:河北省食品质量监督检验研究院提供;0.45 μm有机相微孔滤膜:天津市沃尔孚科技发展有限公司;高纯氮气:纯度大于99.999%。
无水硫酸钠需在450℃下灼烧4 h~6 h除去含有的结晶水;正己烷需要重蒸处理。
1.2 仪器与设备
LC-20A型高效液相色谱仪(配有SPD-20A紫外检测器、7725i手动进样器、C70-1AS柱温箱、LC-solution色谱工作站):日本Shimadzu公司;KUDOSSK5200LHC超声处理器:上海科导超声仪器有限公司;XW-80A涡旋混合器:苏州江东精密仪器有限公司;超纯水制备装置:上海康雷分析仪器有限公司;高速离心机(LG16-A):北京雷勃尔有限公司;Welch C18SPE固相萃取小柱(20 mg/6 mL,5PK):Welch Material,Inc.公司;氮气吹干仪:上海济成分析仪器有限公司。
1.3 方法
1.3.1 溶液的配制
混合标准溶液:称取DEP和DBP各1.000 0 g,放入同一100 mL容量瓶中,用甲醇溶解并稀释至刻度,摇匀,配成浓度为10 g/L的混合标准溶液。用移液管移取5 mL的10 g/L混合标准溶液于100 mL容量瓶中,用甲醇定容至刻度,混匀,配成浓度为0.5 g/L的混合标准溶液,于4℃冰箱中冷藏备用。
1.3.2 标准曲线的绘制
用移液管分别移取0.1、0.5、1.0、2.0、4.0 mL的0.5 g/L混合标准溶液放于不同的50 mL容量瓶中,用甲醇定容至刻度,混匀,配成浓度为1、5、10、20、40 mg/L的混合标准溶液。
将配好的5种浓度的混合标准储备液各取20 μL按下述色谱条件进样分析。以标准样品的质量浓度为横坐标、相应的峰面积为纵坐标,得到DEP和DBP的标准曲线及相关系数。
1.3.3 样品的前处理
取5.0 g样品于干燥的玻璃离心管(避免用塑料的实验仪器)中,加入正己烷5.0 mL,旋涡振荡混合2 min,超声处理10 min后,以7 000 r/min的转速离心5 min,取上清液移取至玻璃试管中。离心管中的残存物再经上述过程提取1次,然后合并上清液,用氮气将其吹至5 mL,等待净化。
向Welch C18 SPE柱中依次加入5 mL丙酮、5 mL正己烷淋洗SPE柱后,再向柱子中加入1.0 g无水硫酸钠,用洗耳球轻轻敲SPE柱,使无水硫酸钠铺平,加入待净化液,流速控制在1 mL/min,依次加入5 mL丙酮、5 mL丙酮-正己烷(1∶25,体积比)洗脱液进行洗脱,收集洗脱液,然后用氮气吹干,再用1.5 mL正己烷溶解,过0.45 μm有机滤膜过滤后,供HPLC分析。
1.3.4 色谱条件
色谱柱为Eclipse XDB-C18柱(150 mm×4.6 mm,5 μm);柱温25℃;流速1.0 mL/min;检测波长227 nm;进样量20 μL;流动相为甲醇-水体系(85∶15,体积比)。
1.3.5 样品的测定
将前处理好的样品在1.3.4的色谱条件下平行测定5次,根据标准品的色谱图,对试样中的DEP和DBP的含量进行定性和定量分析。
2 结果与分析
2.1 提取剂选择
实验分别考察了用甲醇、石油醚、正己烷等溶剂作为提取剂,提取样品中的塑化剂成分。从HPLC检测的结果来看,甲醇作为提取剂时,饮料样品中没有检测出DEP和DBP,见图1。
而对于相同样品用正己烷或石油醚作为提取剂后,高效液相色谱的测定结果表明,饮料中不但存在DEP和DBP,而且正己烷提取的样品在高效液相色谱图上杂质峰少,效果较为理想,见图2。因此,选用正己烷作为提取剂。
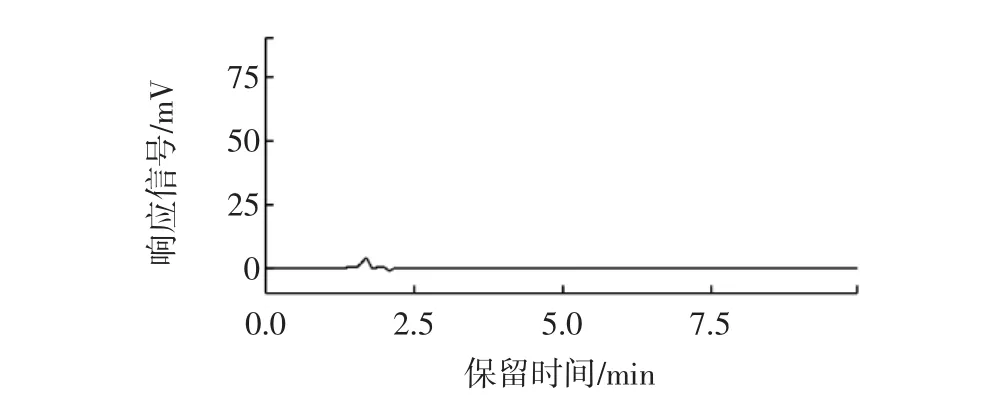
图1 甲醇做提取剂的高效液相色谱图Fig.1 HPLC chromatogram of methanol extract
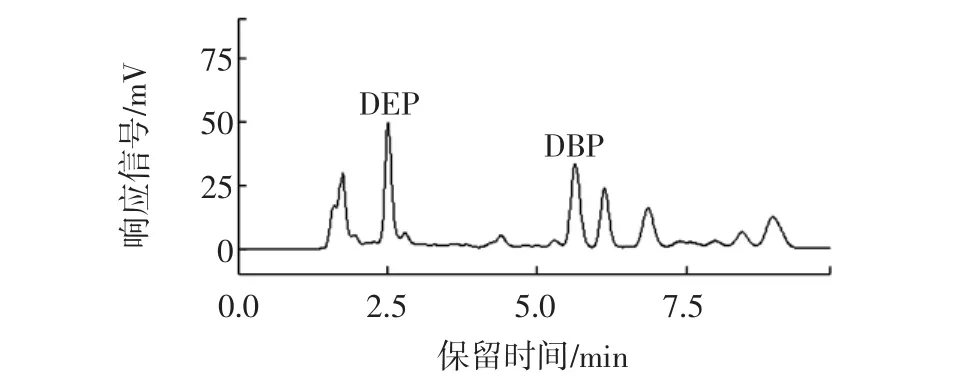
图2 正己烷做提取剂的高效液相色谱图Fig.2 HPLC chromatogram of n-hexane extract
2.2 色谱条件的优化
由于PAEs是一类极性较弱的化合物,其结构中含有苯环,所以在选择色谱柱时应当选择非极性或弱极性的固定相,结合本实验室现有的条件,故以Eclipse XDB-C18为本研究分析所用色谱柱。
邻苯二甲酸酯类物质在227、245 nm和280 nm处有均有特征吸收峰,由于DEP和DBP在227 nm处的吸收强度优于245 nm和280 nm处,因此选择227 nm作为本研究的检测波长,这样得到的检出限较低。
以甲醇—水体系作为流动相,流动相的配比能显著地影响分离效果。当甲醇—水流动相体积比为90∶10时,尽管可以在4分钟内完成DEP和DBP的分离,但DEP有拖尾现象。之后对V甲醇∶V水分别为75∶15、80∶20、85∶15的流动相亦进行了详细的探讨,发现V甲醇∶V水=85∶15时,DEP和DBP两个峰的分离效果最好,如图3所示,故选择流动相甲醇—水体系配比为85∶15。
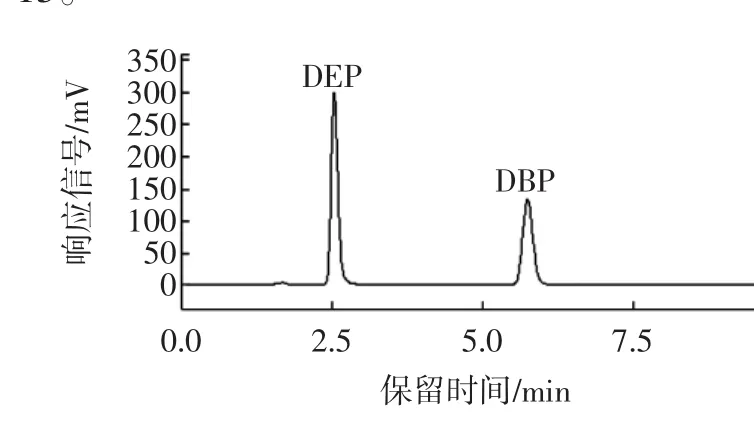
图340 mg/mL DBP和DEP混合标准溶液的高效液相色谱图Fig.3 HPLC chromatogram of 40 mg/mL DBP and DEP standard solution
2.3 混合标准品的标准曲线和检出限
按1.3.4的色谱条件,分别取20 μL的1、5、10、 20、40 mg/L的混合标准溶液进行测定。分别以DEP和DBP的质量浓度为横坐标,峰面积为纵坐标进行线性回归,得到的回归方程及相关系数见表1。

表1 DBP和DEP的回归方程、相关系数和检出限Table 1Regression equations,correlation coefficients and detection limits of DEP and DBP
DEP和DBP在1 mg/L~40 mg/L范围内峰面积与浓度呈现良好的线性关系,相关系数R2均大于0.999。根据3倍噪音的峰面积响应值和方法回收率,得到DEP和DBP的最低检出限[19]。测定表明,DEP的检出限为0.1 mg/L,DBP的检出限为0.05 mg/L,此数值低于国标《食品中邻苯二甲酸酯的测定》中各邻苯二甲酸酯化合物的检出限(1.5 mg/kg),可以满足对饮料中DBP和DEP的检测分析。
2.4 方法回收率及精密度的测定
本试验分别取5.0 g的饮料样品3份,DEP和DBP的添加水平分别是5、10、20 mg/L,按照前述样品前处理方法及检测条件分别测定,同时做空白样品2份,每份样品检测6次,确定加标回收率。测得的回收率及相对标准偏差如表2所示。
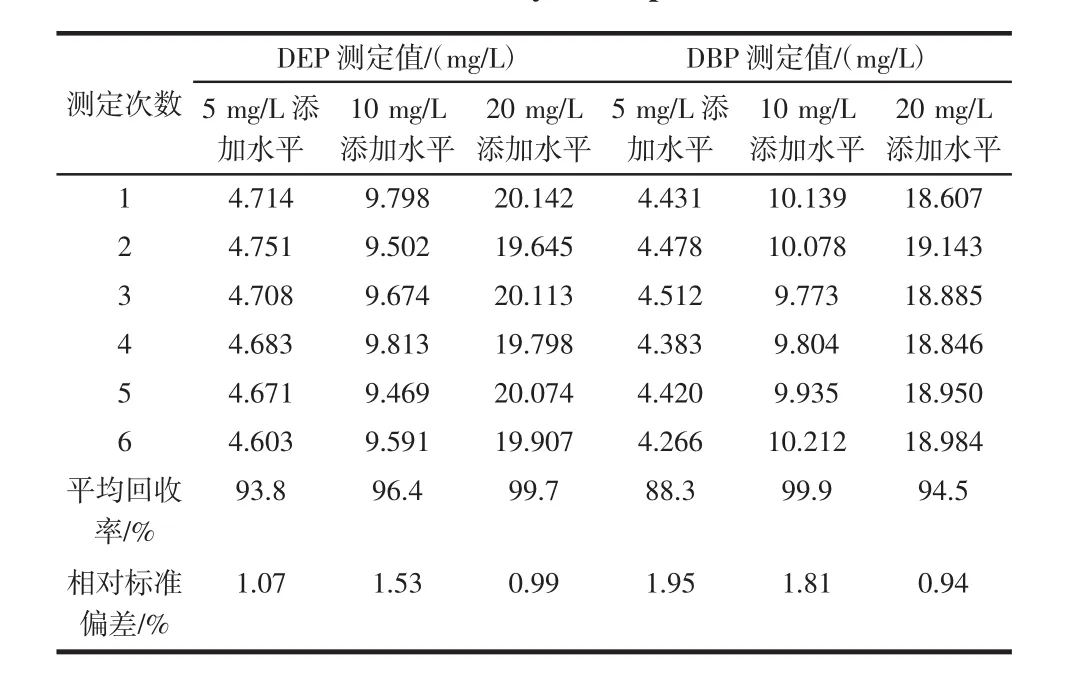
表2 样品的加标回收率(n=6)Table 2Recovery of sample(n=6)
结果表明,饮料样品在3个添加水平下,DEP和DBP的回收率在88.3%~99.9%之间,相对标准偏差在0.94%~1.95%之间,说明该方法准确度和精密度良好,能够满足样品测试的要求。
2.5 饮料中DEP和DBP的含量测定
饮料中DEP和DBP的含量测定的高效液相色谱图见图4。
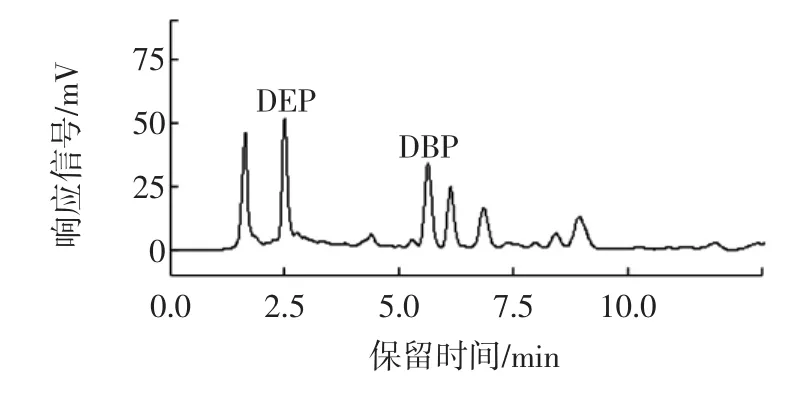
图4 饮料样品的高效液相色谱图Fig.4 HPLC chromatogram of beverage sample
由图4可知,DEP的保留时间在2.6 min左右,DBP的保留时间在5.7 min左右。图4同图3相对照可知,饮料样品中含有DEP和DBP。根据表1的相关方程,通过外标法计算得出饮料样品中DEP和DBP的含量分别为2.713 mg/kg和4.628 mg/kg。这表明饮料在生产加工或储运过程中可能被PAEs类增塑剂污染。
2011年6月国家卫生部办公厅发布了《卫生部办公厅关于通报食品及食品添加剂中邻苯二甲酸酯类物质最大残留量的函》(卫办监督函[2011]551号),规定食品、食品添加剂中DBP最大残留量为0.3 mg/kg,DEP的限量在我国并没有明确规定。由此可以看出本实验所用样品中DBP的含量已经超出了国家规定限量值。分析原因可能为:一方面是饮料在生产加工过程中被PAEs类增塑剂污染;另一方面是包装容器中的PAE s向饮料中的迁移引起的。
3 结论
该研究表明,饮料样品经超声波辅助正己烷提取、SPE小柱净化、富集等预处理后,可以用高效液相色谱法测定样品中的邻苯二甲酸酯类塑化剂。该方法的回收率高、重现性好、检出限较低,操作简单,可推广应用于一般单位检测饮料中邻苯二甲酸酯类物质。
从对饮料样品的检测结果来看,饮料中塑化剂的含量超过了国家标准要求的限量。造成塑化剂超标的原因有待于进一步探索。由于塑化剂从包装材料迁移进入食品中与食品的储存时间、储存温度、包装材料的成分等因素关系密切,建议可从上述几个方面对包装材料中塑化剂的迁移情况进行深入探讨,为制定塑料包装饮料的储存条件提供基础数据。
[1]刘超,李来生,许丽丽,等.HPLC测定一次性塑料用品中邻苯二甲酸酯类增塑剂[J].化学研究与应用,2007,19(7):834-837
[2]王东辉,李懿睿,田玉平,等.食品包装用塑料中八种邻苯二甲酸酯的检测方法[J].氨基酸与生物资源,2010,34(3):83-86
[3]中华人民共和国卫生部,中国国家标准化管理委员会.GB9685-2008.食品容器、包装材料用添加剂使用卫生标准.北京:中国标准出版社,2008
[4]刘风云.塑化剂的应用及危害[J].广东化学,2011,38(11):77-78
[5]陈洪涛,王力清,黄翠莉,等.邻苯二甲酸酯毒理学研究进展[J].食品与机械,2012,28(5):251-254
[6]Swan S H,Main K M,Liu F,et al.Decrease in anogenital distance among male infants with prenatal phthalate exposure[J].Environ Health Persp,2005,113:1056-1061
[7]刘晓毅,蒋可心,石维妮.国内外食品接触材料中邻苯二甲酸酯类塑化剂迁移量对比分析[J].食品工业科技,2011,32(10):397-399,446
[8]Larsen S T,Hansen J S,Hansen E K,et al.Airway inflammation and adjuvant effect after repeated airborne exposures to di-(2-ethylhexyl)phthalate and ovalbumin in BALB/c mice[J].Toxicology, 2007,235:119-129
[9]陈文婕,戴红,陈敏,等.邻苯二甲酸二乙基己酯(DEHP)对小白鼠肝脏毒性及脂质过氧化损伤[J].生态毒理学报,2012,7(1):93-98
[10]Matthias Wittassek,Angerer,Marike Kolossa-Gehring,et al.Fetal exposure to phthalates[J].Int J Hyg Environ Health,2009,212:492-498
[11]王丽霞,王明林.高效液相色谱法测定塑料袋装食品中的邻苯二甲酸酯[J].分析实验室,2007,26(9):13-16
[12]王美丽,陈海婷,张会娜,等.高效液相色谱法测定肉制食品中五种邻苯二甲酸酯[J].分析实验室,2009,28(6):49-52
[13]王少杰,孟雨吟,李秋顺,等.高效液相色谱法测定蔬菜中的邻苯二甲酸二丁酯残留[J].山东农业科学,2012,44(1):112-114
[14]佟晓波,李莹,矫筱曼,等.HPLC法测定化妆品中十六种邻苯二甲酸酯类化合物[J].香精香料化妆品,2012,3(6):33-38
[15]王美丽,陈海婷,张会娜,等.高效液相色谱测定肉制食品中的五种邻苯二甲酸酯[J].分析实验室,2009,28(6):49-50
[16]蔡全英,莫测辉,李云辉,等.广州、深圳地区蔬菜生产基地土壤中邻苯二甲酸酯(PAEs)研究[J].生态学报,2005,25(2):283
[17]张磊,吴青,梁建华,等.高效液相色谱法同时测定食品塑料包装材料中8种邻苯二甲酸酯的含量[J].食品科学,2012,33(20): 184-188
[18]陈再洁,杨晓燕,李小侠,等.HPLC同时测定欧盟限用6种塑化剂的含量[J].广州化工,2010,38(1):151-153
[19]朱明华.仪器分析[M].第三版.北京:高等教育出版社,2007:44
Determination of Two Phthalic Acid Esters in Fruit Beverage by High Performance Liquid Chromatography
LI Qiao-ling1,WEI Guan-mian1,2,LI Shao-tong1,LIU Feng1
(1.College of Bioscience and Bioengineering,Hebei University of Science and Technology,Shijiazhuang 050018,Hebei,China;2.School of Food Science and Technology,Jiangnan University,Wuxi 214122,Jiangsu,China)
A method based on high performance liquid chromatography(HPLC)was developed for the determination of diethyl phthalate(DEP)and dibutyl phthalate(DBP)in fruit beverage.The sample was dissolved by n-hexane,extracted by ultrasonic wave,centrifuged by the high-speed centrifuge,next was purified with Welch C18 SPE column,then identified and quantified by HPLC.The results showed that linearity of response over 2 phthalic acid esters was good from 1.0 to 40.0 mg/L with correlation coefficients higher than 0.999.The average recoveries ranged from 88.3%to 99.9%for two compounds at three different spiked levels. The relative standard deviations were in the range of 0.94%-1.95%.The detection limits of DEP and DBP were 0.1 mg/L and 0.05 mg/L,respectively.
high performance liquid chromatography;diethyl phthalate;dibutyl phthalate;fruit beverage
2013-12-23
10.3969/j.issn.1005-6521.2015.02.027
国家科技支撑计划(2012BAD29B04-1-1);河北省科技支撑项目(12220402D)
李巧玲(1973—),女(汉),教授,博士后,研究方向:食品安全与检测。

