螺旋CT对肺部1cm以下孤立局限性磨玻璃密度结节的诊断价值
韩砆石, 孙希文
(同济大学附属肺科医院影像科,上海 200433)
·临床研究·
螺旋CT对肺部1cm以下孤立局限性磨玻璃密度结节的诊断价值
韩砆石, 孙希文
(同济大学附属肺科医院影像科,上海 200433)
目的 探讨多排螺旋CT高分辨率扫描对肺部1cm以下孤立局限性磨玻璃密度结节(focal ground-glass opacity, fGGO)的诊断及鉴别诊断。方法 分析经手术病理证实93例肺部1cm以下孤立性fGGO结节的多排螺旋CT征象,其中: 浸润性腺癌15例,微浸润腺癌19例,浸润前病变52例,炎性病变7例。观察病灶形态、大小、边缘、内部结构及临近改变等,评估fGGO结节内实变比例。将观测数据与病理结果进行对照,并采用χ2检验进行统计学分析。结果 1cm以下fGGO结节出现分叶征、毛刺及血管增粗这3种CT征象在浸润性腺癌与浸润前病变之间差异有统计学意义(χ2分别为12.678、6.043、7.147,P值均<0.05)。随病灶直径增大,fGGO由浸润前病变到浸润性腺癌发生率增加。随着病灶中实变增多,fGGO由浸润前病变到浸润性腺癌发生率增加,小于1cm纯磨玻璃密度结节无浸润性腺癌,而炎性病灶缺少特征性。结论 多层螺旋CT可根据fGGO大小、有无实变,并参照病灶边缘分叶、毛刺以及血管有无增粗,对浸润性腺癌与浸润前病变的诊断及鉴别诊断有一定价值。
肺肿瘤; 体层摄影术,X线计算机; 不典型腺瘤样增生
近年来,多层螺旋CT(multi-slice spiral CT, MSCT)高分辨率扫描对孤立性肺结节(solitary pulmonary nodule, SPN)的检出率明显增多,文献报道多为3cm以下的局限性磨玻璃密度结节,而对1cm 以下GGO的CT诊断价值研究较少。病灶越小发展成浸润性腺癌几率越低,治疗的预后越好。本研究收集经手术病理证实1cm及以下肺内孤立fGGO结节93例,探讨MSCT高分辨率扫描对1cm以下肺内孤立fGGO病灶的诊断及鉴别诊断。
1 资料与方法
1.1 一般资料
入选同济大学附属肺科医院2006年6月至2013年12月经手术病理证实直径≤1cm肺内孤立fGGO结节93例。其中男性21例,女72例。年龄25~70岁,平均年龄(51±10)岁。临床症状: 咳嗽25例、咳痰13例、胸痛6例、胸闷3例、痰中带血5例、发热5例、无症状体检58例;吸烟史8例。术前随访6例,随访时间3~24个月,平均随访时间为16个月。术后病理诊断: 浸润性腺癌15例(高分化腺癌12例、高中分化腺癌3例),微浸润性腺癌(minimally invasive adenocarcinoma, MIA)19例,浸润前病变52例(原位癌19例、不典型腺瘤样增生33例),炎性病变7例。
1.2 检查方法
检查采用Philips 40排Briliance CT扫描仪;所有患者取仰卧位,横断面扫描;定位扫描成像确定扫描范围,包括自胸廓入口到横膈;扫描层面角度: 与扫描层面90°,扫描机架0°;扫描显示(FOV): 30~50cm;扫面层厚: <1mm;螺旋扫描,螺距1;矩阵: 512x512;曝光条件: 120kv,<50mA;扫描图像观察: 纵隔窗(窗位: 30~50HU;窗宽: 250~350HU);肺窗(窗位: -450~-600HU;窗宽: 1500~2000HU)。
1.3 图像处理及分析方法
CT扫描结束后将图像上传到后处理PACS工作站,进行MPR矢状面、冠状面重建,多角度显示病灶形态、直径,病灶与胸膜、气管及血管的关系。
所有fGGO按如下方法进行判定。(1) fGGO的类型: MSCT图像上有实性成分的判定为混合型GGO(mixed ground glass opacity, mGGO),其余为纯GGO(pure ground glass opacity, pGGO)。(2) fGGO直径: 在HRCT图像上fGGO的最大横断面直径。(3) fGGO量化分型: 按照fGGO内实变率分型,分为0~4型,0型实变率为0,1型实变率为1%~25%,2型实变率为26%~50%,3型实变率为51%~75%,4型实变率为76%~100%,含有实变的1~4型又称为mGGO。(4) 所有图像由放射科两名副主任以上医生负责判断,结论不统一时协商解决,对fGGO的直径取两位医生的平均值。
1.4 统计学处理
使用SPSS 16.0软件对CT征象计数资料采用χ2检验进行统计学分析。P<0.05为差异有统计学意义。
2 结 果
2.1 CT表现
(1) 病灶发生部位: 本组病例均为单发病灶,右肺上叶44个,右肺下叶16个,右肺中叶7个,左肺上叶16个,左肺下叶10个;(2) 病灶形状: 圆形或类圆形61个,不规则形32个;(3) 病灶大小: 0.4~1.0cm,平均0.78cm,其中浸润性腺癌平均0.9cm,微浸润性腺癌0.84cm,原位癌(adenoca-rcinoma in situ, AIS)0.78cm,不典型腺瘤样增生(atypical adenomatous hyperplasia,AAH)0.68cm,炎症 0.77cm。fGGO≤6mm的病灶浸润前病变(图1)的检出率明显高于浸润性腺癌(χ2=7.761,P<0.01);而8mm
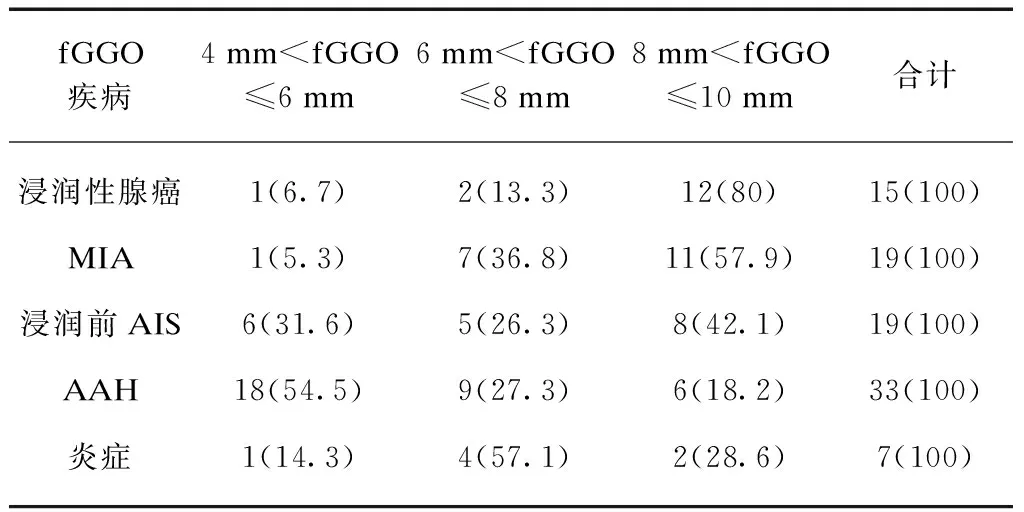
表1 不同病理类型与fGGO直径之间的发生比率Tab.1 Incidence rate ratios between different pathological types and fGGO diameter [n(%)]
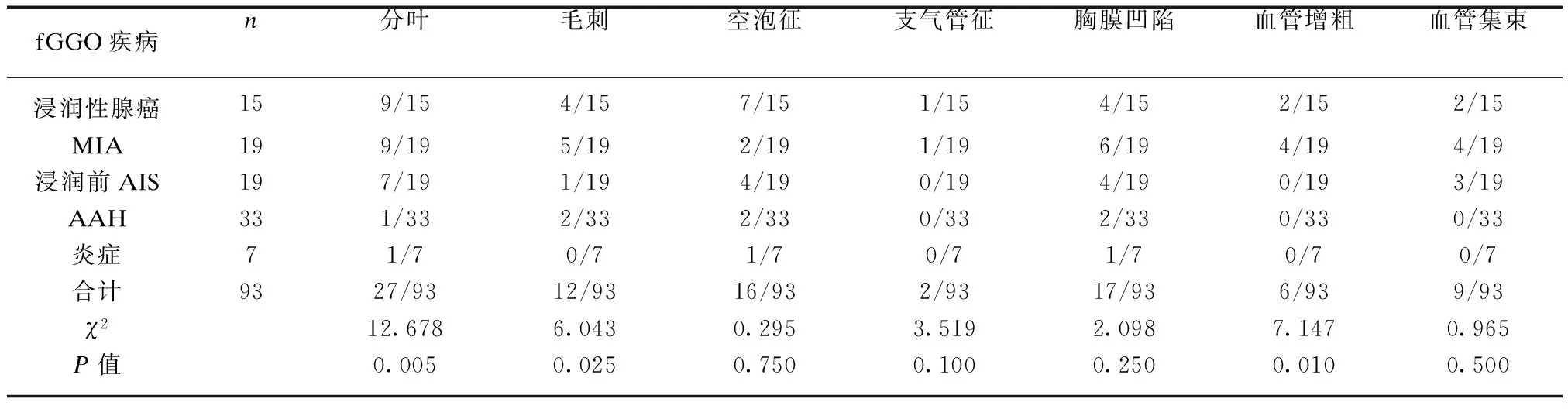
表2 不同病理类型fGGO的MSCT征象Tab.2 FGGO different pathological types of MSCT signs
注: 浸润性腺癌与浸润前病变(原位癌、AAH)进行对比
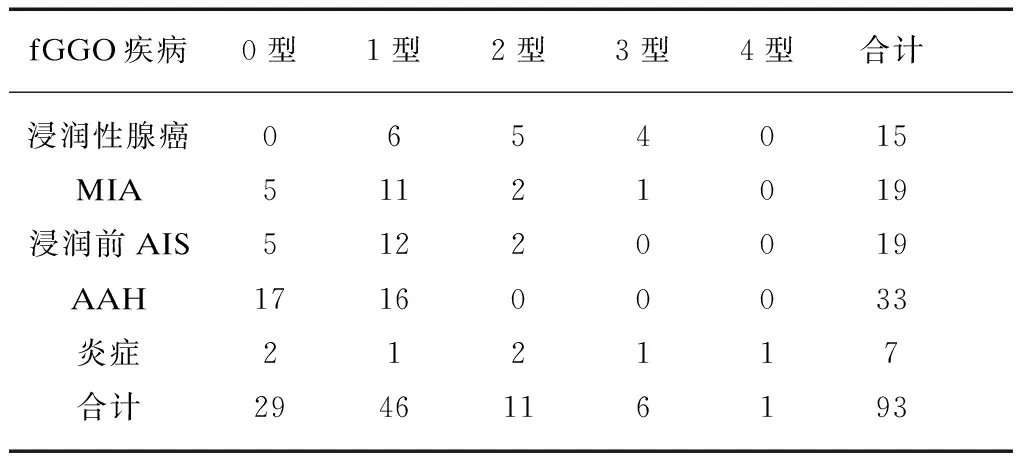
表3 不同病理类型fGGO的实变结果Tab.3 Proportional consolidation of different pathological types fGGO (n)
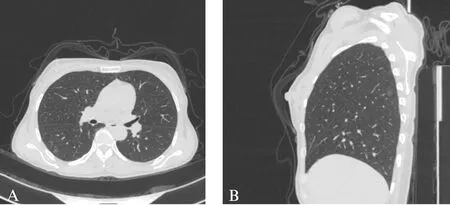
图1 右肺不典型腺瘤样增生MSCT图像Fig.1 Atypical adenomatous hyperplasia lung MSCT imageA: 横轴位显示右肺下叶背段pGGO结节,直径0.5cm,边界清晰;B: MPR 矢状位重建病灶位于右肺下叶背段

图2 右肺原位腺癌MSCT图像Fig.2 Lung adenocarcinoma in situ MSCT imageA: 横轴位显示右肺上叶后段mGGO,直径0.8cm,有空泡征;B: MPR矢状位重建,病灶累及斜裂胸膜
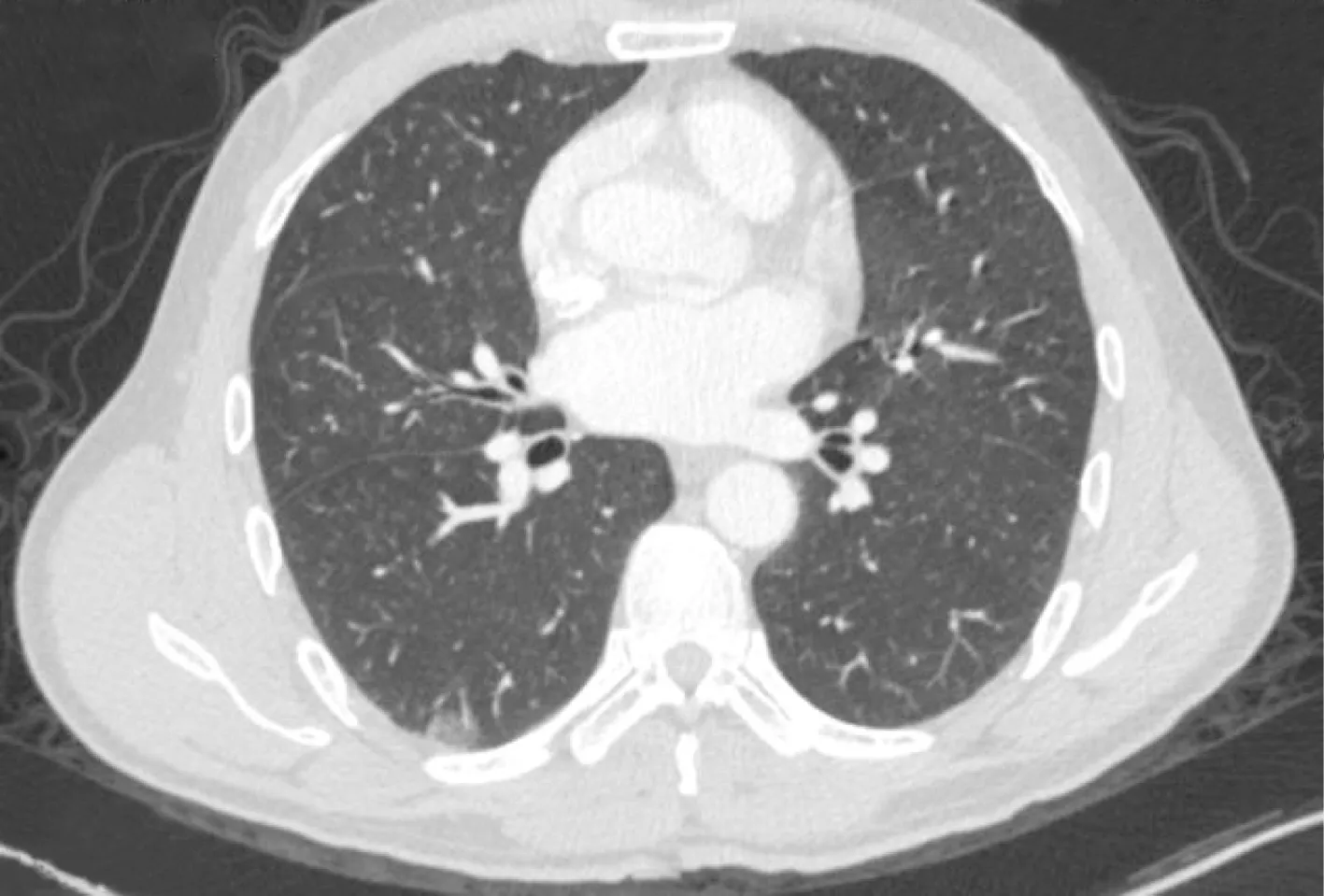
图3 右肺浸润性腺癌MSCT图像Fig.3 Invasive adenocarcinoma lung MSCT image右肺下叶mGGO结节,实变1型,大小约1.0cm,紧贴胸膜,周围血管增粗
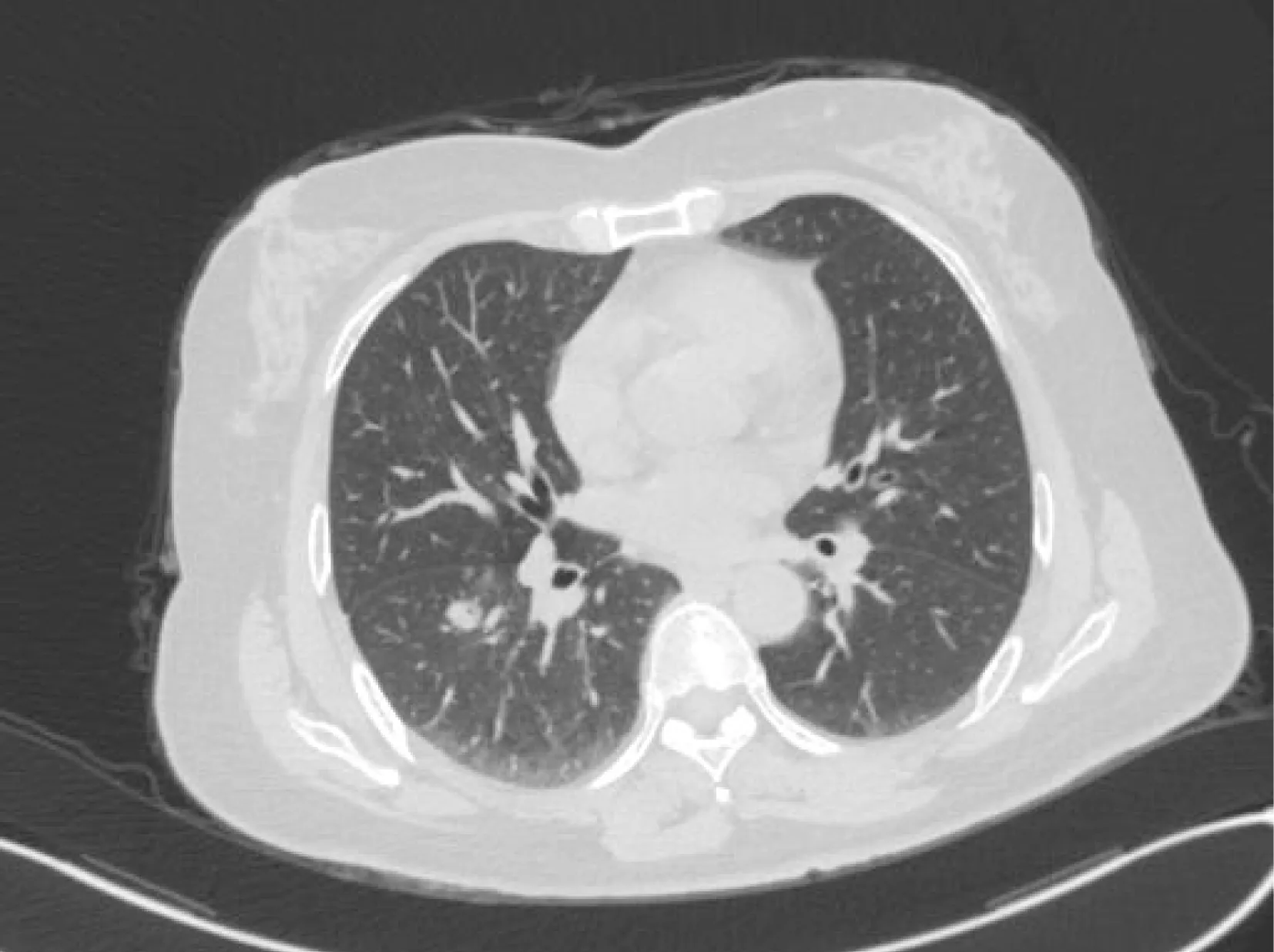
图4 右肺浸润性腺癌MSCT图像(高分化型)Fig.4 Invasive adenocarcinoma lung MSCT image右肺下叶基底段一mGGO,呈实变3型,直径0.8cm,周围可见毛刺,病灶内有空泡征
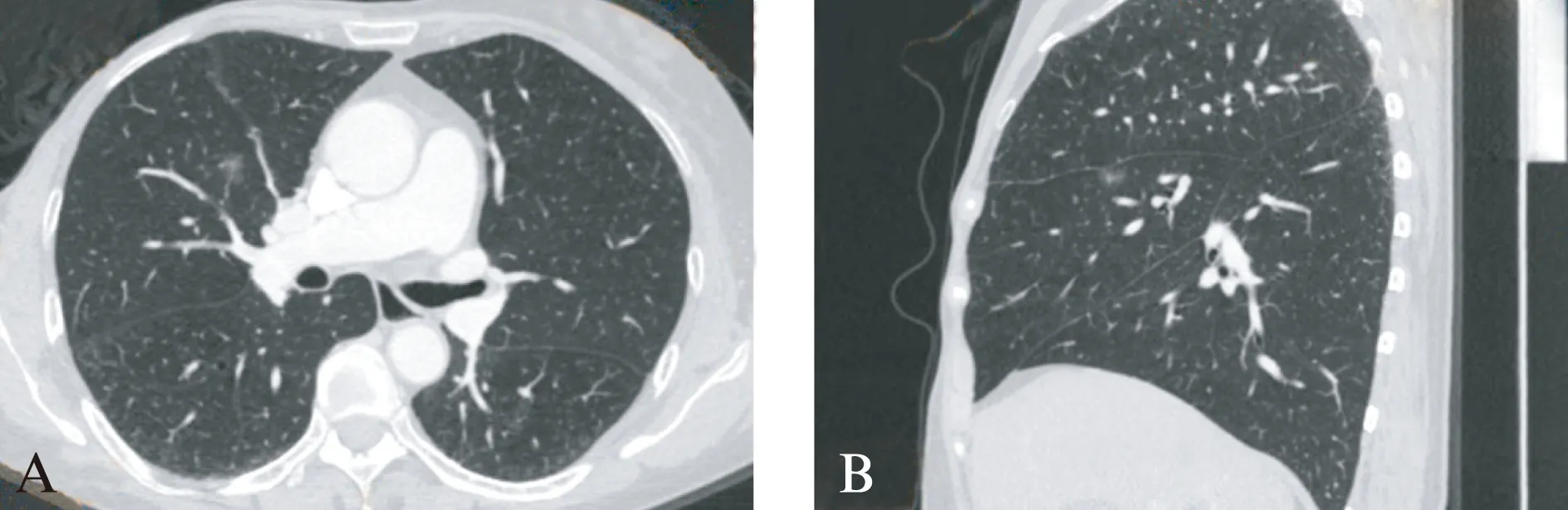
图5 右肺微浸润性腺癌MSCT图像Fig.5 Micro-invasive lung adenocarcinoma MSCT imageA: 横轴位显示右肺中叶mGGO,大小约为0.9cm,呈实变1型,有浅分叶;B: MPR矢状位重建,水平叶间胸膜有凹陷
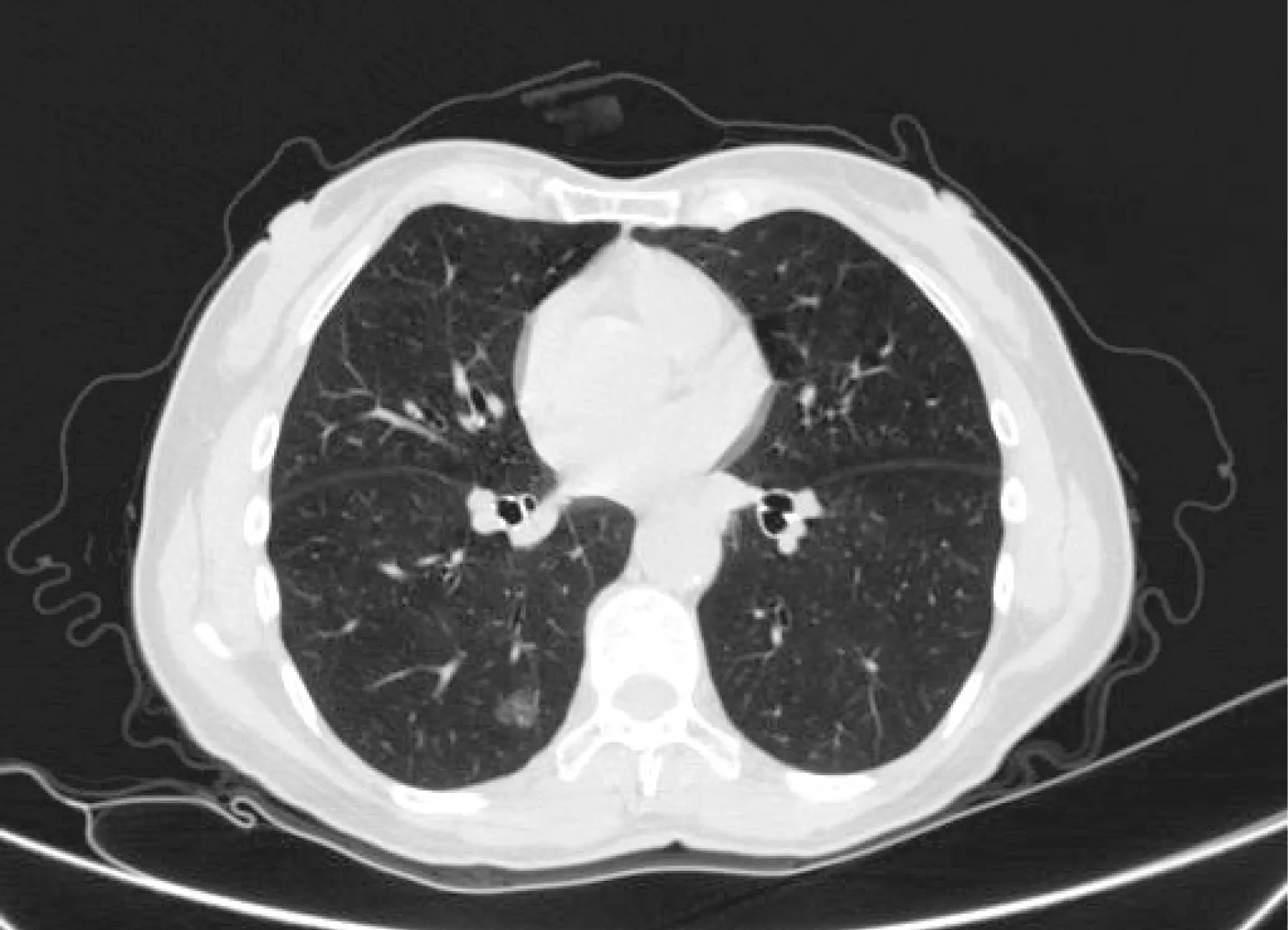
图6 右肺下叶原位腺癌MSCT图像Fig.6 Lobe of the right lung adenocarcinoma in situ under MSCT image右肺下叶可见一mGGO,直径约1cm,边界清晰
2.2 随访结果
随访6例,3例浸润性腺癌均表现为mGGO,其中2例分别在随访3、24个月实变增多,1例随访12个月病灶增大;微浸润腺癌1例,表现为pGGO,24个月时病灶增大;浸润前病变2例,均表现为mGGO,1例AIS 9个月时复查病灶增大,1例AAH随访24个月病灶无变化。
3 讨 论
在临床CT诊断的SPN常常表现为fGGO,病理上GGO是由肺泡腔的不完全填充、肺间质增厚、水肿、纤维化、肿瘤性增生、肺泡部分萎陷、正常呼吸状态或毛细血管的血容量增加所致[1-2],周围型肺腺癌CT常常表现为fGGO。肺癌表现为fGGO的结节大小与分期有关。本研究观察了96例≤1cm的fGGO病灶,其中肿瘤性病变86例,占92.47%。fGGO≤6mm的在肿瘤性病变中占30.23%,其中92.31%为浸润前病变,检出率明显高于浸润性腺癌(P<0.01);而8mm 3.1 1cm以下fGGO结节内实变率与定性诊断 本研究参照Sergiacorui等[4]的研究,根据CT内fGGO实变,将fGGO分为0~4型,1~4型为mGGO。本组中,表现为fGGO的肿瘤性病变86例,pGGO占31.4%,mGGO占68.6%,浸润前病变与浸润性腺癌之间mGGO发生率差异有统计学意义。由此可以看出,浸润前病变与浸润性腺癌中fGGO实变比例不同,浸润性腺癌CT主要表现为mGGO。本研究显示,对于浸润性腺癌、微浸润腺癌及浸润前病变,当病灶≤1.0cm时fGGO结节内实变量主要表现为1型。在本组64例mGGO结节中,共有46例为1型,占71.9%。浸润性腺癌、微浸润腺癌、浸润前病变实变1型的发生率差异无统计学意义。本研究显示,≤1.0cm的pGGO以AAH为主,浸润性腺癌少见,而在实变1型中仅凭实变量对腺癌定性诊断无价值。 3.2 浸润性腺癌的MSCT诊断 本研究显示,分叶征、胸膜凹陷征、空泡征及毛刺征的发生率分别为29.03%、18.28%、17.2%、12.9%,较其他征象具有较高的发生率。浸润性腺癌与AIS均可出现空泡征,浸润性腺癌与浸润前病变均可出现胸膜凹陷,胸膜凹陷及空泡征在浸润前后的发生率差异无统计学意义,而浸润性腺癌与浸润前病变之间分叶征、毛刺差异有统计学意义。血管增粗和血管集束征尽管发生率较低,分别为6.45%和9.68%,但是均发生在肿瘤性病变,尤其血管增粗在浸润前后差异有统计学意义。由于直径≤1cm 的fGGO病灶小,病灶形态、病灶边缘及内部结构在高分辨率CT表现其信息均少于直径≤3cm组的病灶,部分表现缺少特征性。因此,在诊断过程中要对影像表现综合分析,参照病灶大小、有无实变,以及治疗经过方能提高浸润性腺癌的诊断正确率。 3.3 癌前病变的MSCT诊断 癌前病变包括AAH和AIS。本组33例AAH,病灶平均直径6.8mm,pGGO结节17个(51.5)%,mGGO结节16个(48.5%),mGGO均表现为实变1型。AAH CT表现与其病理改变相关,此期呼吸性支气管及肺泡壁上皮增厚,病灶没有完全实变,主要表现为pGGO。因支气管及肺泡壁增厚引起的内分泌物排出不畅及萎陷可能是导致病灶CT表现为部分实变的原因,此期fGGO结节的分叶、毛刺、空泡征及胸膜凹陷等征象均不明显。在癌前病变中BAC与AAH之间存在一些相似的分子异常改变,从组织细胞形态到组织结构BAC有时与AAH鉴别困难,多学科肺腺癌组织学分类在2011年做了进一步调整,建议废弃BAC的名称,将病灶直径≤3cm且无间质浸润、胸膜侵犯及脉管瘤栓的支气管肺泡癌定义为原位腺癌[5-6]。AIS分为黏液型和非黏液型,以非黏液型多见,AIS细胞异型性不明显,常见肺泡间隔增宽伴纤维化。从本组19例AIS可见,病灶平均直径0.78cm,略大于AAH,分叶占36.8%,空泡征及胸膜接触胸膜粘连占21.1%,均高于AAH。实变率为63.2%也高于AAH,AIS实变主要表现为实变1型,少数可以表现为实变2型。 MIA是浸润前病变发展成浸润癌的路径。本组有MIA19例,平均直径8.4mm,大于浸润前病变组,实变11例,占57.9%,实变比率较AAH增加,实变以1型为主。MIA的MSCT表现介于浸润性腺癌与浸润前病变之间,MIA与AIS无论病灶大小还是fGGO实变率CT表现更接近,仅空泡征AIS略高于MIA,分叶、毛刺、胸膜凹陷、血管增粗和血管集束等征象MIA均略高于AIS, CT表现鉴别诊断困难。 3.4 随访对pGGO定性诊断的价值 研究[7]表明,表现为GGO的早期支气管肺泡细胞癌生长缓慢,其倍增时间常超过800d,因此即使是早期肺癌随访3~6个月也不会引起肿瘤明显增大或扩散。本组对6例进行了术前随访,随访时间3~24个月,有3例随访发现病灶增大,有2例仅表现为密度增高,有1例随访病灶无变化,能显示病灶变化最短时间为3个月。本研究认为,fGGO第1次随访间隔应该在3个月时间比较合适。本组这1例随访2年无变化的病例,因表现为mGGO而接受手术治疗,术后结果为AAH。对于肺内mGGO,当病灶直径>1cm、周围有毛刺、分叶,尤其增强扫描有强化的病灶,随访发现病灶增大或密度增加,以及发现病灶内血管增粗,提示为浸润性腺癌可能极大,应尽快行有创检查明确病理诊断或直接行手术治疗。如果病灶<1cm,虽然表现为mGGO,随访2年无变化,可以继续随访观察。 随着病灶增大浸润性腺癌的发生率增加,浸润性腺癌与微浸润性腺癌及腺癌浸润前病变在病灶大小方面有差异。直径≤1cm表现为fGGO结节浸润性腺癌、微浸润腺癌及浸润前病变实变率低,实变量也低,实变主要为1型。fGGO中GGO含量对定性诊断有价值,表现为1cm以下pGGO以AAH为主,也可以发生AIS或MIA,浸润性腺癌少见。fGGO出现的分叶、毛刺及血管增粗等征象提示浸润前病变向浸润性腺癌进展。随访对GGO定性诊断有价值,GGO的第1次CT复查时间一般为3个月,mGGO结节随访出现变化应明确病理行穿刺诊断或手术治疗。 [1] Rudin CM,Avila-Tang E,Harris CC,et al.Lung cancer in never smokers: molecular profiles and therapeutic implications[J]. Clin Cancer Res,2009,15(18): 5646-5661. [2] Samet JM,Avila-Tang E,Boffetta P,et al. Lung cancer in never smokers: clinical epidemiology and environ-mental risk factors[J].Clin Cancer Res,2009,15(18): 5626-5645. [3] 沈亮,黄海涛.局限性肺部磨玻璃影在早期肺癌诊治中的意义[J].同济大学学报: 医学版,2013,34(1): 88- 90. [4] Sergiacorui G, Ciccio C, Boi L, et al. Ground-glass opacity: hish-resolution computed tomography and 64-multi-slice computed tomography findings comparison[J].Eur J Radiol,2010,74(3): 479-483. [5] Travis WD,Brambilla E,Noguchi E, et al.International Association for the Study of Lung Cancer/American Thoracic Society/European Respir-atory Society Internati-onal Multidisciplinary Classifica-tion of Lung Adenocarcinoma[J].J Thorac Oncol,2011,6(2): 244-285. [6] Maeshima AM, Tochigi N, Yoshida A, et al. Histological scoring for small lung adenocarcinomas 2cm or less in diameter: a reliable prognostic indicator[J]. J Thorac Oncol, 2010, 5(3): 333-339. [7] Soda H,Yoichi N,Nakatomi K,et al. Stepwise progression from ground-glass opacity towards invasive adenocarcinoma: long-term follow-up radiological findings[J]. Lung Cancer, 2008,60(2): 298-301. Diagnostic value of spiral CT for pulmonary small isolated nodules with focal ground-glass opacity HANFu-shi,SUNXi-wen (Dept. of Radiology, Pulmonary Hospital, Tongji University, Shanghai 200433, China) Objective To investigate the diagnostic and differential diagnostic value of high-resolution multi-slice spiral CT (MSCT) scan for≤1cm isolated nodules with focal ground-glass opacity (fGGO) in the lung. Methods The features of 93 pulmonary isolated nodules≤1cm with fGGO on MSCT were retrospectively reviewed. All lesions were pathologically confirmed, including 15 cases of invasive adenocarcinoma, 19 cases of micro-invasive adenocarcinoma, 52 cases of infiltrated precancerous lesions and 7 cases of inflammatory. The morphology, size, edge, and changes in internal and adjacent structure were observed, and the fGGO ratio of nodular consolidation was assessed. The association of MSCT features with pathological findings was analyzed by χ2test. Results There were significance differences in CT signs of lobulation, glitches and vascular thickening between invasive adenocarcinoma and pre-invasive lesions (χ2=12.678, 6.043, 7.147, respectively,P<0.05). The incidence of transition from pre-invasive to invasive adenocarcinoma was increased with the increasing diameter and consolidation of nodules with fGGO; invasive adenocarcinoma was not found in fGGO nodules<1cm in diameter. Meanwhile the inflammatory lesions were lacking of characteristics. Conclusion Multi-slice spiral CT scan can provide valuable information for differential diagnosis of pulmonary isolate nodules≤1cm with focal ground-glass opacity. lung cancer; tomography, X-ray computed; atypical adenomatous hyperplasia 10.16118/j.1008-0392.2015.01.017 2014-10-14 韩砆石(1988—),男,硕士研究生.E-mail: 753487774@qq.com 孙希文.E-mail: xwsun@citi2.net R 814.42 A 1008-0392(2015)01-0078-05

