不适当窦性心动过速
蔡思宇 吴 祥
●古树新枝
不适当窦性心动过速
蔡思宇 吴 祥
不适当窦性心动过速(IST)是以静息时心率持续增快,或心率与生理需求不成比例为特征,表现为心悸、虚弱、疲乏、头晕或近似晕厥的综合征[1]。患者轻微运动后心率加速过度,而恢复时间延长。1939年Codvelle和Boucher首先报道了该现象[2],1979年Bauernfeind等[3]对7例患者的临床特点进行系统描述,并命名为IST。
1 IST的临床表现
IST的定义中未确定具体心率值,但IST患者白天静息心率普遍在100次/min以上,24h平均心率超过90次/min,而且无法用生理因素或已知可增加心率的原因解释。IST患者常有多个症状,包括心悸、呼吸困难、头晕、乏力和近似晕厥,但症状的严重程度不一定与心动过速有关。患者常伴随情绪和心理问题,但与IST的关系并不确定。有时单纯治疗心动过速并不能消除患者症状。
多数患者是年轻女性,发作突然,持续数月数年,自然病史不清楚,预后一般良好。尽管IST患者心率快,但睡眠时或白天某些情况下心率减慢。缺少长期随访研究,一般很少发生心动过速性心肌病。Still等[4]从604例OPERA研究受试者中识别出7例符合IST标准的患者(静息时窦性心率>100次/min或24h平均心率>90次/min),随访(6.0±2.4)年,虽然患者有心悸、平均心率增快,但预后良好,与基线相比,随访期各项超声心动图指标无显著变化。
2 IST的发生机制
窦房结结构复杂,由超过16种受自主神经影响的离子流控制,未发现导致IST的特定离子流。起搏电流(If)普遍认为是与窦性心率调控相关的主要离子流。静息心率的副交感调节依赖于M2毒蕈碱受体介导的IKAch的激活,后者通过G蛋白偶联的内向整流钾通道引起膜超极化。M2受体还通过抑制腺苷环化酶的活化,使cAMP生成减少,进而减少钙通道的磷酸化,使L型钙通道(ICa-L)电流减小,cAMP生成减少也可直接抑制If。两者都产生负性变时效应,使心率减慢。
IST的发生机制是多因素、复杂的,主要表现为自主神经功能紊乱和(或)窦房结内在异常,见表1。

表1 IST的潜在机制
Bauernfeind等研究发现IST患者使用普萘洛尔降低心率的程度高于对照组,而阿托品增快心率的程度低于对照组,提示IST患者交感神经张力过高、副交感神经张力减退,导致窦房结对外界环境改变不能做出正常心率反应。除了自主神经异常,窦房结本身病变也参与IST的发生,表现为完全阻滞自主神经后,IST患者窦房结固有频率显著升高。在3例IST患者切除的窦房结标本中还发现了脂褐质小泡。Still等[5]观察18例IST患者和对照组β肾上腺素能和胆碱能阻滞后对腺苷的反应。腺苷未能终止IST患者心动过速,IST组腺苷减慢心率的作用弱于对照组,支持固有心率加快是IST发生的主要机制,IST可能是乙酰胆碱敏感和腺苷敏感钾通道功能缺陷的结果。
Chiale等[6]在21例IST患者血液中发现11例患者有β抗肾上腺素能受体抗体。抗β受体免疫球蛋白G抗体导致cAMP的持续增加,继而激活ICa-L和If,诱发IST,推测循环抗β受体免疫球蛋白G抗体与IST有关。此外,静脉池(包括内脏池)、β受体敏感度增加、毒蕈碱受体敏感度下降、压力反射功能障碍、低血容量、脑干调节功能减退也可能参与IST的发生。
3 IST的诊断
IST的诊断主要根据12导联心电图或长期监测显示持续性或反复窦性心动过速,且无法用其他原因解释。诊断标准包括:(1)静息或轻微活动后心率过度增快(>100次/min),心动过速与伴随症状呈非阵发性;(2)24h动态心电图监测平均心率>90次/min;(3)P波形态和心内电图激动顺序与窦性心律时相同;(4)排除可引起窦性心动过速的其他原因,如甲状腺功能亢进症、嗜铬细胞瘤、贫血等。IST诊断的关键是必须排除引起窦性心动过速的生理和心理诱因(表2)。侵入性电生理检查对诊断没有帮助,但可用于排除伴随的室上性心动过速。对窦性心动过速的评估必须考虑心动过速是阵发性还是持续性。仔细分析12导联心电图,观察P波形态,如果与正常窦性节律时相同或相似,可能是IST。如果是阵发性,需排除房性心动过速包括窦房折返性。如心动过速是持续性,且可以确定潜在病因,则不是IST。如心动过速持续发作,找不到原因,可以诊断为IST。IST的诊断是一种排除诊断。
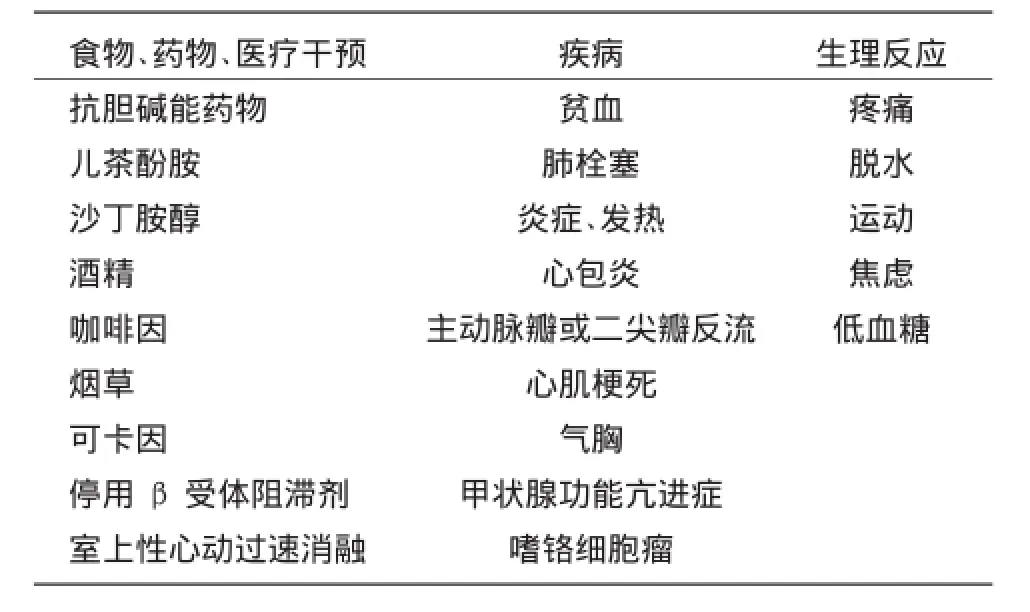
表2 引起生理性窦性心动过速的原因
IST需要与体位性直立性心动过速综合征(POTS)鉴别(表3)。POTS患者倾斜试验时心率逐渐加快,而IST时由于压力反射减弱,心率迅速加快,与体位无关,与运动关系更密切。POTS时,从仰卧位到直立位的10min内,在没有体位性低血压的情况下,心率增加持续超过30次/min,或心率超过120次/min。
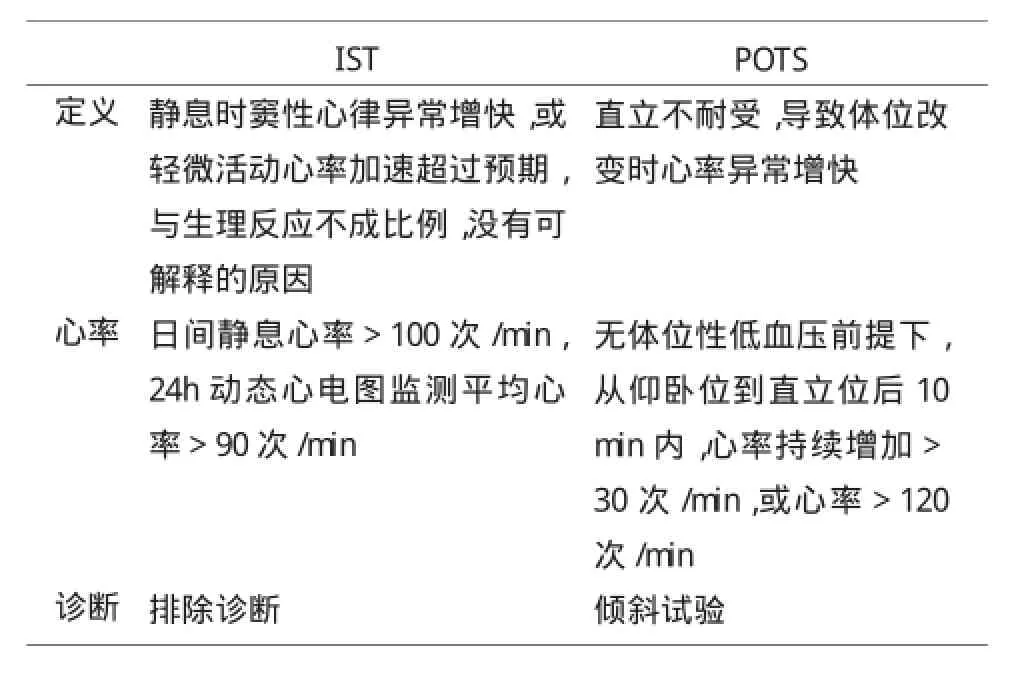
表3 IST与POTS鉴别
4 IST的治疗
IST患者症状繁多,常合并心理疾患,因此密切关怀、有效沟通可以改善预后,治疗起始即应与患者探讨生活方式的改变,有明确诱因的需去除(如避免酒精、咖啡因等)。治疗原则包括控制症状、减慢心率,但心率控制不一定能消除症状。由于治疗可能加重症状,导致病情恶化,因此对无症状IST患者控制心率存在争议。对疾病的复杂性和病因缺乏深入了解,导致没有一种治疗方法能够完全有效减慢心率和控制症状,应告知患者每一种治疗方法的利与弊并予权衡。
β受体阻滞剂和非二氢吡啶类钙通道阻滞剂可降低窦房结自律性,必要时还可使用胺碘酮和普罗帕酮等抗心律失常药物。但长期使用β受体阻滞剂后疗效降低,即使加大剂量也常常无效,这些药物还可引起头晕、乏力、血压降低等副作用。
小样本研究和一些病例报告已证明If阻滞剂伊伐布雷定是治疗IST最有前途的药物。10例女性IST患者接受伊伐布雷定5~7.5mg,2次/d,联合β受体阻滞剂或单药治疗[7],最高心率[从(176±45)至(137±36)次/min]和平均心率[从(84±11)至(74± 8)次/min]均显著降低,最低心率无变化,在平均16个月的随访时症状减轻或消失。另一研究在18例有症状的患者中观察伊伐布雷定的疗效和安全性[8],6个月时中位和最高心率显著降低,最低心率轻微改变,同时运动耐量改善。在一项前瞻性伊伐布雷定与琥珀酸美托洛尔的对照研究中,20例IST患者先服用琥珀酸美托洛尔47.5mg/d并加量至190mg/d,4周后改服伊伐布雷定5mg,2次/d,根据耐受程度加量至7.5mg,2次/d,共4周,记录静息心电图与24h动态心电图。两组静息心率与24h平均心率较基线均有显著且相同程度的下降,但伊伐布雷定组日常活动时心率下降幅度大于美托洛尔组,且平板试验运动耐量(最大运动当量与运动时间)明显改善。目前最强证据来自一个小样本随机、双盲、安慰剂对照、交叉研究,21例IST患者随机分入伊伐布雷定5mg,2次/d或安慰剂治疗,6周后两组交叉,总疗程12周。伊伐布雷定组24h动态心电图记录的白天、夜间和最高心率均显著降低,运动耐量明显改善[9],还使75%患者的IST相关症状消除[10]。伊伐布雷定可引起显著心动过缓,尤其与β受体阻滞剂或钙通道阻滞剂合用时,还可引起头痛。禁止与强CYP3A4抑制剂合用,也禁用于严重肝肾功能不全、低血压、妊娠、哺乳者。
近年来曾先后提出一些治疗方法,如采用氟氢可的松、苯巴比妥、可乐定、促红细胞生成素等药物或采用容量扩张、弹力袜、精神评估、运动训练等[11],均因疗效不确切而未广泛使用。
射频导管消融(下标消融)术通过改良窦房结或消除交感输出,降低IST患者心率,主要适于药物疗效差且症状严重的患者。目前大部分中心采用窦房结改良术,在界嵴上侧部消融,在保留窦房结变时性的前提下减慢心率。手术成功的标准包括静息心率下降>10%或绝对心率降至<90次/min,输注异丙肾上腺素后最高心率下降>20%~25%或20~30次/min或绝对心率<120次/min,窦房结激动向尾端移动[12]。Lee等[13]对16例药物无效、症状明显的IST患者进行窦房结完全消融(4例)或窦房结改良术(12例),针对最早心房激动部位发放射频能量。窦房结改良患者变时反应仍然存在,最高心率降低[(179.5±3.6)次/min降至(132.8±6.5)次/min],长期随访动态心电图显示最高心率与平均心率均降低。2例患者需要起搏治疗,1例出现一过性右膈麻痹,另1例出现一过性上腔静脉综合征。Man等[14]的研究中,29例IST患者接受消融术,22例窦性心率降至90次/min以下。其中13例术中随着心率逐渐降低,最早心内膜激动部位从高位右心房迁移,而其余9例心率降低是突然发生的。22例中6例症状在术后(4.4±3.0)个月复发,3例经再次手术症状完全消除。Marrouche等[15]对39例患者使用三维标测技术指导消融并进行长期随访,比较消融与β受体阻滞剂对最早窦房结激动部位迁移的影响。消融术后患者平均心率正常(72±8)次/min,激动沿界嵴向尾端迁移较艾司洛尔组更明显。但有21%的患者IST复发,接受再次手术。术中观察到心动过速频率随窦房结消融部位而发生变化,故三维标测有助于精确定位,提高手术成功率。
部分IST患者在窦房结上部消融后,心动过速起搏点发生迁移,而外科消融甚至切除窦房结后,也观察到心动过速可来源于窦房结其余部位或房室交界处。因此部分患者消融术后虽然窦性心率减慢,但仍有症状或症状仅暂时改善。
POTS患者行窦房结消融术后将产生灾难性后果,症状加重、血流动力学恶化。如将POTS误诊为IST并行窦房结消融后,体位改变时窦房结反应受抑制,心率加速反应迟钝,将出现严重体位性低血压。
为提高消融成功率,患者的选择非常重要[12],首先要选择生活方式干预与药物均无效的患者,其次心悸症状明显者可以获益,而其他非特异症状如胸痛、气短、乏力、头痛、晕厥等与心率无关者消融术后获益小,最好心悸出现的同时能证实IST发生。此外,必要时使用心外膜消融和超高密度标测技术。
消融术可导致上腔静脉狭窄、膈神经损伤,严重心动过缓需起搏器治疗,后者可见于消融术后数天。目前报道的IST患者消融治疗均为小样本研究[12-15],缺乏长期前瞻性随机对照大样本研究。由于术后复发率高、部分患者症状并无缓解,长期疗效不确定,而手术并发症多,其严重不良后果可能超过潜在获益,2015年HRS专家共识不推荐对IST患者常规进行窦房结消融[16]。
窦性心动过速一般均可找到原因,否则就需怀疑IST。后者是窦房结自律性增加、自主神经功能异常或两者联合作用的结果。对患者的评估需判断和排除所有可能引起窦性心动过速的原因。区分POTS与IST非常重要,将POTS患者误诊为IST并进行不适当治疗(窦房结消融)将产生灾难性后果。IST的非药物治疗包括避免心动过速的诱因和运动训练。由于单纯窦性心动过速很少引起严重血流动力学效应或威胁生命的后果包括心动过速性心肌病,因此治疗目标主要是改善症状而不是控制心率。使用中等剂量β受体阻滞剂开始治疗。伊伐布雷定5~7.5mg,2次/d,是一种有前途的药物治疗方法。仅在窦性心率极快、患者症状完全由窦性心动过速引起、所有其他治疗方法失败的情况下,考虑消融术。
[1]吴祥.病理性窦性心动过速[J].心电学杂志,2001,20(1)∶59-63.
[2]Codvelle M M,Boucher H.Tachycardie sinusale permanente a haute frequence sans troubles fonctionolles[J].Bull Mem Soc Med Hop Paris,1939,54∶1849-1852.
[3]Bauernfeind R A,Amat-Y-Leon F,Dhingra R C,et al.Chronic nonparoxysmal sinus tachycardia in otherwise healthy persons[J]. Ann InternMed,1979,91(5)∶702-710.
[4]Still A M,Raatikainen P,Ylitalo A,et al.Prevalence,characteristics and natural course of inappropriate sinus tachycardia[J].Europace, 2005,7(2)∶104-112.
[5]Still A M,Huikuri H V,Airaksinen K E,et al.Impaired negative chronotropic response to adenosine in patients with inappropriate sinus tachycardia[J].J Cardiovasc Electrophysiol,2002,13(6)∶557-562.
[6]Chiale P A,Garro H A,Schmidberg J,et al.Inappropriate sinus tachycardia may be related to an immunologic disorder involving cardiac beta andrenergic receptors[J].HeartRhythm,2006,3(10)∶1182-1186.
[7]ZellerhoffS,Hinterseer M,Felix Krull B,etal.Ivabradine in patients with inappropriatesinus tachycardia[J].Naunyn Schmiedebergs Arch Pharmacol,2010,382(5-6)∶483-486.
[8]CalòL,Rebecchi M,Sette A,et al.Efficacy of ivabradine administration in patients affected by inappropriate sinus tachycardia[J]. Heart Rhythm,2010,7(9)∶1318-1323.
[9]Ptaszynski P,Kaczmarek K,Ruta J,et al.Metoprolol succinate vs. ivabradine in the treatment of inappropriate sinus tachycardia in patients unresponsive to previous pharmacological therapy[J].Europace,2013,15(1)∶116-121.
[10]Cappato R,Castelvecchio S,Ricci C,et al.Clinical efficacy of ivabradine in patients with inappropriate sinus tachycardia:a prospective,randomized,placebo-controlled,double-blind,crossover evaluation[J].JAm CollCardiol,2012,60∶1323-1329.
[11]Olshansky B,Sullivan R M.Inappropriate sinus tachycardia[J].J Am CollCardiol,2013,61(8)∶793-801.
[12]GianniC,Di Biase L,Mohanty S,etal.Catheter ablation of inappropriate sinus tachycardia[J].J Interv Card Electrophysiol,2015 Aug27.[Epub ahead of print].
[13]Lee R J,Kalman JM,Fitzpatrick A P,etal.Radiofrequency catheter modification of the sinusnode for"inappropriate"sinus tachycardia [J].Circulation,1995,92(10)∶2919-2928.
[14]Man KC,KnightB,Tse H F,etal.Radiofrequency catheterablation of inappropriate sinus tachycardiaguided by activationmapping[J].J Am Coll Cardiol,2000,35(2)∶451-457.
[15]Marrouche N F,Beheiry S,TomassoniG,etal.Three-dimensional nonfluoroscopic mapping and ablation of inappropriate sinus tachycardia.Procedural strategies and long-term outcome[J].J Am Coll Cardiol,2002,39(6)∶1046-1054.
[16]Sheldon R S,Grubb B P,Olshansky B,et al.2015 heart rhythm society expert consensus statement on the diagnosis and treatment of postural tachycardia syndrome,inappropriate sinus tachycardia,and vasovagal syncope[J].Heart Rhythm,2015,12(6)∶e41-63.
2015-09-06)
(本文编辑:马雯娜)
310009浙江大学医学院附属第二医院心脏中心

