盐酸吡格列酮/盐酸二甲双胍缓释片的研制
柳 杨,李 辉,张宵翔,黄守正
(1.合肥工业大学医学工程学院,合肥230009;2.安徽商瑞医药技术有限公司,合肥230001)
盐酸吡格列酮/盐酸二甲双胍缓释片的研制
柳 杨1,李 辉2,张宵翔1,黄守正2
(1.合肥工业大学医学工程学院,合肥230009;2.安徽商瑞医药技术有限公司,合肥230001)
以体外释放度为考察指标,优选缓释片的填充剂、粘合剂、成膜剂、致孔剂等筛选盐酸吡格列酮/盐酸二甲双胍缓释片处方及工艺,确定以羟丙甲纤维素(5mPa·s)、乙基纤维素(20mPa·s)作为成膜剂,聚乙二醇6000作为填充剂和粘合剂,硬脂酸作为润滑剂和助流剂,聚乙二醇400作为增塑剂和致孔剂,二氧化钛作为遮光剂的处方。制备的缓释片其释放行为与参比制剂基本相似。结果表明优选的处方合理,工艺稳定、可行,且降低了生产成本。
盐酸二甲双胍;盐酸吡格列酮;缓释;处方工艺;释放度;
盐酸吡格列酮(pioglitazone hydrochloride,PH)属于噻唑烷二酮类药物,是胰岛素增敏剂,直接靶向胰岛素抵抗,主要通过增强外周葡萄糖的利用发挥降糖作用[1-2];盐酸二甲双胍(metformin hydrochloride,MH)是双胍类药物,主要通过降低内源性肝葡萄糖的生成从而发挥降糖作用[3],是治疗II型糖尿病的一线药物,二者均为临床上应用广泛的降血糖药物。国外对此两种机制互补药物作用研究较多,例如史密丝克莱恩比彻姆有限公司提出的“用噻唑烷二酮和二甲双胍治疗糖尿病”的专利,该专利中率先提出了用噻唑烷二酮和二甲双胍治疗糖尿病的组合,而目前国内此复方缓释片制备的文献报道较少。临床研究表明将此两种作用机制互补的抗高血糖药组合在一起,优于单一用药并可减少不良反应[4-5],可提高治疗依从性,用于饮食和锻炼结合的II型糖尿病的治疗,可获得良好的临床疗效[6-7],增加了临床上用药的选择余地[8],近年来亦有报道称两药联用对多囊卵巢综合症有不错的疗效[9-10]。国外上市的二甲双胍缓释片规格较为多样化,以每片1000mg,850mg,500mg为主,而国内市场均为每片500mg未见1000mg规格。由于盐酸二甲双胍缓释片每日服用最大剂量大,为了进一步提高患者的顺应性,本文研制的复方缓释制剂,以武田药品(http://www.chemdrug.com/)工业株式会社的盐酸匹格列酮和盐酸二甲双胍的复方制剂ACTOPLUSMET®XR为参比试剂(规格为15mg/1000mg),采用膜控技术制备,制备工艺简单,能够控制二甲双胍释放,达到8~12 h持续释药,保持平稳的血药浓度,具有重要的临床价值。
1 材料
1.1药品与试剂
盐酸吡格列酮原料(北京太洋药业有限公司),盐酸二甲双胍原料(山东科源制药有限公司),参比制剂ACTOPLUS MET®XR(武田药品工业株式会社),盐酸吡格列酮对照品(中国药品生物制品检定所),盐酸二甲双胍对照品(中国药品生物制品检定所),乙基纤维素(泰安瑞泰纤维素有限公司;20mPa·s),羟丙甲基纤维素(泰安瑞泰纤维素有限公司;5mPa·s,50mPa·s),聚乙二醇(南京化学试剂有限公司;PEG400,PEG6000),硬脂酸(湖州展望药业有限公司),二氧化钛(江苏宏运药业有限公司)。
1.2仪器设备
AG285型电子天平(德国梅特勒公司),6010型紫外分光光度计(安捷伦科技上海仪器有限公司),RCZ-8G型智能溶出仪(天大天发),SF-130型万能粉碎机(江苏黎明制药机械有限公司),BY-30型包衣机(上海天和制药机械厂),TDP-单冲压片机(上海天和制药机械厂)。
2 方法与结果
2.1溶出度和释放度检测法
盐酸吡格列酮:取样品,按溶出度测定法(中国药典2010年版二部附录X C第二法),以0.1mol/L盐酸溶液900 mL为溶剂,桨法,转速100 r/min,依法操作,经5、10、20、30、45和60min时,分别取溶液5mL滤过,及时补液,照紫外-分光光度法(中国药典2010版二部附录IV A),在269 nm波长处分别测定其吸光度;另精密称取盐酸吡格列酮对照品适量,加0.1mol/L盐酸溶液溶解制成18μg/mL的溶液,同法测定,按外标法计算盐酸吡格列酮的溶出度。
盐酸二甲双胍:取样品,按溶出度测定法(中国药典2010年版二部附录XC第二法),以pH值6.8磷酸盐缓冲液1000mL为溶剂,桨法,转速100 r/min,依法操作,经1、2、4、6、8、10和12 h时,分别取溶液5mL滤过,及时补液,续滤液稀释200倍,照紫外-分光光度法(中国药典2010版二部附录IV A),在233 nm波长处分别测定其吸光度;另精密称取盐酸二甲双胍对照品适量,加pH值6.8磷酸盐缓冲液溶解制成5μg/mL的溶液,同法测定,按外标法计算盐酸二甲双胍的累积释放度。
2.2盐酸吡格列酮/盐酸二甲双胍缓释片的制备及处方筛选
2.2.1膜控型缓释层素片片芯的制备
称取盐酸二甲双胍100 g,粉碎过100目筛,取7.5 g PEG6000用等量30%乙醇加热溶解,加入1.0gHPMC(50m Pa· s),搅拌混匀后加入到主药中,搅拌制软材,过16目制粒,60℃干燥1 h,14目整粒,加入硬脂酸1.5 g,混匀压片。
2.2.2隔离层包衣研究
对缓释片芯进行隔离层包衣可有效防止药物迁移泄露,避免在储存过程中由于迁移导致盐酸二甲双胍释放加快或者泄露造成毒副作用。取HPMC(5mPa·s)和PEG6000按4∶1质量比混匀,加水溶解,配制成隔离层包衣液,称取上述制备工艺的片芯,置包衣锅中,温度控制在40℃±2℃,转速为(25±5)r/min,包衣增重分别为1%、2%、3%和5%,将样品置40℃±2℃干燥2 h,考察不同包衣增重的隔离衣对片芯溶出度影响(桨法,水∶1000mL,转速∶100 r/min),优选合适的包衣增重范围,结果如下。

表1 不同包衣增重对盐酸二甲双胍溶出度影响Table1 Effectofdifferentcoating levelson the dissolution rateofmetformin hydrochloride
从本品片芯经膜控层缓释释放12 h的角度来看以及缩短包衣时间及对控释层膜的稳定性考虑,隔离层包衣增重为1%范围即可。
2.2.3控释层包衣研究
1)不同包衣液组方研究。按表2配制包衣液,称取隔离层包衣增重1%的片芯置包衣锅中,温度控制在35℃±5℃,转速为(30±10)r/min,进行控释层包衣,包衣增重约3.0%后,40℃±2℃干燥2 h,取出冷却,室温干燥12 h,即得盐酸二甲双胍缓释层片芯,分别测定盐酸二甲双胍释放度,结果如下。
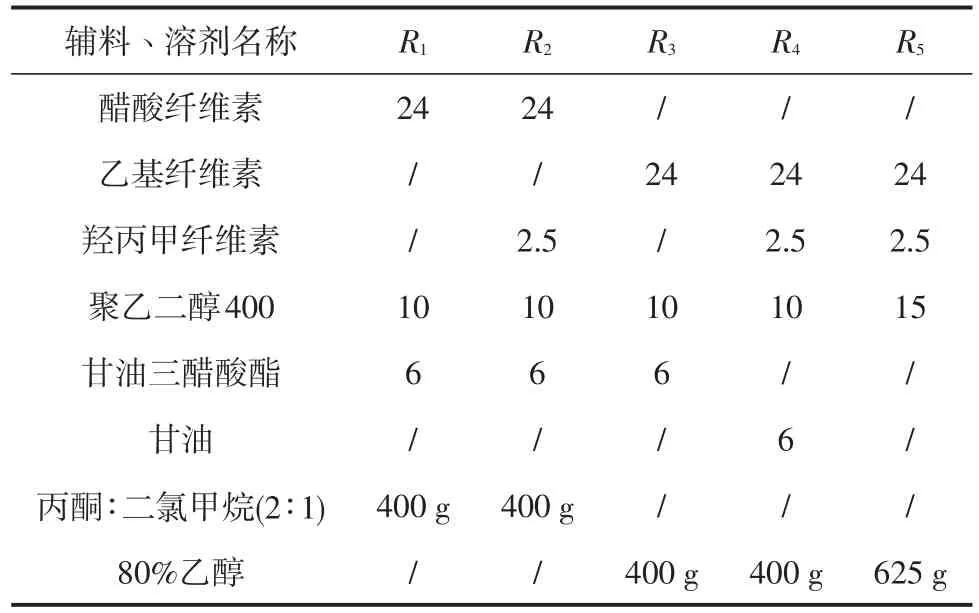
表2 不同包衣液组方配比Table 2 The formulamatching ofdifferentcoatingsolutions
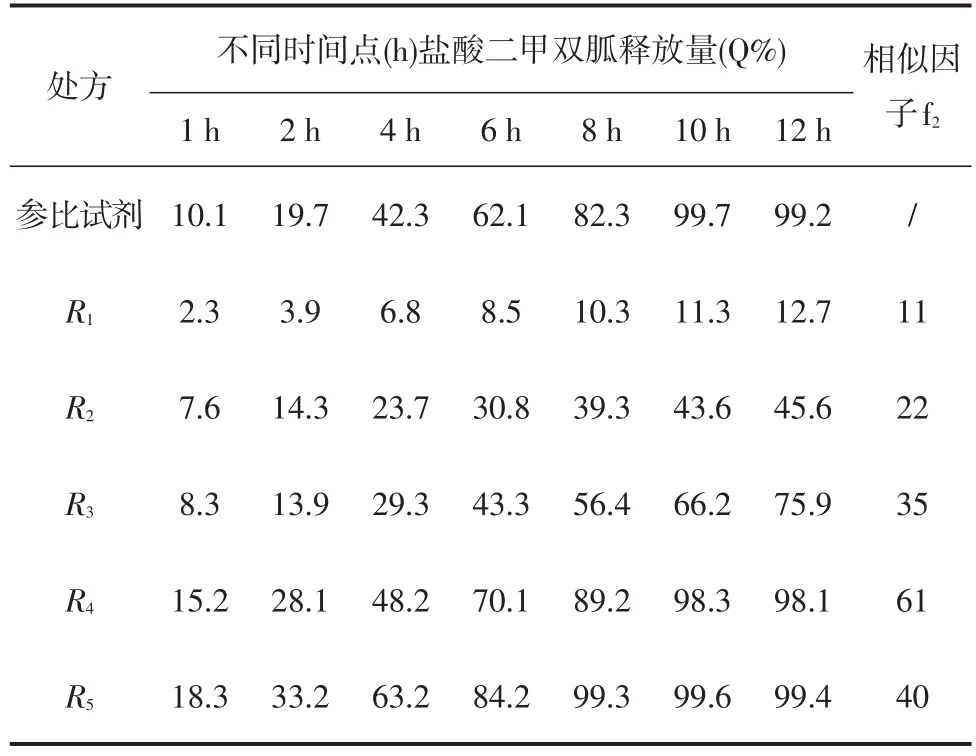
表3 不同包衣液配方对盐酸二甲双胍释放量影响Table3 Effectofdifferentcoating solution on the release rate ofmetformin hydrochloride
从相似因子角度,结合速释层包衣后会降低缓释层片芯释放速度,优选适度释放偏快的包衣组方R4进行进一步包衣研究。
2)不同包衣增重研究。以R4为包衣液组方,分别包衣增重2%、3%和4%,分别测定盐酸二甲双胍释放量。
从表中释放量及各相似因子看,优选包衣增重3%(见表4)。
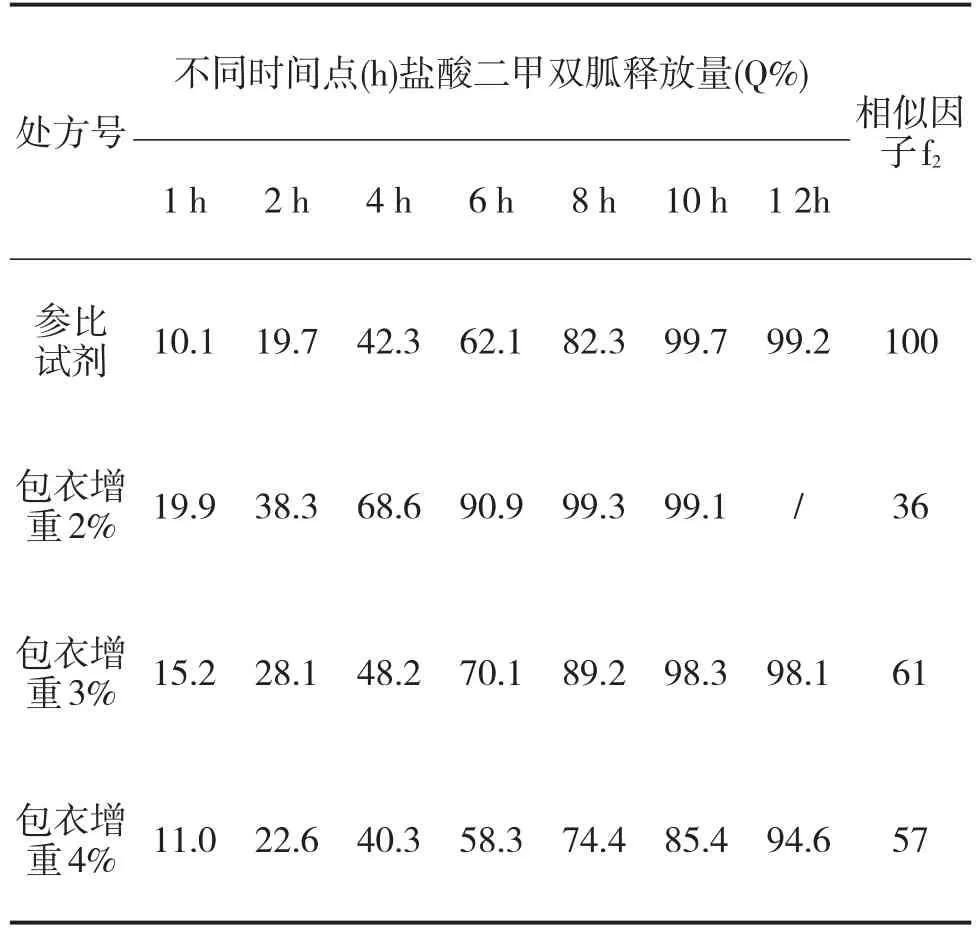
表4 不同包衣增重对盐酸二甲双胍释放量的影响Table4 Effectofdifferentcoating levelson the release rateofmetformin hydrochloride
2.2.4盐酸吡格列酮速释层的制备
取盐酸吡格列酮1.66 g、HPMC(50 mPa·s)1.3 g及PEG6000 0.3 g,用80%乙醇溶液搅拌溶解;二氧化钛0.4 g用80%乙醇溶液搅拌分散均匀过筛后,加入到上述溶液中,搅拌均匀即得含盐酸吡格列酮包衣液。称取缓释层片芯置包衣锅中,温度控制在35℃±2℃,转速为(30±5)r/min,包衣增重约3.5%停止包衣,片子在35℃±2℃干燥2 h后,于室温干燥12 h即得缓释片。
2.2.5工艺流程图
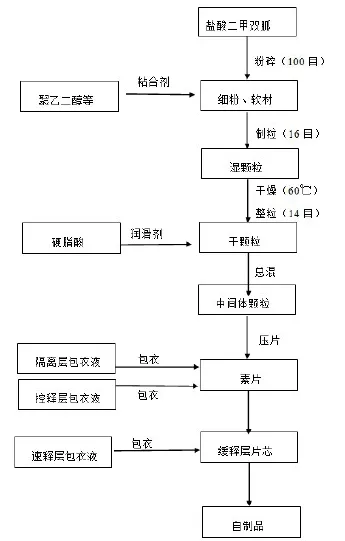
2.3溶出介质及溶出曲线相似性研究
取本品与参比试剂,按“2.1”项方法在不同溶出介质进行体外溶出、释放度测定,进行比较,见表5和表6。
结果显示盐酸吡格列酮和盐酸二甲双胍在不同介质中的溶出、释放曲线与市售品相似程度均较好,并且盐酸二甲双胍在各介质中释放度均高于对照药。
2.4线性范围
精密称取盐酸吡格列酮对照品18.0mg置50mL量瓶中,加0.1mol/LHCl溶液溶解定容作为储备液,精密量取适量用0.1mol/LHCl溶液制成浓度分别为7.0、11.0、14.0、18.0、22.0和25.0μg/mL的溶液,照紫外-可见分光光度法(中国药典2010年版二部附录IVA),在269 nm波长处测定其吸光度,对吸光度A进行线性回归,得标准曲线方程:A=0.0218C+ 0.0125,r=0.9997,表明PH在7.0~25.0μg/mL的浓度范围内线性关系良好。
精密称取盐酸二甲双胍对照品10.0mg用pH值6.8磷酸盐缓冲液配制成浓度分别为1.0、2.0、3.0、4.0、5.0和6.0μg/ mL的溶液,照紫外-可见分光光度法(中国药典2010版二部附录ⅣA)在233 nm波长处测定其吸光度,对吸光度A进行线性回归,得标准曲线方程:A=0.81C+0.0077,r=0.9999,表明MH在1.0~6.0μg/mL的浓度范围内线性关系良好。
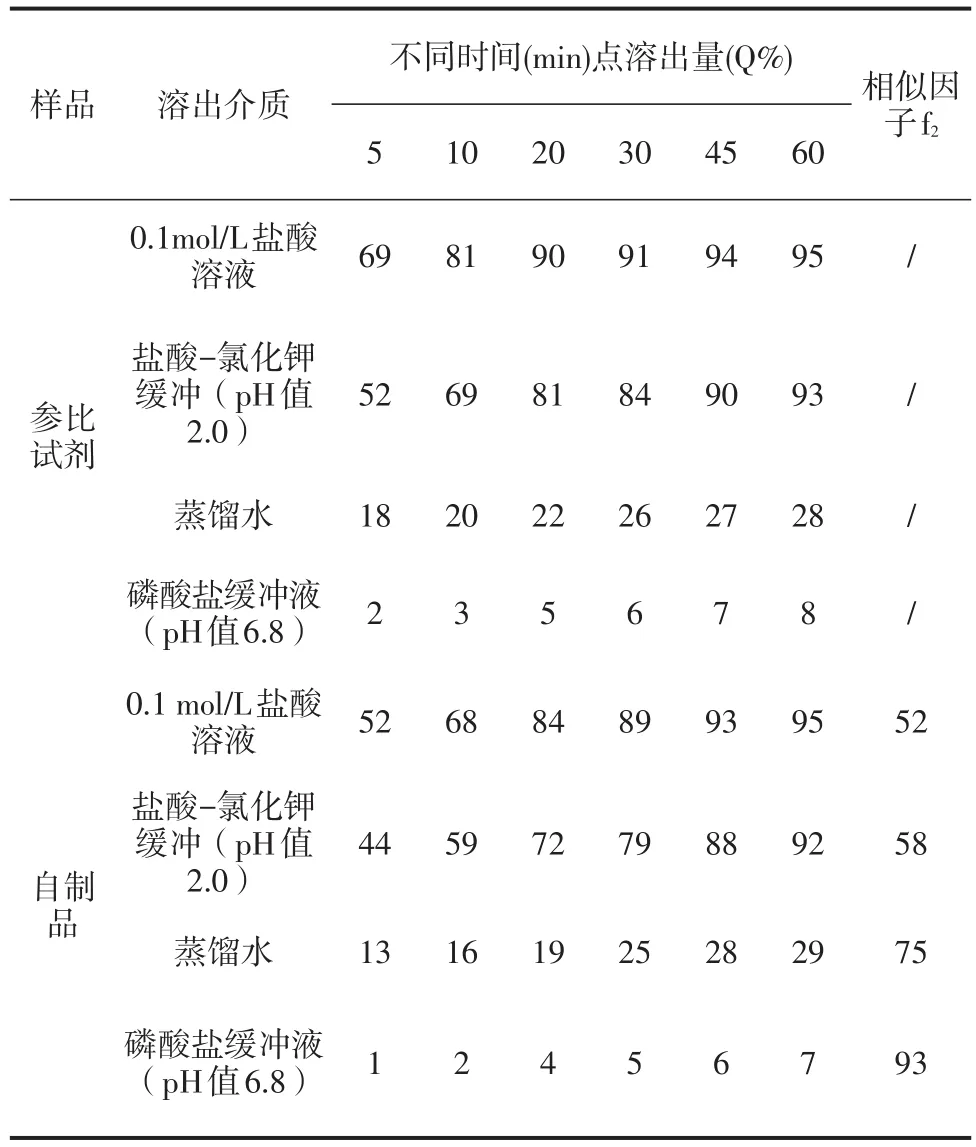
表5 不同溶出介质对盐酸吡格列酮溶出度的影响Table 5 Effectofdifferentmedia on the dissolution rate ofpioglitazone hydrochloride
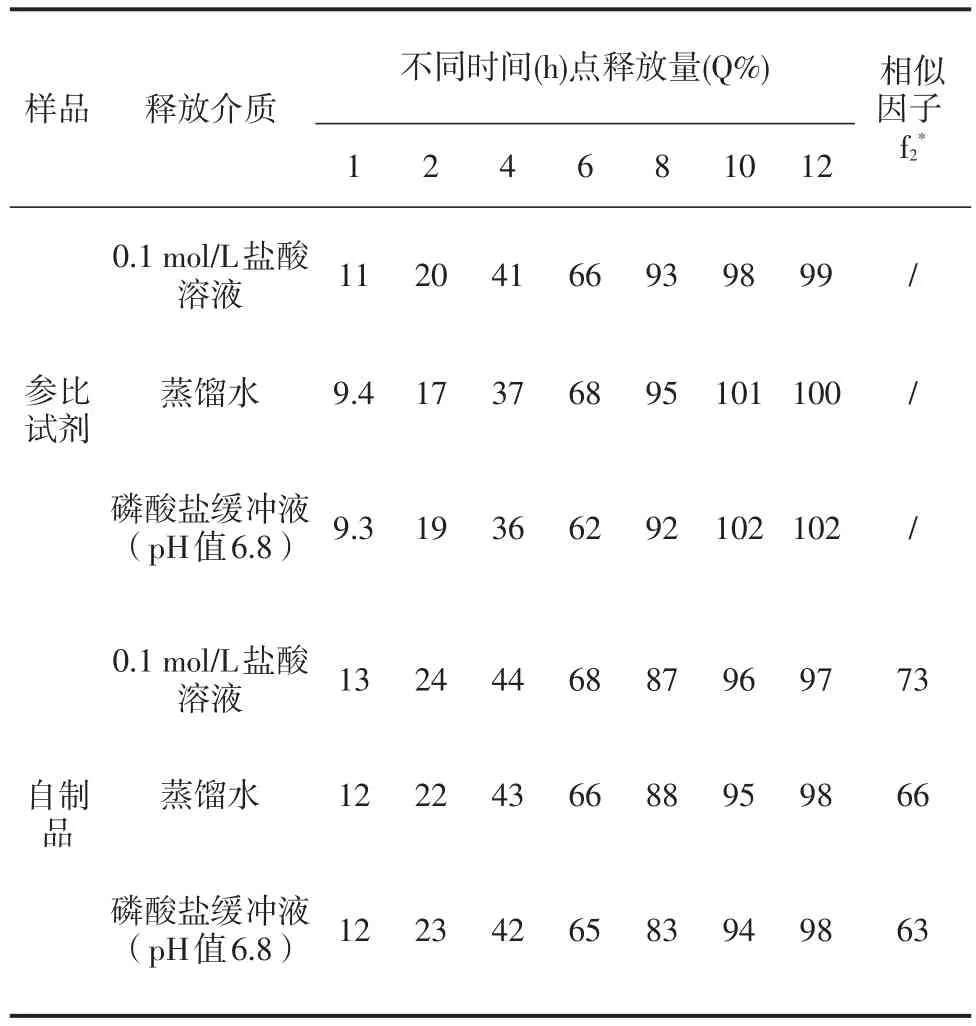
表6 不同释放介质对盐酸二甲双胍释放度的影响Table 6 Effectofdifferentmediaon the release rate ofmetformin hydrochloride
2.5均一性试验
取参比试剂及3批自制品各12片,按“2.1”项方法,测定盐酸吡格列酮累积溶出量和盐酸二甲双胍累积释放度。计算得,PH:参比试剂RSD为2.0%,3批自制品RSD分别为2.2%、2.9%和2.1%,自制品溶出度平均RSD=2.3%<5%,表明本品PH溶出度均一性较好。MH:参比试剂RSD为7.9%,3批自制品RSD分别为7.3%、2.3%和3.6%,自制品平均RSD= 3.8%<5.0%,参比试剂释放度不同片间差异偏大(因有部分片沉淀并黏附在杯底,使片面中一面释药小孔被阻塞,导致片子个体差异较大),自制品均一性相对较好。
2.6回收率试验
pH:取速释层细粉精密称定适量,按高、中、低浓度分别各配制3份样品,依法操作,计算得本品的高、中、低3种浓度样品的平均回收率为98.66%,RSD为0.92%(n=9),符合规定。MH:取片芯层细粉精密称定适量,按高、中、低浓度分别各配制3份样品,依法操作,计算得本品的高、中、低3种浓度样品的平均回收率为98.63%,RSD为0.73%(n=9),符合规定。
2.7溶出液稳定性试验
取PH溶出度项下溶出液,过滤后室温放置,分别在0、1、2、4、8和10 h,依法测定吸光度,RSD%=0.68,说明本品溶出液在0.1mol/LHCl溶液中10 h内稳定。取MH释放度项下供试液过滤后室温放置,分别在0、2、4、8、10、12和24 h,依法测定吸光度,RSD%=0.89,说明本品在pH值6.8磷酸盐缓冲液中24 h内较稳定。
2.8溶出、释放曲线
取3批自制品,按“2.1”项方法,测定盐酸吡格列酮累积溶出量和盐酸二甲双胍累积释放度,并与参比试剂比较(见图1和图2),可看出,关于PH参比试剂在前20min较自制品溶出偏快,而在30min后参比试剂和自制品溶出基本较一致,两者在45min后基本释放完全。关于MH,本品缓释片10~12 h后基本全部释放出来,参比试剂释放度前慢后快,自制品释放度前快后慢,但总体两者释放曲线相似。
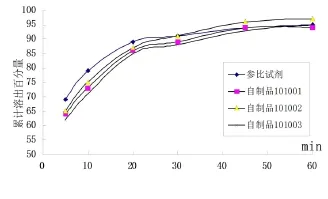
图1 不同样品盐酸吡格列酮溶出曲线Fig1 The stripping curveofdifferentsamplesofpioglitazonehydrochloride
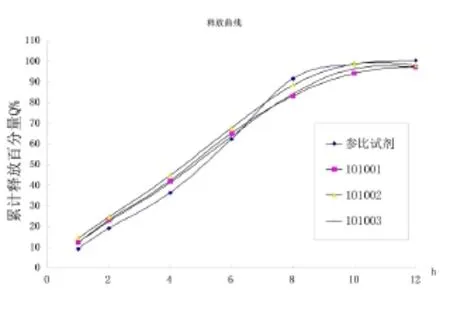
图2 不同样品盐酸二甲双胍释放曲线Fig 2 Thedissolution curve ofdifferentsamplesofmetformin hydrochloride
2.9盐酸二甲双胍释放曲线拟合
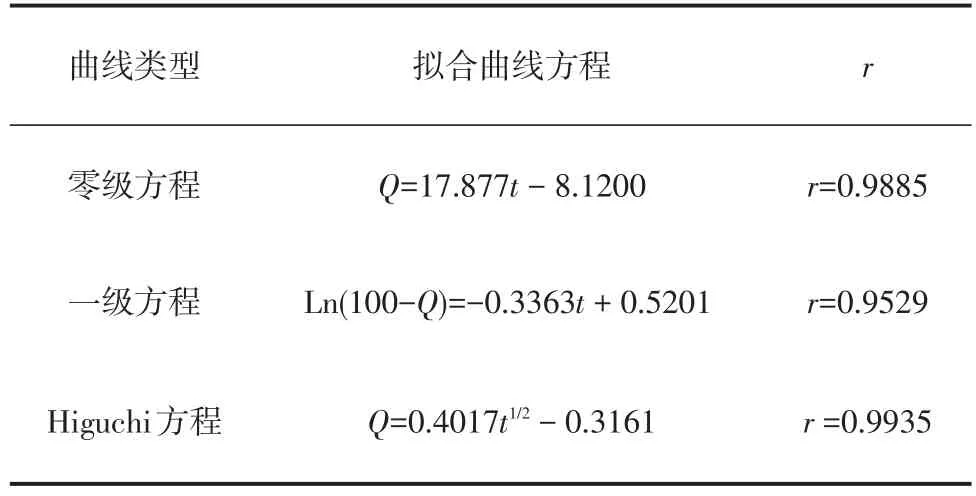
表7 药物释放模型拟合Table 7 mathematicalmodelsused to describe thedrug’sdissolution curve
从表7中看出:在自制品的三种曲线拟合:零级方程、一级方程和Higuchi方程中,Higuchi方程的拟合系数最大,尽管缓释片制备是膜控及缓释薄膜包衣的技术制备,但从拟合结果来看该缓释片的体外释放更为符合Higuchi方程。
3 讨论
市售品中缓释成分MH采用单式渗透泵专利技术(SCOTTM)制备,体外释放符合零级方程,自制品采用膜控及缓释薄膜包衣的技术制备,制备工艺相对简单,通过曲线拟合发现自制缓释片最符合反应扩散机制的Higuchi方程,说明缓释片的释药机制是以扩散机制为主,推测可能是药物与介质接触后,缓释膜上的致孔剂溶解,介质通过衣膜中的微孔扩散进入片芯,片芯表面的药物溶解并通过微孔扩散溶出[11-12]。介质不断透过微孔进入片芯,片芯体积膨胀,同时缓释膜溶胀破裂,通透性增强,内部药物进一步溶解扩散[13]。
由于本品中盐酸二甲双胍规格较大(1000mg),辅料用量相对受限,同时对粉末的流动性、堆密度及可压性及对素片的压力和硬度有一定要求。从各处方工艺组成中粉体参数和素片特性研究发现,由于盐酸二甲双胍原料流动性和可压性较差,制粒成为必要工序,同时在处方中用适量润滑剂和助流剂辅料PEG6000或硬脂酸,以增加粉体流动性和可压性及改善素片的光泽度和脆碎度,压片压力近15 KN左右,硬度约(50±5)N,压片可依据机械性能采用高速或中速压片(4万~10万片/h)。盐酸二甲双胍具有高溶解、低渗透性特点,属于BCS[14]3类药物,如片芯直接包控释层衣,其包衣层可能迁移渗透入活性成分或赋形剂,导致控释层衣中致孔剂增多,影响药物释放速率,因此在片芯中先包一层高亲水性隔离衣,降低片芯中原辅料对控释层衣的影响[15]。自制片中有效成分盐酸吡格列酮和盐酸二甲双胍在不同介质中的溶出、释放曲线与市售参比试剂相似程度均较好,可以达到与市售品相似的体外释放曲线,并且盐酸二甲双胍释放度均高于对照药。
[1]杨 杨,戚 筠,谢 军,等.吡格列酮对初诊2型糖尿病患者血脂水平的影响及临床意义[J].微循环学杂志,2011,21(1):30-31,34.
[2]王旭萍,陈玉松,汪金华,等.吡格列酮和二甲双胍治疗2型糖尿病的疗效观察[J].黑龙江医药,2009,22(1):30-31.
[3]FDA.美国W atson公司&日本武田公司.ACTOPLUSMET XR FDA说明书[EB/OL].[2012-12-28].http://www.accessdata.fda.gov/drug⁃satfda_docs/label/2011/022024s007s008lbl.pdf.
[4]田艳娟.二甲双胍联合比格列酮治疗2型糖尿病临床研究[J].中国实用医药,2012,7(3):88-89.
[5]梁文杰.二甲双胍配伍吡格列酮治疗2型糖尿病临床效果及安全性分析[J].中国医药导刊,2013,15(3):473-474.
[6]王国洪.吡格列酮和二甲双胍治疗新发2型糖尿病[J].江汉大学学报:自然科学版,2010,38(1):84-85.
[7]戚 筠,杨 杨.吡格列酮联用二甲双胍对新发2型糖尿病FIns,HOMAIR,和ISI指标的影响[J].中国现代药物应用,2013,7(8):101-102.
[8]胡红琳,王长江,张木勋,等.吡格列酮二甲双胍片治疗2型糖尿病的多中心随机双盲平行对照临床试验[J].中国临床药理学杂志,2009,25(6): 483-486.
[9]范桂芳.二甲双胍联合吡格列酮治疗多囊卵巢综合征30例[J].中国现代药物应用,2013,7(13):160-161.
[10]韩亭亭,郑 俊,胡耀敏.噻唑烷二酮类药物和二甲双胍联合治疗多囊卵巢综合征的系统评价[J].第二军医大学学报,2010,31(4):412-416.
[11]马成孝,蔡春萍,赵建宗.盐酸二甲双胍缓释片的实验研究[J].药学进展,2006,30(1l):505-509.
[12]林巧平,李 薇,山莽挺,等.盐酸吡格列酮/盐酸二甲双胍缓释片的体内外评价[J].中国新药杂志,2014,23(2):154-160
[13]李丽杰,王洪光,杨 航.膜控释盐酸二甲双胍缓释片的研制[J].青岛科技大学学报:自然科学版,2007,28(5):380-383.
[14]EMEA.2006,Scientific discussion.[EB/OL].(2012-12-08).http:// www.ema.europa.eu/docs/en_GB/document_library/EPAR_Sci⁃entific_Discussion/human/000655/WC500097069.pdf.
[15]李嘉煜,马越峰,李 华,等.包衣技术在盐酸二甲双胍缓释片制备中的应用[J].中国新药杂志,2003,12(5):348-353.
Study on pioglitazone hydrochlorideandmetform in hydrochloride sustained release tablets
LIUYang1,LIHui2,ZHANGXiao-xiang1,HUANGShou-zheng2
(1.College ofMedical Engineering,HefeiUniversity of Technology,Hefei230009; 2.AnhuiShangruiPharmaceutical Technology Co.,Ltd.,Hefei230001,China)
To optimize the formula and preparation procedureofpioglitazonehydrochloride(PH)andmetformin hydrochloride(MH)sustained release tablets,We took release rate of PH and MH as indexes to potimize the suitable fillers,adhesive,film formers and porogen The optimized formulawas determined as follows:with hypromellose(5mPa·s)and ethylcellulose(20mPa·s)as film formers,PEG6000 as fillers and adhesive,stearic acid as lubricantand glidant,PEG400 as plasticizer and porogen,and titania as opacifier.The sustained release tablets showed a similar release rate as the reference samples.This formula is reasonable,the preparation procedure is stable and feasible,and the production cost issignificantly reduced.
metformin hydrochloride;pioglitazone hydrochloride;sustained release;formula and preparation procedure;release rate
R943
B
2095-1736(2015)03-0088-05
10.3969/j.issn.2095-1736.2015.03.088
2014-10-24;
2014-12-03
安徽商瑞医药技术有限公司
柳 杨,硕士研究生,研究方向为药物合成技术与工艺;
张霄翔,副教授,硕士生导师,研究方向为药物制剂,E-mail:zxxwyfzsy@sina.com。

